Allgemeine Informationen
Definition
EinSchlaganfall:Schlaganfallgefäßbedingte(Apoplex)ErkrankungenäußertdessichGehirnsinmiteinemdem gemeinsamen Merkmal einer plötzlicheinsetzendenauftretendenfokalenSchädigung von Hirngewebe aufgrund eines Gefäßverschlusses oderglobaleneinerFunktionsverlust, neurologischen Ausfällen, die durch Blutzirkulationsstörungen im Gehirn verursacht werden.Hirnblutung1Wenn der Funktionsverlust weniger als 24 Stunden andauert, wird von einer transitorischenTransitorisch ischämischenmische Attacke (TIA):gesprochen.umschriebene neurologische Funktionsstörung mit vollständiger Reversibilität innerhalb von 24 h1DieDermeistenBegriffTIAbasiertdauern kürzer als 1 Stunde.
Weitere Informationen siehe auch ArtikelRehabilitation nach einem Schlaganfall.
Klassifikationen und Einteilungen
Ein Schlaganfall kannallein aufviele verschiedene Arten klassifiziert werden. Üblich ist aber die Haupteinteilung nach der Pathologie.Hirnblutung (hämorrhagischer Schlaganfall) (10–15 %)Subarachnoidalblutung(3–5 % aller Schlaganfälle)intrazerebrale Blutung (10–12 % aller Schlaganfälle)
Hirninfarkt (ischämischer Schlaganfall) (80–85 %)UrsachenklassifikationKardiogene Embolie (20–25 % aller Schlaganfälle): Im Herzen befindet sich eine potenzielle Emboliequelle.„Großgefäßerkrankung” (35–50 % aller Schlaganfälle): Ist in den großen und mittelgroßen Arterien lokalisiert, häufig Embolien von PlaquesBefunden aus derAortaklinischenoder aus extrakraniellen GefäßenUntersuchung.„Kleingefäßerkrankung” (20–30 % aller Schlaganfälle): Verschluss von kleinen perforierenden subkortikalen Gefäßen, der häufig auf lokale Degenerationen in der Gefäßwand zurückgeführt wird; verursacht kleine Infarkte, auch lakunärer Infarkt genannt.seltene Ursachen (2–5 % aller Schlaganfälle): z. B. bei Blutdruckabfall, Vaskulitis,arteriellen Dissektionen, Sinusvenenthrombosen
Einteilung nach der LokalisierungHirninfarkte im vorderen Versorgungsgebiet (A. carotis), 85 %Hirninfarkte im hinteren Versorgungsgebiet (A. vertebralis), 15 %
Häufigkeit
InzidenzSchlaganfall ist weltweit:1-2geschdie zweithätztufigsteca. 220.000 pro Jahr in DeutschlandTodesursacheDarunterdiesindHauptursacheetwavon80–85Behinderung%und- ein
ischämischewesentlicherSchlaganfälleKostenfaktor(Hirninfarkte),fürca. 10–15 % sind hämorrhagische Schlaganfälle (Hirnblutungen)Gesundheitssysteme.
- Inzidenz
DarüberinhinausDeutschlandtretenca.mindestens 80270.000TIASchlaganfälleprojährlich1- ca.
Jahr200.000aufErstereignisse - ca. 70.000 Rezidive
- ca.
- 1-Jahres-Inzidenz ca. 336/100.000 Einw.3
IschIn den letzten 15 Jahren ist die Hämischeufigkeit von Schlaganfällellenkommenetwaauchgleich gegeblieben.- Die Sterblichkeit am Schlaganfall ist in den letzten 15 Jahren erheblich zurückgegangen – bei
KindernFrauenvor;vondie500,jbei MährlichennernInzidenzvonwird600mitauf0,6–7,9300/100.000(USA) angegeben; die Diagnose wird häufig erst spät gestellt, weil selten daran gedacht wirdEinw.4
PrävalenzAlterInansteigendeDeutschlandInzidenzlebenmitcadem Alter, ab dem 65.1,76LebensjahrMio.häufigerMenschen,alsdiekoronareeinen Schlaganfall erlitten haben. Etwa 2/3 von ihnen leiden an einem Funktionsausfall aufgrund des Schlaganfalls und sind dauerhaft behindert.Lebenszeitprävalenz: 15 % der Bevölkerung erleidet im Lauf des Lebens einen Schlaganfall.Ereignisse5
SterblichkeitGeschlechtImLebenszeitprävalenzerstendesJahr nach dem Schlaganfall versterben 1/4 bis 1/3 der betroffenen Menschen.In Deutschland sterben jährlich etwa 60.000 Personen an einem Schlaganfall. Das sind 6,6 % aller Todesfälle, und dies istSchlaganfalls bei Männerndiegeringfügigdritthäufigstehöherundals bei Frauendie zweithäufigste Todesursache.2,5Die Sterblichkeit an Schlaganfall geht in Deutschland bei beiden Geschlechtern seit über 15 Jahren jährlich weiter zurück. Seit 1998 hat sich die Sterblichkeit bezogen auf 100.000 Einwohner*innen mehr als halbiert.Weltweit ist der Schlaganfall noch die zweithäufigste Todesursache: 4,5 Mio. Menschen im Jahr sterben an einem Schlaganfall.
DemografieSozioökonomischer Status90Inzidenz%amder Schlaganfallpatient*innen sind über 60 Jahre alt, das Durchschnittsalter liegthöchsten bei75niedrigemJahren.Sozialstatus und am niedrigsten bei hohem Sozialstatus2
Infolgebei Frauen deutlichere Ausprägung desSchlaganfallssozialenentstehen die meisten Pflegetage.Gradienten
Ätiologie und Pathogenese
IschÄtiologie des ischä
mischermischenSchlaganfallSchlaganfalls (ca. 85 %)85Arterielle Ischämie am häufigsten, anhand der TOAST-Kriterien kann eine Einteilung der Ätiologie erfolgen in:8-11
- Makroangiopathie (ca. 10 %)
- extrakranielle oder intrakraniellen Arterie mit Obstruktion ≥ 50 % (z. B. Karotisstenose)
- Mikroangiopathie (ca. 25 %)
- lakunäre Infarkte in der zerebralen Bildgebung
- Kardioembolie (ca. 25 %)
- Vorhofflimmern/-flattern, intrakardialer Thrombus, Herzklappenprothese, Vorhofmyxom
- andere Ursachen (ca. 10 %)
- z. B. Dissektion, Vaskulitis, Koagulopathien, Vasospasmen, Drogen
- ungeklärte Ätiologie („kryptogen“): ca. 30 %
- ESUS (Embolic Stroke of Determined Source, ca. 15 %) stellt eine Weiterentwicklung des Konzepts des kryptogenen Schlaganfalls dar.8-9
- Es beruht darauf, dass die Mehrzahl der kryptogenen Schlaganfälle
entstehenwahrscheinlichdurch einen Hirninfarkt aufgrund eines Gefäßverschlusses, entweder durch Thromben, die direkt im Gefäß entstehen, oder durch Embolienembolisch ausdemeinerHerzenverstecktenoderQuelledengetriggertArterien. Lakunäre Infarktesind,die durch einen Verschluss in den kleinen, subkortikalen Arterien (lokale Thrombose oder Embolie) ausgelöst werden, machen etwa 25 % aller Hirninfarkte aus.Die übrigen Hirninfarkte scheinen in 75–80 % der Fälle durch Embolien verursacht zu sein.Karotisarterien, AortaundHerzerfordertzähleneineheutestandardisiertezu den häufigsten Ausgangspunkten für Embolien.Je nach Auslegung der diagnostischen Kriterien werden 15–35 % der ischämischen Schlaganfälle als kardiale Embolie klassifiziert.Studien zeigen, dass sich durch den Einsatz von Eventrekordern der Anteil von einem unentdeckten proxysmalenVorhofflimmernals Ursache für Schlaganfall oder TIA deutlich erhöhen lässtDiagnostik.8-9
HirnblutungVenöse Ischämie deutlich seltener durch Sinusvenenthrombose/ Hirnvenenthrombose5,12
Ätiologie des hämorrhagischen Schlaganfalls (ca. 15 %)
15Intrazerebrale% der Schlaganfälle werden auf eine Hirnblutung zurückgeführt, entweder intrazerebral (10 %) oder als Subarachnoidalblutung an der Oberfläche des Gehirns (3–5 %).Blutung- Subarachnoidalblutung
Pathogenese
Schlaganfall
HatHauptursache des Schlaganfalls ist der Abfall des Blutflusses unter den Grenzwert, der für den Erhalt der funktionellen Integrität der Gehirnzellen erforderlich ist.13- Die ungenügende Blutzufuhr triggert eine
anderekomplexeSymptomatikschädigende Kaskade biochemischer Mechanismen.13-15- u. a. Entzündung,
hohemangelndeinitialeEnergiebereitstellung,SterblichkeitAzidose, Exzitotoxizität, Toxizität durch freie Radikale undeineZytokine,andereKomplementaktivierung,initialeVerschlechterungBehandlung.der Blut-Hirn-Schranke, Leukozyteninfiltration
- u. a. Entzündung,
intrazerebraleLetztlichBlutungführen diese Mechanismen zum Zelltod.
TIA
- Das pathogenetische Verständnis der TIA (reversibles neurologisches Defizit mit vollständiger Rückbildung innerhalb 24 h) hat sich durch die moderne Bildgebung (MRT) verändert.
Bluthochdruck16 - Streng genommen sollte der Begriff auf Patient*innen ohne Läsionsnachweis im MRT eingeschränkt werden.17
- Die transiente Symptomatik mit nachgewiesener Läsion ist
der wichtigste Risikofaktor. erhöhte Häufigkeit bei Personenmitzerebraler Amyloidangiopathie, Aneurysmen oder arteriovenöser FehlbildungMedikamente, die die Gerinnung beeinflussen (Antikoagulationoder plättchenhemmende Behandlung),Alkoholkonsum, Drogenmissbrauch und Vaskulitiden sind andere Faktoren, die mit einemerhöhtenhtem Risiko fürHirnblutungenSchlaganfall mit bleibender Behinderung verbunden.17- Das Problem bei flüchtigen neurologischen Ereignissen ohne pathologischen Befund in
Verbindungderstehenzerebralen Bildgebung ist, dass es auch viele andere Ursachen geben kann, die nicht zwangsläufig zu einer lebenslangen Medikation führen müssen.
- Die transiente Symptomatik mit nachgewiesener Läsion ist
- Makroangiopathie (ca. 10 %)
TransitorischischSo kann beispielsweise eine MigrämischeneAttackemit dem Bild eines Schlaganfalls einhergehen (TIAsiehe auch Differenzialdiagnosen)Eine.transitorischKompliziertischwird dies dadurch, dass eine MigrämischeneAttackeund(TIA)speziellistaucheineineAnzeichenBehandlung mit Triptanen das Risiko füreinenSchlaganfälledrohendenerhöhenSchlaganfallkönnen.Eine schnelle und richtige Behandlung beugt einem manifesten Schlaganfall und anderen vaskulären Erkrankungen vor.18
Arteriosklerose und SchlaganfallArterielle Embolien sind gut für die Hälfte aller Schlaganfälle verantwortlich.Instabile Plaques sind die Ausgangsquelle arterieller Embolien.Instabile Plaques der Karotiden können morphologisch mit dem Ultraschall festgestellt werden.
Herzerkrankungen und SchlaganfallHerzerkrankungen können infolge von kardialen Embolien (Vorhofflimmern) oder einem kardial verursachten Blutdruckabfall (Herzinsuffizienz) einen Schlaganfall auslösen.Patient*innen mit akutem Hirninfarkt sollten auf mögliche kardiale Emboliequellen überprüft werden.
Hirninfarkt bei jungen MenschenDie Karotisdissektion wird zu den häufigsten Ursachen für einen Schlaganfall bei Patient*innen unter 50 Jahren gezählt.Bis zu 20 % aller Fälle bei Patient*innen unter 30 Jahren können auf eine Karotisdissektion zurückgeführt werden.
Körperliche Aktivität und HerzgefäßerkrankungenEs besteht ein umgekehrter Zusammenhang zwischen Herz- und Gefäßerkrankungen sowie körperlicher Aktivität.Aus epidemiologischer Sicht besteht ein wahrscheinlicher Zusammenhang zwischen niedriger körperlicher Aktivität und Schlaganfallrisiko.9Dennoch kann aus den Daten solcher Beobachtungsstudien nicht geschlussfolgert werden, dass körperliche Aktivität das Schlaganfallrisiko senkt.
TIAEine vorübergehende neurologische Schwäche, die sich innerhalb von 24 Stunden vollständig zurückbildet.Durch den Einsatz moderner MRT-Technologien konnte gezeigt werden, dass diese Ereignisse kleinen Schlaganfällen entsprechen.10Das Risiko im Verlauf einen manifesten Insult mit bleibenden Schäden zu erleiden, ist erhöht.
Die meisten „echten” TIA dauern kürzer als 15 Minuten.
Disponierende Faktoren
DerEswichtigstegibtRisikofaktornicht-modifizierbare und modifizierbare Risikofaktoren für einen ischämischen und hämorrhagischen Schlaganfall.
Nicht-modifizierbare Risikofaktoren19
- Alter
- zunehmendes Risiko mit dem Alter
- Geschlecht
- Bei jungen Frauen ist das
steigendeRisikoLebensalter.etwasWeiterehöherRisikofaktoren sindhoher Blutdruck,Rauchen,Übergewicht, Bewegungsmangel,Diabetes mellitus, Hypercholesterinämie undVorhofflimmern. Die INTERSTROKE-Studie identifizierte 10 Risikofaktoren, die mit etwa 90 % aller Schlaganfälle korreliert wurden (II):11Hypertonie(OR 2,64)Rauchen (OR 2,09)Taille-Hüft-Verhältnis: abdominaleAdipositas(OR 1,65)Wennals bei Männern, bei Älteren ist dasVerhRisiko für Mältnisnner>geringfügig0,96höherbzw.als< 0,91 oder- bei Frauen
> 0,93 bzw. < 0,86 ist.
ungesunde Ernährung (OR 1,35)InaktivitEthnizität(OR für körperliche Aktivität 0,69)Diabetes mellitus (OR 1,36)Alkoholkonsum(OR 1,5)- erhöhtes Risiko bei
mehrafrikanischeralsAbstammung30–AlkoholeinheitenundimzugleichMonatschlechtereoderprotektivemanifesterWirksamkeitAlkoholabhängigkeitvon Betablockern und ACE-Hemmern
- erhöhtes Risiko bei
- Genetik
- erhöhtes Risiko bei positiver Familienanamnese
Modifizierbare Risikofaktoren für ischämischen Schlaganfall
- In der Interstroke-Studie wurden 10 modifizierbare Risikofaktoren identifiziert:19-20
- arterielle Hypertonie
- Rauchen
- abdominale Adipositas: erhöhtes Taille-Hüfte-Verhältnis
- ungesunde Ernährung
- Inaktivität
- Diabetes mellitus
- erhöhter Alkoholkonsum
- psychosozialer Stress
(ORund1,30) - Depression
(OR 1,35) - kardiale Ursachen
(OR 2,38)
- Verhältnis Apolipoprotein B/Apolipoprotein A1, d. h. LDL/HDL
(OR 1,89); betrifft höchstes vs.niedrigstes Drittel
- Verhältnis Apolipoprotein B/Apolipoprotein A1, d. h. LDL/HDL
DepressionEineÖstrogenhaltigeMetaanalyseOvulationshemmerbestätigterhöhendiedasVerbindung zwischen Depression und Schlaganfall (HR 1,45)Schlaganfallsrisiko.12
NSARModifizierbare Risikofaktoren für hämorrhagischen Schlaganfall19-20
EineArterielleStudieHypertonie- Rauchen
- Abdominale
zeigt einAdipositas: erhöhtesRisiko fTaille-Hür Tod durch ischfte-Verhämischen Schlaganfall innerhalb von 30 Tagen bei aktuellem Gebrauch von COX-2-Hemmern (III).13ltnis Beim Gebrauch von nichtselektiven NSAR wurde kein erhöhtes Risiko für Tod durch ischämischen Schlaganfall oder für Hirnblutungen festgestellt.
Epileptischer Anfallbei Älteren ohne bekannte EpilepsieDies kann ein Warnzeichen für Schlaganfall (RR ca. 3) sein (Marker einer unbekannten zerebrovaskulären Erkrankung).14
Substitutionsbehandlung mit Östrogenen- Erhö
ht das Risiko für einen (ischämischen) Schlaganfall (OR 1,29) (Ia).hter15Alkoholkonsum Die Verwendung vonoralen Kontrazeptivamit Ethinylestradiol führt bei Frauen in der Altersgruppe 15–49 Jahre zu einer geringen Erhöhung des Schlaganfallrisikos.16bei Ethinylestradiol 20 µg OR 0,9–1,7; bei 30–40 µg OR 1,3–2,3
- Erhö
InfektionEine britische Studie (III) zeigte, dass das Risiko für Schlaganfall undHerzinfarktin den ersten 3 Tagen nach einer akuten Atemwegsinfektion deutlich angestieg.17Das Inzidenzverhältnis für Schlaganfälle lag bei 3,2 (95 % KI 2,8–3,6) und für Myokardinfarkt bei 5,0 (95 % KI 4,4–5,5).Das Risiko verringerte sich schrittweise über die nächsten 4 Wochen.Es wurde auch eine Verbindung zwischen invasiver Zahnbehandlung und erhöhtem Risiko für Schlaganfall innerhalb der ersten 4 Wochen nachgewiesen (III).18
SalzEine erhöhte tägliche Salzzufuhr durch dieUngesunde Ernährungerhöht das Schlaganfallrisiko.19
Manipulation des NackensNach einem systematischen Review kann ein Zusammenhang zwischen chirotherapeutischer Nackenmanipulation und Schlaganfall weder nachgewiesen noch ausgeschlossen werden (Ia).20
ICPC-2
- K89 Transiente zerebrale Ischämie /TIA
- K90 Schlaganfall/zerebrovask. Insult
- K91 Zerebrovaskuläre Erkrankung
ICD-10
- I61 Intrazerebrale Blutung
- I61.0 Intrazerebrale Blutung in die Großhirnhemisphäre, subkortikal
- I61.1 Intrazerebrale Blutung in die Großhirnhemisphäre, kortikal
- I61.2 Intrazerebrale Blutung in die Großhirnhemisphäre, nicht näher bezeichnet
- I61.3 Intrazerebrale Blutung in den Hirnstamm
- I61.4 Intrazerebrale Blutung in das Kleinhirn
- I61.5 Intrazerebrale intraventrikuläre Blutung
- I61.6 Intrazerebrale Blutung an mehreren Lokalisationen
- I61.8 Sonstige intrazerebrale Blutung
- I61.9 Intrazerebrale Blutung, nicht näher bezeichnet
- I63 Hirninfarkt
- I63.0 Hirninfarkt durch Thrombose präzerebraler Arterien
- I63.1 Hirninfarkt durch Embolie präzerebraler Arterien
- I63.2 Hirninfarkt durch nicht näher bezeichneten Verschluss oder Stenose präzerebraler Arterien
- I63.3 Hirninfarkt durch Thrombose zerebraler Arterien
- I63.4 Hirninfarkt durch Embolie zerebraler Arterien
- I63.5 Hirninfarkt durch nicht näher bezeichneten Verschluss oder Stenose zerebraler Arterien
- I63.6 Hirninfarkt durch Thrombose der Hirnvenen, nichteitrig
- I63.8 Sonstiger Hirninfarkt
- I63.9 Hirninfarkt, nicht näher bezeichnet
- I64 Schlaganfall, nicht als Blutung oder Infarkt bezeichnet
- G45 Zerebrale transitorische Ischämie und verwandte Syndrome
- G45.9 Zerebrale transitorische Ischämie, nicht näher bezeichnet
DiagnostikDiagnostische Kriterien
- Akut aufgetretene neurologische Symptome
- Nachweis einer Ischämie/Blutung in der zerebralen Bildgebung
Differenzialdiagnosen (Stroke Mimics)
- Auch im Zentrum einer Maximalversorgung liegt die initiale Fehldiagnose bei ca. 10 %, im präklinischen Bereich ist von höheren Quoten auszugehen.21
- Wesentliche „Stroke Mimics“ sind:21
Leitlinie:ZerebraleSchlaganfall2Ursachen (die 3 häufigsten)AkutversorgungEpileptischer Anfall (vor allem Todd-Parese = passagere Lähmung nach einem epileptischen Anfall)- Migräne mit Aura
- Funktionelle/dissoziative Störung
Zerebrale Ursachen (andere)
- Intrakranielle Raumforderung
- Entzündlich
- Synkopen
Isolierte Hirnnervenausfälle
- Periphere Fazialisparesen
- Vestibulopathien
Metabolische Ursachen
- Hypoglykämie, Hyperglykämie
- Elektrolytstörungen
Verschlechterung des
SchlaganfallsAllgemeinzustands (insb. bei älteren Menschen)- Exsikkose
- Infekt, Sepsis
Pseudolähmungen
- Orthopädisch bedingte Bewegungseinschränkungen (z. B. Schenkelhalsfraktur, Rotatorenmanschettenruptur)
Präklinische Diagnostik und Versorgung
- Schlaganfall/TIA sind grundsätzlich medizinische Notfälle, bei jedem Verdacht soll unverzüglich die Notruf-Telefonnummer 112 gewählt werden.1
- Jeder andere Versuch, medizinische Hilfe zu organisieren, führt zu potenziell bedrohlicher Verzögerung der
TIAVersorgung.1
- Jeder andere Versuch, medizinische Hilfe zu organisieren, führt zu potenziell bedrohlicher Verzögerung der
Initiale Untersuchung
- Die initiale klinische Untersuchung soll nach dem ABCDE-Schema erfolgen:1
- Airway (Atemwege)
- Breathing (Beurteilung der Atmung)
- Circulation (Kreislauf)
- Disability (neurologischer Zustand)
- Exposure (Beurteilung in entkleidetem Zustand).11
- Ggf. sollen bereits nach ABC lebensrettende Maßnahmen durchgeführt werden.1 (siehe auch Basic Life Support, Advanced Life Support)
- Hiervon sind aber nur wenige Patient*innen mit Schlaganfall betroffen.1
- Ansonsten wird im nächsten Schritt der neurologische Status überprüft.1
- Hierfür soll ein standardisierter neurologischer Untersuchungsalgorithmus (z. B. FAST) verwendet werden, dieser weist mit hoher Sicherheit neurologische Defizite nach und ermöglicht eine gezielte Einweisung.1
Initiale Versorgung
- Wenn zeitnah möglich, sollte ein venöser Zugang zur vorsorglichen Absicherung gelegt werden. Vorteile sind:1
- bei Bedarf i. v. Applikation von Medikamenten
- Möglichkeit zur Blutzuckermessung
- Volumengabe bei Exsikkose
- Abnahme von Laborblut (je nach rettungsdienstlichem Versorgungskonzept).
- Eine Hypoglykämie ist ein typisches „Stroke Mimic“ und sollte daher ausgeschlossen werden.
- Zurückhaltendes Blutdruckmanagement bei initial häufig erhöhtem Blutdruck: Zu rasche Senkung kann eine Ischämie verstärken, ein zu hoher Blutdruck ist bei Blutung ungünstig (klinische Unterscheidung der Ätiologie aber nicht möglich).
- Der Nutzen einer routinemäßigen Sauerstoffgabe ist nicht belegt.1
- Antikoagulation (Heparin) oder Thrombozytenaggregationshemmer (ASS) sollten vor Bildgebung in der Klinik nicht verabreicht werden, da eine Blutung präklinisch nie ausgeschlossen werden kann.5
DEGAM-Empfehlungen zur vorstationären Diagnostik und Versorgung1
Initiale Untersuchung
ABCDE-Schema
- Die initiale Untersuchung von Notfallpatient*innen soll
(Airway, Breathing, Circulation, Disability, Environment/Exposure)erfolgen. - Ergibt sich aus ABC ein sofortiger Handlungsbedarf, soll entsprechend gehandelt werden.
Ein standardisierter neurologischer Untersuchungsalgorithmus (z. B. FAST [Face Arm Speech-Test]) weist mit hoher Sicherheit neurologische Defizite nach und macht so eine gezielte Einweisung möglich.
FAST
TIAFacePlötzlichLasseneinsetzender fokaler, neurologischer Ausfall aufgrund von Störungen in der Blutzirkulation des Gehirns, mit Symptomen,Sie diesichPersoninnerhalblächeln.vonHängt24einStundenMundwinkelzurückbildenherab? Dies kann auf Gesichtslähmung/Halbseitenlähmung hinweisen.
SchlaganfallPlötzlich einsetzender fokaler neurologischer Ausfall aufgrund von Störungen in der Blutzirkulation des Gehirns, mit Symptomen, die über 24 Stunden hinaus bestehen bleiben.
FAST-TestFazialispareseArm- Bitten Sie die
Patient*innenPerson, die Arme nach vorne zulächelnstrecken und dabei dieZHandflähnechen nach oben zuzeigendrehen. - Bei
AchteneinerSieLähmungaufkönneneinenichtneubeideaufgetreteneArmeAsymmetriegehoben werden, ein Arm sinkt ab oder dreht sich.
- Bitten Sie die
ArmpareseSpeechHeben Sie den Arm auf 90 Grad in sitzender Position und auf 45 Grad in liegender Position. BittenLassen Sie diePatient*innen,PersondieseeinenPositioneinfachen5SatzSekundennachsprechen.- Ist
zusiehalten.dazuPositiv,nichtwennin derArm abdriftetLage oderaufklingt dieUnterlageStimmefälltverwaschen, liegt vermutlich eine Sprachstörung vor.
SprachschwierigkeitenTimeBestehenFallsWortfindungsproblememindestensund/odereinerverstehenderdieo.Patient*inneng.mündlicheTestsAnweisungenpositivnicht?ist: Ohne weiteren Verzug 112 anrufen („Time is brain“)!
- Siehe Tabelle
SprechschwierigkeitenFAST-Test. - Neurologisch Versierte können die NIHSS (National Institutes of Health Stroke Scale) zur umfassenderen Beurteilung der klinischen Schwere eines Schlaganfalles benutzen, diese wird aber überwiegend erst in der Klinik verwendet.11,22
AufFürneujedesauftretendeKriterium der NIHSS werden zwischen 0 und max. 4 Punkte vergeben (Gesamtpunktzahl 0–42 Punkte),undeutlichejeAussprachehöherachtendie Punktzahl, desto schwerer der Schlaganfall (NIHSS Rechner).
InterpretationMerke:FIschällt ein Test positiv aus, besteht eine hohe Wahrscheinlichkeit für das Vorliegen eines Schlaganfalls,mische unddiehämorrhagischePatient*innen sollten sofort – „Time is brain“ – eingewiesen bzw. die NotSchlaganfärztin/der Notarzt verständigt werden.Wenn die Symptome vor Ablauf von 24 Stunden vorübergehen, liegt eine TIA vor.Bei einer peripherenFazialispareseist eine Notfalleinweisung nicht notwendig.
Fokale neurologische SymptomeSchwäche oder Ungeschicklichkeit auf einer KörperseiteSprachstörungen/Aphasie: Schwierigkeiten, sich sprachlich auszudrücken oder Sprache zu verstehen.Verminderte Sensibilität in einer KörperhälfteSehverlustauf einem Auge, vollständig oder teilweiseVerlust eines Teils des Sichtfeldes: Hemianopsie, QuadrantenanopsieAmaurosis fugax: vorübergehende Sehstörung aufgrund einer Ischämie der Netzhaut
Kognitive Symptome: Unaufmerksamkeit, Vernachlässigung einer KöperhälfteApraxie: Schwierigkeiten, geplante Bewegungen in der richtigen Reihenfolge durchzuführen, ohne dass es mit einer verminderten Sensibilität oder Motorik erklärt werden kann.
Differenzialdiagnosen5–10 % der Patient*innen, die mit der Diagnose Schlaganfall eingewiesen werden, haben andere Erkrankungen. Dieselle könnensein:SynkopeHypoglykämieHyperglykämieAlkoholvergiftungMedikamentenvergiftungGehirntumorsubdurales Hämatom oder KopfverletzungMeningitisoderEnzephalitispostiktale Lähmung nach einemepileptischen AnfallMigränemultiple Sklerosehypertensive EnzephalopathieVerwirrtheitszuständehysterische LähmungenperiphereFazialisparese.
AnamneseAllgemeinesEin Schlaganfall mit plötzlich einsetzenden Symptomen innerhalb von:Sekunden – typisch für eine arterielle EmbolieMinuten – typisch für HirnblutungMinuten bis Stunden – typisch für Thrombosierung.
Bei 20–30 %anhand derSchlaganfall-Patient*innenklinischenkannUntersuchunginnerhalbnichtder ersten 2–3 Tage nach dem ersten Auftreten der Symptome eine weitere Progression hin zu einem umfassenderen Gehirnschaden festgestelltdifferenziert werden.Die Symptome hängen davon ab, welche Teile des Gehirns betroffen sind, und reichen von verminderter Kraft in einem Arm bis zu Hemiplegien und ausgedehnten Funktionsverlusten wieKoma23,Bewusstseinseintrübungen, abnehmender Sprachfunktion, kognitivem Versagen und emotionaler Labilität.
Differenzialdiagnostische Bewertungen- Bei
VerdachtTelefonkontaktauf TIA oder einen eindeutigen Schlaganfall sollte die Anamnese zusätzlich zum Verlaufmit derakuten Ereignisse folgende Aspekte umfassen:früherer Schlaganfall/TIARisikofaktoren wieRauchen,Alkohol, Inaktivität, Fehlernährung,Übergewicht,Diabetes,HypertoniePraxis undHerzkrankheitmedikamentöse Behandlung inklV.Antikoagulanzienbehandlungund Antidiabetikakürzlich erlitteneKopfverletzungen/Unfällea.
Klinische UntersuchungBei klinischem Verdacht auf einenSchlaganfall/TIA sollen die Patient*innen umgehend eingewiesen werden, und auf umfangreiche Diagnostik soll verzichtet werden! (Jede Minute zählt/Time is brain)Weitergehende Diagnostik im Krankenhaus
Orientierende neurologische UntersuchungBewusstseinszustandSchiefes Gesicht (Fazialis)Bewegung und Kraft in Armen und Beinen (Arm)Wortfindungsstörungen oder undeutliche Aussprache (Sprache und Sprechen)PupillenreflexSteifer Nacken und ReflexeInvertierte Plantarreflexe (Babinski-Reflex) können bei älteren Patient*innen mit steifen Gelenken oder Folgen nach einer früheren Erkrankung im Muskelskelettsystem oder einer neurologischen Erkrankung schwierig zu beurteilen sein.
Herz-Gefäß-StatusPuls, Blutdruckmessung, Herz-Gefäß- und Lungen-Status sind wichtige Untersuchungen für die Prognose und die Behandlung.Puls/Rhythmus messen.Prüfen, ob Stenosegeräusche über den Karotiden und dem Herzen zu finden sind.
VerschiedenesNichtsprachlich-kognitive Symptome nach einem SchlaganfallMessung vonBlutzuckerund Körpertemperatur
Vorkommen verschiedener fokaler neurologischer Befunde bei einem akuten SchlaganfallMotorik 75–85 %Arm-/Handparese 70–85 %Fazialisparese60–70 %Beinparese 65–75 %
Aphasie 20–25 %Sensibilitätsstörungen 30–50 %Visuelle Symptome* 10–20 %21Gleichgewichts-/Koordinationsstörungen* 10–30 %Verhaltens-/Wahrnehmungsstörungen oder kognitive Störungen 10–50 %
*Isolierte visuelle Störungen oder Koordinationsstörungen werden in der Regel nicht als so spezifisch betrachtet, dass sie allein als fokale Schlaganfall-Symptome klassifiziert werden können.Ergänzende UntersuchungenBei klinischem Verdacht auf einen Schlaganfall sollte die sofortige Einweisung nicht durch Blutentnahmen verzögert werden.
Indizierte Untersuchungen, wenn nicht akute Zeichen eines Schlaganfalls ohnehin zur Klinikeinweisung führenEKG, um kardiale Ursachen für einen Schlaganfall zu ermitteln.Arrhythmie, insbesondereVorhofflimmern. Eine Langzeit-EKG kann notwendig sein, um mögliches paroxysmales Vorhofflimmern abzuklären.8kürzlich erlittenerHerzinfarktals Quelle einer Embolie
Kleines Blutbild,BSG,CRP,Glukose, Elektrolyte (Na,K,Ca),Kreatinin,GPT (ALT), Gerinnungsstatus und Serumlipide (Cholesterin,HDL)22-23
Diagnostik bei Spezialist*innenIm KrankenhausPatient*innen mit Symptomen eines akuten Schlaganfalls sollten sofort mit CT oder MRT untersucht werden. Hämorrhagische Infarkte lassen sich mit beiden Methoden nachweisen und – ein genügend langes Zeitfenster vorausgesetzt – ausschließen. Eine akute Ischämie lässt sich nur im MRT zeigen.24Bei Patient*innen, bei denen eine Thrombolyse indiziert ist, sollte eine bildgebende Untersuchung des Gehirns innerhalb von 20–30 Minuten nach der Einweisung stattfinden.Eine Duplex-Sonografie der Halsgefäße sollte bei allen Patient*innen mit Hirninfarkt oder TIA durchgeführt werden und/oder eine MR-Angiografie (MRA) oder CT-Angiografie.
Indikationen zur KrankenhauseinweisungLeitlinie: Schlaganfall2Hausärztliches TIA-ManagementPatient*innen mit TIA-Symptomatik innerhalb der letzten 48 Stunden sollten umgehend einer Stroke Unit zugewiesen werden.Bei Patient*innen, bei denen die Symptomatik länger als 14 Tage zurückliegt, ist in der Regel eine ambulante Abklärung ausreichend, die schnellstmöglich, jedoch binnen eines Monats nach Symptombeginn komplettiert werden sollte.Im intermediären Zeitraum sollten Patient*innen mit vielen Risikofaktoren, hohem ABCD2-Score (z. B. ≥ 4), bekanntemVHF, bekannten Stenosen hirnversorgender Arterien oder früheren kardiovaskulären Erkrankungen einer Stroke Unit zugewiesen werden.Wird die Abklärung ambulant durchgeführt, unterscheiden sich Diagnostik und Sekundärprävention nicht von Patient*innen nach vollendetem Schlaganfall.Konstellationen, die gegen eine Krankenhauseinweisung sprechen könnenHausärzt*innen obliegt es, zwischen möglichem Nutzen und Schaden einer Krankenhauseinweisung im individuellen Fall abzuwägen.Bestehen Hinweise, dass eine palliative Therapie dem Patienten- und/oder Betreuerwunsch entspricht, sind supportive Maßnahmen zu besprechen und einzuleiten und auf die Einbeziehung des Rettungsdiensts zu verzichten.In folgenden Situationen ist in der Regel kein kurativer Nutzen einer stationären Krankenhausbehandlung anzunehmen:Infauste Prognose durch aktuelles Ereignis oder andere ErkrankungenMultimorbiditätFortgeschrittene KrebserkrankungMehrere vorausgegangene Insulte mit massiven neurologischen Defiziten
Schulung des PraxisteamsFalls sich im Laufe eines Telefonats zeigt, dass ein Schlaganfall vorliegen könnte,sollten medizinische Fachangestellte den FAST-Test anwenden undunter der Telefonnummer 112.
Edukation von Risikopatient*innenPersonen mit einem erhöhten Schlaganfallrisiko (z. B.Hypertonie,Rauchen, ein kardiovaskuläres Ereignis in der Vorgeschichte) sollten über Schlaganfall-Symptome(zTelefon-Nr.B. anhand des FAST-Tests), Warnzeichen und erforderliche Maßnahmen (wie z. B. Aktivierung des Rettungsdiensts unter112)aufgeklärt werden.
SchlaganfallInitialeund TIAVersorgungPatient*innen mit Symptomen eines akuten Schlaganfalls sollten zur Diagnostik und Akutbehandlung sofort in ein Krankenhaus mit entsprechender Station – Stroke Unit – eingewiesen werden.2Ausnahmen: Patient*innen mit rezidivierenden Schlaganfällen, die für eine Thrombolyse nicht mehr infrage kommen – sowie Patient*inne mit anderweitig stark eingeschränkter Lebenserwartung.Beachtung des Patientenwillens/Patientenverfügung (falls vorhanden)!
DerFAST-Testwird als Hilfsmittel empfohlen, um Patient*innen mit einem akuten Schlaganfall zu identifizieren.
Bei Patient*innen mit akuten Schlaganfall-Symptomen sollte direkt eine Notärztin/ein Notarzt gerufen werden.Die Differenzierung in TIA oder Insult lässt sich nur retrospektiv treffen und auch Patient*innen mit einer TIA sollten umgehend eingewiesen werden.25-26Hausärzt*innen/Bereitschaftsärzt*innen sollten bei Patienten mit Verdacht auf einen Schlaganfall eine schnelle Einweisung veranlassen, evtl. auch ohne vorhergehende Untersuchung.
Vor dem Durchführen einer CT keine Ass- oder Heparin-Gabe. Auch i. m. Injektionen sollten unterbleiben.
Checkliste zur ÜberweisungBehandlung nach der Akutphase bei SchlaganfallZweck der ÜberweisungDiagnostik? Therapie? Sonstiges?
AnamneseErkrankungsbeginn? Spätere Entwicklung? Komplikationen?SymptomeSonstige relevante Vorerkrankungen? Regelmäßige und aktuelle Medikamente?Evtl. durchgeführte Behandlungsmaßnahmen und deren Wirkung?Konsequenzen: soziale, Hilfebedürftigkeit, Pflege, anderes?
Klinische UntersuchungAllgemeinzustand?Gesichtslähmung? Arm-/Beinparese? Sprach- oder Ausspracheschwächen?Blutdruck, Puls, Herz
TherapieTherapiezieleHirnschäden und Funktionsminderung begrenzen.Erneuten Schlaganfällen vorbeugen.Die gesamte kardiovaskuläre Mortalität verringern.
AllgemeinesDie Behandlung zielt auf:Begrenzung der HirnschädenAusschalten oder Kontrolle der auslösenden oder disponierenden ErkrankungenVorbeugen oder Verringern des Risikos für KomplikationenWiederherstellung der FunktionenEinleitung von Maßnahmen, die die Möglichkeiten für spätere kardiovaskuläre Krankheitsepisoden verringern.
Es wird zwischen Akutbehandlung und Behandlung nach der Akutphase unterschieden.In der Akutphase unterscheiden sich die Behandlungspläne bei Hirninfarkt und Hirnblutung.
Empfehlungen für Patient*innenVeränderung des Lebensstils, z. B. mit demRauchen aufhörenoder dieErnährung umstellen.Regelmäßige Bewegung(einschließlich Spaziergänge) undKrafttraining(insbesondere für den Oberkörper) nach einem Schlaganfall wirken positiv auf die Kognition, die Armfunktion, das Gleichgewicht und die Gehfunktion sowie evtl. auch gegenMüdigkeitundDepressionen.27Aktives Training ist wichtig für das Funktionsniveau.Engagement und Motivation für die Reha-Behandlung scheinen bei den Patient*innen zu Hause größer zu sein als im Krankenhaus.
Hirninfarkt: AkutbehandlungLeitlinie: Schlaganfall2Venöser Zugang
- Sofern ein venöser Zugang in einem akzeptablen Zeitrahmen herstellbar ist, soll er als Absicherungsmaßnahme angelegt werden, da jeder Schlaganfall eine potenziell akut lebensbedrohliche Situation darstellt.
Blutzucker
- Die Blutzuckermessung soll erfolgen, um die Differentialdiagnose einer Hypoglykämie sicher auszuschließen.
SauerstoffapplikationBei niedrigen BZ-Werten (< 60 mg/dl) soll Glukose i. v. gegeben werden.
Sauerstoff
- Die Gabe von Sauerstoff sollte erst ab einer Sättigung < 95 % erfolgen.
BlutzuckermessungBlutdruck
Die Blutzuckermessung soll erfolgen, um die Differenzialdiagnose einerHypoglykämiesicher auszuschließen.Bei niedrigen BZ-Werten (< 60 mg/dl [3,3 mmol/l]) soll Glukose i. v. gegeben werden.
Medikamentöse Therapie bei erhöhten BlutdruckwertenBei Patient*innen mit vermutetem Schlaganfall soll der Blutdruck gemessen werden.- Bei einem Wert < 120 mmHg systolisch und Hinweisen auf eine Exsikkose sollte
einekristalloide Infusionslösung verabreicht werden. - Blutdruckwerte ≥ 220 mmHg können per vorsichtiger medikamentöser Titration (z. B. mit Nitrendipin-Trinkampullen) um 15 % gesenkt
Andere präklinische BasismaßnahmenSonstiges
- Die anamnestischen Daten, einschließlich der Beginn der Symptomatik und mögliche Lyse-Kontraindikationen sowie bereits erfolgte therapeutische
- Ein Medikamentenplan soll zur Mitgabe vorbereitet werden.17
- Die anamnestischen Daten, einschließlich der Beginn der Symptomatik und mögliche Lyse-Kontraindikationen sowie bereits erfolgte therapeutische
Ärztliche Betreuung in der Akutphase- Die Zeit des Wartens auf den Rettungsdienst sollte
denPatient*innen undihrenBezugspersonen grundlegende Informationen zu
- Die Zeit des Wartens auf den Rettungsdienst sollte
Indikationen zu Klinikeinweisung bzw. ambulanter Abklärung
Akuter Schlaganfall oder TIA innerhalb der letzten 48 h1,17,24
einzuwirken- Diese Patient*innen sollen umgehend auf einer Stroke Unit behandelt werden.
TIA > 48 h und < 14 Tage1,17
- Hochrisikopatient*innen sollen einer Stroke Unit zugewiesen werden:
- bekanntes Vorhofflimmern
- bekannte Stenosen hirnversorgender Arterien
- sonstige frühere kardiovaskuläre Erkrankungen
- Hoher ABCD2-Score (≥ 4): berücksichtigt für den Score werden Alter, Blutdruck, Art der Symptome, Symptomdauer und Vorliegen eines Diabetes mellitus.
AllgemeinesSymptomatik > 14 Tage zurückliegend1,17EineInschnellederEinweisungRegel ist eine ambulante Abklärung ausreichend,genauediese sollte schnellstmöglich innerhalb eines Monats nach Symptombeginn komplettiert werden.- Bei ambulanter Abklärung unterscheiden sich Diagnostik und
guteSekundärprävention nicht von Patient*innen nach vollendetem Schlaganfall.
Gründe gegen Krankenhauseinweisung1
- Hausärzt*innen können sich unter Abwägung von Nutzen und Schaden und Berücksichtigung des Wunsches von Patient*innen/Betreuer*innen für eine palliative Therapie und gegen eine stationäre Einweisung entscheiden.
- In diesem Fall Verzicht auf Rettungsdienst und Einleitung supportiver Maßnahmen
Diagnostik und Therapie in der Stroke Unit
Konzept der Stroke Unit
- Stroke Units (Schlaganfall-Spezialstationen) sind Sondereinrichtungen mit einem integrativen Behandlungskonzept für Schlaganfallpatient*innen im Akutstadium.17
- Dieses Konzept umfasst Früherkennung, präklinische Notfallversorgung, zügige Ü
berwachungberweisung in Zentren mit derartigen Stationen, dortige Notfallaufnahme, neuroradiologische und sonstige apparative Sofortdiagnostik, Einbeziehung einer Intensivstation, schließlich Weiterverlegung auf Allgemeinstationen, in Rehabilitationseinrichtungen oder häusliche Pflege.17 - In ländlichen Regionen telemedizinische Anbindung der Notaufnahmen regionaler Krankenhäuser an überregionale Stroke Units (Tele-Stroke-Units)17
Diagnostik
Initiale Bildgebung17
- In der Stroke Unit
sinderfolgt eineVoraussetzungrasche Bildgebung durch CT oder MRT zur Unterscheidung zwischen Ischämie und Blutung. - Computertomografie (CT)
- diagnostischer Standard: breit verfügbar, universell anwendbar
- Durch CT-Angiografie mit Kontrastmittel können mit hoher Sicherheit extra- und intrakranielle Gefäßpathologien erfasst werden.
- Informationen zur Gewebsperfusion und Differenzierung zwischen abgestorbenem Gewebe (Infarkt) und minderperfundiertem Gewebe (Penumbra)
- Magnetresonanztomografie (MRT)
- im Vergleich zur CT höhere Sensitivität zum sicheren Nachweis infarzierten Hirngewebes in der Schlaganfallfrühphase, Abschätzung des Infarktalters möglich
- Nachteile sind höherer logistische Aufwand, längere Untersuchungsdauer und geringere Verfügbarkeit.
Monitoring17
- Akute Schlaganfallpatient*innen (TIA und Hirninfarkt) sollten zumindest in den ersten 2–3 Tagen apparativ überwacht werden.
- Das apparative Monitoring sollte mindestens umfassen: Blutdruck, Herzfrequenz, EKG, Atmung, Sauerstoffsättigung und Körpertemperatur.
Sonstige Diagnostik17
- EKG-Monitoring
- Ein mehrtägiges EKG-Monitoring (Telemetrie, im weiteren Verlauf evtl. LZ-EKG) sollte erfolgen, wenn der Nachweis von Vorhofflimmern oder anderer Rhythmusstörungen therapeutische Konsequenzen hat.
- Darstellung der extra- und intrakraniellen hirnversorgenden Gefäße
- So früh wie möglich (innerhalb von 24–48 Stunden) sollte eine nichtinvasive Diagnostik der extra- und intrakraniellen Gefäße erfolgen.
- In Betracht kommen je nach Verfügbarkeit und Expertise:
- Duplexsonografie
- CT-Angiografie
- MR-Angiografie.
- Echokardiografie (TTE, TEE)
- Eine transthorakale Echokardiografie (TTE) sollte zur Bestimmung der Ätiologie durchgeführt werden, wenn diese durch die initiale Diagnostik nicht geklärt werden konnte (z. B. Vorhofflimmern oder hochgradige Karotisstenose).
- Ist die Ätiologie nach Routinediagnostik (zerebrale Bildgebung, Darstellung der extra- und intrakraniellen Gefäße, EKG, Langzeit-EKG und TTE) ungeklärt, sollte bei therapeutischer Konsequenz ergänzend eine transösophageale Echokardiografie (TEE) durchgeführt werden.
Akuttherapie des ischämischen Schlaganfalls
- Ziel der therapeutischen Intervention beim ischämischen Hirninfarkt ist die Wiederherstellung einer ausreichenden Perfusion mit der Rettung des Penumbra-Gewebes (Penumbra = Halbschatten: Differenzareal zwischen bereits nekrotischem und umgebendem noch vitalem Hirngewebe)5
- Die Ausdehnung der Penumbra kann näherungsweise mit CT- oder MRT-Verfahren abgeschätzt werden („Mismatch“ zwischen diffusions- und perfusionsgestörtem Areal).5
Rekanalisation – Thrombolyse
- Die systemische Thrombolysetherapie ist die Standardtherapie beim ischämischen Schlaganfall im Zeitfenster bis 4,5 h.17
- Gelingt der Therapiebeginn innerhalb von 3 Stunden, so erhöht sich die Wahrscheinlichkeit eines guten Ergebnisses weiter.5
- Mit zunehmendem Zeitfenster sinkt der Nutzen im Vergleich zum Blutungrisiko.5
- Blutungsrisiko unter Thrombolyse 3–7 % im Vergleich zu sonst 0,5–2 %
- Dennoch kann eine Thrombolyse auch verzögert sinnvoll sein, wenn die Bildgebung eine relevante Penumbra zeigt.11,17
- im Zeitfenster 4,5–9 h
- bei unbekanntem Symptombeginn („Wake-up“-Schlaganfall)
- Abhängigkeit der Thrombolyseindikation vom klinischen Schweregrad17
- Eine Thrombolyse soll bei behindernden Schlaganfallsymptomen durchgeführt werden.
- Bei milden, nicht behindernden Symptomen kann auf die Thrombolyse verzichtet werden.
Rekanalisation – endovaskuläre Therapie
- Die endovaskuläre Schlaganfalltherapie durch mechanische Thrombektomie ist lange bekannt, war zwischenzeitlich in den Hintergrund getreten, ist aufgrund günstiger Studienergebnisse aber mittlerweile fester Bestandteil der Behandlung.17,25-28
- Die Thrombektomie wird zusätzlich zur vorher begonnen systemischen Thrombolyse durchgeführt.
- Insbesondere Verschlüsse der großen Gefäße (distale Arteria carotis und Hauptstamm der A. cerebri media) durch große embolisch bedingte Thromben sprechen teilweise ungenügend auf die systemische Thrombolyse an.5
- Diese Thromben werden kathetergestützt (Stent-Retriever) durchdrungen und mit einem Stent-Gitter eingefangen.5
Leitlinie: Rekanalisation bei ischämischem Schlaganfall17
Systemische Thrombolyse, Standardtherapie
- Patient*innen mit ischämischem Schlaganfall, die innerhalb von 4,5 h nach Symptombeginn bzw. dem Zeitpunkt, an dem sie zuletzt gesund gesehen wurden, behandelt werden können und keine Kontraindikationen aufweisen, sollen mit einer systemischen Thrombolyse mit Alteplase behandelt werden.
- Die systemische Thrombolyse im 4,5-h-Zeitfenster erwachsener Patient*innen soll unabhängig vom Alter erfolgen.
Systemische Thrombolyse im erweiterten oder unklaren Zeitfenster
- Bei Patient*innen mit ischämischem Schlaganfall im unklaren Zeitfenster oder nach dem Erwachen, die mehr als 4,5 h zuvor zuletzt gesund gesehen wurden, sich aber innerhalb von 4,5 h nach Erkennen der Symptome in der Klinik vorstellen und bei denen ein DWI/FLAIRMismatch (Diffusion Weighted Imaging: DWI; Fluid-Attenuated Inversion-Recovery-Bildgebung: FLAIR, bei Mismatch liegt Ereignis maximal 4–5 Stunden zurück, Anm. der Redaktion) in der MRT vorliegt, soll eine i. v. Thrombolyse mit Alteplase erfolgen.
- Bei Patient*innen mit ischämischem Schlaganfall im 4,5- bis 9-h-Zeitfenster (bekannter Beginn oder ab der Mitte des Schlafs bei unbekannter Symptomdauer) und einem Mismatch zwischen im CT oder MRT dargestelltem Infarktkern und Penumbra sollte eine i. v. Thrombolyse mit Alteplase erfolgen.
Endovaskuläre Therapie
- Bei Patient*innen mit ischämischem Schlaganfall, klinisch relevantem neurologischem Defizit und Verschluss einer großen Arterie im vorderen Kreislauf soll, wenn innerhalb von 6 h möglich, eine mechanische Thrombektomie erfolgen, um das funktionelle Ergebnis zu verbessern.
- Jenseits des 6-h-Zeitfensters soll eine mechanische Thrombektomie relevanter Verschlüsse im vorderen Kreislauf erfolgen, wenn durch erweiterte Bildgebung (z. B. Darstellung eines kleinen Infarktkerns, Mismatch) im Kontext der klinischen Symptomatik zu vermuten ist, dass rettbares Risikogewebe vorliegt.
- Patient*innen, die für eine
effektiveendovaskuläreAkutbehandlungSchlaganfalltherapie in Betracht kommen und die keine Kontraindikation für eine systemische Thrombolyse haben, sollen so früh wie möglich auch mit Alteplase behandelt werden, wobei keine der beiden Behandlungen die andere verzögern darf.
Akuttherapie des hämorrhagischen Schlaganfalls
Intrakranielle Blutung
- Grundsätzlich senkt eine Blutdrucksenkung auf Werte um 140 mmHg und noch tiefer die Ausdehnung der Blutung und die Häufigkeit von Nachblutungen.
285- Da präklinisch Ischämie vs. Blutung nicht differenziert werden kann, sind Werte um 160 mmHg tolerierbar.
- Je nach Verlauf werden im Rahmen der stationären Behandlung erforderlich:5
- Anlage einer externen Liquordrainage
- mikrochirurgische Hämatomausräumung
- neuroprotektive und hirndrucksenkende Intensivtherapie.
Subarachnoidalblutung (SAB)
- SAB sind in 85 % der Fälle durch Ruptur eines Aneurysmas ausgelöst, Ausschaltung erfolgt katheterinterventionell (Coiling) oder operativ (Clipping).5
SchlaganfallstationWeitere Maßnahmen im Rahmen der intensivmedizinischen Behandlung sind Therapien gegen Vasospasmen und/oder Hirndruck, Anlage einer Liquordrainage.5
Weitere Maßnahmen in der Akutphase
Physiotherapie
DieBeiAkutbehandlungallenaufSchlaganfallpatient*innen sollte innerhalb von 48 h nach Schlaganfallbeginn mit der Mobilisierung („Out-of-Bed“-Aktivität) begonnen werden.17- Dauer von 30–60 min pro Tag, durchgeführt an 5–7 Tagen pro Woche29
Ergotherapie
- Durch frühzeitige, gezielte Ergotherapie sollten z. B. Defizite u. a. der oberen Extremität inkl. Feinmotorikstörungen der Hand baldmöglichst verbessert werden.17
Logopädie
- Frühzeitige logopädische Evaluation zur Detektion und Behandlung einer
SchlaganfallstationDysphagie(StrokewirdUnit)empfohlen.17 - Zur Verbesserung einer Aphasie oder Dysarthie gibt es keine Evidenz.17
Sekundärprävention
Antithrombotische Therapie
Thrombozytenaggregationshemmer
- Mit der Thrombozytenfunktionshemmung wird die frühe Sekundärprävention bereits in der Akutphase eingeleitet.11
- Basis ist die
wichtigsteMonotherapieMaßnahmemit ASS 100 mg/d oder Clopidogrel 75 mg/d.1- Clopidogrel als Monotherapie ist in Deutschland nur in Ausnahmefällen verordnungsfähig und deutlich teurer,
umdaherdenistVerlaufineinesderakutenRegelSchlaganfallsASS zubeeinflussenbevorzugen.1
- Clopidogrel als Monotherapie ist in Deutschland nur in Ausnahmefällen verordnungsfähig und deutlich teurer,
- Bis
Metaanalysenzuzeigen3 Wochen nach einem ischämischen Schlaganfall soll eine doppelte Plättchenhemmung (IaDAPT):mit ASS und Clopidogrel angeboten werden.2830-31- Die
Sterblichkeit3-wöchigeverringertDAPTsichistumals14erweiterte%Akutbehandlungnachzu verstehen, für eine generelle Empfehlung einer dualen Plättchenhemmung gibt es Hinweise darauf, dass der Schaden durch Blutungen den Benefit deutlich überschreitet.1Jahr Verlaufsbeobachtung.
- Die
SterblichkeitDen Hausärzt*innen kommt eine wichtige Rolle zu bei der Beendigung der dualen undPflegebedÜberleitung zu einer Monotherapie.1- Auch bei wiederholtem Schlaganfall unter Behandlung gibt es keine allgemeine Empfehlung zur Erweiterung oder Umstellung der antithrombotischen Therapie.1,29
- Eine Beurteilung der Wirksamkeit der Thrombozytenaggregationshemmer durch Thrombozytenfunktionstest wird nicht empfohlen.29
- Ein großzü
rftigkeitgigerverringernbegleitendersichEinsatzumvon18PPI%bei Patient*innen ohne gastrointestinale Probleme sollte vermieden werden.29- Um mögliche unerwünschte Wirkungen durch einen Dauereinsatz von PPI zu vermeiden, kann stattdessen der H2-Antagonist Famotidin eingesetzt werden.
DerBeiBehandlungseffektKomedikationwirdmitdurchNSAR sollte dieKombinationreduzierte Wirksamkeit vonakuterASSmedizinischerberücksichtigtBehandlung,werden:rascherzeitlichMobilisierungversetzteundGabeRehabilitationdererreichtNSAR (i. d. R. mindestens 30 min) nach Einnahme des ASS empfohlen.29StudienZeitpunktzeigendesaußerdemBeginns der Thrombozytenaggregationshemmung- Beginn erst nach sicherem Ausschluss einer intrakraniellen Blutung29
- Im Übrigen frühestmöglicher Zeitpunkt nach ischämischem Schlaganfall oder TIA,
dassauch wenn diebesserenSchlaganfallursachenabklärungErgebnissenochdernichtPatient*innenabgeschlossenauch nach 10 Jahren Verlaufsbeobachtung bestehen bleiben (Ib)ist.29
Überwachung in der Akutphase (Klinik)AntikoagulationDieBeimMaßnahmen,kardioembolischendieSchlaganfallinsollte statt derKlinikThrombozytenaggregationshemmunggetroffeneinewerden,oralekönnenAntikoagulationsich je nachmit denGegebenheitenPatient*innenunterscheiden und obliegen nicht dem hausärztlichen Management.Mindestens in den ersten 12–24 Stunden nach der Einweisung sollte eine nichtinvasive Beobachtung des Herzrhythmus, Messungen von Blutdruck, Sauerstoffgehalt, Temperatur und Atmung durchgeführtbesprochen werden.30-31Diese Überwachung sollte auf der Stroke Unit geschehen.
Akute Mobilisierung/RehabilitationFrühe Mobilisierung und früher Beginn eines planmäßigen Trainings gehören zu den wichtigsten Maßnahmen, um gute Behandlungsergebnisse nach einem Schlaganfall zu erreichen.3211FunktionsniveauVerhinderungverbessernvonund2/3Komplikationenderverringern.Rezidive
SieheDie DEGAM sieht keine ausreichende Evidenz, um NOAK gegenüber Vitamin-K-Antagonisten (VKA) zu bevorzugen, die DGN präferiert im Allgemeinen NOAK.1- Zu Details der Differenzialtherapie mit VKA bzw. NOAK siehe Artikel
Rehabilitation nach einem SchlaganfallAntikoagulation.
- Zu Details der Differenzialtherapie mit VKA bzw. NOAK siehe Artikel
HirninfarktLeitlinie:
medikamentöseAntithrombotischeBehandlungSekundärprävention1,17,29-30ThrombolyseThrombozytenaggregationshemmung, Monotherapie (Standard)I. v. Thrombolyse mit r-tPA (Alteplase) ist eine wirkungsvolle Behandlung, die bei ausgewählten Schlaganfall-Patient*innen möglichst innerhalb von 3 Stunden nach dem Infarkt durchgeführt und immer so früh wie möglich begonnen werden sollte.Es besteht eine dokumentierte Wirkung für bis zu 4,5 Stunden.33Alteplase wird innerhalb dieses Zeitraums routinemäßig durchgeführt.Ein Cochrane-Review (2014) stellt eine positive Wirkung der Thrombolyse auch noch innerhalb von 6 Stunden fest, mit den besten Ergebnissen bei einer Behandlung in den ersten 3 Stunden.34I. a. Thrombolyse oder i. a. Embolektomie kann bei ausgewähltenDen Patient*innenmitsollKontraindikationenASSgegen100einemg/di.(nurv.beiThrombolyseechteroderUnverträglichkeitproximalenClopidogrel 75Okklusionenmg/d)erwogenangeboten werden.,GenaueEntscheidungEmpfehlungenüberkönnendieerstMedikation nachweitererindividuellenForschungklinischengegeben werden.Die Thrombolyse hat zahlreiche KontraindikationenUmständen undlimitierendeindividuellerFaktoren, vglVerträglichkeit.den ArtikelThrombolyse bei Herzinfarkt.Eine Metaanalyse mit Daten aus 12 Studien mit 7.020 Schlaganfall-Patient*innen zeigte, dass eine Thrombolyse das funktionelle Ergebnis der Betroffenen (Freiheit von Behinderung) um 4,2 % verbesserte, die Zahl an Hirnblutungen stieg allerdings um 5,8 % an – die Gesamtsterblichkeit unterschied sich nicht.35-36
ThrombektomieBei einem ischämischen SchlaganfallThrombozytenaggregationshemmung,derdualedurch eine Okklusion in einer proximalen Arterie im vorderen Kreislauf verursacht wurde, zeigen Studien, dass eine intraarterielle Thrombektomie (innerhalb von 6 Stunden nach dem Auftreten der ersten Symptome)zusPlätzlichzur üblichen Behandlung (Lyse) zu besseren Ergebnissen führt als die übliche Behandlung (Ib).37-43ForschungsergebnisseDas Ergebnis nach 90 Tagen war in der Thrombektomie-Gruppe besser. Hier waren 44,6 % funktionell unabhängig gegenüber 31,8 % in der Gruppe, die nicht interventionell behandelt wurde.41Laut einer Metaanalyse liegt NNT bei 2,6 (Number Needed to Treat), um ein besseres Funktionsniveau nach 90 Tagen zu erreichen.In einer Studie (2018) wurden gute Behandlungsergebnisse durch Thrombektomie auch im erweiterten Zeitraum von 6-16 Stunden nach Symptombeginn bei sorgfältig ausgewählten Patient*innen erreicht.44
ThrombozytenaggregationshemmerttchenhemmungLeitlinie: Neue Thrombozyten-Aggregationshemmer, Einsatz in der Hausarztpraxis45Die Thrombozytenaggregationshemmung mit ASS ist Standard bei stattgehabtem ischämischem Insult (wenn eine Blutung ausgeschlossen wurde, Beginn sobald wie möglich).
- Patient*innen
mit akutem Hirninfarkt (CT hat Blutung ausgeschlossen) sollten mit täglich 100 mg Acetylsalicylsäure (ASS) behandelt werden. Die Behandlung sollte so früh wie möglich beginnen, innerhalb von 48 Stunden.ASS kann oral, rektal oder über eine transnasale Magensonde verabreicht werden.
Patient*innen mit Hirninfarkt während der laufenden Behandlung mit ASS sollten zusätzlich eine extra Aufsättigungsdosis erhalten (z. B. ASS 250–300 mg).Patient*innen mit akutem Insult undVorhofflimmernsollten initial mit ASS behandelt werden und später – nach gemeinsamer Entscheidungsfindung mit den Betroffenen und Informationen über die Vor- und Nachteile der Behandlung – in eineAntikoagulationsbehandlungüberführt werden.Eine Behandlung mit ASS wird nicht in den ersten 24 Stunden nach einer thrombolytischen Behandlung empfohlen.
Leitlinie: Neue Thrombozyten-Aggregationshemmer, Einsatz in der Hausarztpraxis45Verordnungsfähigkeit zu Lasten der gesetzlichen Krankenversicherung (GKV)Clopidogrel-Monotherapiezur Prävention atherosklerotischer Ereignisse bei Patient*innen mitHerzinfarkt, ischämischem Schlaganfall oder nachgewiesenerPAVKBei ASS-Unverträglichkeit, soweit wirtschaftliche Alternativen nicht eingesetzt werden können.bei PAVK-bedingter Amputation oder Gefäßintervention oder bei diagnostisch eindeutig gesicherter typischer Claudicatio intermittens mit Schmerzrückbildung in < 10 Minuten in Ruhe
Clopidogrel in Kombination mit täglich 75–325 mg ASSbei ischämischem Schlaganfall keine Zulassung für die Kombination von Clopidogrel und ASS und damit keine Verordnungsfähigkeit
Ticagrelor und Prasugrelbei ischämischem Schlaganfall nicht zugelassen und nicht verordnungsfähig
Mehrere Studien und eine entsprechende Metaanalyse untersuchten die Kombination von ASS und Clopidogrel in den ersten Wochen nach Schlaganfall oder TIA46Cave: off label!Ein Benefit ist in den ersten 1–3 Wochen zu vermuten – eine doppelte Plättchenhemmung sollte für diese Zeit im Sinn einer verlängerten Akutbehandlung angeboten werden.45Bei einer längeren doppelten Plättchenhemmung im Sinn einer Sekundärprävention ist das Nutzen-Schaden-Verhältnis ungünstig.
Nur bei echter ASS-Intoleranz sollte Clopidogrel als langfristiger Ersatz für ASS erwogen werden.
Antikoagulation in der AkutphaseEineAntikoagulationsbehandlungin therapeutischen Dosen wird bei einem akuten Hirninfarkt initial nicht empfohlen.Dies gilt für alle Typen von Antikoagulanzien.
Patient*innen mit einem akuten Hirninfarkt undVorhofflimmernsollten akut mit ASS behandelt werden.Eine Antikoagulationsbehandlung beginnt später.ASS wird bis zu einer stabilenINRgegeben.
Bei Patient*innen, die unter einer Antikoagulation einen Hirninfarkt erleiden und das therapeutische INR-Niveau noch nicht erreicht haben, kann eine zusätzliche Behandlung mit ASS 75 mg täglich erwogen werden.
Prophylaxe gegen venöse ThromboseEine gute medizinische Behandlung und eine frühe Mobilisierung sind wichtig, um thromboembolischen Komplikationen vorzubeugen.Bei hohem Risiko für Thromboembolien wird ASS zusammen mit niedrigdosiertem, niedermolekulärem Heparin gegeben.Bei Patient*innen mit Hirnblutung und entsprechenderPareseoder Mobilisierungsproblemen werden initial Kompressionsstrümpfe empfohlen. Niedermolekuläres Heparin sollte frühestens eine Woche nach dem Auftreten der Hirnblutung gegeben werden.
Statinbehandlung?Eine Behandlung mit Statin (vor dem Schlaganfall begonnen) kannnach einem ischämischen Schlaganfalldie Prognose verbessern (II).47-50Allerdings ist die NNT mit mindestens 53/5 Jahren hoch. Daraus leitet sich ab, dass in der Hausarztpraxis nicht automatisch die Klinikempfehlung für ein Statin übernommen werden muss. Vielmehr sollten die absolute Risikoreduktion und die NNT erklärt werden und gemeinsam eine Entscheidung für oder gegen eine Statin-Behandlung getroffen werden. Siehe ArtikelHyperlipidämieund die DEGAM-LeitlinieHausärztliche Risikoberatung zur kardiovaskulären Prävention.
Neuropathische SchmerzenEinige Schlaganfall-Patient*innen können neuropathische Schmerzen bekommen.Indizierte Medikamente können Antidepressiva und Antiepileptika sein.z. B. Amitriptylinz. B. Gabapentin
SchulterschmerzenAlle Personen, die Patient*innen mit Armparese pflegen/unterstützen/trainieren, sollten wissen, wie sie mit dem Arm umgehen müssen, um Verletzungen der Schultergelenke zu vermeiden.Ziehen und Drehen des Armes sollten vermieden werden. Passive Bewegungen sollten mit Vorsicht ausgeführt werden; eine Abduktion von über 90 Grad im Schultergelenk sollte vermieden werden.Funktionelle elektrische Stimulierung, Verband und/oder Schlinge können bei einem Risiko für Subluxation oder bei auftretenden Schulterschmerzen erwogen werden.Medikamentöse BehandlungParacetamol bei Bedarf, gegen SchmerzenAntiphlogistika, evtl. Steroide können zusätzlich zu Paracetamol indiziert sein.Bei älteren Patient*innen und bei Ulkusanamnese sollten bei Behandlung mit Antiphlogistika PPI zur Ulkusprophylaxe eingesetzt werden.
Botulinumtoxin A kann bei einer spastischen, schmerzenden Schulter indiziert sein.
Hirnblutung: AkutbehandlungSubarachnoidalblutungEine Subarachnoidalblutung (SAB) wird in über 85 % der Fälle auf eine spontane Blutung im Subarachnoidalraum durch ein rupturiertes, angeborenesAneurysmain der Gehirnbasis zurückgeführt.SAB hat eine höhere Akutsterblichkeit als andere Formen des Schlaganfalls, 25–35 % sterben vor der Hospitalisierung.SAB wird mit körperlicher Schonung und Bettruhe behandelt sowie evtl. mit einem frühen operativen Eingriff oder Coiling, um Rezidivblutungen vorzubeugen.Patient*innen mit SAB sollten deshalb immer in Zusammenarbeit mit der Neurochirurgie behandelt werden.Die Behandlung auf der Schlaganfallstation (Stroke Unit) ist für diese Patient*innen nicht evaluiert.
Intrazerebrale BlutungEine intrazerebrale Blutung kann auf angeborene und erworbene Verletzungen in kleinen intrazerebralen Arterien zurückgeführt werden.RisikofaktorenBluthochdruckist der wichtigste Risikofaktor.Medikamente, die die Gerinnung beeinflussen (Antikoagulationsbehandlung, thrombolytische Behandlung oder plättchenhemmende Behandlung),Alkoholkonsum, Drogenmissbrauch und Vaskulitiden sind andere Faktoren, die mit einem erhöhten Risiko für Hirnblutungen in Verbindung stehen. In geringem Umfang erhöhen Statine das Risiko für Hirnblutungen. Ihre Indikation sollte sorgfältig geprüft werden.
BehandlungDie Behandlung soll den erhöhten intrakraniellen Druck verringern, evtl. mit operativer Ausräumung des Hämatoms, inklusive der Einleitung medikamentöser Maßnahmen zum Stoppen der Blutung.
OperationIn der Regel ist keine akute/frühe Operation indiziert.Bei Patient*innen mit Blutung im Kleinhirn und bei Patient*innen mit progredienter Bewusstseinseintrübung besteht Konsens, dass eine Operation zur Evakuierung des Hämatoms sinnvoll sein kann (Absprache mit Neurochirurgen).
Hirnblutung unterAntikoagulationEine Hirnblutung unter Behandlung mit Phenprocoumon oder bei anderen Ursachen eines erhöhten INR-Werts sollte mit Prothrombinkomplex-Konzentrat oder, falls ein solches Konzentrat nicht zur Verfügung steht, mit Frischplasma behandelt werden bisINR< 1,5 (evtl. bis zu 2,0 bei mechanischer Herzklappe).
Frühe RehabilitationZahlreiche Studien dokumentieren die Wirkung von frühzeitiger Rehabilitation bei einem ischämischen Schlaganfall. Eine Studie zeigt auch eine positive Wirkung bei Patient*innen mit Hirnblutung.51
Die Behandlung auf der Schlaganfallstation wirkt sich für Patient*innen mit intrazerebraler Blutung mit Hirninfarkt gleichermaßen günstig aus.In der Sekundärprophylaxe ist vor allem eine intensive Kontrolle des Blutdrucks wichtig.
RehabilitationLeitlinie: Schlaganfall2Rehabilitation in der hausärztlichen VersorgungIn die Therapieplanung und -durchführung sollten verschiedene Berufsgruppen einbezogen werden.Künstlerische Therapien (Musiktherapie etc.) können bei Stimmungsstörungen/Depression, Aphasie, kognitiven (Aufmerksamkeit, Neglect) und sensomotorischen Störungen ergänzend zu anderen Therapieformen empfohlen werden.
Therapieplanung, Zielsetzung und Verlauf der Rehabilitation nach SchlaganfallEntscheidungen über die Indikation und die Dauer der Therapie sollten sich danach richten, ob dadurch realistische und patientenrelevante Funktions-, Aktivitäts- und Teilhabeziele erreicht werden können.Patient*innen sollten unterstützt werden, ihre persönlichen Therapieziele zu definieren.Rehabilitationsziele sollten gemeinsam von den Patient*innen und Therapeut*innen genau, d. h. evaluierbar, zeitlich bestimmt und schriftlich festgelegt werden.Zudem sollten die Ziele regelmäßig überprüft und bei Bedarf angepasst werden.
Empfehlungen zur Therapie nach SchlaganfallBewegungsapparatSchlaganfall-Patient*innen mitParesensollen spezifische Maßnahmen zur Verbesserung der Muskelkraft sowie der Bein- und Armaktivität angeboten werden.Schlaganfall-Patient*innen mit Paresen sollten zusätzlich elektrische Muskelstimulationsverfahren zur Behandlung angeboten werden.
Hand- und Handgelenksorthesen sollen bei Patient*innen mit einer Armparese nicht routinemäßig eingesetzt werden, da sie keine Wirkung auf Schmerz, Funktion oder Bewegungsausmaß haben.Schlaganfall-Patient*innen mit Geh- und Gangstörungen soll Gehtraining angeboten werden.Patient*innen mit einer orofazialen Beeinträchtigungen sollten Maßnahmen zur Verbesserung der motorischen Funktion der mimischen Muskulatur angeboten werden.Im Rahmen der Ergotherapie kann Schlaganfall-Patient*innen mit einer Apraxie nach individuellem Bedarf alltagsorientierte Therapie (unter Einsatz von Kompensationsstrategien oder fehlerfreiem Lernen) angeboten werden.Physiotherapie sollte bei allen Formen der Spastik angeboten werden.Krafttraining sollte bei Spastik nach Schlaganfall angeboten werden.Schlaganfall-Patient*innen mit einem gesteigerten Dehnungswiderstand in der Muskulatur sollten Maßnahmen zur Förderung der motorischen Funktion, zur Kräftigung und Tonusregulation angeboten werden.Die elektrische Stimulationstherapie der paretischen Muskulatur bei spastischer Fehlhaltung kann nach Schlaganfall eingesetzt werden.
Die lokale intramuskuläre Injektion von Botulinumtoxin (BoNT) soll bei der fokalen Spastik der oberen (A) und sollte bei der fokalen Spastik der unteren Extremität (B) angeboten werden.Bei der multisegmentalen oder generalisierten Spastik sollten orale antispastische Medikamente wie Baclofen, Tizanidin, Dantrolen oder Diazepam angeboten werden unter Berücksichtigung der Nebenwirkungen.Bei der multifokalen Spastik kann ergänzend intrathekales Baclofen erwogen werden.
Schlaganfall-Patient*innen mit Störungen der posturalen Kontrolle oder des Gleichgewichts sollen Maßnahmen zur Verbesserung des Gleichgewichts, der Ausdauer und der Muskelkraft angeboten werden.Eine Einschätzung desSturzrisikoseinschließlich der Sturzangst soll durchgeführt und dokumentiert werden.
Herz-Kreislauf-ProblemeBeiSchwindelals einzigem Symptom einer akuten zerebrovaskulären Ischämie soll eine differenzialdiagnostische Abgrenzung zu malignen Herzrhythmusstörungen, einerAortenstenoseoder einer obstruktivenKardiomyopathieerfolgen.Bei Schwindel sollen abwendbar gefährliche Verläufe abgeklärt werden, wenn er auftritt in Verbindung mit:neurologischen StörungenSehstörungenSynkopenventrikulären und bradykarden Rhythmusstörungen mit Bedrohungspotenzial.
Sprech- und SprachstörungenBei einerAphasiesoll eine hochfrequente Sprachtherapie angeboten werden unabhängig von der Erkrankungsdauer und von der Schwere der sprachlichen Ausfälle.Patient*innen mit einerDysarthriesollte eine sprachtherapeutische Diagnostik und Therapie angeboten werden.Das Sprechen soll bei Bedarf durch den Einsatz von elektronischen und nicht elektronischen Hilfsmitteln unterstützt werden.
Neurologische StörungenSpezifisches übendes Training zur Verbesserung der Raumkognition unter Einbezug von Alltagsanforderungen kann empfohlen werden.Schlaganfall-Patient*innen soll eine den kognitiven Fähigkeiten angepasste, zumindest orientierende Visusprüfung und Gesichtsfelduntersuchung durch die Hausärztin/den Hausarzt angeboten werden.Ein Neglect tritt in verschiedenen Modalitäten auf. Daher soll die Exploration der vernachlässigten Raumhälfte in allen therapeutischen Disziplinen gefördert werden.Patient*innen sollten Maßnahmen zur Verbesserung der Sensibilität angeboten werden (z. B. sensorische Stimulation, sensomotorisches Training, Bobath-Therapie, Spiegeltherapie, thermale Stimulation).
SchmerzenSchlaganfall-Patient*innen, die unter Schmerzen leiden, sollen physiotherapeutische Maßnahmen zur Schmerzreduktion angeboten werden.Bei Patient*innen mit leichter bis mäßiger Schwäche eines Armes oder einer Hand, komplexem regionalem Schmerzsyndrom und/oder Vernachlässigung einer Körperseite kann die Spiegeltherapie als Ergänzung zur Routinebehandlungzur Verbesserung der Armfunktion nach einem Schlaganfall eingesetzt werden.Schlaganfall-Patient*innen mitneuropathischem Schmerzsollte initial Amtriptylin, Duloxetin, Gabapentin oder Pregabalin angeboten werden.Kann mit der Basistherapie keine ausreichenden Schmerzreduktion erzielt werden, sollte auf ein anderes Schmerzmedikament der Basisempfehlung zurückgegriffen werden.Um eine Schmerzreduktion zu erzielen, sollten die sollten Patient*innen zu Bewegung, Haltungsveränderungen und optimierten Bewegungs- und Lagerungspositionen angeleitet werden.Bei ausbleibender Wirkung können weitere Schmerzmedikamente wie Opioide in Erwägung gezogen werden.
BeiSchulterschmerzennach Schlaganfall oder regionalen Schmerzsyndromen kann eine Behandlung mit Schienen oder Orthesen erwogen werden.Bei Schulterschmerzen nach Schlaganfall oder regionalen Schmerzsyndromen sollte eine Tape-Behandlung angeboten werden.Bei Schulterschmerzen nach Schlaganfall oder regionalen Schmerzsyndromen soll eine Lagerungsbehandlung des gelähmten Armes angeboten werden.Bei Schulterschmerzen nach Schlaganfall oder regionalen Schmerzsyndromen soll eine elektrische Stimulationsbehandlung des M. deltoideus und der Schulter umgebenden Muskulatur angeboten werden.Bei Schulterschmerzen nach Schlaganfall oder regionalen Schmerzsyndromen können folgende Therapieoptionen angeboten werden:die Injektion von Botulinumtoxin in die Mm. subscapularis und/oder pectoralis maiorsubacromiale Infiltration mit einem Lokalanästhetikumorale NSAR-Therapieorale Kortikoidtherapie.
In der Schlaganfall-Rehabilitation sollten zentrale Schmerzstörungen (CPSP) anamnestisch explizit erfragt werden.Ein medikamentöser Therapieversuch kann mit Amitriptylin und Lamotrigin erfolgen.Pregabalin, Gabapentin, Carbamazepin oder Phenytoin können als Therapeutika der 2. Wahl berücksichtigt werden.
Kognitive BeeinträchtigungenDie differenzialdiagnostische Untersuchung kognitiver Störungen sollte möglichst durch Neuropsycholog*innen erfolgen.Zur Behandlung von Aufmerksamkeitsstörungen sollte ein übendes Funktionstraining auf Basis einer neuropsychologischen Diagnostik störungsspezifisch angeboten werden.Zur Entwicklung von Kompensationsstrategien und um den Transfer in den Alltag zu fördern, sollten die übenden, die Restitution anregenden Verfahren durch andere neuropsychologische Maßnahmen (wie z. B. kognitiv-verhaltenstherapeutische Methoden) ergänzt werden.
Zur Behandlung von Gedächtnisstörungen bei leicht bis mittelschwer betroffenen Schlaganfall-Patient*innen soll übendes Funktionstraining auf Basis einer differenzierten neuropsychologischen Diagnostik störungsspezifisch angeboten werden.Bei Schlaganfall-Patient*innen mit schweren Gedächtnisstörungen, insbesondere bei Patient*innen mit kognitiven Störungen vom Schweregrad einerDemenz, sollte eine kognitive Aktivierung über multisensorische Stimulation oder körperliches Training angeboten werden. Hierauf sollten pflegerische und therapeutische Maßnahmen abgestimmt sein.Für Patient*innen, bei denen Verhaltensauffälligkeiten im Vordergrund stehen, sollten Verhaltensmanagementansätze angeboten werden, insbesondere die Methode des Zielmanagements.
Anst/Depression/affektive StörungenSchlaganfall-Patient*innen mit Hinweisen aufAngstoderDepressionsollte ein strukturiertes Assessment angeboten werden.Schlaganfall-Patient*innen mit emotionalen Beschwerden (Angst, Depression) können von einer Behandlung mit Antidepressiva profitieren.Nach einem Schlaganfall sollen Antidepressiva zur Verhinderung einer Depression präventiv nicht routinemäßig angeboten werden.Schlaganfall-Patient*innen mit Depression kann eine Psychotherapie, vor allem eine kognitive Verhaltenstherapie, angeboten werden.Schlaganfall-Patient*innen mit affektiven Störungen sollte eine Kombination von nicht-pharmakologischer und pharmakologischer Behandlung angeboten werden.Mit Schlaganfall-Patient*innen mit emotionaler Labilität (PSEI) und Affektstörungen sollte eine Therapieoption mit SSRI besprochen werden.Mit Schlaganfall-Patient*innen mitAngststörungensollte über die Möglichkeit einer Psychotherapie gesprochen werden.
SchluckbeschwerdenBei Patient*innen mitSchluckbeschwerdenund/oder pathologischem Screeningbefund sollte ein weiterführendes Assessment der Schluckfunktion angeboten werden.Patient*innen mit einer Dysphagie soll eine oropharyngeale Schluckrehabilitation angeboten werden, die sich aus restituierenden, kompensatorischen und/oder adaptiven Maßnahmen zusammensetzt.Ist parenterale Ernährung voraussichtlich länger erforderlich (> 28 Tage), soll, bei nicht-palliativer Intention, nach 14–28 Tagen die Anlage einer PEG-Sonde angeboten werden.
Harn- und Stuhlinkontinenz/SexualitätAlle Schlaganfall-Patient*innen sollten bezüglichHarn-undStuhlinkontinenzexploriert werden.Patient*innen mit Inkontinenzbeschwerden sollte ein strukturiertes Inkontinenzassesment (z. B. ICIQ) angeboten werden sowie eine Ultraschalluntersuchung der Harnwege mit Restharnbestimmung.Bei Harninkontinenz sollte eine Urinuntersuchung mittels Teststreifen angeboten werden.Zur Reduktion der Inkontinenzepisoden sollte körperliches Training und ggf. eine Gewichtsreduktion empfohlen werden.Patient*innen mitDranginkontinenzsoll ein Blasen- und Beckenbodentraining angeboten werden.Schlaganfall-Patient*innen mit Dranginkontinenz kann nach Ausschluss eines relevanten Restharns eine anticholinerge Therapie angeboten werden.Patient*innen mit Belastungs- und/oder gemischter Inkontinenz sollte Beckenbodentraining empfohlen werden.Zur Reduktion von Inkontinenzepisoden bei mittelschwerer Belastungsinkontinenz kann Duloxetin angeboten werden.Patientinnen mitBelastungsinkontinenzsollte eine Pessartherapie als Option angeboten werden.
Schlaganfall-Patient*innen mitObstipationsneigungkann eine Beratung bezüglich der Flüssigkeitszufuhr, eine Ernährungsberatung und eine Empfehlung zumkörperlichen Trainingangeboten werden.Die medikamentöse Therapie derStuhlinkontinenzkann mit Loperamid (und bei Unverträglichkeit mit Kodeinphosphat) durchgeführt werden.Störungen der sexuellen Funktionsfähigkeit sollten exploriert werden.
Alltagstraining/Kraftfahreignung/UnterstützungIm häuslichen Umfeld lebenden Schlaganfall-Patient*innen mit Einschränkungen der persönlichen und instrumentellen Aktivitäten des täglichen Lebens soll ergotherapeutisches Alltagstraining angeboten werden.Für die Beurteilung der emotionalen Kontrollfähigkeit, Einsichtsfähigkeit und krankheitsbedingter Persönlichkeitsveränderungen, die ggf. dieKraftfahreignunggefährden können, sollte eine Fahrverhaltensprobe mit einem Neuropsychologen angeboten werden.Einschränkungen oder Verluste von Extremitätenfunktionen in Folge einer Störung des zentralen oder peripheren Nervensystems erfordern eine neurologische/verkehrsmedizinische Begutachtung.Bei Einschränkungen der visuellen Wahrnehmung soll überprüft werden, ob die gesetzlichen Mindestanforderungen erfüllt sind.
Angehörige von Betroffenen sollen in allen Phasen des Genesungsprozesses individuell erforderliche Informationen und Unterstützung erhalten.Schlaganfall-Patient*innen und deren Angehörige sollen überfinanzielle Hilfen und sozialstaatliche Leistungen, psychosoziale und sozialrechtliche Beratungsangebote und Selbsthilfegruppeninformiert werden.
Vergleiche den ArtikelRehabilitation nach einem Schlaganfallund folgende Patienteninformationen:Schlaganfall, TherapieplanSchlaganfall, NotfalltherapieSchlaganfall, RehabilitationSchlaganfall, Risikofaktoren und VorbeugungAcetylsalicylsäure bei Herz-Kreislauf-ErkrankungenSchlaganfall, Maßnahmen in der RehabilitationSchlaganfalltherapie ‒ Was können Patienten und Angehörige tun?Schlaganfall, Vorbereitung auf die Krankenhausentlassung
ErgotherapieEine ergotherapeutische Behandlung kann Menschen, die einen Schlaganfall hatten, helfen, ihre täglichen Aufgaben wieder auszuführen und ggf. die berufliche Tätigkeit fortzusetzen (Ia).52
Rehabilitation zu HauseBesonders Patient*innen mit leichtem bis mittelgradig schwerem Schlaganfall können von diesem Angebot profitieren (Ia).53Rehabilitation kann als Training zu Hause oder in Tages-Reha-Abteilungen stattfinden oder in Kombination.
PräventionLeitlinie: Schlaganfallprävention bei Patient*innen mit hohem Schlaganfallrisiko und Sekundärprävention2ErnährungPersonen mit einem erhöhten Schlaganfallrisiko sollten beraten werden, ihre Ernährung abwechslungsreich zu gestalten und sie an den Empfehlungen der mediterranen oder nordischen Kost auszurichten. Bei Bedarf sollten Hausärzt*innen die Ernährungsberatung intensivieren und eine Teilnahme an einer strukturierten Schulung empfehlen.Personen mit hohem Schlaganfallrisiko, v. a. Patient*innen mitHypertonie, sollten beraten werden, ihre Salzaufnahme zu reduzieren.Eine Supplementierung mit Vitamin- bzw. Antioxidantien-Präparaten sollte nicht generell empfohlen werden.Vitamin B und Folsäure zur Senkung des Homocysteinspiegels sollen in der kardiovaskulären Prävention bei unselektierten Personen nicht verwendetwerden.
Körperliche AktivitätPersonen mit einem erhöhten Risiko für Schlaganfall sollen beraten werden,wöchentlich mindestens 150 Minuten mäßige oder 75 Minuten intensive körperliche Aktivität oder eine Mischung von mäßiger und intensiver körperlicher Aktivität auszuübenund wöchentlich mindestens 2-mal ein Krafttraining aller großen Muskelgruppen durchzuführen.
Personen, die nicht in der Lage sind, körperlich aktiv zu sein, sollten so intensiv üben wie es individuell sicher möglich ist und versuchen, jeden Tagaktiv zu sein und die im Sitzen verbrachte Zeit zu minimieren.Alle Personen sollten zu regelmäßiger körperlicher Aktivität ermutigt werden. Die Kombination bzw. Auswahl der körperlichen Aktivität sollten sich an den Vorlieben und Fähigkeiten der einzelnen Person orientieren.
Körpergewicht/Adipositas-BeratungHausärzt*innen solltenübergewichtigenund adipösen Personen mit hohem Schlaganfallrisiko ein unterstützendes Gespräch anbieten, um bei einerGewichtsreduktionzu helfen. Die Beratung soll individualisiert, praxisnah und zielorientiert erfolgen und explizit psychosoziale Faktoren einbeziehen.
AlkoholkonsumPersonen mit erhöhtem Schlaganfallrisiko sollte empfohlen werden, den Alkoholkonsum zu beschränken.
RauchenHausärzt*innen sollen Personen mit erhöhtem Schlaganfallrisiko empfehlen, dasRauchen vollständig einzustellen.
HormontherapieFrauen vor der Menopause sollten nach Schlaganfall keine kombinierte orale Kontrazeption erhalten. Zur Verhütung sollten stattdessen Alternativen bedacht werden (wie reine Progesteronpille, nicht-hormonelle Verfahren).Nach einem Schlaganfall sollte eine laufende Hormonersatztherapie beendet werden. Frauen in der Postmenopause, die zur Linderung von Wechseljahresbeschwerden diese beginnen oder fortführen wollen, sollten zum Nutzen-Risiko-Verhältnis beraten werden unter Beachtung ihrer Wünsche und Präferenzen.Eine Hormonersatztherapie zur Prävention von Schlaganfall bei Frauen in der Postmenopause wird nicht empfohlen.
HypertoniePersonen mit Hypertonie mit einem hohen Schlaganfallrisiko oder nach stattgehabtem Schlaganfall soll eine medikamentöse antihypertensive Therapie angeboten werden.Der Blutdruck sollte langfristig unter 140/90 mmHg gesenkt werden. Individuelle Gegebenheiten und Komorbiditäten sollen bei der Entscheidung miteinbezogen werden.
Diabetes mellitusPersonen mit Diabetes mellitus mit einem hohen Schlaganfallrisiko und nach stattgehabtem Schlaganfall sollen entsprechend den Empfehlungen derNVL Diabetesund der DEGAM-LeitlinieHausärztliche Risikoberatung zur kardiovaskulären Präventionberaten werden.
Thrombozytenaggregationshemmung (TAH)Zur Primärprävention zerebrovaskulärer Ereignisse sollte Personen mit einem kardiovaskulären Gesamtrisiko > 20 %/10 Jahre ASS 100 mg/d angeboten werden.Zur Sekundärprophylaxe nach Schlaganfall – wenn keine Indikation zur OAK vorliegt – soll den Patient*innen eine thrombozytenaggregationshemmende Therapie mit ASS 100 mg/d angeboten werden.Für 3 Wochen nach ischämischem Schlaganfall ist die Kombination von ASS mit Clopidogrel zu empfehlen. Eine länger durchgeführte doppelte Plättchenhemmung hat mehr Nebenwirkungen, als sie nützt.Personen mit einem nicht schwerwiegenden Hirninfarkt mit mutmaßlich erhöhtem Rezidivrisiko sollten innerhalb von 12 Stunden mit einer dualen Plättchenhemmung aus Clopidogrel und ASS behandelt werden, wenn keinVorhofflimmernoder eine hochgradige symptomatischeKarotisstenosevorliegen.Patient*innen nach einem nicht-schwerwiegendem Hirninfarkt mit mutmaßlich erhöhtem Rezidivrisikosollte eine duale Plättchenhemmung fürmaximalmax. 30 Tage angeboten werden.- Die DEGAM empfiehlt ASS 100 mg/d + Clopidogrel 75 mg/d
- Eine Kombination von Ticagrelor mit Clopidogrel ist, anders, als die DGN empfiehlt, keine Alternative – Ticagrelor hat keinen Netto-Vorteil vor einer Gabe von ASS allein (Anm. des Reviewers).32-33
- Bei
wiederholtemPatient*innenSchlaganfallmituntererhöhtemlaufender TAHintra- oderOAKextrakraniellenkannBlutungsrisiko sollte keineallgemeinedualeEmpfehlungTherapie zurErweiterungfrühenbzw.Schlaganfall-SekundärpräventionIntensivierung der antithrombotischen Therapie gegeben werden. Grundsätzlich werden in diesem Fall alle Gefäßrisikofaktoren reevaluiert und ggf. behandelterfolgen. LipidmanagementOrale Antikoagulation
Personen mit einem hohen Schlaganfallrisiko sollten zu einem Lebensstil mit günstigen Auswirkungen auf den Lipidstoffwechsel beraten werden.Gerade in der Primärprävention helfen Risikokalkulatoren wieARRIBAbeim hausärztlichen Gespräch über Nutzen und Risiken der medikamentösen Lipidtherapie gegenüber Nichtbehandlung.- Patient*innen
nachübereinem18 Jahre mit ischämischem Schlaganfall oder TIA und permanentem, persistierendem oder paroxysmalem Vorhofflimmern sollzur–SekundärpräventionsoferneinkeineStatinKontraindikation besteht – eine dauerhafte OAK mittels Vitamin-K-Antagonisten (Phenprocoumon) oder mittels der neuen direkten Nicht-Vitamin-K-Antagonisten (NOAK) angeboten werden.DabeisollDiedemonstriert werdenEntscheidung,dasswelchedieSubstanzgruppeRisikosenkunggewählt wird, fällt im gemeinsamen Gespräch zwischen Patient*in und Ärzt*in nach WürrdigungeinenvonnKomorbiditächstent,SchlaganfallKomedikationdurchundeinPatientenpräferenz. - Höheres
Statin geringLebensalter ist– in der SPARCL-Studie mussten 53bei Patient*innen nachSchlaganfall 4,9 Jahre lang hoch dosiertes Atorvastatin einnehmen, um einen neuenischämischem SchlaganfallzuoderverhindernTIA mit Vorhofflimmern keine Kontraindikation für eine orale Antikoagulation. Auch Gebrechlichkeit und Sturzgefahr sind nicht per se Kontraindikationen. - Eine orale Antikoagulation bei Patient*innen mit Vorhofflimmern und kognitiven Einschränkungen oder einer Demenz ist gerechtfertigt, solange die regelmäßige Medikamenteneinnahme und Kontrolle gewährleistet ist.
OraleVKA
Antikoagulationvs.(OAK) beiVorhofflimmern(VHF)NOAKPrimärprävention: Bei Vorhofflimmern soll mit denPatient*innen das Schlaganfallrisiko und das Nebenwirkungspotenzial der OAK-Therapie anhand validierter Risiko-Scores (z. B. CHA2DS2-VASc-Score) besprochen und auf dieser Grundlage gemeinsam über die Behandlung entschieden werden.Sekundärprävention: Bei Vorhofflimmern soll eine dauerhafte Therapie mit OAK angeboten werden.Hochbetagte, multimorbide, insbesondereniereninsuffizientePatient*innen und diejenigen mit Multimedikation finden sich nicht in den Populationen der NOAK-Zulassungsstudien. Sie profitieren in besonderem Maß von einem Gerinnungsmanagement, wie sie dieINR-kontrollierte Therapie mit VKA ermöglicht.Speziell fürdiesehochbetagte,Patientengruppemultimorbide, niereninsuffiziente und mit Multimedikation behandelte Patient*innen könntedaher dieeine VKA-Therapievorteilhaftvon Vorteil sein (in den NOAK-Zulassungsstudien nicht abgebildet).- Bei einer Antikoagulation mit VKA soll eine Ziel-INR von 2,5 ± 0,5 angestrebt werden.
- Die Dosierung der NOAK
soll ausreichend sein undsollte sich strikt an den Empfehlungen der Hersteller orientieren, um häufig zu beobachtende Unterdosierungen zu vermeiden.- Kontrollen der Nierenfunktion sollen mindestens
1x1 x jährlich erfolgen,
- Kontrollen der Nierenfunktion sollen mindestens
- Real-World-Untersuchungen haben in Deutschland keinen Vorteil von NOAK gegenüber VKA gezeigt, eher sogar eine Überlegenheit der VKA hinsichtlich der Verhinderung embolischer Ereignisse. Allenfalls Hirnblutungen traten unter NOAK etwas seltener auf.
- NOAK sollten nicht eingesetzt werden bei:
- Patient*innen mit einer gut funktionierenden Antikoagulation mit VKA (TTR > 70 %)
- einer unsicheren Adhärenz – die deutlich kürzere HWZ der DOAK verzeiht Fehler weniger als beim lang wirkenden Phenprocoumon.
- hohem Risiko für gastrointestinale Blutungen
- schweren Nierenfunktionsstörungen (eGFR < 30 ml/min)
- nach Herzklappenersatz und/oder relevanter Mitralstenose.
- DOAK können eine Indikation sein bei:
- spezifischen Interaktionen von VKA mit Arznei- und Nahrungsmitteln
- spezifischen Kontraindikationen von VKA (z. B. schwere
InfekteLebertoxizität) - stark schwankenden INR-Werten unter VKA trotz guter Therapie-Adhärenz
- hohem Risiko intrazerebraler Blutungen
- frisch diagnostiziertem Vorhofflimmern, das akut einer Rhythmisierung oder
Volumenverschiebungen)Ablationhzugeführt werden soll.
Weitere medikamentöse Therapie
Lipide
- Patient*innen sollen nach einem Schlaganfall eine Sekundä
ufigerrprävention mit einem Statin angeboten werden.1,29 Sie sollen dabei über eine geringe Größenordnung des Schutzeffektes durch Statine informiert werden – in der größten diesbezüglichen Studie34 betrug die absolute Risikoreduktion in 4,9 Jahren 1,9 %. EsDiegibtArtkeinederIndikation,DurchführungPatient*innen,einerdieStatintherapiestabilistund komplikationslosseitmitlängeremVKAGegenstandbehandeltkontroversersind, auf NOAK umzustellenDiskussion.HöheresDieLebensalterDEGAMistempfiehltbeidiePatient*innenGabenacheinerischämischemFixdosisSchlaganfalleinesoderStatins.1- Die
TIADGNmitempfiehlt eine zielwertorientierte Statintherapie, dasVorhofflimmernLDL soll < 70 mg/dl gesenkt werden.29- Zur Erreichung des Zielwerts empfiehlt die DGN ggf. die zusätzliche Gabe von Ezetimib.29Allerdings gibt es keine
KontraindikationStudienbelege für eineoraleSchutzwirkungAntikoagulation.vonAuchEzetimibGebrechlichkeithinsichtlichundderSturzgefahrsindVerhinderungnichtneuerper se KontraindikationenSchlaganfälle.
- Zur Erreichung des Zielwerts empfiehlt die DGN ggf. die zusätzliche Gabe von Ezetimib.29Allerdings gibt es keine
Arterielle Hypertonie
Eine orale Antikoagulation beiPatient*innen mitVorhofflimmernarteriellerund kognitiven Einschränkungen oder einerDemenzHypertonieistsollengerechtfertigtnach Schlaganfall langfristig antihypertensiv behandelt werden.1,29- Der
solangeBlutdruckdie regelmäßigesollMedikamenteneinnahme<und140/90KontrollemmHggewährleistetgesenktistwerden.1,29- Eine weitere Blutdrucksenkung bringt in der Regel keinen Vorteil.
ObstruktivesDie Behandlung soll möglichst mit dem Thiazid-Diuretikum ChlortalidonSchlafapnoe35 und/oder ACE-SyndromHemmer (OSASbei Unverträglichkeit AT-Rezeptorblocker) erfolgen.Ergeben sichinsbesondere bei älteren/multimorbiden Patient*innen Auswahl der Antihypertensiva unter Berücksichtigung von Begleiterkrankungen und Medikamenteninteraktionen
- Zeitpunkt des Behandlungsbeginns
- Die antihypertensive Behandlung kann in den ersten Tagen nach Symptombeginn begonnen werden.29
Diabetes mellitus
- Patient*innen mit Diabetes mellitus und nach stattgehabtem Schlaganfall sollen entsprechend den Empfehlungen der NVL Diabetes und der DEGAM-S3-Leitlinie „Hausärztliche Risikoberatung zur kardiovaskulären Prävention“36 beraten werden.1
Hormontherapie
- Nach einem Schlaganfall sollte eine laufende Hormontherapie beendet werden.1
- Frauen in der Postmenopause, die eine Hormonersatztherapie zur Linderung von Wechseljahresbeschwerden beginnen oder fortführen wollen, sollten zum Nutzen-Risiko-Verhältnis beraten werden unter Beachtung ihrer Wünsche und Präferenzen.1
Diagnostik und Behandlung eines OSAS
- Bei V. a. OSAS nach Schlaganfall
oder/TIAHinweise auf ein OSAS,sollte eine Überweisung zu Spezialist*innen zur weiteren Diagnostikund/ggf. Therapieeinleitung angebotenAllerdings gibt es bislang keine Belege dafür, dass eine CPAP-Behandlung vor einem Rezidiv-Schlaganfall schützt.1 Personen nach einem Schlaganfall mitBei OSASsolltenberaten werden,sollte auf abendlichen Alkoholgenuss und die Einnahme von Hypnotikaoder/Sedativazu verzichtenverzichtet und ggf. eine Gewichtsreduktion angestrebt werden.Gewichtsreduktion1anzustreben. Eine- CPAP
-Therapieundgeltensindals TherapeutikaTherapie der 1. Wahl.1
Interventionelle/operative Maßnahmen
Extra- und intrakranielle Stenosen
- Zu Diagnostik und Therapie extrakranieller Stenosen siehe Artikel Karotisstenose.
- Patient*innen mit intrakraniellen Stenosen werden im Allgemeinen mit Thrombozytenaggregationshemmern behandelt, bei rezidivierenden Symptomen/Hirninfarkten kann im Einzelfall Stentimplantation erwogen werden.37
Persistierendes Foramen ovale (PFO)
- Patient*innen unter 60 Jahren mit einem PFO und
einemHirninfarktohneinalternativedenÄtiologieletztentrotz6umfassenderMonatenSuche soll
ein mindestens mäßiger Shunt und/oder ein
Lebensstilmodifikation
- Auch wenn für die Sekundärprävention im Gegensatz zur Primärprävention wenig Evidenz vorliegt, ist anzunehmen, dass Lebensstilmodifikationen in der Sekundärprävention ähnlich wichtig sind wie in der Primärprävention37
- Entsprechend können daher die DEGAM-Empfehlungen zur Primärprävention angewendet werden:1,36
Ernährung und
trotzGenussmittel- Die
umfassenderErnährungSuchesolltekeineabwechslungsreichalternative Ätiologieundgefundenanwurdeden Empfehlungen zur mediterranen oder nordischen Kost ausgerichtet sein. undBeidieBedarfbehandelndensollteÄdurch Hausärzt*innen dieStärken und EinschränkungenIntensivierung derzugrundeErnährungsberatungliegendendurchStudienTeilnahmekennenan strukturierter Schulung empfohlen werden.- Salz
- Die Salzaufnahme sollte reduziert werden, insbesondere bei arterieller Hypertonie.
- Alkohol
- Der Alkoholkonsum sollte beschränkt werden.
- Rauchen
- Das Rauchen sollte eingestellt werden.
OAK und TAH nach intrakranieller BlutungNahrungsergänzungsmittel
EsEinegibtSupplementierungHinweise,mitdassVitamin- bzw. Antioxidanzien-Präparaten sollte nicht generell empfohlen werden.
Körperliche Aktivität
- Die Patient*innen
mitsollteneinemzuhohen kardioembolischenregelmäßigerRisikokörperlicher(VHFAktivität ermutigt werden,mechanischeorientiertHerzklappen)anauchFähigkeitennachundstattgehabterVorliebenintrakraniellerBlutungdesvon einer OAK profitieren könnten. Es ist empfehlenswertEinzelnen - Patient*innen, die
Entscheidungnur eingeschränkt in der Lage sind, körperlich aktiv zu sein, sollten so intensiv überben, wie es individuell sicher möglich ist, und dieWiederaufnahmesitzendeinerverbrachteAntikoagulationZeitin enger Absprache mit einem neurovaskulären Zentrum zu treffenminimieren.
DauerstressÜbergewicht/Adipositas
UnterHausärzt*innenpsychogenemsollenDauerstressdurchleidendeunterstützendePersonen mit hohem Schlaganfallrisiko profitieren von hausGesprärztlicher Beratung, um Unterstützungche beiBewältigungGewichtsreduktionzu erfahren und ambulante Hilfsangebote kennenzulernenhelfen.- Die Beratung soll individualisiert, praxisnah und zielorientiert erfolgen und explizit psychosoziale Faktoren einbeziehen.
Rehabilitation im Rahmen der hausärztlichen Versorgung
- Zu den allgemeinen Prinzipien der stationären und poststationären Reha siehe auch Schlaganfall, Rehabilitation.
- Nach der Akutbehandlung (Phase A) erfolgen Frührehabilitation (Phase B) und weiterführende neurologische Rehabilitation (Phase C) stationär, die Anschlussheilbehandlung kann stationär oder ambulant erfolgen.1
- Innerhalb von 3 Monaten nach einer Rehabilitationsmaßnahme kann zudem eine Intensivierte Rehabilitationsnachsorge (IRENA, Kostenträger Rentenversicherung) durchgeführt werden, diese wird durch Rehabilitationsärzt*innen empfohlen und veranlasst.
KryptogenerHausärzt*innen versorgen die Patient*innen in allen Phasen nach dem Schlaganfall, da nicht jede Patient*in stationär aufgenommen wird und auch nur ein Teil eine Rehabilitationsmaßnahme erhält.
Zielsetzung und Planung
- Der Erfolg einer Reha-Maßnahme hängt auch davon ab, in welchem Maß Patient*innen das Rehabilitationsziel mitbestimmen. Therapieziele sollten daher unter Berücksichtigung der Komponenten Teilhabe, Aktivitäten und Körperfunktionen mit den Patient*innen gemeinsam erarbeitet werden.1
- Patient*innen sollten unterstützt werden, ihre persönlichen Therapieziele zu definieren.
- Die Ziele sollten evaluierbar und zeitlich bestimmt sein und schriftlich festgelegt werden.
- Patient*innen, soziales Umfeld und das Rehabilitationsteam sollten fortlaufende Kenntnis der festgelegten Rehabilitationsziele haben.
- Die Ziele sollten regelmäßig überprüft und bei Bedarf angepasst werden.
- Die Entscheidung über Auswahl und Verordnung von Therapien sollte auf der Grundlage standardisierter Assessmentverfahren getroffen werden.1
- Bei ambulanter Versorgung führen Heilmittelerbringer im Rahmen ihrer jeweiligen Therapie standardisierte Assessments durch, deren Ergebnisse den Hausärzt*innen als Befundbericht zur Verfügung gestellt werden.
- Vom hausärztlichen Team kann der gebräuchliche und unkomplizierte Barthel-Index durchgeführt werden, der komplexe Tätigkeiten allerdings nur unzureichend erfasst.
Versorgungsbereiche
- In der ambulanten Versorgung übernimmt in den meisten Fällen die Hausarztpraxis die Koordination der Therapie, in die Planung und Durchführung sollten verschiedene Berufsgruppen einbezogen werden.1
Heilmittelversorgung
- Zu den Heilmitteln zählen Ergotherapie, die physikalische Therapie (Krankengymnastik bzw. Physiotherapie) und die Stimm-, Sprech- und Sprachtherapie (Logopädie).
- U. a. folgende Indikationsschlüssel stehen zur Verfügung:
- physikalische Therapie ZN2 (ZNS-Erkrankungen) mit den Heilmitteln KG-ZNS (spezielle Krankengymnastik zur Behandlung von Erkrankungen des ZNS unter Einsatz neurophysiologischer Techniken nach
HirninfarktBobath,ohneVojtaklareoderUrsachePNF oder KG) - Ergotherapie EN2 (ZNS-Schädigungen) mit den Heilmitteln MFB (motorisch-funktionelle Behandlung), NOB (Hirnleistungstraining/neuropsychologisch orientierte Behandlung), PFB (psychisch-funktionelle Behandlung) und SPB (sensomotorisch-perzeptive Behandlung)
- Logopädie SP5 (Störungen der Sprache nach Abschluss der Sprachentwicklung), SP6 (Störungen der Sprechmotorik) und SC1 (Störungen des Schluckakts).
- physikalische Therapie ZN2 (ZNS-Erkrankungen) mit den Heilmitteln KG-ZNS (spezielle Krankengymnastik zur Behandlung von Erkrankungen des ZNS unter Einsatz neurophysiologischer Techniken nach
Hilfsmittelversorgung
- Durch Hilfsmittel sollen Teilhabe und Aktivität im Alltag auf einem möglichst hohen Niveau wiederhergestellt werden.
- Eine Listung im Hilfsmittelverzeichnis des GKV-Spitzenverbandes ist entgegen verbreiterter Auffassung für die Verordnungsfähigkeit eines Hilfsmittels nicht entscheidend, da es sich nicht um eine Positivliste handelt.
Pflegerische Versorgung
- Es gibt verschiedene Leistungen der Kranken- und Pflegversicherung zur Vermeidung von Versorgungslücken für Schlaganfallpatient*innen mit Unterstützungsbedarf und für pflegende Angehörige.
- Möglichst vor Rückkehr ins häusliche Umfeld Klärung des Bedarfs
trotzanumfangreicherHilfestellungDiagnostikdurch spezielle Ausstattung, räumliche Veränderung und/oder Hilfsmittel
Neuropsychologie
- Die Feststellung der Indikation erfolgt in einem zweistufigen Verfahren:
- fachärztliche Feststellung einer erworbenen Hirnschädigung (im Rahmen der fachärztlichen Erstkonsultation, Entlassbrief nicht ausreichend)
- Feststellung von neuropsychologischen Gesundheitsstörungen durch Psychotherapeut*innen/Ärzt*innen mit neuropsychologischer Zusatzqualifikation.
Empfehlungen zur Therapie nach Schlaganfall
- Die DEGAM hat umfangreiche Empfehlungen zur Therapie verschiedener residueller Störungen veröffentlicht, die im Detail der DEGAM-Leitlinie entnommen werden können.1
- Im Folgenden eine Auswahl der Empfehlungen:
DEGAM-Empfehlungen zur Therapie nach Schlaganfall1
Bewegungsapparat
- Schlaganfallpatient*innen mit Paresen sollten angeboten werden:
- Maßnahmen zur Verbesserung von Muskelkraft, Bein- und Armaktivität
- zusätzlich elektrische Muskelstimulationsverfahren.
- Bei Geh- und Gangstörungen soll Gehtraining angeboten werden.
- Hand- und Handgelenksorthesen sollen bei Armparese nicht routinemäßig eingesetzt werden (keine Wirkung auf Schmerz, Funktion, Bewegungsausmaß).
- Bei orofazialer Beeinträchtigung sollten Maßnahmen zur
SekundVerbesserung der motorischen Funktion der mimischen Muskulatur angeboten werden. - Bei Spastik sollten Physiotherapie und Krafttraining angeboten werden, ergä
rprnzend können angeboten werden: elektrische Stimulation, lokale intramuskuläventionreeinInjektionThrombozytenaggregationshemmervon Botulinumtoxin (fokale Spastik), intrathekales Baclofen (multifokale Spastik), orale antispastische Medikamente wie Baclofen, Tizanidin, Dantrolen oder Diazepam (generalisierte Spastik). - Bei Störungen der posturalen Kontrolle/des Gleichgewichts sollen Maßnahmen zur Verbesserung von Gleichgewicht, Ausdauer und Muskelkraft angeboten werden.
- Bei hohem Sturzrisiko sollte eine Beurteilung der Sturzgefahren im häuslichen Umfeld erfolgen, Beratung zur Beseitigung von Gefahrenquellen.
Schwindel
- Physiotherapie (sog. Schwindelkompensationstraining) und Physiotherapie am Gerät (v. a. Laufbandtraining) sind die wichtigsten Behandlungsempfehlungen.
Sprech- und Sprachstörungen, Dysphagie
- Bei Aphasie soll hochfrequente Sprachtherapie angeboten werden.
- Bei Dysarthrie sollte eine sprachtherapeutische Therapie angeboten werden.
- Bei Dysphagie soll eine Schluckrehabilitation angeboten werden.
Grundsätzliche Maßnahmen54WahrnehmungsstörungenEmpfohleneSpezifischesBehandlungübendesvorTrainingdemzurHintergrundVerbesserung derdesRaumkognition10-Jahres-Risikosunterfür Tod aufgrundEinbezug vonHerz-Gefäß-ErkrankungenZusatzfaktorenAlltagsanforderungenberücksichtigen,kanndie das kalkulierte Risiko erhöhen könnten: Endorganschäden, Dyslipidämie,Übergewicht,Fehlernährung, Bewegungsmangel, psychische Belastungen.Siehe auch den ArtikelKardiovaskuläre Primärprävention.
Antikoagulation2Wegen des hohen Risikos einerAntikoagulationsbehandlungist es unumgänglich, den potenziellen Nutzen wie auch die Risiken einer solchen Behandlung zunächst mit den Patient*innen zu besprechen. Hierfür sollten Kalkulatoren wie der CHA2D2Vasc-Score55und HAS-BLED-Score56sowie eine sich hieraus ergebende Entscheidungshilfe verwendetempfohlen werden(siehe Tabellen unten).Für Patient*innen mit einemVorhofflimmernWie groß ist das Risiko, einen Schlaganfall zu erleiden?Wie groß ist das Risiko einer Blutung durch eine Blutverdünnung?
Der CHA2DS2-VASc-Score gibt 1 Punkt für Alter 65–75 und 2 Punkte für Alter > 75 und zusätzlich 1 Punkt für eine nachgewiesene vaskuläre Erkrankung und 1 Punkt für Frauen.57-58In schwedischen Registerdaten wurde bei CHA2DS2-VASc-Score 2 eine jährliche Inzidenz für Schlaganfall bei 0,1–0,2 % der Frauen und bei 0,5–0,7 % der Männer festgestellt.59

siehe Tabelle: Schlaganfall-Risiko (CHA2DS2-VASc-Score)Der HAS-BLED-Score ermittelt das Risiko einer größeren Blutung unter Blutverdünnung (deshalb im Krankenhaus, Hirnblutungen sind nicht berücksichtigt).

siehe Tabelle: Blutungsrisiko unter Blutverdünnung (HAS-BLED-Risiko-Score)Erst nach entsprechender Information der Patient*innen sollte eineAntikoagulationbegonnen werden. Die Datenlage spricht bei guter Qualität einer Antikoagulation (hoher Prozentsatz der TTR = Zeit im therapeutischen Bereich, meistINR2–3) für den Einsatz von Phenprocoumon bzw. Warfarin. Nur bei Unverträglichkeit, schlechter Qualität der Antikoagulation – z. B. in einer Praxis oder Unmöglichkeit,INR-Kontrollendurchzuführen – sollte statt Phenprocoumon ein NOAK eingesetzt werden. Weil Dabigatran die Rate anMyokardinfarktenerhöht und weil es unter Rivaroxaban gehäuft zu Rebound-Insulten kommt, sollte dann vorrangig Apixaban eingesetzt werden.60
SekundärpräventionAntithrombotische BehandlungLeitlinie: Neue Thrombozyten-Aggregationshemmer, Einsatz in der Hausarztpraxis45Siehe auch AbschnittMedikamentöse Therapie.
EmpfehlungenPatient*innen nach nicht-embolischem ischämischem Hirninsult oder TIA sollen ASS angeboten bekommen (A/Ia).- Bei
Patient*innen mit gastrointestinalen Symptomen unter ASS sollte nicht auf Clopidogrel gewechselt, sondern ASS mit einem Protonenpumpenhemmer, z. B. 20 mg Omeprazol kombiniert werden (B/IIb). Clopidogrel soll als Alternative bei ASS-Intoleranz angeboten werden (A/IIb).Zulassung ab Tag 7 nach Insult als Monotherapie bei ASS-Unverträglichkeit
Nach KarotisstentGesichtsfelddefiziten kanneine DAPT (duale Plättchenhemmung) mit ASS und Clopidogrel für die Dauer von 4 Wochen durchgeführt werden (A/IIb).schlechte DatenlageEmpfehlung in Analogieschluss zur Stentimplantation an Koronararterienhohes BlutungsrisikoCave: off label für Dauertherapie!
Nach ischämischem Insult sollte eine doppelte Plättchenhemmung mit ASS plus Clopidogrel nicht über einen Zeitraum von 10–21 Tagen hinaus zur Sekundärprävention oder Rezidivprophylaxe eingesetzt werden (A/Ia).Die Daten aus der CHANCE-Studie61und entsprechende Metaanalysen sprechen für eine durchzuführende verlängerte Akuttherapie nach frischem Schlaganfall – nicht aber für eine längerfristige Sekundärprävention.
Nach Insult oder TIA bei nichtvalvuläremVorhofflimmernsoll eine oraleAntikoagulationeiner DAPT vorgezogen werden (A/Ia).Prasugrel und Ticagrelor sollten bei ischämischem Schlaganfall weder in der Akuttherapie noch in der Primär- oder Sekundärprävention eingesetzt werden.
Patient*innen mit Hirninfarkt oder TIA ohne kardiale Ursache (und damit Indikation für eine Antikoagulation-Behandlung) sollten eine plättchenhemmende Therapie erhalten.ASS ist das Mittel der 1. Wahl. Nur bei echter ASS-Unverträglichkeit oder vorbestehenderPAVKwird Clopidogrel eingesetzt.
ASS + Dipyridamol: Da die Datenlage negativ ist, wird für diese Kombination keine Empfehlung ausgesprochen.7kein Vorteil gegenüber einer ASS-MonotherapieCave: keine Wirtschaftlichkeit, sehr hohe Regressgefahr!
ASS + ClopidogrelDie sekundärpräventive Wirkung von ASS ist gut belegt.62-63Die Kombinationstherapie für 10–21 Tage nach ischämischem Insult kann erwogen werden.61,64-67Die Blutungsgefahr ist unter dualer Therapie (DAPT) hoch.Die DEGAM-Leitlinie45sieht einen möglichen Benefit für die duale Plättchenaggregation mit ASS + Clopidogrel für bis zu max. 21 Tage nach Insult.Zu bedenken ist, dass die Verordnung off label erfolgt!
Diabetes mellitusEine optimale Einstellung des Diabetes mellitus kann bei Senkung sehr hoherBlutglukosewertegefäßprotektiv sein.Siehe die ArtikelTyp-2-DiabetesundTyp-1-Diabetes.
Beim Diabetes wird empfohlen, bei einem Blutdruck von über 140/90 eine Blutdruckbehandlung zu beginnen. Der Blutdruck sollte unter 140 mmHg liegen.68Individuelle Gegebenheiten sollten dabei berücksichtigt werden.
BlutdruckbehandlungAllen Patient*innen mit Schlaganfall oder TIA und einem Blutdruck ≥ 140/90 mmHg sollte eine medikamentöse blutdrucksenkende BehandlungKompensationstraining angeboten werden.- Eine
blutdrucksenkendevernachlässigtenBehandlungRaumhälfte (Neglect) sollteauchexploriertPatient*innenundüber 80 Jahren mit Blutdruck ≥ 140/90 mmHgFunktionstraining angeboten werden. BehandlungszielBlutdruckMaßnahmen<zur140/90Verbesserung dermmHgSensibilitätbzwsollten angeboten werden (z.<B.140/85sensorischemmHgDie Behandlungsziele setzen vorausStimulation,dasssensomotorischesbeiTraining,den Patient*innen keine inakzeptablen Nebenwirkungen auftreten.2
PräparatewahlAm konsistentesten ist die Evidenz für Kalziumantagonisten und Thiazideu.Betablocker erzielen nur eine geringe Risikoreduktiona.2
Lipidsenkende BehandlungSchmerzenStatinePhysiotherapeutische Maßnahmen zur Schmerzreduktion sollen angeboten werden.- Bei chronischen Schmerzen sollte interdisziplinäre Behandlung (ärztlich, physio-ergo-, psychotherapeutisch, pflegerisch) angeboten werden.
- Bei leichter bis mäßiger Schwäche eines Armes oder einer Hand kann die Spiegeltherapie ergänzend zur Verbesserung der Armfunktion eingesetzt werden.
- Schlaganfall-Patient*innen mit neuropathischem Schmerz sollte initial Amitriptylin, Duloxetin, Gabapentin oder Pregabalin angeboten werden.
SieheBeiauchungenügenderArtikelSchmerzreduktion sollte auf einHyperlipidämie.
StatineanderessolltenSchmerzmedikamentempfohlender Basisempfehlung zurückgegriffen werden, wenn das kardiovaskuläre Gesamtrisiko stark erhöht ist.Zur Risikokalkulation empfiehlt sich derARRIBA-Rechner.- Die
DEGAM-LeitlinieHausärztliche Risikoberatung zur kardiovaskulären Präventionempfiehlt:69Die NNT zur Verhinderung eines Insult-Rezidives (Sekundärprävention!) ist mit 53/5 Jahren hoch. Daraus leitet sich ab, dass in der Hausarztpraxis nicht automatisch die Klinikempfehlung für ein Statin übernommen werden muss. VielmehrPatient*innen solltenmithilfezuvonBewegung,Entscheidungshilfen wie ARRIBA die absolute RisikoreduktionHaltungsänderungen unddieoptimiertenNNT von 53/5 Jahren demonstriert werdenBewegungs- undgemeinsamLagerungspositioneneine Entscheidung für oder gegen eine Statinbehandlung getroffenangeleitet werden.Für den Nutzen einer Dosis-Titration der Statine auf möglichst niedrigeLDL-Werte existiert keine genügende Evidenz. Daraus ergibt es sich, dass bei einmal gefasster Entscheidung für eine Statinbehandlung weitere LDL-Kontrollen nicht erforderlich sind.
BeiOptionenPatient*innenbei Schulterschmerzenmit akutem ischämischemnach Schlaganfall oderTIA,beidieregionalenbereitsSchmerzsyndromen- Behandlung mit
einemSchienenStatinoderbehandelt werdenOrthesen,sollTape-Behandlung,dieLagerungsbehandlung,StatingabeelektrischefortgeführtStimulation,werden.Injektion von Botulinumtoxin oder Lokalanästhetikum, orales NSAR oder Kortikoid
Weitere- Behandlung mit
- Schmerzhypersensitivität
indizierte(CentralMedikamentePost-Strope Pain = CPSP)Antidepressiva-Behandlung?EineEinMetaanalyseTherapieversuchzeigte, dass eine Behandlungkann mitSSRI die häufig auftretendenAngststörungenAmitriptylin undDepressionenLamotriginnach einem Schlaganfall verbessern könnte.70Aber die Ergebnisse sind nicht eindeutig, und neue Studien sind notwendig, um festzustellen, ob SSRI routinemäßig nach einem Schlaganfall verabreicht werden sollerfolgen.Eine dänische Studie zeigtPregabalin,dassGabapentin,SSRICarbamazepinnachodereinemPhenytoinischämischenkönnenSchlaganfallalszuTherapeutikaeinemderniedrigeren Risiko für neue kardiovaskuläre Ereignisse führt2.AllerdingsWahlist die Anwendung mit einem erhöhten Blutungsrisiko verbunden. Unter den Anwendern von SSRI besteht eine erhöhte Mortalität, was mit einem erhöhten Blutungsrisiko zusammenhängen kann (III).71Trizyklika wie Amitriptylin sind ähnlich wirksam und verträglich. Sie sollten nur bei kognitiver Verschlechterung nicht verwendetberücksichtigt werden.
KarotisstenoseKognitive FunktionenWeiterfBei Aufmerksamkeitsstörungen sollte ührendebendesInformationenFunktionstrainingsieheaufArtikelKarotisstenose.symptomatische KarotisstenosePatient*innen mitBasis einersymptomatischenneuropsychologischenKarotisstenoseDiagnostiksoll ASSangeboten werden(A/Ib).45
Leitlinie: Karotisendarteriektomie (TEA) –Sekundärprophylaxe72Die TEA wird bei Patient*innen empfohlen,beievtl.denenergänztmildedurch anderebisMaßnahmenmittelgradigewieStenosenz.imB.vorderenkognitiv-verhaltenstherapeutischeKreislaufMethoden,mitBewegungstraining,Stenosegrad ≥ 70 % (NASCET) in der Karotisarterie (ACI) lokalisiert wurdenFreizeitaktivitäten.- Bei
einemGedächtnisstörungenStenosegradsoll übendes Funktionstraining auf Basis einer neuropsychologischen Diagnostik angeboten werden, bei schweren Gedächtnisstörungen multisensorische Stimulation oder körperliches Training. - Zur Verbesserung der Problemlösefähigkeit und des Arbeitsgedächtnisses soll übendes Training angeboten werden.
- Kognitive übende Verfahren sollten mit Methoden des Verhaltensmanagements kombiniert werden.
Angst/Depression/affektive Störungen
- Nach Schlaganfall sollte regelmäßig ein Assessment bezüglich Angst und Depression angeboten werden.
- Schlaganfallpatient*innen mit emotionalen Beschwerden (Angst, Depression) können von
50–69einer%Behandlung mit Antidepressiva profitieren, diese sollen aber nicht routinemäßig angeboten werden. - Bei Depression oder Angststörung kann eine
TEAPsychotherapiefürangebotenausgewähltewerden.
Harn- und Stuhlinkontinenz
- Alle Patient*innen
nachsollteneinerhinsichtlichindividuellenHarn-Bewertungund Stuhlinkontinenz exploriert werden, diagnostische und therapeutisch sollten angeboten werden:- strukturiertes Inkontinenzassessment (z. B. ICIQ), Ultraschalluntersuchung der Harnwege mit Restharnbestimmung, Urinteststreifen
- Zur Reduktion der Inkontinenzepisoden sollte körperliches Training und ggf. eine Gewichtsreduktion empfohlen werden.
Eine TEA istOptionen beieinemDranginkontinenz:StenosegradBlasen-vonund<Beckenbodentraining,50evtl.%anticholinergienichtTherapieempfehlenswert.(nach Ausschluss Restharn)EineOptionenTEAbeisollteBelastungsinkontinenz:innerhalbBeckenbodentraining,vonDuloxetin,2Pessartherapie- Die
WochenmedikamentösenachTherapiedemeinerAuftretenStuhlinkontinenzeineskannHirninfarktsmitoderLoperamidTIA(und bei Unverträglichkeit mit Codeinphosphat) durchgeführt werden. Eine endovaskuläre Behandlung wird nicht routinemäßig empfohlen.
Operative Behandlung von AneurysmenAkuteSubarachnoidalblutungenwerden, wenn möglich, mit einem operativen Eingriff behandelt.Es wurden Studien durchgeführt, um den Nutzen des Screenings von Patient*innen mit Aneurysmablutung nach einem Aneurysma bei Verwandten 1. Grades zu untersuchen.Die Ergebnisse rechtfertigen ein solches Screening nicht.
WeiteresSexualitätMigrLiegen Störungen der sexuellen FunktionsfäneFür Migräne mit Aura ist ein erhöhtes Schlaganfallrisiko nachgewiesen, vor allem bei jungen Frauen.Es liegen bisher jedoch keine ausreichenden Datenhigkeit vor,umsollten Hausärzt*innen einespezifischeBeratungvorbeugendeundBehandlungeinezurAbklärungVerringerungmöglicherdiesesUrsachenRisikos zu empfehlenanbieten.
GrippeimpfungEingeschränkte Selbstversorgung
ReduziertImlauthäuslicheneinerUmfeldMetaanalyse das Risiko für größere schwere kardiovaskuläre Ereignisse. Der Effekt war beilebenden Patient*innen mitdemEinschränkungenhder persöchstennlichenRisikoundaminstrumentellengrößAktivitäten(la)des täglichen Lebens soll ergotherapeutisches Alltagstraining angeboten werden.73
Soziale Teilhabe
- Patient*innen und Angehörige sollen informiert werden über: finanzielle Hilfen und sozialstaatliche Leistungen (inkl. Unterstützung bei Anträgen), psychosoziale und sozialrechtliche Beratungsangebote, Selbsthilfegruppen.
Verlauf, Komplikationen und Prognose
VerlaufKomplikationenDieZumeisten Patient*innen, die einen Schlaganfall überlebt haben, erleben eine Verbesserung der neurologischen AusfälleKomplikationen undihresihrerFunktionsniveaus.InitialeBehandlungVerbesserungDiessiehekannArtikelauf den Rückgang des Ödems, die Normalisierung des Kreislaufs, die Entwicklung von anderen Impulswegen im Gehirn, die Entwicklung neuer Synapsen und die Übertragung der Funktionen auf andere Teile des Zentralnervensystems (Neuroplastizität), die nicht beschädigt wurden, zurückgeführt werden. Die genauen Mechanismen sind allerdings bislang nicht geklärt.
Wie lange können die Verbesserungen fortdauern?Patient*innen mit leichten oder mäßigen neurologischen Ausfällen erleben vor allem in den ersten Wochen nach dem Schlaganfall eine deutliche Verbesserung, während diejenigen mit schweren Ausfällen messbare Fortschritte bis zu 6 Monate nach dem Schlaganfall haben können.Ausfälle, die nach 3–6 Monaten noch bestehen, bleiben in der Regel dauerhaft.Patient*innen sollten sich deshalb nach 3–6 Monaten auf die bestehenden Funktionsverluste einstellen und versuchen herauszufinden, welche Möglichkeiten und Grenzen sie damit haben.
DemenzRehabilitation nach einem Schlaganfall.
Verlauf und Prognose
- Das Risiko, an einem Schlaganfall zu versterben, hat sich in Deutschland nahezu halbiert, die Überlebensraten betragen:
7438 - 93 % nach 30 Tagen
- 75–93 % nach 1 Jahr
- 55 % nach 5 Jahren.
- Bei hämorrhagischen Schlaganfällen ist die Prognose schlechter als bei ischämischen.38
- Bei den
kognitivenischämischenFunktionenSchlaganfällenkannhaben dieBesserungkardioembolischdesbedingtenZustandsdielängerschlechtestedauern als bei anderen neurologischen Ausfällen. Bei einem Teil der Patient*innen mit Demenz nach einem Schlaganfall ist der Demenzzustand reversibel (Ia)Prognose.75
- Bei den
KomplikationenDetaillierte Beschreibung der Komplikationen und der Umgang damit ist im ArtikelRehabilitation nach einem Schlaganfallzu finden.Neuer SchlaganfallPneumonie, AspirationHarnwegsinfektInkontinenzInkontinenz ist nach einem Schlaganfall ein häufiges Problem.Die Ursachen sind vielfältig, sodass eine fachübergreifende Untersuchung und Rehabilitation Grundlage für alle Behandlungen ist.Es gibt spezifische Behandlungsmöglichkeiten.
Tiefe VenenthrombosenDie Anwendung von elastischen Kompressionstrümpfen bis zum Oberschenkel hat das Vorkommen von TVT nach einem Schlaganfall nicht verringert (10,5 % in der Behandlungs- und Kontrollgruppe), aber zu einer signifikanten Erhöhung der Hautkomplikationen geführt (Ib).7639
- 35 % der Betroffenen sind in den ersten Monaten auf pflegerische Versorgung angewiesen.
Lungenembolie38 StürzeSchmerzhafte, hemiplegische Schulter, KontrakturenDruckgeschwürDepression,Angstund andere emotionale SymptomeEmotionale Symptome kommen bei ca. der Hälfte der Patient*innen nach einem Schlaganfall vor.Die häufigsten Symptome sind Angst, Depression, emotionale Instabilität, Krisenreaktionen und geschwächte Initiative.Es wurde auch ein erhöhtes Vorkommen vonposttraumatischen Belastungsstörungennachgewiesen.
Deliriumim Verlauf der ersten Wochen nach einem Schlaganfall wurde bei 1240–50 % der Patient*inneneinerweisenSchlaganfallstationchronischeinmittelschwereden(z.USAB.festgestelltgehfähig, aber Hilfe im Alltag nötig) bis schwere Behinderungen auf.7738,40- Prädiktoren für ein gutes Behandlungsergebnis sind:38,40
ZuAufnahme in Stroke Unit- kurze Zeit zwischen Symptom- und Behandlungsbeginn
- junges Alter
- kleine Infarktgröße
- guter Zustand früh nach dem Schlaganfall (Sprachfähigkeiten, Kraft in den
Risikofaktoren zählen frühes kognitives VersagenArmen,Infektion und ausgeprGehfägter Schlaganfall.higkeit) DieTherapieadhärenz- Selbständigkeit
EntwicklungvoreinesdemDeliriumsSchlaganfall - Berufstätigkeit
- Hilfe
standdurchin Verbindung mit einer verschlechterten PrognoseFamilienangehörige.
KognitiveNichtBeeintrzu unterschächtigungtzendeundBedeutungDemenz74Akute zerebrovaskuläre Erkrankungen (ZVE) sind häufige Ursachen schwerer und anhaltender Gedächtnisstörungen.Zu den wichtigsten ZVE,hat dieeineMotivation:GedächtnisstörungJeverursachen können, gehören ischämische Infarkte, Hämatome (intrazerebrales, subdurales Hämatom), eineSubarachnoidalblutungundVaskulitiden.Läsionsorte bei den ZVE, die häufig mit einer Gedächtnisstörung einhergehen, sind der Hippocampus, der Thalamus, Strukturen des basalen Vorderhirns sowie des mediofrontalen Kortex, z. B. bei Ruptur von Aneurysmen der Arteria communicans anterior.
Exekutive Fähigkeiten, psychomotorische und motorische Schnelligkeit sind besonders betroffen und können z. B. durch verbalen Wortfluss, Coding und Finger-Tapping-Test überprüft werden.Eine prospektiven Observationsstudie aus England zeigte ein Auftreten vonDemenzbei 34 % der Betroffenen 1 Jahr nach einem ausgedehnten Schlaganfall, bei 8 % nach einem kleineren Schlaganfall und bei 5 % nach einer TIA.78Das Risiko, eine Demenz zu entwickeln, war nach einem ausgedehnten Schlaganfall im Vergleich zur Normalbevölkerung gleichen Alters und Geschlechts um den Faktor 47 erhöht.
PrognoseAllgemeinesBei TIA gehen die Symptome per Definition innerhalb von 24 Stunden vollständig zurück.Patient*innen mit Hirnblutung haben eine höhere Sterblichkeit und verbleiben länger in medizinischen Institutionen alsaktiver Patient*innenmit einem Hirninfarkt.Der Verlust des Bewusstseins nach einem zerebralen Infarkt zieht eine schlechtere Prognose nach sich.ErhöhteTroponinwertebei Einweisung führen zu einer erhöhten Sterblichkeit nach einem Schlaganfall, zu vermehrter Invaliditätmitwirken undzusicheineranstrengen,häufigerenumsoUnterbringunggrößerinsindeinerdiePflegeeinrichtungFortschritte.79Der funktionelle Status 6 Monate nach einem Schlaganfall hat eine große Bedeutung für die Langzeitüberlebensrate.Die Mortalität bei Schlaganfall wird durch moderne Behandlungen verringert und hat sich im Vergleich zu 1969 um 25 % verringert. Weitere Verbesserungen sind zu erwarten.
Prognose bei TIAÜberlebensrate: 70 % leben 5 Jahre nach der ersten TIA.Risiko für erneute TIA oder Schlaganfallnach TIA ereigneten sich bei 1,5 % der Betroffenen Schlaganfälle nach 2 Tagen, bei 2,1 % nach 7 Tagen, bei 2,8 % nach 1 Monat und bei 5,1 % nach 1 Jahr.8040
DieInErgebnissederausdeutschenverschiedenenRegelversorgungStudiengibtsindesnichtbislang keine einheitlich.EinegeregelteneueflächendeckendeStudie (n = 4.583) beziffert das 1-Jahres-Risiko eines Schlaganfalls nach TIA nur mit 5 %Schlaganfallnachsorge.8141- Bestandteile
beiderHirninfarktNachsorge sind:Überlebenszeit- Beurteilung des neurologischen, neuropsychologischen und psychischen Verlaufs
80–85 %Kontrolle dervon einem Schlaganfall betroffenen Patient*innen überleben die ersten Monate nach dem Schlaganfall.Risikofaktoren70–75Anpassung%derüberlebennichtmedikamentösendas(Lebensstil)ersteundJahr.medikamentösen Therapie, Beurteilung der TherapieadhärenzDie durchschnittliche Überlebenszeit nach einem Schlaganfall liegt bei rund 5 Jahren.Ein embolischer Schlaganfall hat eine etwas schlechtere Prognose als ein thrombotischer Schlaganfall.95 % derjenigen, die einen Schlaganfall in der Akutphase überleben, haben einen Hirninfarkt.
FunktionDie meisten Schlaganfall-Patient*innen erleben in den ersten Monaten nach dem Schlaganfall eine deutliche VerbesserungErfassung desFunktionsniveaus.90Bedarfs%ander Verbesserungen geschehen in den ersten 3 Monaten.Wenige Betroffene erleben eine Verbesserung noch nach 6 Monaten.
Status ein halbes Jahr nach dem SchlaganfallJede/jeder 4. Patient*in hat keine Funktionsverluste mehr.80 % haben so gute Bewegungsfähigkeiten, dass sie gehen können.2/3 können die grundsätzlichen täglichen Aktivitäten selbstständig erledigen.15–20 % sind so hilfebedürftig, dass sie in einer Pflegeeinrichtung versorgt werden müssen.
Verlaufskontrolle
PrognosePrognose bei HirnblutungPatient*innen mit Hirnblutung haben in der Akutphase eine 2Heil-bis 3-mal höhere Sterblichkeit als Patient*innen mit einem Hirninfarkt.Fast die Hälfte stirbt in den ersten Monaten,undnur 20 % sind nach 6 Monaten selbstständig.
Überlebt eine Patientin/ein Patient mit Hirnblutung die AkutphaseHilfsmitteln,ist die Prognose etwa genauso gut wie bei einem HirninfarktRehabilitation,sowohlPflegebeiunddenggf.Lebensaussichtenentsprechendeals auch fUnterstür das Funktionsniveau.
Prognose in Abhängigkeit vom BewusstseinszustandKrankenhauseinweisung im komatösen Zustand: 75 % Sterblichkeit in der AkutphaseKrankenhauseinweisung im wachen Zustand: < 5 % Sterblichkeit in der Akutphase
Bedarf an MaßnahmenVon denjenigen Patient*innen, die die Akutphase überleben, werden etwa80–85 % direkt oder über eine Rehabilitationseinrichtung nach Hause entlassen.15–20 % so viel Hilfe benötigen, dass sie in der Regel in einer Pflegeeinrichtung untergebracht werden müssentzung.
VerlaufskontrolleFahreignungAllgemeinesPsychischeEmpfehlenswertBeschwerdenistwiedieAngst, Unruhe undDepressiontreten bei fastÜberprüfung derHälfteFahreignung schon in derSchlaganfall-Patient*innenbetreuendenauf.RehabilitationseinrichtungBeiimca.Rahmen20einer%eingehendendauertneuropsychologischendieEvaluationDepressionmit Dokumentation darüber1imJahr anEntlassungsbrief.82Schlaganfall-Patient*innen haben im Vergleich zur übrigen Bevölkerung ein doppelt so großesSuizidrisiko. Niedriges Alter ist mit einem erhöhten Risiko verbunden.831
- Bei Zweifelsfällen im weiteren Verlauf ist eine Fahrverhaltensprobe durch Neuropsycholog*in sinnvoll (Beurteilung der emotionalen Kontrollfähigkeit, Einsichtsfähigkeit und krankheitsbedingter Persönlichkeitsveränderungen).1
SozialeEinschränkungenIsolationoderist normal und wird durch die häufig vorhandene gleichzeitige Aphasie verstärkt.Die Meinung der Angehörigen darüber, wie schwer der Schlaganfall war, istVerluste vongroßerExtremitätenfunktionenBedeutung dafür, wie die Patient*innen ihre Isolation und Antriebslosigkeit selbst wahrnehmen und bewerten.Die Betreuung und Information der Angehörigen ist daher für den Erfolg der Rehabilitation von Schlaganfall-Patient*innen von großer Bedeutung.
MaßnahmenDie eingeleiteten sekundärprophylaktischen Maßnahmen sollten regelmäßig kontrolliert werden.Die Behandlunginfolge einerDepressionmitAntidepressivaStörunghatdesinzentralenkleinenoderStudienperipheren Nervensystems erfordern eineguteneurologische/verkehrsmedizinischeWirkung gezeigtBegutachtung.Die Behandlung sollte auf der Grundlage einer sorgfältigen Diagnose begonnen werden.Eine Sensibilität von Ärzt*innen und Pflegepersonal für dieses Thema ist wichtig, um das Entstehen eines Teufelskreises zu verhindern.Die Teilnahme an Reha-Sport-Aktivitäten kann für die Patient*innen sinnvoll sein.Verlaufskontrolle der nichtmedikamentösen und medikamentösen sekundärprophylaktischen MaßnahmenFunktion: Bedarf an Hilfsmitteln wie Gehhilfen, Toilettensitzerhöhung, Duschsitz, Badewannenbrett etc.?Stimmungslage: Depression?Isolation: Maßnahmen, die Patient*innen gesellschaftlich einzubinden.
Klinische KontrolleFührerscheinNach einem Schlaganfall sollte überprüft werden, ob die Patient*innen der Lage sind, einAuto zu fahren.Wenn notwendig, sollte mündlich oder schriftlich ein Autofahrverbot verordnet werden.Achten sollte man vor allen Dingen auf einen möglichen Gesichtsfeldausfall sowie auf kognitive Störungen nach einem Schlaganfall. Ggf. sollten sich die Patient*innen in einer augenärztlichen Praxis vorstellen.- Siehe auch Artikel Beurteilung der Fahreignung.
Patienteninformationen
Worüber sollten Sie die Patient*innen informieren?Es ist wichtig, den Patient*innen und den Angehörigen Gelegenheit zu geben, über die Folgen eines Schlaganfalls zu sprechen.Berechnen des kardiovaskulären Gesamtrisikos
Patienteninformationen in Deximed
Schlaganfall/TIA und BehandlungTransitorischeSchlaganfallischämischeundAttacke (TIA)SchlaganfallSchlaganfall, Störungen der WahrnehmungSchlaganfall, TherapieplanSchlaganfall, Notfalltherapie- Rehabilitation nach einem Schlaganfall
Acetylsalicylsäure bei Herz-Kreislauf-ErkrankungenSchlaganfall, Maßnahmen in der RehabilitationSchlaganfalltherapie ‒ Was können Patienten und Angehörige tun?Schlaganfall, Vorbereitung auf die Krankenhausentlassung
KomplikationenWeitere MaßnahmenSchlaganfall, Risikofaktoren und VorbeugungErnährungsempfehlung bei erhöhten BlutfettwertenVollwertige Ernährung – Empfehlungen der Deutschen Gesellschaft für ErnährungFettarme LebensmittelBallaststoffe in der NahrungRauchen schadet Ihrer GesundheitWarum sollten Sie das Rauchen aufgeben, und wie gelingt es?HomocysteinAlkohol und Herz- und Gefäßerkrankungen
Patienteninformationen der DEGAM
Weitere Informationen
- Siehe Artikel Beurteilung der Fahreignung.
Video
-
Hemichorea nach Schlaganfall im Bereich der Stammganglien (mit freundlicher Genehmigung von Herrn Dr. Dagge)
Illustrationen
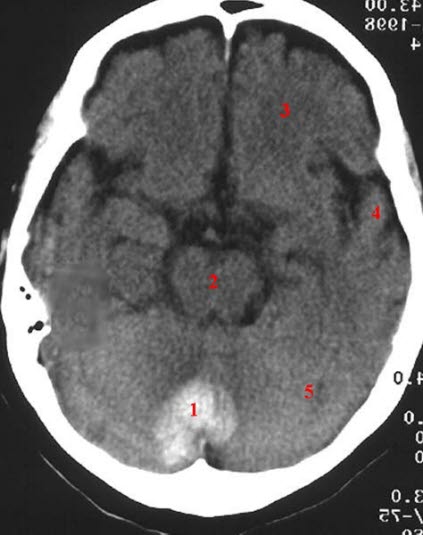 Hämatom im Zerebellum, CT
Hämatom im Zerebellum, CT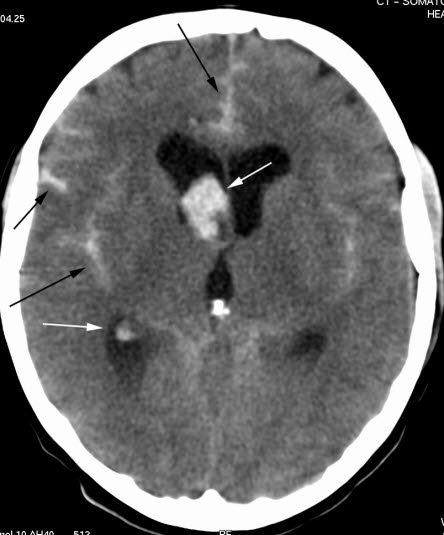 Subarachnoidalblutung (CT)
Subarachnoidalblutung (CT)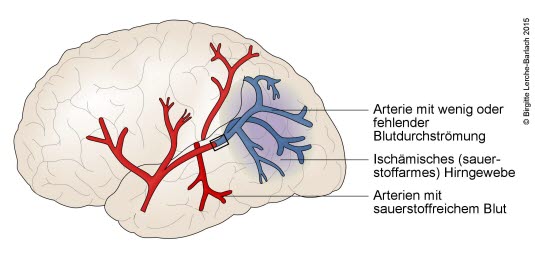 Schlaganfall
Schlaganfall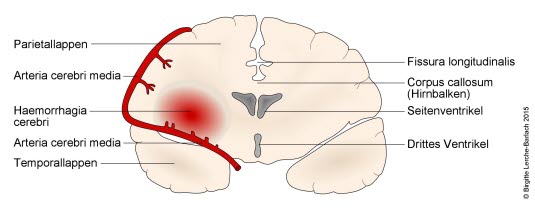 Hirnblutung
Hirnblutung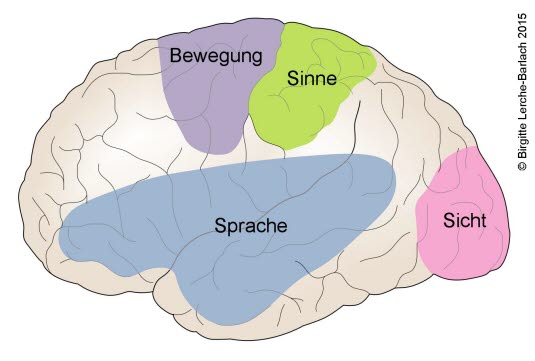 Anatomie des Gehirns, funktionell
Anatomie des Gehirns, funktionell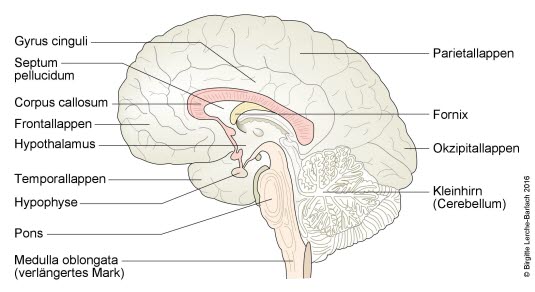 Anatomie des Gehirns, medialer Längsschnitt
Anatomie des Gehirns, medialer Längsschnitt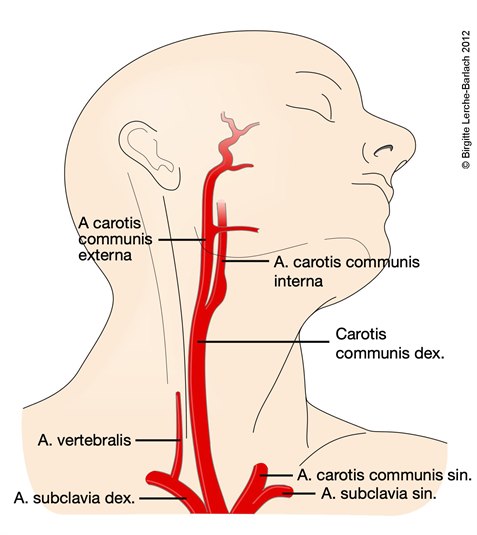 Arterie carotis und vertebralis
Arterie carotis und vertebralisQuellen
Leitlinien
- Deutsche Gesellschaft für Allgemeinmedizin und Familienmedizin. Schlaganfall. AWMF-Leitlinie Nr. 053-011. S3, Stand 2020. www.awmf.org
- Deutsche Gesellschaft für Allgemeinmedizin
(DEGAM)und Familienmedizin.Leitlinie:Hausärztliche Risikoberatung zur kardiovaskulären Prävention. AWMF-Leitlinie 053-024. S3, Stand20172016. Deutsche Gesellschaft für Neurologie. Diagnostik und Therapie von Gedächtnisstörungen. AWMF-Leitlinie Nr. 030-124. S2e, Stand 2020.www.awmf.org- Deutsche Gesellschaft für Allgemeinmedizin und Familienmedizin: Neue Thrombozyten-Aggregationshemmer
., Einsatz in der Hausarztpraxis. DEGAM-Leitlinie. AWMF-Leitlinie Nr. 053-041. S2e, Stand 2019. www.awmf.org - Deutsche Gesellschaft für Neurologie, Deutsche Schlaganfall-Gesellschaft. Akuttherapie des ischämischen Hirninfarktes. AWMF-Leitlinie Nr. 030-046. S2e, Stand 2021. www.awmf.org
- Deutsche Gesellschaft für Neurologie, Deutsche Schlaganfall
:-Gesellschaft. Sekundärprophylaxe ischämischer Schlaganfall und transitorische ischämische Attacke – Teil 1: Plättchenhemmer, Vorhofflimmern, Hypercholesterinämie und Hypertonie.S3S2k, Stand20152022. LeitlinienDeutschezurGesellschaftRehabilitationfürfindenNeurologie,Sie im ArtikelRehabilitation nach einemDeutsche Schlaganfall-Gesellschaft. Sekundärprophylaxe ischämischer Schlaganfall und transitorische ischämische Attacke – Teil 2: Lebensstil, arterielle Stenosen, andere Antithrombotika-Indikationen, Hormone, Diabetes mellitus, Schlafapnoe. AWMF-Leitlinie Nr. 030-143. S2k, Stand 2022. www.awmf.org.
Literatur
Robert Koch-Institut und Destatis. Gesundheit in Deutschland. Gesundheitsberichtserstattung des Bundes. Berlin.www.rki.de- Deutsche Gesellschaft für Allgemeinmedizin und Familienmedizin. Schlaganfall. AWMF-Leitlinie Nr. 053-011, Stand 2020. www.awmf.org
DAKBuschGesundheitsreport 2014, Hamburg 2015.www.dak.deRafay MF, Pontigon A-M,ChiangSchienkiewitzJA, Nowossadeck E, et al.DelayPrävalenztodesdiagnosisSchlaganfallsinbeiacuteErwachsenenpediatricimarterial ischemic stroke. Stroke 2009; 40: 58-64.StrokeHeuschmann PU et al.. Schlaganfallhäufigkeit und VersorgungAlter vonSchlaganfällen40 bis 79 Jahren in Deutschland.AktBundesgesundheitsblNeurol 20102013;3756:333656-340660. doi:10.1007/s00103-012-1659-0 DOI- Stahmeyer J, Stubenrauch S, Geyer S, et al. Häufigkeit und Zeitpunkt von Rezidiven nach inzidentem Schlaganfall. Dtsch Arztebl Int 2019; 116: 711-717. www.
kompetenznetz-schlaganfallaerzteblatt.de - Robert Koch-Institut (Hrsg). Gesundheit in Deutschland 2015. Gesundheitsberichterstattung des Bundes. Gemeinsam getragen von RKI und Destatis. www.rki.de
- Groß N, Erbguth F. Könnte es ein Schlaganfall sein? CME 2017; 14: 9-23. doi:10.1007/s11298-017-5978-1 DOI
- Kolominsky-Rabas PL, Heuschmann PU, Marschall D et al. Lifetime cost of ischemic stroke in Germany: results and national projections from a population-based stroke registry: the Erlangen Stroke Project. Stroke 2006; 37: 1179-83. www.ncbi.nlm.nih.gov
WinterLuengo-FernandezYR,Wolfram C, Schöffski O et al. Langzeitkrankheitskosten 4 Jahre nach Schlaganfall oder TIA in Deutschland. Nervenarzt 2008; 79: 918-926.www.ncbi.nlm.nih.govGladstone DJ, SpringViolato M,DorianCandio P, et al.AtrialEconomicfibrillationburdenin patients with cryptogenicof stroke across Europe: A population-based cost analysis.NEurEnglStroke JMed. 20142020;3705:246717-7725. doi:10561177/NEJMoa13113762396987319883160 DOILeeDienerIMHC,PaffenbargerGrondRSM.PhysicalEmbolicactivityStrokeandof Undetermined Source. Cardiovasc 2018; 18: 38-40. doi:10.1007/s15027-018-1405-0 DOI- Böttger P, Grond M, Lemm H, et al. 10 Kernaussagen zum Embolic Stroke of Undetermined Source und kryptogenen Schlaganfall. Med Klin Intensivmed Notfmed 2018; 113: 664–671. www.springermedizin.de
- Adams H Jr, Bendixen B, Kappelle L, et al. Classification of subtype of acute ischemic stroke
incidence.TheDefinitionsHarvardforAlumniuseStudyin a multicenter clinical trial. TOAST. Trial of Org 10172 in Acute Stroke Treatment. Stroke19981993;2924:204935-5441. pubmed.ncbi.nlm.nih.gov - Küpper C, Heinrich J, Müler K, et al. Der akute Schlaganfall. MMW - Fortschritte der Medizin 2019; 51: 22-28. doi:10.1007/s15006-019-0008-8 DOI
- Berlit P. Schlaganfall: Differenzialdiagnostische Übersicht. eMedpedia. Zugriff 17.07.22. www.springermedizin.de
- Hossmann K. Pathophysiological basis of translational stroke research. Folia Neuropathol 2009; 47: 213-227. www.termedia.pl
- Heiss W. The Pathophysiology of Ischemic Stroke Studied by Radionuclide Imaging. J Neurol Neuromedicine 2016; 1: 22-28. www.jneurology.com
- Kuriakose D, Xiao Z. Pathophysiology and Treatment of Stroke: Present Status and Future Perspectives. Int J Mol Sci 2020; 21: 7609. doi:10.3390/ijms21207609 DOI
- Easton
JDJ, AlbersGWG, CaplanLRL, et al. Discussion: Reconsideration of TIA terminology and definitions. Neurology. 2004; 62: 29-34.PubMedpubmed.ncbi.nlm.nih.gov - Deutsche Gesellschaft für Neurologie, Deutsche Schlaganfall-Gesellschaft. Akuttherapie des ischämischen Hirninfarktes. AWMF-Leitlinie Nr. 030-046. Stand 2021. www.awmf.org
- Gudmundsson L, Scher A, Aspelund T et al. Migraine with aura and risk of cardiovascular and all cause mortality in men and women: prospective cohort study. BMJ 2010;341:c3966. www.bmj.com
- Boehme A, Esenwa C, Elkind M. Stroke Risk Factors, Genetics, and Prevention. Circ Res 2017; 120: 472-495. doi:10.1161/CIRCRESAHA.116.308398 DOI
- O'Donnell MJ, Xavier D, Liu L, et al. Risk factors for ischaemic and intracerebral haemorrhagic stroke in 22 countries (the INTERSTROKE study): a case control study. Lancet 2010; 376: 112-23.
PubMed Pan A, Sun Q, Okereke OI, et al. Depression and risk of stroke morbidity and mortality: a meta-analysis and systematic review. JAMA 2011; 306: 1241-9.pubmed.ncbi.nlm.nih.govSchmidtLakatos L, Christ M,Hováth-PuhóMüllerE, Christiansen CFM, et al.Preadmission„Strokeusemimics“of–non-aspirinDifferenzialdiagnosenonsteroidaldesanti-inflammatorySchlaganfallsdrugsinandder30-day stroke mortalityNotfallmedizin.NeurologyNotfall2014Rettungsmed 2021;8324:2013-22990–996. doi:10.12121007/WNL.0000000000001024s10049-021-00877-x DOIClearySchuler L, Bolognese M, Lakatos L. Strukturierte Erkennung von Patienten mit Schlaganfall in der Notfallsituation. Notfall Rettungsmed 2021; 24: 984-989. doi:10.1007/s10049-021-00916-7 DOI- Kraft P,
ShorvonNasri S,TallisDreikornRM.Late-onsetDiagnostikseizuresundasAkuttherapieadespredictorischämischenof subsequent strokeSchlaganfalls.LancetDNP2004- Die Neurologie und Psychiatrie 2019;36320:118428-632.PubMed Bath PMW, Gray LJdoi:10.Association between hormone replacement therapy and subsequent stroke: a meta1007/s15202-analysis. BMJ 2005; 330: 342.019-2118-7PubMedLidegaard Ø, Løkkegaard E, Jensen A, Skovlund CW, Keiding N. Thrombotic stroke and myocardial infarction with hormonal contraception. N Engl J Med 2012; 366: 2257-66.New England Journal of MedicineSmeeth L, Thomas SL, Hall AJ et al. Risk of myocardial infarction and stroke after acute infection and vaccination. N Engl J Med 2004; 351: 2611-8.New England Journal of MedicineMinassian C, D'Aiuto F, Hingorani AD, Smeeth L. Invasive dental treatment and risk for vascular events: a self-controlled case series. Ann Intern Med 2010; 153: 499-506.pubmed.ncbi.nlm.nih.govStrazzulo P, D'Elia L, Kandala N-B, Cappuccio FP. Salt intake, stroke, and cardiovascular disease: a meta-analysis of prospective studies. BMJ 2009; 339: b4567.BMJ (DOI)Haynes MJ, Vincent K, Fischhoff C, et al. Assessing the risk of stroke from neck manipulation: a systematic review. Int J Clin Pract 2012; 66: 940-7.PubMedKerkhoff G. Neurovisual rehabilitation: recent developments and future directions. J Neurol Neurosurg Psychiatry 2000; 68: 691-706.PubMedEuropean Stroke Initiative Executive Commitee and Writing Committee. Recommendations for stroke management. Cerebrovasc Dis 2003; 16: 311-8.PubMedAdams H jr, Adams RJ, Brott T, et al. Guidelines for the early management of patients with ischemic stroke. a scientific statement from the Stroke Council of The American Stroke Association. Stroke 2003; 34: 1056-83.pubmed.ncbi.nlm.nih.govChalela JA, Kidwell CS, Nentwich LM, et al. Magnetic resonance imaging and computed tomography in emergency assessment of patients with suspected acute stroke: a prospective comparison. Lancet 2007; 369: 293-8.www.ncbi.nlm.nih.govRothwell PM, Giles MF, Chandratheva A, et al. Effect of urgent treatment of transient ischaemic attack and minor stroke on early recurrent stroke (EXPRESS study): a prospective population-based sequential comaprison. Lancet 2007; 370: 1432-42.www.ncbi.nlm.nih.govLuengo-Fernandez R, Gray AM, Rothwell PM. Effect of urgent treatment for transient ischaemic attack and minor stroke on disability and hospital costs (EXPRESS study): a prospective population-based sequential study. Lancet Neurol 2009; 8: 235-43.www.ncbi.nlm.nih.govSaunders DH, Greig CA, Mead GE. Physical activity and exercise after stroke: review of multiple meaningful benefits. Stroke. 2014;45(12):3742-7.www.ncbi.nlm.nih.gov- Stroke Unit Trialists' Collaboration. Organised inpatient (stroke unit) care for stroke. Cochrane Database Syst Rev. 2013 Sep 11;9:CD000197.
doi: 10.1002/14651858.CD000197.pub3.DOI Drummond AE, Pearson B, Lincoln NB, Berman P. Ten year follow-up of a randomised controlled trial of care in a stroke rehabilitation unit. BMJ 2005; 331: 491-2.British Medical JournalRoffe C, Nevatte T, Sim J, et al. Effect of routine low-dose oxygen supplementation on death and disability in adults with acute stroke. The Stroke Oxygen Study Randomized Clinical Trial. JAMA 2017; 318: 1125-35. doi:10.1001/jama.2017.11463DOIHajat C, Hajat S, Sharma P. Effects of poststroke pyrexia on stroke outcome: a meta-analysis of studies in patients. Stroke 2000; 31: 410-4.pubmed.ncbi.nlm.nih.govIndredavik B, Fjærtoft H, Ekeberg G, Løge A, Mørch B. Benefit of an extended stroke unit service with early supported discharge. A randomized controlled trial. Stroke 2000; 31: 2989-94.pubmed.ncbi.nlm.nih.govAhmed N, Wahlgren N, Grond M, et al. Implementation and outcome of thrombolysis with alteplase 3-4,5 h after an acute stroke: an updated analysis from SITS-ISTR. Lancet Neurol 2010; 9: 866-74.PubMedWardlaw JM, Murray V, Berge E, et al. Thrombolysis for acute ischaemic stroke. Cochrane Database Syst Rev. 2014, 7.pubmed.ncbi.nlm.nih.govGumbinger C, Reuter B, Stock C, et al. Time to treatment with recombinant tissue plasminogen activator and outcome of stroke in clinical practice: retrospective analysis of hospital quality assurance data with comparison with results from randomised clinical trials. BMJ 2014; 348: g3429. doi:10.1136/bmj.g3429DOIWardlaw JM, Murray V, Berge E et al. Recombinand tissue plasminogen activator for acute stroke: an updated systematic review and meta-analysis. Lancet 2012;379:2364-72.www.ncbi.nlm.nih.gov- Berkhemer OA, Fransen PSS, van den Berg LA, et al. A randomized trial of intraarterial treatment for acute ischemic stroke. N Engl J Med 2014. doi:10.1056/NEJMoa1411587 DOI
- Goyal M, Demchuk AM, Menon BK, et al for the ESCAPE Trial Investigators. Randomized assessment of rapid endovascular treatment of ischemic stroke. N Engl J Med 2015. doi:10.1056/NEJMoa1414905 DOI
- Campbell BCV, MitchellPJ, Kleinig TJ, et al for the EXTEND-IA Investigators. Endovascular therapy for ischemic stroke with perfusion-imaging selection. N Engl J Med 2015. doi:10.1056/NEJMoa1414792 DOI
Saver J, Goyal M, Bonafe A, et al for the SWUFT PRIME Investigators. Primary results. Nashville, february 2015.my.americanheart.org- Jovin TG, Chamorro A, Cobo E, et al. Thrombectomy within 8 Hours after Symptom Onset in Ischemic Stroke. N Engl J Med 2015. doi:DOI: 10.1056/NEJMoa1503780 DOI
TheDeutscheISTGesellschaft für Neurologie, Deutsche Schlaganfall-3 collaborative groupGesellschaft.TheSekundärprophylaxebenefitsischämischerandSchlaganfallharmsundoftransitorischeintravenousischämischethrombolysisAttackewith–recombinantTeiltissue plasminogen activator within 6 h of acute ischaemic stroke (the third international stroke trial (IST-3))1:aPlättchenhemmer,randomisedVorhofflimmern,controlledHypercholesterinämietrialund Hypertonie.LancetAWMF-Leitlinie2012 Jun 23; 379 (9834): 2352-63Nr.pmid:030-133.22632908Stand 2022.PubMedPowers WJ, Derdeyn CP, Biller J, et aldgn.2015 AHA/ASA focused update of the 2013 guidelines for the early management of patients with acute ischemic stroke regarding endovascular treatment. Stroke 2015. doi:10.1161/STR.0000000000000074DOIAlbers GW, Marks MP, Kemp S, et al. Thrombectomy for Stroke at 6 to 16 Hours with Selection by Perfusion Imaging. New Engl J Med 2018 Feb 22; 378(8): 708-718. pmid:29364767PubMedorg- Deutsche Gesellschaft für Allgemeinmedizin und Familienmedizin: Neue Thrombozyten-Aggregationshemmer. Einsatz in der Hausarztpraxis. DEGAM-Leitlinie. AWMF-Leitlinie Nr. 053-041. S2e. Stand 2019 www.awmf.org
RahmanGe F, Lin H,KhanLiuS,YNasiretF, Meyer M, Kaluski Eal.OptimalDual antiplatelet therapy after stroke or transient ischaemic attack – how long to treat? The duration of aspirin plus clopidogrelafterinischemicstroke or transient ischaemic attack: a systematic review and meta-analysis Eur J Neurol. 2016;23:1051-7. pubmed.ncbi.nlm.nih.gov- Johnston C, Amarenco P, Albers G et al for the SOCRATES Steering Committee and Investigators. Ticagrelor versus Aspirin in acute stroke or transient ischemic attack.
ANsystematicEnglreviewJandMedmeta2016;375:35-analysis. Stroke 2019;50:947-95343. www.ahajournalsnejm.org NiJohnstonChroinin DC,AsplundAmarencoKP,AsbergDenisonSH, et al.Statinfortherapythe THALES Investigators. Ticagrelor andoutcomeaspirinafteror aspirin alone in acute ischemic stroke:systematicorreview and meta-analysis of observational studies and randomized trialsTIA.StrokeN2013.EnglpmidJ Med 2020;383:23287777PubMedHeart Protection Study Collaborative Group. MRC/BHF Heart Protection Study of cholesterol207-lowering with simvastatin in 5963 people with diabetes: a randomised placebocontrolled trial. Lancet 2003; 361: 2005–1617. www.ncbinejm.nlm.nih.govorg- Amarenco P, Bogousslawsky J, Callahan A, et al. The Stroke Prevention by Aggressive Reduction in Cholesterol Levels (SPARCL) Investigators
High-Dose Atorvastatin after Stroke or Transient Ischemic Attack. N Engl J Med 2006;355549:549-59. www.nejm.org ManktelowFurbergBNC,Potter JF Interventions in the management of serum lipids for preventing stroke recurrence. The Cochrane Library 2009, Issue 3.www.ncbi.nlm.nih.govLiu N, Cadilhac DA, Andrew NE, et al. Randomized controlled trial of early rehabilitation after intracerebral hemorrhage stroke: difference in outcomes within 6 months of stroke. Stroke. 2014 Dec;45(12):3502-7.PubMedLegg LA, Drummond AE, Langhorne P. Occupational therapy for patients with problems in activities of daily living after stroke. Cochrane Database of Systematic Reviews 2006: 4: CD003585. doi:10.1002/14651858.CD003585.pub2.europepmc.orgLanghorne P, Taylor G, Murray G et al. Early supported discharge services for stroke patients: a meta-analysis of individual patients' data. Lancet 2005; 365: 501-6.PubMedGorelick P, Sacco RL, Smith DB et al. Prevention of a first stroke. A review of guidelines and a multidisciplinary consensus statement from the national stroke asssociation. JAMA 1999; 281:1112-20.www.researchgate.netLip G, Nieuwlaat R, Pisters R, Lane D, Crijns H. Refining Clinical Risk Stratification for Predicting Stroke and Thromboembolism in Atrial Fibrillation Using a Novel Risk Factor-Based Approach The Euro Heart Survey on Atrial Fibrillation. CHEST 2010; 137(2):263–272).www.ncbi.nlm.nih.govFriberg L, Rosenqvist M, Lip G. Evaluation of risk stratification schemes for ischaemic stroke and bleeding in 182 678 patients with atrial fibrillation: the Swedish Atrial Fibrillation cohort study. European Heart Journal (2012) 33, 1500–1510.www.ncbi.nlm.nih.govOlesen JB, Lip GYH, Hansen ML, et al. Validation of risk stratification schemes for predicting stroke and thromboembolism in patients with atrial fibrillation: nationwide cohort study . BMJ 2011; 342: d124.BMJ (DOI)Hobbs FD, Roalfe AK, Lip GY, et al. Performance of stroke risk scores in older people with atrial fibrillation not taking warfarin: comparative cohort study from BAFTA trial. BMJ 2011; 342: d3653.BMJ (DOI)Friberg L, Skeppholm M, Terènt M. Benefit of anticoagulation unlikely in patients with atrial fibrillation and a CHA2DS2-VASc score of 1. J Am Coll Cardiol 2015: 27; 65:225. PMID: 25614418PubMedDeutsche Gesellschaft für Allgemeinmedizin und Familienmedizin. Neue orale Antikoagulantien (bei nicht valvulärem Vorhofflimmern). AWMF-Registernr. 053/031. S1, Stand 2013.www.degam.deWang Y, Wang Y, Zhao X, et al. Clopidogrel with aspirin in acute minor stroke or transient ischemic attack. N Engl J Med 2013.www.nejm.orgLee M, Saver JL, Hong KS, et al. Risk-Benefit Profile of Long-Term Dual- Versus Single-Antiplatelet Therapy Among Patients With Ischemic Stroke: A Systematic Review and Meta-analysis. Ann Intern Med 2013 Oct 1;159(7):463-470.PubMedKwok CS, Shoamanesh A, Copley HC, et al. Efficacy of antiplatelet therapy in secondary prevention following lacunar stroke: pooled analysis of randomized trials. Stroke 2015; 46: 1014-23. doi:10.1161/STROKEAHA.114.008422DOIGouya G, ArrichWright J,WolztDavisM, et al. Antiplatelet treatment for prevention of cerebrovascular events in patients with vascular diseases: a systematic review and meta-analysis. Stroke 2014 Feb;45(2):492-503.PubMedGeeganage CM, Diener HC, Algra AB et al for theacuteALLHATantiplatelet stroke trialists collaborationofficers.DualMajor outcomes in high-risk hypertensive patients randomized to angiotensin-converting enzyme inhibitor ormonocalciumantiplateletchanneltherapyblockerforvspatients with acute ischemic stroke or transient ischemic attack: systematic review and meta-analysis of randomized controlled trialsdiuretic.Stroke2012JAMA 2002;43288:10582981-6697. pubmed.ncbi.nlm.nih.govZhou YH, Wei X, Lu J et al. Effects of combined aspirin and clopidogrel therapy on cardiovascular outcomes: a systematic review and metaanalysis. PLoS One 2012;7:e31642.journals.plos.orgPalacio S, Hart RG, Pearce LA, et al. Effect of addition of clopidogrel to aspirin on mortality: systematic review of randomized trials. Stroke. 2012;43:2157-62.www.ncbi.nlm.nih.govBundesärztekammer (BÄK), Kassenärztliche Bundesvereinigung (KBV), Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften (AWMF). Nationale VersorgungsLeitlinie Therapie des Typ-2-Diabetes – Langfassung, 1. Auflage. Version 4. 2013, zuletzt geändert: November 2014.www.awmf.org- Deutsche Gesellschaft für Allgemeinmedizin (DEGAM). Leitlinie: Hausärztliche Risikoberatung zur kardiovaskulären Prävention. S3, Stand 2017 www.
degamawmf.de Mead GE, Hsieh CF, Lee R, et al. Selective serotonin reuptake inhibitors (SSRIs) for stroke recovery. Cochrane database of Systematic Reviews 2012; 11: CD009286.Cochrane (DOI)Mortensen JK, Larsson H, Johnsen SP, et al. Post stroke use of selective serotonin reuptake inhibitors and clinical outcome among patients with ischemic stroke: a nationwide propensity score-matched follow-up study. Stroke 2013 Feb;44(2):420-6. doi: 10.1161/STROKEAHA.112.674242.DOIorg- Deutsche Gesellschaft für Neurologie, Deutsche Schlaganfall-Gesellschaft.
Schlaganfall:Sekundärprophylaxe ischämischer Schlaganfall und transitorische ischämische Attacke – Teil 2: Lebensstil, arterielle Stenosen, andere Antithrombotika-Indikationen, Hormone, Diabetes mellitus, Schlafapnoe. AWMF-Leitlinie Nr. 030-133,143. Stand20152022. dgn.org - Siegmar N, von Büdigen H. Lebenserwartung und Prognose nach einem Schlaganfall. Schlaganfall Begleitung, Zugriff 01.08.22. schlaganfallbegleitung.de
- Jauch E. Ischemic stroke. Medscape, updated Jul 14, 2022. Zugriff 01.08.22 emedicine.medscape.com
- Prognose und Verlauf bei Schlaganfall. Neurologen und Psychiater im Netz. Zugriff 01.08.22. www.
awmfneurologen-und-psychiater-im-netz.org UdellKunzJAJ,ZawivonR,BüdigenBhatt DL, et alH.Association between influenza vaccination and cardiovascular outcomes in highSchlaganfall-risk patients: a meta-analysisNachsorge.JAMAZugriff2013 Oct 23;310(16):1711-2001.08.22.PubMedDeutsche Gesellschaft für Neurologie. Diagnostik und Therapie von Gedächtnisstörungen. AWMF-Leitlinie Nr. 030-124. Stand 2020www.awmf.orgSnaphaan L, de Leeuw FE. Poststroke memory function in nondemented patients: a systematic review on frequency and neuroimaging correlates. Stroke 2007; 38: 198-203.PubMedThe CLOTS Trials Collaboration. Effectivness of thigh-length graduated compression stockings to reduce the risk of deep vein thrombosis after stroke (CLOTS trial 1): a multicentre, randomised controlled trial. Lancet 2009; 373: 1958-65.PubMedOldenbeuving AW, de Kort PL, Jansen BP, et al. Delirium in the acute phase after stroke: Incidence, risk factors, and outcome. Neurology 2011; 76: 993-9.pubmed.ncbi.nlm.nih.govPendlebury ST, Rothwell PM, Oxford Vascular Study. Incidence and prevalence of dementia associated with transient ischaemic attack and stroke: analysis of the population-based Oxford Vascular Study. Lancet Neurol 2019; 18: 248-58. pmid:30784556PubMedJames P, Ellis CJ, Whitlock RML et al. Relation between troponin T concentration and mortality in patients presenting with an acute stroke: observational study. BMJ 2000; 320:1502-4.pubmed.ncbi.nlm.nih.govBonarenco P, Lavallée PC, Labreuche J et al for the TIAregistry.org Investigators, One-year risk of stroke after transient ischemic attack or minor stroke. NEJM 2016;374:1533-42.www.nejm.orgAmarenco P, Lavallée PC, Labreuche J et al., for the TIAregistry.org Investigators. One-Year Risk of Stroke after Transient Ischemic Attack or Minor Stroke. NEJM 2016; 374(16): 1533-42. pmid:27096581PubMedGesundheitsfragebogen für Patienten (PHQ-D). Universitätsklinikum Heidelberg, 2002.www.klinikum.uni-heidelbergschlaganfallbegleitung.deEriksson M, Glader E-L, Norrving B, Asplund K. Poststroke suicide attempts and completed suicides. Neurology 2015. doi:10.1212/WNL.0000000000001514DOI
Autor*innen
CarolineMichaelBeierHandke,DrProf.med. Fachärztin für Allgemeinmedizin, HamburgDirk Nonhoff,Dr. med., Facharzt fürAllgemeinmedizinInnere Medizin,KölnKardiologie und Intensivmedizin, Freiburg i. Br.- Günther Egidi, Dr. med., Arzt für Allgemeinmedizin, Bremen (Review)
Ehemalige- Die
Autor*innenBentursprünglicheIndredavikVersion dieses Artikels basiert auf einem entsprechenden Artikel im norwegischen hausärztlichen Online-Handbuch Norsk Elektronisk Legehåndbok (NEL,drhttps://legehandboka.medno/)., seksjonsoverlege, seksjon for hjerneslag, Medisinsk avdeling, St. Olavs Hospital, TrondheimIngard Løge, spesialist i allmennmedisin, redaktør NEL
- Bei jungen Frauen ist das