Allgemeine Informationen
Definition
- Eine Epilepsie ist eine Erkrankung des Gehirns, die durch eine der folgenden Bedingungen definiert ist (laut aktueller Definition der Internationalen Liga gegen Epilepsie, ILAE):1
- Mindestens 2 nicht provozierte Anfälle oder Reflexanfälle (s. u.), die im Abstand von mehr als 24 Stunden auftreten.
- Ein nicht provozierter Anfall oder Reflexanfall verbunden mit einer Wahrscheinlichkeit, während der nächsten 10 Jahre weitere Anfälle zu erleiden, die vergleichbar ist mit dem allgemeinen Rückfallrisiko (mindestens 60 %) nach 2 nicht provozierten Anfällen.
- Diagnose eines Epilepsie-Syndroms
- Eine Epilepsie gilt unter folgenden Voraussetzungen als überwunden:1
- Bei Patient*innen mit einem altersabhängigen Epilepsie-Syndrom, die jenseits des entsprechenden Alters sind.
- Bei Patient*innen, die mindestens 10 Jahre anfallsfrei sind und seit mindestens 5 Jahren keine Antiepileptika mehr einnehmen.
- Kritik der Leitlinienkommission der Deutschen Gesellschaft für Neurologie2
- „Diese neue Definition ist deshalb nicht ganz befriedigend, weil ein Rezidivrisiko von 60 % in vielen Fällen durch entsprechende Studien nicht belegt ist.“
- „Für eine operative Umsetzung der Definition gilt daher die in der Leitlinie gegebene Empfehlung für den Beginn der Therapie nach einem ersten (unprovozierten) Anfall. Dies ist vor allem ein wichtiger Aspekt beim Abschluss von Versicherungen.“
- „Die Definition, wann eine Epilepsie als überwunden gelten kann, basiert nicht auf Evidenz. Es liegen zurzeit keine Studien vor, wie hoch das Rezidivrisiko ist bei Menschen, die mindestens 10 Jahre anfallsfrei sind, davon mindestens 5 Jahre ohne Antiepileptika.“
- „Problematisch ist auch das Beenden einer Epilepsietherapie. Hier suggeriert die neue Definition, dass Epilepsie 'ausheilen' kann, ohne dass dafür – abgesehen von bestimmten Epilepsien in der Kindheit – Evidenzen bestehen.“
- „Eine praktische operative Handlungsweise oder therapeutische Konsequenzen lassen sich aus der Definition nicht ableiten.“
Epileptischer Anfall
- Vorübergehendes Auftreten neurologischer Symptome aufgrund einer pathologisch exzessiven oder synchronen neuronalen Aktivität im Gehirn1-2
- Epileptische Anfälle werden in generalisierte und fokale (partielle) Formen eingeteilt.
- Reflexanfall: Anfall, der durch sensorische Reize provoziert wurde, z. B.:
- Flackerlicht
- Geräusche, Lärm, Musik
- propriozeptive Reize
- somatosensorische Reize.
Generalisierte Anfälle1-2
- Gemeinsame Merkmale
- Primär generalisierte Anfälle sind nicht verbunden mit einem fokalen Beginn oder einer Aura.
- Es kommt häufig zu Bewusstseinsstörungen.
- Motorisch
- tonisch-klonisch (früher „Grand-mal-Anfälle“)
- klonisch
- tonisch
- myoklonisch-tonisch-klonisch
- myoklonisch-atonisch
- atonisch
- epileptische Spasmen
- Nichtmotorisch (Absencen)
- typisch (früher „Petit-mal-Anfälle“)
- atypisch
- myoklonisch
- Augenlid-Myoklonien
Fokale Anfälle (früher auch „partielle Anfälle“)1-2
- Nach Bewusstseinsstatus
- mit erhaltenem Bewusstsein
- nach früherer Klassifikation weiter unterteilt in Anfälle mit sichtbaren motorischen oder autonomen Komponenten (einfache partielle Anfälle) und Anfälle mit nur subjektiven sensorischen oder psychischen Phänomenen (Aura)
- mit eingeschränktem Bewusstsein
- mit erhaltenem Bewusstsein
- Nach Beginn
- Beginn mit motorischen Symptomen
- Automatismen
- atonisch
- klonisch
- epileptische Spasmen
- hyperkinetisch
- myoklonisch
- tonisch
- Beginn mit nicht-motorischen Symptomen
- autonome Symptome
- Verhaltensarrest
- kognitiv
- emotional
- sensorisch
- von fokal zu bilateral tonisch-klonisch
- früher: „sekundär generalisiert tonisch-klonisch“
- Beginn mit motorischen Symptomen
- Mit unklarem Beginn
- motorisch
- tonisch-klonisch
- epileptische Spasmen
- nicht-motorisch
- Verhaltensarrest
- motorisch
- Unklassifizierbar
Status epilepticus3
- Epileptischer Anfall, der länger als 5 min anhält oder mehrere aufeinander folgende epileptische Anfälle über einen Zeitraum > 5 min ohne zwischenzeitliche Wiedererlangung des vorbestehenden neurologischen Befundes.
- Näheres siehe Artikel Status epilepticus.
Häufigkeit
- Prävalenz2,4-5
- Beträgt ca. 0,5‒1,0 %, d. h. in Deutschland gibt es ca. 400.000‒800.000 Personen mit Epilepsie.
- Etwa 4‒10 % der Bevölkerung hat irgendwann im Verlauf des Lebens einen epileptischen Anfall. Meist sind das einmalige Anfallsereignisse im Kindesalter, etwa Fieberkrämpfe oder andere symptomatische Anfälle infolge einer akuten Erkrankung. Bei etwa 1 % aller 20-Jährigen wird letztlich die Diagnose Epilepsie gestellt.
- Inzidenz5
- Die Inzidenz liegt in Deutschland bei etwa 40 neuen Fällen pro 100.000 jährlich, d. h. ca. 30.000 Neuerkrankungen.
- Alter5
- Epilepsie kommt in allen Altersgruppen vor. Am höchsten ist die Inzidenz bei unter 5-Jährigen und über 60-Jährigen.
- Art der Epilepsie4-5
- Bei etwa 1/3 der Erwachsenen sind erstmalig aufgetretene Anfälle primär generalisiert.
- Fokale Epilepsien machen etwa 2/3 der Fälle aus, etwa 80 % davon mit sekundärer Generalisierung.
- Bei Kindern unter 5 Jahren sind neu aufgetretene Anfälle meist generalisiert, danach zu mehr als der Hälfte fokal.
Ätiologie und Pathogenese
- Die Klassifikation der ILAE teilt Epilepsien nach Ursachen ein:1-2
- genetisch
- strukturell
- infektionsbedingt
- metabolisch
- immunologisch
- unbekannt (früher „kryptogen“).
- Bei Epilepsie spielt Vererbung eine Rolle, jedoch nicht bei allen Epilepsiearten gleich ausgeprägt. Es gibt monogene, polygene und multifaktorielle Epilepsien.
- Häufig lässt sich keine eindeutige Ursache feststellen (in 25‒30 % der Fälle).
- Nachweisbare Ursachen sind morphologische Anomalien im Gehirn oder metabolische Störungen, doch häufig ist die Ätiologie multifaktoriell bedingt.
- Mentale oder kognitive Funktionseinschränkungen sind bei 1/3 der Kinder und 1/4 der Erwachsenen mit Epilepsie festzustellen.
- Bei Kindern kommt es häufig zu einer Zerebralparese (20 %).
- Alle Formen von Hirnschädigungen können ‒ oft mit vielen Jahren Latenz ‒ eine sekundäre Epilepsie verursachen. Kopfverletzungen mit Schädel-Hirn-Trauma erhöhen das Risiko für Epilepsie um den Faktor 2‒7. Auch 10 Jahre danach besteht immer noch ein signifikant erhöhtes Risiko.2
Alter2,4-5
- Die Ursachen von Epilepsie variieren abhängig vom Alter der Patient*innen.
- Bei Kindern und Jugendlichen
- dominieren Geburtsschäden und angeborene Erkrankungen des Nervensystems.
- Bei Erwachsenen
- sind Epilepsien häufiger die Folge von Kopfverletzungen und Hirntumoren.
- Bei älteren Menschen
- zählen zerebrovaskuläre Erkrankungen und neurodegenerative Krankheiten zu den häufigen Ursachen.
Pathophysiologie2
- Tendenz zur synchronisierten Hyperaktivierung von Hirnzellen
- Tendenz, dass eine solche Hyperaktivierung ungewöhnlich lang anhält und sich auf angrenzende Gehirnareale ausbreitet, sodass es zu einem Anfall kommt.
Temporallappen-Epilepsie2,5
- Eine Sonderform der fokalen Epilepsie (lokalisiert, partiell), die altersunabhängig jederzeit beginnen kann.
- Die Erkrankung wird als Ergebnis einer fokalen Hirnanomalie definiert.
- Eine mesiotemporale Sklerose im Hippocampus ist die häufigste zugrunde liegende Ursache für eine Temporallappen-Epilepsie.
- Fieberkrämpfe in der Kindheit könnten möglicherweise eine Prädisposition darstellen.
- Es handelt sich um eine Erkrankung, die zahlreiche andere Krankheitszustände imitieren kann. Etwa 1/3 der Patient*innen entwickelt generalisierte Krampfanfälle zusätzlich zu komplex fokalen Anfällen.
Frontallappen-Epilepsie
- Die Anfälle treten dabei häufig im Schlaf auf und sind von kurzer Dauer. Sie können auch in Anfallsserien auftreten. Oft kommt es zu motorischen und verbalen Symptomen.
- Ist der Epilepsieherd in der Zentralfurche lokalisiert, sind fokale Zuckungen ohne „Wanderung“ (Jackson-Marsch) festzustellen.
- Es kann zu bizarren Anfallausformungen mit heftigen motorischen Automatismen kommen, wie sexuell anmutende Hüftbewegungen oder Radfahrbewegungen mit den Beinen, häufig begleitet von Grunzen oder Schnauben etc.
- Die Betroffenen sind dabei in der Regel bei Bewusstsein.
- Häufig lässt sich ein nächtlicher Fronttallappen-Anfall nur schwer von Parasomnien oder anderen Schlafstörungen unterscheiden.
- Bei Parasomnien liegt meist eine positive Familienanamnese vor.
- Sie lassen im Erwachsenenalter nach, es kommt dann nachts weniger häufig zu Anfällen.
- Sie werden durch Schlafmangel ausgelöst.
- Ihr motorischer Ablauf ist komplexer und variabler als bei Frontallappen-Epilepsien.
Parietallappen-Epilepsie
- Derartige Anfälle können sich in Form von fokaler Taubheit, Schmerzen, Bewegungsdrang in einem Körperteil, einem Gefühl von fehlenden Gliedmaßen, Vertigo oder Übelkeit äußern.
- Anfälle im dominanten Parietallappen können zu Sprachstörungen führen.
Okzipitallappen-Epilepsie
- Diese Anfälle lösen vor allem verschiedene Arten von Sehstörungen oder Bewegungen von Auge oder Augenlid aus.
Epileptische Anfälle mit Primärursache außerhalb des Hirns
- Hypoxie, etwa bei kardialer oder vaskulärer Ursache
- Elektrolytstörungen
- Metabolische Störungen
- Intoxikationen
- Medikamente
- Drogen- oder Alkoholentzug
- Fieber
- Erkrankungen und Verletzungen, die zu einer Beeinträchtigung der Hirnfunktion führen können.
Prädisponierende Faktoren
Erhöhtes Risiko für eine spätere Epilepsie2,4-5
- Schlaganfall (alle Altersgruppen) 10 %
- Schlaganfall (bei Älteren) 30‒40 %
- Angeborene Hirnschädigung 10 %
- Kopfverletzungen 5‒10 %
- Das relative Risiko (RR) bei Kindern und jungen Erwachsenen nach leichten Schädeltraumata betrug in einer dänischen Kohortenstudie 2,2 und nach schweren Schädeltraumata 7,4.
- Nach 10 Jahren besteht ein geringeres, aber weiterhin erhöhtes Risiko: RR 1,5 und 4,2 nach leichten bzw. schweren Kopftraumata.
- Tumoren 5 %
- Degenerative Erkrankungen < 5 %
- Infektionen < 5 %
- Fieberkrämpfe erhöhen das Risiko für eine spätere Entwicklung von Epilepsie.
- Vererbung
- Soziale Deprivation
- Bei sozial und wirtschaftlich schlechter gestellten Personen scheint Epilepsie häufiger vorzukommen.
Auslösende Faktoren2,4-5
- Schlafmangel
- Alkohol: Überkonsum oder plötzliche Abstinenz
- Hypoglykämie
- Photostimulation
- Stress
- Hyperventilation
ICPC-2
- N88 Epilepsie
ICD-10
- Nach ICD-10-GM Version 20216
- G40 Epilepsie
- G40.0 Lokalisationsbezogene (fokale) (partielle) idiopathische Epilepsie und epileptische Syndrome mit fokal beginnenden Anfällen
- G40.1 Lokalisationsbezogene (fokale) (partielle) symptomatische Epilepsie und epileptische Syndrome mit einfachen fokalen Anfällen
- G40.2 Lokalisationsbezogene (fokale) (partielle) symptomatische Epilepsie und epileptische Syndrome mit komplexen fokalen Anfällen
- G40.3 Generalisierte idiopathische Epilepsie und epileptische Syndrome
- G40.4 Sonstige generalisierte Epilepsie und epileptische Syndrome
- G40.5 Spezielle epileptische Syndrome
- G40.6 Grand-Mal-Anfälle, nicht näher bezeichnet (mit oder ohne Petit-Mal)
- G40.7 Petit-Mal-Anfälle, nicht näher bezeichnet, ohne Grand-Mal-Anfälle
- G40.8 Sonstige Epilepsien
- G40.9 Epilepsie, nicht näher bezeichnet
- G41 Status epilepticus
- G41.0 Grand-Mal-Status
- G41.1 Petit-Mal-Status
- G41.2 Status epilepticus mit komplexfokalen Anfällen
- G41.8 Sonstiger Status epilepticus
- G41.9 Status epilepticus, nicht näher bezeichnet
Diagnostik
Diagnostische Kriterien
Einzelanfall
- Ausgehend von nur einem Anfall ist keine Epilepsie-Diagnose möglich.
- Typische Krankengeschichte mit Schilderung des Anfalls durch Augenzeugen
- Ggf. Befunde, die morphologische Anomalien oder zerebrale Funktionsstörungen bestätigen.
- Keine Anzeichen für andere Ursachen
Epilepsie
- Wie beim Einzelanfall, zusätzlich eindeutige Belege für wiederholte Anfälle
Differenzialdiagnosen
- Es kommt häufig zu Fehldiagnosen. Mehrere Studien deuten darauf hin, dass etwa 1/3 der von Anfällen Betroffenen fälschlicherweise die Diagnose Epilepsie erhält.2,4-5
- Folgende Differenzialdiagnosen sind in Betracht zu ziehen:2,4-5
- Synkope
- psychogene nicht-epileptische Anfälle
- zerebrovaskuläre Erkrankung, TIA oder Schlaganfall
- kardiovaskuläre Erkrankung, Arrhythmie
- Migräne (z. B. Basilaris-Migräne)
- Schlafstörungen
- Hypoglykämie
- neurologisch bedingte Bewegungsstörungen
- nächtliche Albträume
- Hyperventilation
- Narkolepsie
- andere neurologische und psychiatrische Erkrankungen
- motorische Stereotypien zur Selbststimulation, etwa bei Autismus oder Intelligenzminderung.
Anamnese
- Es ist wichtig, den Verlauf der Anfälle zu dokumentieren, da dieser für die Behandlung von Bedeutung ist.
Häufige Anfallsformen1-2,4-5
- Generalisierter tonisch-klonischer Anfall (GTKA, früher: Grand mal)
- plötzlicher Bewusstseinsverlust und Sturz, dann tonische und danach klonische Krämpfe
- Während des Anfalls sind eine Zyanose und evtl. Zungenbisse und/oder der Abgang von Exkrementen zu beobachten.
- Ein Anfall dauert in der Regel 0,5‒5 min, in etwa 90 % der Fälle länger als 2 min.
- Wenn die Person wieder zu sich kommt, ist sie oft desorientiert und müde. Manche schlafen nach dem Anfall ein.
- Über die Zeit vor dem Anfall liegt eine Amnesie vor.
- Manchmal erlebt die betroffene Person kurz vor dem Bewusstseinsverlust eine Aura, an die sie sich oft auch noch danach erinnert.
- Typischer generalisierter nichtmotorischer Anfall (früher: Absencen, Petit mal)
- plötzlicher Bewusstseinsverlust ohne Tonusänderungen oder Krampfanfälle
- Die betroffene Person fällt nicht, wirkt aber abwesend, hat einen starren Blick, verliert den Faden in der Konversation.
- Es kann zu kleinen Zuckungen oder Blinzeln kommen.
- Der Anfall dauert 0,5‒2 min, und es kommt zu einer Amnesie für die Zeit vor dem Anfall.
- meist sehr häufige Anfälle, in einigen Fällen zahlreiche Anfälle täglich
- selten bei Erwachsenen
- Generalisierter nichtmotorischer myoklonischer Anfall (früher: myoklonisch-atonisch oder -astatisch)
- lokalisierte Myoklonien und Sturz aufgrund eines plötzlichen Tonusverlustes
- Das Bewusstsein bleibt meist erhalten.
- charakteristische Epilepsieform bei Kindern
- Einzelne fokale (früher: partielle) Anfälle
- z. B. stationäre Zuckungen in einem Körperteil
- Der Anfall kann einige Minuten andauern, hin und wieder auch länger, wie bei einem fokalepileptischen Status.
- Die Betroffenen sind meist bei vollem Bewusstsein.
- Fokale Anfälle mit Bewusstseinseinschränkung (früher: komplexe partielle Anfälle)
- unterschiedliche Grade der Bewusstseinstrübung: Die Betroffenen reagieren bis zu einem gewissen Grad auf ihre Umwelt oder sind gar nicht ansprechbar.
- evtl. Automatismen und auffällige Verhaltensmuster
- evtl. zu Beginn spontane Geruchs- oder Geschmackssensationen oder Déjà-vu
- Fokale Anfälle, Beginn mit autonomen Symptomen
- z. B. bei Temporallappenepilepsie (s. o.)
- oft mit leichter, von der betroffenen Person unbemerkter Bewusstseinseinschränkung
- vegetative Symptome, z. B.:
- Übelkeit
- plötzliche Verdauungsbeschwerden
- Blutdruckschwankungen
- Erröten
- Palpitationen.
- evtl. begleitet oder gefolgt von motorischen epileptischen Symptomen
- Die Symptome können von Anfall zu Anfall variieren.
- Gedächtnisstörungen oder andere kognitive Störungen während oder nach den Anfällen können die Diagnose erschweren, weil die Betroffenen die Symptome uneindeutig wiedergeben.
- Erscheinung und Verhalten der Person ändern sich im Vergleich zu vor dem Anfall.
- Wird immer wieder als psychische Störung fehlinterpretiert.
- Umstritten ist, ob zwischen Temporallappen-Epilepsie und neurologischen Funktionsstörungen oder psychischen Symptomen ein unmittelbarer Zusammenhang, unabhängig von evtl. begleitenden strukturellen Hirnschäden besteht.
Status epilepticus
- Wiederholte Anfälle, ohne dass die betroffene Person zwischen den Anfällen zu Bewusstsein kommt.
- Ein potenziell lebensbedrohlicher Zustand
- Folgen die Anfälle dicht aufeinander, kommt die betroffene Person jedoch dazwischen zu Bewusstsein, spricht man von Anfallsserien. Diese können in einen Status epilepticus übergehen und sind daher ebenfalls als ernste Erkrankung einzustufen.
Anamnese
- Sollte möglichst detaillierte Informationen zum Erscheinungsbild des Anfalls enthalten.
- Zeit kurz vor dem Anfall/den Anfällen?
- Beginn und Entwicklung des Anfalls, postiktale Phase?
- Gab es bestimmte anfallsauslösende Faktoren?
- Genetik?
- Frühere Verletzungen?
- Erkrankungen, die Epilepsie verursachen können?
- Psychosozialer Zustand?
Komorbidität
- Zahlreiche andere gleichzeitig auftretende Erkrankungen können die Bewertung der Epilepsie und die Planung einer Therapie erschweren, z. B.:
- Lernschwierigkeiten
- anhaltende neurologische Schädigungen
- progressive Erkrankungen
- psychische Störungen
- internistische Erkrankungen, vor allem bei älteren Menschen.
Klinische Untersuchung
- Während des Anfalls
- Evtl. Blickdeviation in Richtung des epiletogenen Herds: „Patient*in schaut ihren/seinen Herd an.“
- evtl. invertierte Plantarreflexe
- Unmittelbar nach dem Anfall
- evtl. Bewusstseinstrübung unterschiedlichen Ausmaßes, häufig Somnolenz
- Müdigkeit
- nach tonisch-klonischem Anfall: Muskelschmerzen (Muskelkater)
- Im anfallsfreien Intervall
- evtl. neurologische Auffälligkeiten
Ergänzende Untersuchungen in der Hausarztpraxis
Diagnostik bei Spezialist*innen
- Bei jedem Verdacht auf Epilepsie
- Ggf. infrage kommende Untersuchungen:2-3,5,7
- EEG, Schädel-MRT oder ggf. -CT
- Bei 80 % der Patient*innen mit therapierefraktärer fokaler Epilepsie ist es möglich, mithilfe einer MRT strukturelle Anomalien zu identifizieren.
- Serum-Prolaktin
- Wird bei generalisierten, seltener auch bei fokalen Anfällen freigesetzt.
- Absencen und dissoziative Anfälle gehen nicht mit einem erhöhten Prolaktin einher.
- Kann helfen, zwischen psychogenem und epileptischem Anfall zu differenzieren.
- Prolaktin kann auch nach hypoxischem Ereignis oder sogar nach einer Synkope erhöht sein.
- Blutentnahme innerhalb von 10‒20 Minuten nach dem Anfall
- Der Test wird manchmal eingesetzt, um einen epileptischen Anfall von einem psychogenen nicht-epileptischen Anfall (PNEA) zu unterscheiden.
- Die Bewertung falsch positiver und falsch negativer Befunde ist schwierig; sie sollte daher durch erfahrene Epileptolog*innen erfolgen.
- Wird bei generalisierten, seltener auch bei fokalen Anfällen freigesetzt.
- Autoantikörper in Serum und Liquor
- Um eine Autoimmun- bzw. limbische Enzephalitis auszuschließen.
- Gentests?
- Zur Planung eines epilepsiechirurgischen Eingriffs: neuropsychologische Testung, z. B. Wada-Test
EEG2-3,5,7
- Bei Verdacht auf Epilepsie: Untersuchung mit der höchsten Spezifität
- Ein EEG mit Normalbefund in einer anfallsfreien Situation schließt Epilepsie jedoch nicht aus. Bei etwa der Hälfte aller Patient*innen mit Epilepsie findet sich in der ersten EEG-Aufzeichnung kein Anhalt für epileptische Aktivität.
- Bei begründetem Verdacht sollten wiederholte Aufzeichnungen erfolgen, was die Wahrscheinlichkeit, epilepsietypische Ausschläge nachzuweisen, auf 80‒90 % erhöht.
- Langzeitaufzeichnungen über mehrere Stunden, am besten in Kombination mit Videoaufnahmen und Schlafaufzeichnungen nach Schlafdeprivation erhöhen die Möglichkeit, Veränderungen aufzudecken, zusätzlich.
- Bei Kindern gehören Schlafaufzeichnungen zur Standarddiagnostik.
- Bei Verdacht auf einen nonkonvulsiven Status epilepticus oder zu dessen Abgrenzung gegenüber anderen Ursachen einer Bewusstseinstrübung, z. B. einem Delir, sind längere Aufzeichnungszeiträume (z. B. 24-Stunden-EEG) und wiederholte Aufzeichnungen ratsam.
Bildgebende Diagnostik2-3,5,7
- Die bildgebende Epilepsie-Diagnostik basiert im Wesentlichen auf MRT, PET und SPECT.
- Informationen zur metabolischen Hirnaktivität bei Epilepsie-Patient*innen werden vor und nach einem Anfall durch PET und SPECT gewonnen, wo u. U. ein eingeschränkter Blutdurchfluss und Glukosemetabolismus im epileptischen Herd zu sehen ist. Während eines Anfalls kann mittels SPECT ein fokal erhöhter Blutfluss nachgewiesen werden.
Indikationen zur Überweisung
- Bei Verdacht auf Epilepsie: Überweisung zur Neurologie
- Ideal ist die Überweisung an ein epileptologisches Zentrum.
Indikationen zur Krankenhauseinweisung
- Personen mit bekannter Epilepsie benötigen nach einem einzelnen Anfall keine Einweisung.
- Nach einem erstmaligen Anfall ist eine Einweisung zweckmäßig, sowohl bei Kindern als auch bei Erwachsenen.
- Anfälle ohne vollständige Restitution
- Anfallsserien
- Status epilepticus (ärztlich begleitete Notfalleinweisung mit Intubationsbereitschaft)
Therapie
Therapieziele
- Nach Priorität:2-3,5,7
- Den Anfall beenden.
- Weiteren Anfällen vorbeugen.
- Therapienebenwirkungen begrenzen.
Allgemeines zur Therapie
- Zu unterscheiden sind:
- Behandlung eines Einzelanfalls
- allgemeine Beratung, vor allem hinsichtlich anfallsauslösender Faktoren
- vorbeugende medikamentöse Behandlung
- Behandlung bei Status epilepticus
- chirurgische Behandlung
- psychotherapeutische/psychiatrische Behandlung
- andere/neue Behandlungsformen.
Medikamentenwahl2-3,5,7
- Antikonvulsiva erhöhen im Gehirn die Anfallsschwelle und beugen damit der Entstehung von Anfällen vor. Sie wirken also nicht unmittelbar „antiepileptisch“.
- Orientiert an der exakten Diagnose: Verschiedene Wirkmechanismen sind bei unterschiedlichen Epilepsiearten/Anfallsarten angezeigt.
- Pharmakokinetik, Interaktionen und Nebenwirkungsprofile beachten, mit Rücksicht auf Alter und Lebenssituation der Patient*innen.
- Laut einer Metaanalyse (2017) sind Carbamazepin und Lamotrigin zur Monotherapie fokaler Anfälle und Valproat bei generalisierten Anfällen als Mittel 1. Wahl gut geeignet.8
- alternativ: Levetiracetam bei fokalen Anfällen und Lamotrigin oder Levetiracetam bei generalisierten Anfällen
Therapieerfolg2-3,5,7
- Bei gut 70 % der Betroffenen ist eine zufriedenstellende Anfallskontrolle durch eine medikamentöse Behandlung möglich. Etwa 2/3 erreichen damit Anfallsfreiheit.
- Wird unter der Probebehandlung mit 2‒3 aktuellen Präparaten für die jeweilige Epilepsieform keine Anfallsfreiheit erreicht, ist es wenig wahrscheinlich, dass die Person im weiteren Verlauf eine vollständige Anfallskontrolle erreichen wird.
- Bei den Menschen mit Epilepsie, die gut auf Antikonvulsiva ansprechen, scheinen sich die verschiedenen aktuellen Medikamente kaum hinsichtlich ihrer Wirksamkeit zu unterscheiden.
- Eine gute Anfallskontrolle geht mit einer relativ niedrigen Morbidität und Mortalität einher. Sie korreliert zudem mit höheren Werten auf lebensqualitätsbezogenen Scores.
- Bei ausbleibender Wirkung oder niedriger Serumkonzentration relativ zur Dosierung kann ein pharmakogenetischer Test sinnvoll sein.
- Bei Versagen der medikamentösen Behandlung kann eine operative Therapie erwogen werden.
Empfehlungen für Patient*innen
- Zur Anfallsvermeidung ist Folgendes zu beachten:2-3,5,7
- Menschen mit Epilepsie sollten einen geregelten Lebensstil pflegen, durchwachte Nächte, Alkoholkonsum und Fasten vermeiden.
- Körperliche Aktivität
- Ist in der Regel nicht schädlich, aber Situationen, in denen ein Anfall gefährlich sein könnte, sollten vermieden werden (z. B. Schwimmen ohne Begleitung, Tauchen, Klettern, Fliegen, Surfen).
- Regelmäßiges körperliches Training kann sich bei 30‒40 % der von Epilepsie Betroffenen moderat anfallsvorbeugend auswirken, doch bei 10 % kann körperliche Aktivität einen Anfall provozieren.
- Bei Personen, die zu aktivitätsinduzierten Anfällen neigen, handelt es sich überwiegend um Menschen in schlechter körperlicher Verfassung und mit symptomatischen Epilepsieformen.
- Flackernde Lichter können bei manchen Epilepsiebetroffenen Anfälle auslösen.
- z. B. im Kino, im Club, im Fernsehen, auf dem Bildschirm, Sonnenlicht, Autofahren bei Dunkelheit
Medikamentöse Therapie
Behandlung eines epileptischen Anfalls2-3,5,7
- Achten Sie darauf, dass die Person sich nicht verletzen kann. Näheres dazu im Abschnitt Sofortmaßnahmen bei einem epileptischen Anfall.
- Ein Einzelanfall kürzer als 5 min erfordert keine Behandlung.
- Bei Anfällen, die länger als 5 min andauern, oder bei wiederholten Anfällen wird ein Benzodiazepin verabreicht.
- Lorazepam i. v. hat sich in der Behandlung des Status epilepticus gegenüber Diazepam als leicht überlegen erwiesen und gilt als das Notfall-Antikonvulsivum 1. Wahl. Da das Medikament gekühlt zu lagern ist, steht es jedoch in der Notfallsituation, z. B. im Rettungswagen, oft nicht zur Verfügung.
- Ist es möglich, einen Venenzugang zu legen, bei einem Erwachsenen zunächst langsam (2 mg/min) 4 mg Lorazepam i. v. injizieren. Falls die Anfälle bestehen bleiben oder innerhalb der nächsten 10‒15 min wiederkehren, kann die gleiche Dosis nochmals injiziert werden, danach jedoch frühestens wieder nach 12 Stunden.
- Kinder und Jugendliche sollten eine initiale Dosis von 0,05 mg/kg Körpergewicht erhalten; falls die Anfälle bestehen bleiben oder innerhalb der nächsten 10‒15 min wieder auftreten, kann eine weitere Dosis von 0,05 mg/kg gegeben werden.
- Es gibt Studien, die vor allem bei Kindern für die Gleichwertigkeit intranasaler oder bukkaler Applikationsformen von Lorazepam oder Midazolam im Vergleich zur i. v. Applikation sprechen.3
- Alternativ zu Lorazepam können Erwachsene auch mit Diazepam 10 mg i. v. behandelt werden, und danach mit Dosen von 5 mg bis zur Beendigung des Anfalls.
- Falls eine i. v. Applikation des Benzodiazepins nicht möglich ist, kann es auch als Rektallösung gegeben werden. In diesem Fall eine Venenkanüle bereithalten, um schnell einen Zugang legen zu können, wenn die Konvulsionen abnehmen. Eine halbe Stunde nach einem unterbrochenen Anfall können z. B. 10‒15 mg Diazepam als Klistier verabreicht werden, um einem erneuten Anfall vorzubeugen.
- Bei Kindern sollte die Dosierung von Diazepam wie folgt aussehen:
- rektal mit Diazepam-Klistier
- Kinder unter 10 kg Körpergewicht: 5 mg
- Kinder über 10 kg Körpergewicht: 10 mg
- Diazepam intravenös
- Alter 0‒2 Jahre: 2‒5 mg
- Alter 2‒4 Jahre: 5‒7,5 mg
- Alter 4‒6 Jahre: 5‒10 mg
- Alter über 6 Jahre: 10‒20 mg.
- rektal mit Diazepam-Klistier
- Kontrolle von Atmung und Blutdruck, besonders während der Aufdosierung des Benzodiazepins
- Interaktionen?
- Wurden interagierende Medikamente oder Alkohol eingenommen, sollte die Medikamentengabe aufgrund des Risikos einer Atemdepression besonders vorsichtig erfolgen.
- Besteht die Möglichkeit einer zufriedenstellenden unterstützten Beatmung, ist das übergeordnete Ziel, die Krämpfe zu beenden, auch wenn die Benzodiazepin-Dosis hoch ist.
- Häufig kommt es zu einem Anfallsrezidiv, weil die Benzodiazepin-Konzentration im Serum und im Hirn schnell abfällt.
Alkoholbedingte Anfälle9
- Bei Patient*innen mit Epilepsie und gleichzeitigem Alkoholmissbrauch sind sowohl Alkoholexzesse als auch ein Alkoholentzug mit einem erhöhten Anfallsrisiko verbunden.
- Die Behandlung eines akuten alkoholbedingten Anfalls erfolgt wie bei anderen epileptischen Anfällen.
- Eine qualifizierte Entzugsbehandlung wird bei diesen Patient*innen, getragen von einem breiten Expertenkonsens, ausdrücklich empfohlen. Sie sollte wegen der besonderen Risiken unbedingt unter stationären Bedingungen durchgeführt werden. Danach ist unter Umständen eine Dosisanpassung oder Neueinstellung der antiepileptischen Medikation, ebenfalls stationär, erforderlich.
Vorbeugung von Anfällen2,10
- Indikation
- Nach mehreren Anfällen sollte eine Therapie der Epilepsie begonnen werden, sofern es sich nicht um akut symptomatische Anfälle handelt, sondern von einer chronischen Anfallsdisposition ausgegangen werden muss.
- Bei 2 nicht provozierten Anfällen beträgt das Risiko, dass es innerhalb von 4 Jahren zu einem 3. Anfall kommt, 70 %.
- Nach dem ersten Anfall kann eine Therapie der Epilepsie begonnen werden, sofern es sich nicht um einen akut symptomatischen Anfall handelt, sondern von einer chronischen Anfallsdisposition ausgegangen werden muss.
- Ist der erste Anfall tonisch-klonisch oder bilateral-konvulsiv, ist besonders nach vorhergehenden fokalen Anfällen und morgendlichen Myoklonien zu fragen, da diese Anfälle oft nicht wahrgenommen oder als epileptische Anfälle erkannt werden.
- Eine Behandlung des ersten Einzelanfalls reduziert das Risiko eines neuerlichen Anfalls innerhalb von 2 Jahren, ist aber im Hinblick auf die langfristige Prognose nicht ausschlaggebend.
- Eine britische Studie kommt zu dem Schluss, dass der sofortige Beginn einer Antikonvulsiva-Therapie nach einmaligem Anfall das Risiko für weitere Anfallsereignisse in den darauffolgenden 1‒2 Jahren im Vergleich zu einem späteren Behandlungsbeginn reduziert. Bei Personen mit einzelnen oder seltenen Anfällen hatte die frühe Behandlung aber keinen Einfluss.
- Ein einziger epileptischer Anfall ohne Zusatzbefund stellt nur bei Wunsch der betroffenen Person eine Indikation für eine antiepileptische Therapie dar.
- Bei sehr seltenen oder nicht als belastend empfundenen Anfällen muss das Nutzen/Risiko-Profil einer Therapie unter Gesichtspunkten der Compliance und Lebensqualität abgewogen werden.
- Treten Anfälle in mehrjährigen Abständen auf (Oligo-Epilepsie bei Abständen > 3–5 Jahre), wird die Indikation zur Therapie individuell
gehandhabt, da ein Therapieerfolg nur sehr langfristig überprüfbar ist. - Ein Langzeit-Video-EEG kann hilfreich sein, um nicht wahrgenommene Anfälle zu erfassen.
- Treten Anfälle in mehrjährigen Abständen auf (Oligo-Epilepsie bei Abständen > 3–5 Jahre), wird die Indikation zur Therapie individuell
- Nach mehreren Anfällen sollte eine Therapie der Epilepsie begonnen werden, sofern es sich nicht um akut symptomatische Anfälle handelt, sondern von einer chronischen Anfallsdisposition ausgegangen werden muss.
- Liegen anfallsauslösende Faktoren vor?
- z. B. Nachlässigkeit in der Medikamenteneinnahme, Schlafmangel, Stress, Hormonschwankungen, eine andere Medikation, Fieber, flackernde Lichter etc.
- Maßnahmen gegen evtl. Faktoren ergreifen.
- Monotherapie?
- Die meisten erreichen Anfallsfreiheit mit nur einem Medikament.
- Wird nach schrittweiser Erhöhung der Dosierung bis zur optimalen Dosierung mit dem ersten Medikament keine Anfallsfreiheit erreicht oder kommt es zu belastenden Nebenwirkungen, ist es ratsam, auf eine andere Monotherapie umzustellen.
- Die Dosierung des zweiten Medikamentes wird schrittweise bis zur therapeutischen Dosis erhöht. Dann schleicht man das erste Medikament nach und nach aus, häufig erst, nachdem man die Wirkung der Kombinationsbehandlung über einige Wochen beobachtet hat.
- Es sind viele Antikonvulsiva auf dem Markt. Nicht alle eignen sich als Erstlinientherapie.
- Bei behandlungsresistenter Epilepsie kann die Kombination mit einem zweiten Medikament die Anzahl epileptischer Anfälle reduzieren.
- Dosierung
- Die Dosierung erfolgt individuell. In der Langzeitbehandlung gilt:
- So hoch, wie für eine ausreichende Wirkung nötig und
- So niedrig wie möglich, um Nebenwirkungen zu vermeiden.
- Schnelles oder langsames Aufdosieren?
- Bei Valproat und Phenytoin kann die Tagesdosis schnell erhöht werden, ggf. auch intravenös. Besonders bei der i. v. Gabe von Phenytoin ist das sichere Liegen des venösen Zugangs und die langsame Applikation als Infusion entscheidend, um Venenirritationen, Paravasate und Gewebsnekrosen zu vermeiden.
- Auch bei Levetiracetam und Gabapentin kann die Dosis fast von Beginn an bis zur Erhaltungsdosis erhöht werden. Diese Medikamente scheinen wenige Nebenwirkungen und Interaktionen zu haben.
- Bei den meisten anderen Antikonvulsiva muss die Dosierung schrittweise erhöht werden, um Nebenwirkungen entweder im Zentralnervensystem oder in Form von allergischen Hautreaktionen zu vermeiden.
- Die Dosierung erfolgt individuell. In der Langzeitbehandlung gilt:
- Nebenwirkungen
- Können sehr belastend sein, vor allem Schläfrigkeit, Schwindel, Konzentrations-, Gedächtnis- und Lernschwierigkeiten.
- Absetzen der Medikamente
- Sollte von Neurolog*innen entschieden werden, z. B. nach 5-jähriger Anfallsfreiheit bei Epilepsiekranken, die vorher wenige leichte Anfälle hatten.
- Schrittweise und langsam ausschleichen.
Auswahl des Medikaments2
- Es gibt nur wenige vergleichende Studien. Die verschiedenen Medikamente scheinen vergleichbar wirksam zu sein.
- Bei der Auswahl der Medikamente, insbesondere zu Therapiebeginn, spielt außerhalb der idiopathisch-generalisierten Epilepsien oder spezieller Syndrome die Wirksamkeit eines Medikaments daher eine untergeordnete Rolle.
- Zur Entscheidung sollte insbesondere die individuelle Situation der Patient*innen berücksichtigt werden, z. B.:
- Patientenwunsch
- Körpergewicht
- Geschlecht
- kognitive Leistungsfähigkeit
- psychische Komorbidität
- Komedikation.
- Pharmakokinetik beachten.
- Langzeiteffekte und -probleme durch Enzymhemmung und -induktion
- orale Kontrazeption
- Interaktionen mit anderen Medikamenten
- Da die Mehrzahl aller Betroffenen eine Langzeittherapie (oft lebenslang) benötigt, sind Medikamente ohne Enzyminduktion oder -hemmung – wenn möglich – zu bevorzugen.
- Da im Lebensverlauf in der Regel weitere behandlungsbedürftige Krankheiten auftreten, sollten medikamentöse Interaktionen bedacht werden.
- Paradoxe Reaktion erkennen.
- Eine besondere Herausforderung bei der medikamentösen Einstellung kann sein, Personen zu identifizieren, die aufgrund der Antikonvulsiva mehr Anfälle erleiden.
- Eine solche paradoxe Reaktion lässt sich beim Einsatz vieler Medikamente feststellen, wie
- gehäufte nicht-motorische generalisierte Anfälle (Absencen), etwa unter Vigabatrin
- myoklonische Anfälle, z. B. unter Phenytoin, Carbamazepin und Lamotrigin.
- Besondere Vorsichtsmaßnahmen bei Valproat
- Frauen im fertilen Alter sollten sich bei der Einnahme von Valproat einschließlich Valproinsäure um eine wirksame Verhütung kümmern, weil bei einer Einnahme während einer Schwangerschaft ein erhöhtes Risiko für den Fetus besteht.
- Die Europäische Arzneimittel-Agentur (EMA) hat 2014 die Empfehlung ausgesprochen, Valproat nicht nur bei Frauen im gebärfähigen Alter, sondern auch bei Mädchen erst dann einzusetzen, wenn alternative Therapien versagt haben.11 Dem hat sich die Arzneimittelkommission der deutschen Ärzteschaft mit einem Rote-Hand-Brief angeschlossen.12
- Die Leitlinienkommission der Deutschen Gesellschaft für Neurologie weist darauf hin, dass in diesem Statement die Dosisabhängigkeit und der Einfluss von prophylaktischer Folsäuregabe auf die Kognitionsreduktion unberücksichtigt blieb. Die Empfehlung der EMA sei ohne Beteiligung der internationalen Fachgesellschaft (ILAE) erstellt worden. Für die Behandlung von Frauen in der Prämenopause habe dies erhebliche Konsequenzen, da Valproat nicht selten alternativlos in der Behandlung sei. Eine schriftlich bestätigte Zustimmung der Patientin zur Valproat-Therapie sei zu empfehlen.
- Das Bundesinstitut für Arzneimittel und Medizinprodukte (BfARM) schreibt seit April 2017 vor, dass jede Packung eines Valproat-haltigen Arzneimittels eine Patientenkarte enthält, die der Patientin vor jeder Abgabe oder Verschreibung von Valproat auszuhändigen ist.13
- Phenobarbital nicht als 1. Wahl
- Wurde früher als Hauptmedikament eingesetzt.
- U. a. wegen seiner sedativen Wirkung, der Beeinträchtigung kognitiver Funktionen und des hohen Abhängigkeitspotenzials werden mittlerweile andere Antikonvulsiva bevorzugt.
- Insbesondere bei älteren und multimorbiden Personen ist angesichts des Nebenwirkungsprofils und der Vielzahl potenzieller Arzneimittelinteraktionen Vorsicht geboten.
- Bei von Epilepsie Betroffenen allerdings, die seit langem auf Phenobarbital gut eingestellt sind, ist es in der Regel ratsam, diese Medikation trotz der erwähnten Vorbehalte beizubehalten.
Fokale Epilepsien
- Auf der Basis der obigen Argumentation sind bei fokalen Epilepsien, evtl. mit sekundär generalisierten Anfällen, Lamotrigin und Levetiracetam die bevorzugten Mittel der 1. Wahl.2
- mögliche Alternativen:
- Gabapentin
- Lacosamid
- Oxcarbazepin
- Topiramat
- Zonisamid
- Carbamazepin
- Valproat (Vorsichtsmaßnahmen beachten!)
- Phenytoin
- Eslicarbazepin
- Perampanel.
- Carbamazepin als Enzyminduktor sowie Valproat als Enzymhemmer und problematisches Medikament in der Schwangerschaft (Näheres siehe Abschnitt Vorsichtsmaßnahmen) sollten nachrangig betrachtet werden.
- mögliche Alternativen:
- Bei Kombinationen sind die Empfehlungen schwieriger.2
- Wenn Levetiracetam die Ausgangssubstanz ist, kann im Prinzip mit allen zugelassenen Antiepileptika kombiniert werden.
- Ist die Erstmedikation eines der anderen Antiepileptika, können pharmakokinetische und -dynamische Probleme auftreten (z. B. Abfall der Lamotrigin-Blutspiegel durch Enzyminduktoren, Anstieg durch Enzymhemmer etc.).
Idiopathische Epilepsien2
- Mittel der 1. Wahl bei idiopathischer Epilepsie, nach Relation Wirksamkeit/Nebenwirkungen:
- Valproat (Vorsichtsmaßnahmen beachten!)
- Lamotrigin
- Levetiracetam.
- Nicht indiziert bei idiopathischer Epilepsie:
- Carbamazepin
- Gabapentin
- Oxcarbazepin
- Phenytoin.
Generalisierte Epilepsie mit typischen nichtmotorischen Anfällen (Absencen)2
- 1. Wahl: Valproat (Vorsichtsmaßnahmen beachten!) oder Ethosuximid
- 2. Wahl: Lamotrigin
Generalisierte Epilepsien mit tonisch-klonischen Anfällen2-3
- 1. Wahl: Valproat (Vorsichtsmaßnahmen beachten!)
- Valproat scheint verträglicher zu sein als Topiramat und wirksamer als Lamotrigin.
- 2. Wahl
- Lamotrigin
- Topiramat
- 3. Wahl
- Phenobarbital
- Primodon
Progressive Myoklonusepilepsie2
- Levetiracetam
- Piracetam
- Valproat (Vorsichtsmaßnahmen beachten!)
Seltene Epilepsiesyndrome mit Beginn im Kindesalter
- Näheres siehe entsprechende Artikel:
Keine Anfallsfreiheit?
- Wird nach Behandlungsversuchen mit 1–2 Medikamenten unter einer Monotherapie keine Anfallsfreiheit erreicht, ist es in vielen Fällen nötig, mit einer Kombinationstherapie zu beginnen.
- Es ist dann Aufgabe des epileptologischen Zentrums, eine Kombination von Medikamenten zu finden, mit der eine Anfallsfreiheit bei minimalen Nebenwirkungen möglich ist.
- In der Regel werden dabei verschiedene Wirkmechanismen kombiniert.
- Einige der neueren Medikamente weisen eine geringere Neigung zu Arzneimittelwechselwirkungen auf, z. B. Gapapentin und Levetiracetam. Diese eignen sich daher möglicherweise eher zur Kombination mit einem anderen Antikonvulsivum.
- Es gibt Belege dafür, dass Zonisamid als Zusatzbehandlung bei fokaler Epilepsie ohne Anfallsfreiheit wirksam sein könnte.14
- Ein Wirksamkeitsnachweis für Felbamat in der Zusatzbehandlung bei schwer behandelbarer Epilepsie wurde bisher nicht erbracht.15
- Bei ausbleibender Wirkung oder niedriger Serumkonzentration relativ zur Dosierung – etwa unter der Behandlung mit Lamotrigin ‒ kann ein pharmakogenetischer Test sinnvoll sein.
Ältere Menschen2-3,5
- Oft ausgeprägte Komorbidität und Polymedikation ‒ Achtung Wechselwirkungen!
- Sind empfindlicher gegenüber arzneimittelbedingten Beeinträchtigungen von Kognition, Gleichgewicht und Gehfähigkeit.
- Reduzierte Nieren- und Leberfunktion: verzögerte Elimination, erhöhte Serumspiegel, Verstärkung toxischer Effekte
- Niedrige Albuminkonzentration im Plasma: erhöhte freie, wirksame Fraktion von Medikamenten mit hoher Plasmaproteinbindung, Verstärkung von Nebenwirkungen
- Abwägung im Blick auf die Lebensqualität: vollständige Anfallsfreiheit vs. Vermeidung von Nebenwirkungen
Absetzen der medikamentösen Behandlung?2,16-17
- Die Beendigung einer antiepileptischen Therapie sollte sorgfältig überlegt werden.
- Es gibt bisher keinen Biomarker für das Rezidivrisiko oder für weiterbestehende Anfallsfreiheit.
- Die Zahl der anfallsfreien Jahre ist weniger entscheidend als das Syndrom und die Schwierigkeit der Einstellung.
- Prüfen, ob die Ursachen der Epilepsie weggefallen sind.
- Die Konsequenzen eines Rezidivs sind gegen die Vorteile des Absetzens abzuwägen.
- Etwa 2/3 aller anfallsfreien Betroffenen bleiben auch nach geplantem Absetzen der Medikamente anfallsfrei.
- Allgemeine Empfehlungen zur Mindestdauer der Anfallsfreiheit vor dem Absetzen können nicht gegeben werden.
- Eine Cochrane-Metaanalyse lässt vermuten, dass bei Kindern mindestens 2 Jahre Anfallsfreiheit abgewartet werden sollten, bevor ein Absetzen der Medikamente in Erwägung gezogen wird.17
- Beobachtungsstudien haben gezeigt, dass bei fast 1/3 der Epilepsiekranken, bei denen die Antikonvulsiva-Behandlung beendet wird, innerhalb von 2 Jahren erneute Anfälle auftreten.
- Klinische Prädiktoren für Rezidive
- Alter
- Anfallsform
- Anzahl der Antikonvulsiva
- Anfälle nach Beginn der Therapie
- Länge des Remissionszeitraums vor dem Absetzen
- genetische Disposition (Rückfallraten > 80 %)
- fokale Läsionen
Behandlungsresistente Epilepsie
- Bei einem unzureichenden Ansprechen auf die medikamentöse Therapie kann die Anfallshäufigkeit bei Kindern und Erwachsenen, bei denen die Epilepsie erstmals in der Kindheit auftrat, durch eine ergänzende Behandlung mit einem Cannabidiol-haltigen Arzneimittel reduziert werden, wobei Nebenwirkungen vermehrt auftreten (Ia).18
Weitere Behandlungsmethoden
Sofortmaßnahmen bei einem epileptischen Anfall
- Weiche Unterlage unter den Kopf der betroffenen Person legen.
- Nähe zu Gegenständen vermeiden, die beim Anstoßen Verletzungen verursachen könnten.
- Die Person nicht festhalten.
- Kinder auf eine weiche Unterlage legen. Kleine Kinder können auf dem Arm gehalten werden. Die Myoklonien sollten aber auf keinen Fall durch Festhalten unterdrückt werden.
- Bei Bewusstseinstrübungen nach Abklingen der klonischen Phase: Atemwege freihalten (stabile Seitenlage).
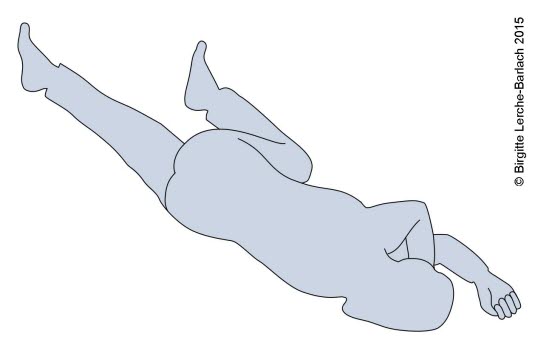 stabile Seitenlage
stabile Seitenlage - Bei Anfallsserien oder länger anhaltendem Anfall: medikamentöse Anfallsunterbrechung
- Näheres siehe Artikel Krampfanfall, Erste Hilfe.
Operative Therapie
- Eine operative Therapie hat zum Ziel, eine Anfallsfreiheit zu erreichen, die Anzahl der Anfälle oder den Schweregrad der Anfälle zu reduzieren,
- indem ein epileptogener Herd entfernt wird.
- indem die Ausbreitung der epileptischen Aktivität innerhalb des Gehirns verhindert wird.
- Unter bestimmten Umständen hat sich eine operative Therapie therapieresistenter Epilepsien als sehr wirksam erwiesen. Sie sollte daher erwogen werden, wenn innerhalb von 2 Jahren unter adäquater medikamentöser Therapie keine Anfallsfreiheit erreicht werden konnte.
- Der häufigste epilepsiechirurgische Eingriff ist die Entfernung eines Schläfenlappenabschnitts.
- Etwa 60 % der operierten Erwachsenen und Kinder werden anfallsfrei.
- Besonders hohe Erfolgsquoten bei Ammonshorn-Sklerose oder einem benignen Tumor
- Weniger erfolgversprechend bei extratemporalen Läsionen, bei denen die Epilepsie nicht mit einer strukturellen Läsion im Zusammenhang steht, oder wenn mehrere Gehirnregionen primär betroffen sind.
Stimulation des N. vagus, evtl. des N. trigeminus
- Diese Verfahren stellen eine Ergänzung der medikamentösen Therapie dar. Eine Anfallsfreiheit wird damit in der Regel nicht erreicht.2
- Die chronisch-intermittierende Stimulation des N. vagus ist eine nichtpharmakologische, invasive Behandlungsmethode, die bei Patient*innen mit schwer kontrollierbarer Epilepsie angewendet wird.19
- Eine elektrische Stimulation des N. vagus kann epileptischen Anfällen vorbeugen oder deren Frequenz und Dauer reduzieren.
- Nebenwirkungen wie Heiserkeit, Husten, Schmerzen, Parästhesien und Dyspnoe scheinen für die Behandelten akzeptabel zu sein.
- Stimulation des N. vagus bei fokaler Epilepsie
- Scheint wirksam und tolerabel zu sein.19
- Nebenwirkungen wie Heiserkeit, Husten, Schmerzen, Parästhesien und Dyspnoe scheinen für die Behandelten akzeptabel zu sein.
- Typische ZNS-Nebenwirkungen wie Ataxie, Schwindel, Abgeschlagenheit, Übelkeit und Somnolenz kommen bei dieser Behandlungsform nicht vor.
- Stimulation des N. trigeminus
- In einer Studie zu medikamentenresistenter Epilepsie hat sich dieses Verfahren als sichere und wirksame Behandlung erwiesen, die Anfälle reduziert.20
Ketogene Diät
- Wird eingesetzt bei behandlungsrefraktärer Epilepsie.
- Die Diät enthält viel Fett und sehr wenig Kohlenhydrate und simuliert die Reaktion des Körpers auf das Fasten. Dies bewirkt, dass der Körper zur Fettverbrennung übergeht. Dadurch verwendet das Gehirn Ketonkörper als Energiequelle anstelle von Zucker.
- Man nimmt an, dass die Energieumstellung und die Restriktion der Kalorienzufuhr anfallsdämpfend wirken.
- Diese Diät erfordert Disziplin und Motivation. Sämtliche Mahlzeiten müssen denselben ketogenen Quotienten (Verhältnis zwischen Fett und der Summe der Proteine und Kohlenhydrate) aufweisen.
- Im Kindesalter ist die Wirksamkeit der ketogenen Diät durch Studien belegt.2
Akupunktur?
- In den bislang wenigen und methodisch unzureichenden Studien konnte kein konsistenter Wirksamkeitsnachweis hinsichtlich der Anfallsfrequenz erbracht werden.21
Rehabilitation
- Aufklärung und Schulung als Basis
- Individuelle Anpassung an den Epilepsietyp, das Alter, die Lebenssituation und den Gesundheitszustand der Betroffenen
- Interdisziplinäre Behandlungsplanung, besonders bei Menschen mit schwerer und therapieresistenter Epilepsie
Prävention
- Medikamentöse Anfallsprävention durch epileptologisches Zentrum
- Potenzielle Anfallsauslöser vermeiden (Näheres dazu auch im Abschnitt Empfehlungen für Patient*innen).
Schwangerschaft
- Eine Konzeption sollte nach vorheriger Planung erfolgen.
- Begleitende Behandlung der Epilepsie durch epileptologisches Zentrum
- Näheres dazu im Abschnitt Fertilität, Schwangerschaft, Geburt
Hormonelle Kontrazeptiva mit verlängertem Zyklus
- Bei 30 % der Frauen mit Epilepsie können die Anfälle durch zyklusbedingte Hormonschwankungen ausgelöst werden.
- Es ist möglich, dass ein hormonelles Kontrazeptivum mit verlängertem Zyklus und damit stabilem Hormonspiegel die Anzahl der Anfälle bei diesen Patientinnen reduziert.
Prävention psychosozialer Probleme2,5,7
- Anfallskontrolle und Vermeidung von Nebenwirkungen der Behandlung sind zentrale Behandlungsziele, auch im Blick auf die Prävention psychosozialer Probleme und auf die Lebensqualität.
- Besonders wenn dies nicht unmittelbar möglich ist, sind profunde Kenntnisse über die eigene Erkrankung und Behandlung von entscheidender Bedeutung. Um die körperlichen und psychosozialen Folgen von Anfällen und Anfallsneigung bewältigen zu können, brauchen die Betroffenen kompetente Beratung und Unterstützung.
- Menschen mit Epilepsie benötigen oft eine langjährige Behandlung. Eine kontinuierliche professionelle Begleitung durch verschiedene Phasen der Erkrankung hindurch wird am besten durch ein interdisziplinäres Team gewährleistet. Dabei können auf Epilepsie spezialisierte Personen aus Pflege, Sozialarbeit und Psychotherapie unter ärztlicher Regie wichtige Teile der psychosozialen Prävention und Behandlung übernehmen.
Vorbeugung von Osteoporose2,5,22
- Die Einnahme von Antikonvulsiva, vor allem von enzyminduzierenden wie Phenobarbital, Phenytoin oder Carbamazepin, führt zu einer herabgesetzten Knochendichte und einem 2- bis 6-fach erhöhten Frakturrisiko.
- Folgendes wird empfohlen:
- 5 Jahre nach Beginn der Behandlung mit enzyminduzierenden Antikonvulsiva und vor der Behandlung postmenopausaler Frauen ‒ Bestimmung von:
- zur Lebensführung
- Sport
- Ernährung reich an Kalzium und Vitamin D
- Raucherentwöhnung
- eingeschränkter Alkoholkonsum
- genügend Sonne
- Kalzium/Vitamin D Supplementierung
- bei postmenopausalen Frauen, die enzyminduzierende Antikonvulsiva und gleichzeitig Valproat einnehmen.
- bei nachgewiesener Osteopenie/Osteoporose
- Tagesdosis: Kalzium 1.000 mg, Vitamin D 800‒1.000 IE
- bei nachgewiesener Osteopenie/Osteoporose evtl. spezifische Therapie, z.B. mit einem Bisphosphonat, selektiven Östrogenrezeptor-Modulator (Raloxifen, Bazedoxifen), Denosumab oder Teriparatid
Fertilität, Schwangerschaft, Geburt
Fertilität
- Die Prävalenz von Epilepsie beträgt ca. 5/1.000 der Menschen im reproduktionsfähigen Alter.
- Bei Männern und Frauen mit Epilepsie ist die Fertilitätsrate reduziert. Die Ursache hierfür liegt wahrscheinlich in einer Kombination psychosozialer und biologischer Faktoren.
- Häufig kommt es zu einer sexuellen Dysfunktion (bei Männern, bei Frauen).
- Unter der antikonvulsiven Behandlung können Hormonspiegel absinken.
- Menstruationsstörungen, polyzystische Ovarien/verminderte Spermaqualität kommen bei Frauen/Männern mit Epilepsie häufiger vor als bei Personen ohne Epilepsie.
Hormonelle Kontrazeption
- Bei Frauen, die enzyminduzierende Antikonvulsiva nehmen, kann eine Dosisanpassung der oralen Kontrazeption oder die Umstellung auf eine andere Verhütungsmethode notwendig werden.
- Umgekehrt können orale Kontrazeptiva die Elimination mancher Antikonvulsiva, etwa Lamotrigin, beschleunigen. Das kann eine Erhöhung der Antikonvulsiva-Dosis, ggf. nach Spiegelbestimmung, erforderlich machen.
- Eine Hormonspirale oder 3-Monats-Spritze kann, im Gegensatz zu Minipillen und Hormonimplantaten, eine Alternative zur herkömmlichen oralen Kontrazeption mit einem Kombinationspräparat sein.
Behandlungsplan bei Patientinnen mit Kinderwunsch
- Die Prävalenz der Epilepsie bei Schwangeren zum Geburtstermin liegt bei 3‒5 pro 1.000.
Vor der Schwangerschaft2
- Ist eine Behandlung immer noch notwendig? Absetzen der Medikamente erwägen.
- Es ist immer eine Monotherapie und möglichst niedrige Dosierung anzustreben.
- Grundsätzlich das Antikonvulsivum einsetzen, das bei der entsprechenden Epilepsieform am besten wirkt.
- Valproat darf nicht während der Schwangerschaft verwendet werden (Vorsichtsmaßnahmen beachten!).
- Wenn möglich, Carbamazepin vermeiden.
- Ist die Verwendung von Valproat und Carbamazepin unverzichtbar, sind Zubereitungen mit einer langsamen Resorption zu bevorzugen.
- Neue Antikonvulsiva vermeiden, bei denen keine ausreichenden Erfahrungswerte zu den Risiken in der Schwangerschaft vorliegen.
- Folsäure-Supplementierung
- Empfohlen wird die Gabe von Folsäure 5 mg täglich, obwohl eine protektive Wirkung gegenüber der Teratogenität von Antiepileptika nicht anhand geeigneter Studien belegt ist.
- Folsäurezufuhr so früh wie möglich beginnen, am besten 1 Monat vor der Schwangerschaft.
- Die hochdosierte Folsäurezufuhr (5 mg/Tag) sollte mindestens während des gesamten ersten Trimenons erfolgen. Danach kann die Dosis vermutlich auf 0,4 mg täglich reduziert werden.
- Die hochdosierte Folsäurezufuhr ist vermutlich besonders wichtig bei Frauen,
- die Valproat oder Carbamazepin einnehmen.
- die früher Kinder mit Neuralrohrdefekten geboren haben.
- die selbst von einem solchen Defekt betroffen sind.
- in deren naher Verwandtschaft solche Fälle auftraten.
Antikonvulsiva und Schwangerschaft2
- Antikonvulsiva wirken bis zur 12. SSW potenziell teratogen.
- Eine Epilepsie-Patientin, die eine Schwangerschaft plant, sollte sich mit der Person, bei der sie in epileptologischer Behandlung ist, im Hinblick auf die antikonvulsive Therapie beraten und vor der Konzeption und während des ersten Trimenons 5 mg Folsäure täglich einnehmen.
- Wurde die Epilepsie durch genetische Faktoren mit verursacht, kann eine genetische Beratung sinnvoll sein.
- Der Bedarf an Antikonvulsiva während der Schwangerschaft erfordert eine kritische Bewertung. Vielleicht ist eine vorübergehende Aussetzung der Therapie möglich?
- Bei bereits eingetretener Schwangerschaft sollte die Therapie möglichst nicht mehr auf andere Medikamente umgestellt werden.
- Das relative Risiko für schwere embryonale Fehlbildungen ist unter Antikonvulsiva um etwa ein Sechstel gegenüber dem Risiko bei Frauen ohne Antikonvulsivaeinnahme erhöht.
- Valproat wird am häufigsten mit fetalen Fehlbildungen in Verbindung gebracht (Vorsichtsmaßnahmen beachten!), während Levetiracetam, Lamotrigin, Gabapentin und Oxcarbamazepin die niedrigste Inzidenz aufweisen.
- Die Vermutung, dass das Risiko für teratogenen Effekte bei Valproat eine kontinuierliche Dosis-Wirkungsbeziehung zeigt, beruht bislang nur auf Registerstudien.Wenn eine Valproattherapie während des ersten Trimenons nicht vermieden werden kann, ist eine Dosierung unter 1.000 mg täglich anzustreben.
- Mono- oder Kombinationstherapien mit Valproat scheinen das Risiko kindlicher Sprachentwicklungsstörungen zu erhöhen.23
Während der Schwangerschaft2
- Kontrolle durch die epileptologisch behandelnde Person etwa einmal pro Trimenon. Der Kontrollbedarf sollte individuell festgelegt werden.
- Das erhöhte Plasmaproteinaufkommen während der Schwangerschaft kann die Pharmakokinetik von Medikamenten verändern. Die Dosierung von Antikonvulsiva nach Messung der Gesamtserumkonzentration sollte nicht geändert, sondern entsprechend der klinischen Wirkung gesteuert werden. Bei ausgeprägten Schwankungen der Serumkonzentration (z. B. > 20‒30 %): Freie Wirkstofffraktionen messen und Dosierung entsprechend anpassen.
- Ergebnisoffen über die Möglichkeiten und Konsequenzen der pränatalen Diagnostik beraten und dabei die persönliche Einstellung der Patientin respektieren.
- Ob die Gabe von Vitamin K 10 mg/d im letzten Schwangerschaftsmonat Blutungskomplikationen beim Neugeborenen wirksam vorbeugt, ist bislang nicht durch geeignete Studien belegt. Dennoch wird die Vitamin-K-Prophylaxe bei Frauen, die enzyminduzierende Arzneimittel einnehmen, oft routinemäßig angewendet.
Bei der Geburt2
- Eine Epilepsie per se ist kein Grund für einen Kaiserschnitt.
- Die Antikonvulsiva sollten zu den gleichen Zeiten eingenommen werden wie sonst auch, auch während der Geburt.
- Sehr lange Geburten vermeiden.
- Hyperventilation vermeiden.
- Vorsicht bei Pethidin, am besten epidural zur Anästhesie einsetzen, falls notwendig.
- Dem Kind nach der Geburt 1 mg Vitamin K geben.
Nach der Geburt
- Epileptologische Nachkontrolle nach 6‒8 Wochen
- Zum Stillen ermutigen.
- Darauf achten, dass die Mutter ausreichend Ruhe und Schlaf bekommt.
- Die Sicherheit beim Tragen, Baden, Füttern etc. diskutieren.
- Ggf. ein Gestell auf einer Matte auf dem Bett oder Boden; beim Baden sollte eine 3. Person anwesend sein. Die Empfehlungen sollten individuell angepasst werden.
- Bedarfsorientierte engmaschige Begleitung
- Hausbesuche
- Evtl. Absprachen mit einem Pflegedienst, der auf die Betreuung von Epilepsie-Patientinnen eingerichtet ist.
Verlauf, Komplikationen und Prognose
Verlauf
- Die Anfallshäufigkeit variiert erheblich.
- 40 % der Betroffenen sind anfallsfrei.
- 35 % haben 1‒11 Anfälle pro Jahr.
- 15 % haben mehrere Anfälle pro Monat.
- 10 % haben mehrere Anfälle pro Woche.
- Bei einer Person können mehrere Epilepsieformen auftreten.
- Das Risiko für einen erneuten Anfall nach einem ersten, nicht provozierten Anfall ist in den ersten 2 Jahren am höchsten (21‒45 %).10
- Erhöhtes Risiko für einen erneuten Anfall bei:
- früheren Hirnschädigungen/-erkrankungen
- epileptiformen Befunden im EEG
- abweichenden Befunden in der MRT
- nächtlichen Anfällen.
Komplikationen
- Im Rahmen des Anfallsgeschehens:2-3,5,7
- Verletzungen
- Quetschungen, Brandwunden, Zungenbisse
- Status epilepticus
- plötzlicher, unerklärter Tod (Sudden Unexplained Death in Epilepsy, SUDEP)
- Kann junge Menschen im Alter zwischen 20 und 45 Jahren treffen.
- Am häufigsten bei Patient*innen mit schwerer refraktärer Epilepsie. Die Häufigkeit beträgt in dieser Patientengruppe 1:200‒300 Fälle pro Jahr.
- Tod durch Ertrinken.
- Verletzungen
- Im Rahmen der Erkrankung:2,5,7
- Depression
- postiktale Psychosen
- Beeinträchtigung der Autonomie in Beruf und Haushalt
- soziale Diskriminierung und Isolation
- erhöhtes Suizidrisiko
Status epilepticus (SE)3
- Anhaltende epileptische Anfälle oder wiederholte Anfälle, die 5 Minuten oder länger andauern, ohne dass die Betroffenen sich zwischen den Anfällen erholen.
- Die häufigsten Formen eines SE sind generalisierter tonisch-klonischer SE, einfacher oder komplex fokaler SE und Absencestatus.
- Ein generalisierter tonisch-klonischer SE ist eine akute schwere Erkrankung, die eine sofortige Behandlung mit Überwachung der Vitalfunktionen und eine spezifische antikonvulsive Behandlung und Einweisung ins Krankenhaus erfordert.
- Den Blutzuckerspiegel überprüfen, um eine Hypoglykämie auszuschließen.
- Atemwegsobstruktionen und Selbstverletzungen vorbeugen.
- Initiale Medikation (auch in der Prähospitalphase)
- bei vorhandenem i. v. Zugang:
- Lorazepam 0,1 mg/kg (max. 4 mg/Bolusgabe, ggf. 1 x wiederholen) – oder –
- Clonazepam 0,015 mg/kg (max. 1 mg/Bolusgabe, ggf. 1 x wiederholen) – oder –
- Midazolam 0,2 mg/kg (max. 10 mg/Bolusgabe, bei < 40–13 kg KG: max. 5 mg/Bolusgabe), ggf. 1 x wiederholen) – oder –
- Diazepam 0,15–0,2 mg/kg (max. 10 mg/Bolusgabe, ggf. 1 x wiederholen).
- ohne i. v. Zugang:
- Midazolam intramuskulär per Applikator oder intranasal (10 mg für > 40 kg, 5 mg für < 40–13 kg KG) als Einzelgabe – oder –
- Diazepam rektal (0,2–0,5 mg/kg, max. 20 mg/Gabe, Einzelgabe) – oder –
- Midazolam bukkal.
- bei vorhandenem i. v. Zugang:
- Aufdosierung wie beschrieben unter Kontrolle der Atmung und des Blutdrucks
- Bei Verdacht auf eine Hypoglykämie oder einen alkoholbedingten Anfall wird eine intravenöse Glukoseinfusion angelegt.
- Zügiger Transport ins Krankenhaus (am schnellsten per Helikopter) mit ärztlicher Begleitung und Intubationsbereitschaft
- Ggf. Sauerstoff verabreichen.
- Die Patient*innen nicht zudecken.
- Die Temperatur im Krankenwagen niedrig halten.
- Grelles Licht und laute Geräusche vermeiden.
- Mögliche Komplikationen
- Hirnödem
- Hirnschädigung
- Hyperthermie infolge der übermäßigen Muskelaktivität führt möglicherweise zu einer schnelleren zerebralen Schädigung.
- Weiterführende Informationen finden Sie im Artikel Status epilepticus.
Prognose
- Zusammenfassung des Wissensstands:2-3,5,7
- Die Prognose variiert mit den Faktoren, die der Epilepsie zugrunde liegen.
- Absencen und benigne fokale Kinderepilepsie remittieren bei den meisten Patient*innen im Laufe der Kindheit und Jugend komplett.
- In Bezug auf die Lebensqualität ist Anfallsfreiheit der wichtigste Faktor.
- Wahrscheinlichkeit für einen erneuten Anfall nach einem ersten nicht provozierten Anfall
- über 40 % innerhalb der folgenden 2 Jahre
- bei generalisierten Anfällen niedriger als bei fokalen
- Wirksamkeit der Behandlung
- Die meisten Epilepsie-Patient*innen erreichen mit Medikamenten eine gute oder vollständige Anfallskontrolle. Einige jedoch erreichen nie eine Anfallsfreiheit.
- Ca. 70 % erleben eine Remission, sind also mit oder ohne Behandlung 5 Jahre lang anfallsfrei.
- 20‒30 % entwickeln eine chronische Epilepsie.
- Ca. 60 % der unbehandelten Patient*innen erleben in einem Beobachtungszeitraum von 2 Jahren nach dem ersten Anfall keinen erneuten Anfall.
- Letalität
- höher als in der Normalbevölkerung
- Eine symptomatische Epilepsie kann die Lebenserwartung um bis zu 18 Jahre reduzieren.
- Plötzlicher Tod, Traumata, Suizid, Pneumonien und Status epilepticus kommen bei Personen mit Epilepsie häufiger vor als bei Personen, die nicht an dieser Krankheit leiden.
- Prognostische Faktoren
- Die beste Prognose haben Patient*innen mit Epilepsie unbekannter Ursache, einem Beginn im Kindesalter und ohne neurologische Symptome.
Verlaufskontrolle
- Antikonvulsive Einstellung durch Neurolog*innen
- Verlaufskontrolle in der Hausarztpraxis in Absprache mit Neurolog*in
- In einer stabilen, anfallsfreien Situation ist es ausreichend, 1- bis 2-mal pro Jahr Kontrollen durchzuführen, davon eine in der neurologischen Praxis.
- Schwangere Epilepsie-Patientinnen benötigen eine besondere Begleitung vor allem im Hinblick auf die Medikation, die Überwachung des Fetus und die Wahl der Entbindungsmethode (Näheres dazu im Abschnitt Fertilität, Schwangerschaft, Geburt).
- Die Wirkung der Medikamente kontrollieren.
- Anfallsfrequenz
- Nebenwirkungen
- Den Patient*innen Zeit geben, über Anfälle und Nebenwirkungen zu berichten und dabei auf Details achten.
- Bluttests zur Erkennung von Nebenwirkungen auf verschiedene Organe
- Blutbildung
- Leber
- Elektrolyte
- Stoffwechsel
- Bei allergischen Reaktionen auf Antikonvulsiva ist das Präparat in der Regel abzusetzen und die Patient*innen schnell in eine Fachabteilung zu überweisen.
Serumkonzentration der Medikamente2,5,7
- Wird häufig bei den Kontrolluntersuchungen bestimmt.
- Die Patient*innen behandeln und nicht den Blutwert. Die angegebenen therapeutischen Bereiche sind nur Richtwerte. Bei einigen Patient*innen ist eine höhere Serumkonzentration notwendig, damit das Medikament wirksam ist, während andere mit Konzentrationen auskommen, die unter dem angenommenen therapeutisch wirksamen Wert liegen.
- Pharmakokinetische Wechselwirkungen beachten.
Patienteninformationen
Worüber sollten Sie die Patient*innen informieren?
Berufsbezogene Risiken
- Ob die Patient*innen eine bestimmte berufliche Tätigkeit ausüben können, ist immer eine Einzelfallentscheidung, abhängig von:
- dem Epilepsietyp
- der Art und Häufigkeit der Anfälle
- der Medikation
- der Komorbidität
- der aktuellen beruflichen Situation der Betroffenen.
- Auch Arbeiten an vielen Maschinen sind heute aufgrund umfangreicher Sicherheitsmaßnahmen nicht von vornherein auszuschließen.
- Bei den meisten Berufsgenossenschaften bleiben Epilepsie-Patient*innen ohne Vorbehalt weiter versichert.
- Entscheidungsfindung im Dialog mit Betriebsärzt*innen und behandelnden Neurolog*innen
- Der Spitzenverband der Deutschen Gesetzlichen Unfallversicherung (DGUV) informiert ausführlich über die Vorschriften zur beruflichen Beurteilung bei Epilepsie und nach erstem epileptischem Anfall.24
Fahrerlaubnis2,5,25
- Bei einer Epilepsie wird eine Fahrerlaubnis nur in genau definierten Ausnahmefällen gewährt, z. B. bei einer länger anhaltenden, dokumentierten Anfallsfreiheit.
- Siehe auch Artikel Beurteilung der Fahreignung.
- Siehe Tabelle: Einschränkung der Kraftfahreignung bei Epilepsie.
- Dabei werden grundsätzlich unterschiedlich beurteilt:
- Fahrerlaubnis Gruppe 1: Kraftfahrzeuge bis 3,5 Tonnen und Motorräder
- Fahrerlaubnis Gruppe 2: Kraftfahrzeuge ab 3,5 Tonnen, Berufskraftfahrer mit und ohne Personenbeförderung
- Die behandelnden Ärzt*innen sind per Gesetz dazu verpflichtet, die Patient*innen über eine bestehende Fahruntauglichkeit aufzuklären.
- Die Aufklärung sollte gut dokumentiert sein, etwa durch einen handschriftlichen, mit Datum versehenen Eintrag in der Patientenakte oder auf einem von den Patient*innen unterzeichneten Aufklärungsbogen.
- Für die Ärzt*innen besteht bei Epilepsie keine generelle Meldepflicht gegenüber den Verkehrsüberwachungsbehörden, aber ein Melderecht in Extremfällen.25
- Uneinsichtige Patient*innen, deren Missachtung des Fahrverbots eine Gefahr für die öffentliche Sicherheit darstellen würde, dürfen die behandelnden Ärzt*innen auch entgegen der ärztlichen Schweigepflicht den Verkehrsüberwachungsbehörden melden.
Schwangerschaft
- Frauen mit Epilepsie sollten eine perinatale Beratung erhalten (Näheres dazu im Abschnitt Fertilität, Schwangerschaft, Geburt).
Freizeitaktivitäten
- Einige Freizeitaktivitäten sind nicht zu empfehlen, z. B. Klettern oder Schwimmen ohne Begleitung.
- Gleichwohl treten Anfälle relativ selten auf, während die Patient*innen aktiv sind; sie können aber danach auftreten.
- Näheres zu diesem Thema finden Sie im Abschnitt Empfehlungen für Patient*innen.
Patienteninformationen in Deximed
- Epilepsie
- Wie entsteht Epilepsie?
- Wie wird Epilepsie nachgewiesen?
- Welche Formen der Epilepsie gibt es?
- Akuter epileptischer Anfall
- Epilepsie – Was können Sie selbst tun?
- Epilepsie und Schwangerschaft
- Epilepsie und Empfängnisverhütung
- Führerschein und Berufswahl bei Epilepsie
Weitere Informationen
- Gesundheitsinformation.de: Epilepsie
Patientenorganisationen
Illustrationen
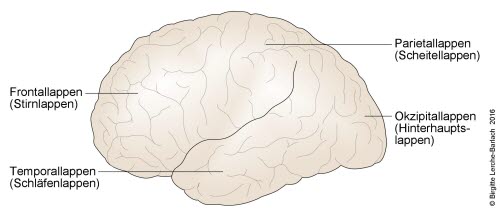
Großhirnrinde: laterale Übersicht
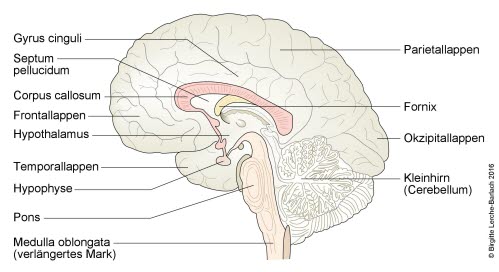
Gehirn: mediale Übersicht
Quellen
Leitlinien
- Deutsche Gesellschaft für Neurologie. Erster epileptischer Anfall und Epilepsien im Erwachsenenalter. AWMF-Leitlinie Nr. 030-041. S1, Stand 2017. www.awmf.org
- Deutsche Gesellschaft für Neurologie. Status epilepticus im Erwachsenenalter. AWMF-Leitlinie Nr. 030-079. S2k, Stand 2020. www.awmf.org
- Gesellschaft für Neuropädiatrie. Diagnostische Prinzipien bei Epilepsien des Kindesalters. AWMF-Leitlinie Nr. 022-007. S1, Stand 2017. www.awmf.org
- Deutsche Gesellschaft für Suchtforschung und Suchttherapie. Alkoholbezogene Störungen: Screening, Diagnostik und Behandlung alkoholbezogener Störungen. AWMF-Leitlinie Nr. 076-001. S3, Stand 2021. www.awmf.org
- Dachverband Osteologie. Prophylaxe, Diagnostik und Therapie der Osteoporose. AWMF-Leitlinie Nr. 183-001. S3, Stand 2017. www.awmf.org
Literatur
- Fisher RS, Acevedo C, Arzimanoglou A et al. ILAE official report: a practical clinical definition of epilepsy. Epilepsia 2014; 475–482, DOI: 10.1111/epi.12550 DOI
- Deutsche Gesellschaft für Neurologie. Erster epileptischer Anfall und Epilepsien im Erwachsenenalter. Entwicklungsstufe S1, AWMF-Leitlinie Nr. 030/041, Stand April 2017. www.awmf.org
- Deutsche Gesellschaft für Neurologie. Status epilepticus im Erwachsenenalter. AWMF-Leitlinie Nr. 030-079, S2k, Stand 2020. www.awmf.org
- Brandt C, Informationszentrum Epilepsie (ize) der Dt. Gesellschaft für Epileptologie e.V.: Epilepsie in Zahlen. Informationsblatt 006; Stand März 2016. www.izepilepsie.de
- Brandt C. Akut-symptomatische epileptische Anfälle: Inzidenz, Prognose und Aspekte der antiepileptischen Behandlung. Aktuelle Neurologie 2012, 480-485. DOI:10.1055/s-0032-1329984 DOI
- Deutsches Institut für Medizinische Dokumentation und Information (DIMDI): ICD-10-GM Version 2021. Stand 18.09.2020; letzter Zugriff 30.03.2021. www.dimdi.de
- Gesellschaft für Neuropädiatrie. Diagnostische Prinzipien bei Epilepsien des Kindesalters. AWMF-Leitlinie Nr. 022/007, Klasse S1, Stand 2017. www.awmf.org
- Nevitt SJ, Sudell M, Weston J, et al. Antiepileptic drug monotherapy for epilepsy: a network meta-analysis of individual participant data. Cochran Database Syst Rev 2017; 6: CD011412. pmid:28661008 PubMed
- Deutsche Gesellschaft für Suchtforschung und Suchttherapie. Alkoholbezogene Störungen: Screening, Diagnostik und Behandlung alkoholbezogener Störungen. AWMF-Leitlinie Nr. 076-001. S3, Stand 2021. www.awmf.org
- Krumholz A, Wiebe S, Gronseth GH, et al. Evidence-based guideline: Management of an unprovoked first seizure in adults. Neurology 2015; 84: 1705-13. doi:10.1212/WNL.0000000000001487 DOI
- PRAC recommends strengthening the restrictions on the use of valproate in women and girls. European Medicines Agency. 10/10/2014 www.ema.europa.eu
- Arzneimittelkommission der deutschen Ärzteschaft (AkdÄ). Wichtige Arzneimittelinformation für Ärzte und Apotheker. Arzneimittel, die Valproat und -verwandte Substanzen enthalten: Risiko für Anomalien des Neugeborenen. Dezember 2014. Internetressource; letzter Zugriff 26.01.2018. www.akdae.de
- Bundesinstitut für Arzneimittel und Medizinprodukte. Informationsbrief zur Einführung einer Patientenkarte für Arzneimittel, die Valproat und verwandte Substanzen enthalten. 13.07.2017; letzter Zugriff 26.01.2018. www.bfarm.de
- Carmichael K, Pulman J, Lakhan SE, et al. Zonisamide add-on for drug-resistant partial epilepsy. Cochrane Database Syst Rev. 2013 ;12:CD001416. doi: 10.1002/14651858.CD001416.pub3. DOI
- Shi LL, Dong J, Ni H, et al. Felbamate as an add-on therapy for refractory epilepsy. Cochrane Database Syst Rev. 2014 Jul 18;7:CD008295. DOI: 10.1002/14651858.CD008295.pub3 DOI
- Brodie MJ, Barry SJE, Bamagous GA et al. Patterns of treatment response in newlydiagnosed epilepsy. Neurology 2012; 1548–1554, DOI: 10.1212/WNL.0b013e3182563b19 DOI
- Strozzi I, Nolan SJ, Sperling MR, Wingerchuk DM, Sirven J. Early versus late antiepileptic drug withdrawal for people with epilepsy in remission. Cochrane Database of Systematic Reviews 2015, Issue 2. Art. No.: CD001902. DOI: 10.1002/14651858.CD001902.pub2. DOI
- Stockings E, Zagic D, Campbell G, et al. Evidence for cannabis and cannabinoids for epilepsy: a systematic review of controlled and observational evidence. J Neurol Neurosurg Psychiatry 2018 Mar 6; pii: jnnp-2017-317168: Epub ahead of print. pmid:29511052 PubMed
- Panebianco M, Rigby A, Weston J, Marson AG. Vagus nerve stimulation for partial seizures. Cochrane Database of Systematic Reviews 2015, Issue 4. Art. No.: CD002896. DOI: 10.1002/14651858.CD002896.pub2. DOI
- DeGiorgio CM, Soss J, Cook IA, et al. Randomized controlled trial of trigeminal nerve stimulation for drug-resistant epilepsy. Neurology 2013 Feb 26;80(9):786-91. doi:10.1212/WNL.0b013e318285c11a. DOI
- Cheuk DK, Wong V. Acupuncture for epilepsy. Cochrane Database Syst Rev. 2014 May 7;5:CD005062. Cochrane (DOI)
- Dachverband Osteologie. Prophylaxe, Diagnostik und Therapie der Osteoporose. AWMF-Leitlinie Nr. 183-001. S3, Stand 2017. www.awmf.org
- Nadebaum C, Anderson VA, Vajda F, et.al. Language skills of school-aged children prenatally exposed to antiepileptic drugs. Neurology 2011; 76: 719-26. pubmed.ncbi.nlm.nih.gov
- Deutsche Gesetzliche Unfallversicherung Spitzenverband: Berufliche Beurteilung bei Epilepsie und nach erstem epileptischen Anfall. DGUV Information 250-001; Stand der Vorschrift: Januar 2015. publikationen.dguv.de
- 50. Deutscher Verkehrsgerichtstag. 25.-27.01.2012. Empfehlungen. Online-Ressource; letzter Zugriff 01.04.2021. www.deutscher-verkehrsgerichtstag.de
Autor*innen
- Thomas M. Heim, Dr. med., Wissenschaftsjournalist, Freiburg
- Die ursprüngliche Version dieses Artikels basiert auf einem entsprechenden Artikel im norwegischen hausärztlichen Online-Handbuch Norsk Elektronisk Legehåndbok (NEL, https://legehandboka.no/).