Prüfungsrelevant für die Facharztprüfung Allgemeinmedizin1
- Lungenfunktion, Reversibilitätstest
- Stadieneinteilungen:
- Grade der Asthmakontrolle nach der NVL Asthma
- Therapeutische Optionen
- Disease-Management Programm Asthma und COPD
Allgemeine Informationen
Definition
- Asthma ist eine heterogene, chronisch-entzündliche Erkrankung der Atemwege, die durch bronchiale Hyperreagibilität und variable Atemwegsobstruktion zu respiratorischen Symptomen führt.2-4
- Man unterscheidet grundsätzlich folgende Formen:2
- allergisches (extrinsisches) Asthma
- Auslöser sind spezifische Allergene.
- Assoziation mit anderen allergischen/atopischen Erkrankungen
- nichtallergisches (intrinsisches) Asthma
- Auslöser sind z. B. Infektionen der Atemwege oder Medikamentenintoleranz (häufig ASS oder NSAR)
- weitere Phänotypen
- z. B. eosinophiles Asthma oder Cough Variant Asthma.
- allergisches (extrinsisches) Asthma
- Die Atemwegsobstruktion bei Asthma basiert in erster Linie auf folgenden Vorgängen:4
- Konstriktion der glatten Bronchialmuskulatur
- Ödem der Schleimhäute in den Atemwegen
- Umbau der Atemwegswände („Remodeling“)
- Sekretansammlung.
- Verschiedene Auslöser können bei bronchialer Hyperreagibilität zu einer Bronchokonstriktion führen:
- Bei akuten Asthmaanfällen bzw. Exazerbationen kommt es zu einer temporären Verschlechterung der Symptomatik und Lungenfunktion.
- Die Ausprägung ist sehr variabel und reicht von leichten bis zu potenziell lebensbedrohlichen Verläufen.
- Die Diagnose des Asthmas ist im Wesentlichen eine klinische, auf Basis der Symptome mit Nachweis einer variablen Atemwegsobstruktion bzw. bronchialen Hyperreagibilität.
- Die Behandlung erfolgt als medikamentöse Stufentherapie und richtet sich nach dem Grad der Asthmakontrolle unter der jeweiligen Behandlung.
- Auch Patientenschulung und Einweisung in Inhalationstechniken sind essenzieller Bestandteil der Therapie.
- Für Asthma existieren eine Leitlinie der Deutschen Gesellschaft für Pneumologie (DGP) und eine Nationale VersorgungsLeitlinie (NVL), die 2020 aktualisiert wurde.2,4
Definition schweres Asthma2
- Bei Erwachsenen liegt ein schweres Asthma vor, wenn unter Therapie mit inhalativen Kortikosteroiden (ICS) in Höchstdosis und mindestens 1 zusätzlichen Langzeitmedikament (langwirkendes Beta-2-Sympathomimetikum oder Montelukast) oder oralen Kortikosteroiden (OCS) > 6 Monate/Jahr mindestens einer der folgenden Punkte zutrifft bzw. bei Reduktion der Therapie zutreffen würde:
- Atemwegsobstruktion: FEV1 < 80 % des Sollwertes (FEV1/FVC < LLN)
- häufige Exazerbationen: ≥ 2 kortikoidsteroidpflichtige Exazerbationen in den letzten 12 Monaten
- schwere Exazerbationen: ≥ 1 Exazerbation mit stationärer Behandlung oder Beatmung in den letzten 12 Monaten
- teilweise kontrolliertes oder unkontrolliertes Asthma.
Häufigkeit
- Häufigkeit von Asthma weltweit
- Die Prävalenz von Asthma ist in den westlichen Industrienationen höher als in Entwicklungs- und Schwellenländern.4
- Weltweit litten im Jahr 2015 geschätzt 358,2 Mio. Menschen an Asthma, und die Zahl der Todesfälle durch Asthma liegt bei etwa 400.000.5
- Während die Prävalenz von Asthma in der westlichen Welt in den letzten Jahrzehnten zugenommen hat, nahm die Zahl der Krankenhauseinweisungen und Todesfälle deutlich ab.5-7
- Als mögliche Gründe für den Anstieg der Häufigkeit in den letzten Jahrzehnten werden diskutiert:
- Häufigkeit in Deutschland (Erwachsene)
- In Deutschland beträgt die 12-Monats-Prävalenz bei Erwachsenen 6,2 %.13
- Frauen sind häufiger als Männer betroffen (7,1 % vs. 5,4 %)
- In der unteren Bildungsgruppe kommt Asthma häufiger vor als in höheren Bildungsgruppen.
- Die Lebenszeitprävalenz liegt bei knapp 10 %.14
- Der Unterschied der Prävalenzen erklärt sich durch die Möglichkeit einer Remission der Erkrankung.
- In Deutschland beträgt die 12-Monats-Prävalenz bei Erwachsenen 6,2 %.13
- Häufigkeit in Deutschland (Kinder und Jugendliche)
Ätiologie und Pathogenese
- Asthma beschreibt eine heterogene Gruppe von Erkrankungen mit unterschiedlichen pathophysiologischen Mechanismen.4
- Die Entstehung von Asthma ist multifaktoriell mit genetischer Disposition und exogenen Faktoren sowie Verstärkung durch psychosoziale Aspekte.2
- Lebensumstände wie Ernährung und Hygiene spielen vermutlich eine große Rolle, da es zwischen verschiedenen Weltregionen große Unterschiede in der Häufigkeit von Asthma gibt.
Ursachen für Asthma
- Genetische und epigenetische Faktoren
- Es existiert eine komplexe, polygene erbliche Veranlagung für Asthma.
- Zahlreiche Gene, die mit einem erhöhten Asthmarisiko assoziiert sind, wurden bisher identifiziert.10
- Genetische Faktoren scheinen vor allem bei Asthma vor dem 12. Lebensjahr eine wichtige Rolle zu spielen.9
- Atopische Erkrankungen, wie das atopische Ekzem, bei den Eltern und Geschwistern erhöhen die Wahrscheinlichkeit, dass das Kind Atopie und Asthma entwickelt.16
- Umweltfaktoren
- Luftverschmutzung, z. B. durch Verkehr in Städten, scheint mit einem höheren Risiko für Asthma assoziiert zu sein.11
- Dieselabgase enthalten polyzyklische aromatische Kohlenwasserstoffe (PAH), Stickoxid (NO) und Mikropartikel. Studien zeigen, dass Exposition zur Verschlechterung von FEV1 und zur Verstärkung der Atemwegsentzündung führt.17
- Verschmutzung und Allergene in Innenräume, z. B. Hausstaubmilben, Rauch oder Hautschuppen von Tieren können zur Entstehung von Asthma beitragen.18
- Ursächliche Faktoren im Arbeitsmilieu sind Allergene von Pelztieren, Fischprodukten, Mehl und Baumaterial, Gase und Chemikalien.
- Exposition gegenüber Zigarettenrauch in der Schwangerschaft und frühen Kindheit führt zu einem erhöhten Erkrankungsrisiko.
- In Schottland wurde nach Einführung des Rauchverbots ein Rückgang der Anzahl stationärer Behandlungen von Kindern mit Asthma von 18 % festgestellt.19
- Eine Kindheit auf einem Bauernhof (Diversität an Mikroorganismen) hat eine protektive Wirkung.20-21
- Allergien gegen Hausstaubmilben und Katzen gelten als wichtiger Faktor bei der Entwicklung von Allergien.15,22
- Exposition gegenüber Tieren
- Die Frage, ob Haustiere allergiefördernd oder -präventiv wirken, ist zum jetzigen Zeitpunkt nicht eindeutig geklärt.4
- Die aktuelle deutsche Leitlinie zur Allergieprävention empfiehlt:23
- Personen ohne erhöhtes Allergierisiko sollten die Haustierhaltung nicht einschränken.
- Familien mit erhöhtem Allergierisiko sollten keine Katzen anschaffen.
- Hundehaltung ist nicht mit einem höheren Allergierisiko verbunden.
- Anhaltende Tierkontakte in den ersten Lebensjahren scheinen mit einem reduzierten Risiko für Asthma oder andere atopische Erkrankungen assoziiert zu sein.20
- Exposition gegenüber Katzenallergen kann zu einer Antikörperproduktion führen, jedoch ohne Sensitivierung. Dies könnte eine Erklärung für das reduzierte Asthmarisiko darstellen.24
- Rezidivierende Virusinfektionen der oberen Atemwege in einer frühen Lebensphase
- Es ist unklar, ob Infektionen an der Entstehung von Asthma beteiligt sind oder dieser vorbeugen (Hygiene-Hypothese).4
- In einer Studie wurde gezeigt, dass Atemwegsinfektionen das Risiko für Asthma vor dem Schulalter reduzieren.25
- Jedoch spielen respiratorische Virusinfektionen, besonders RSV- und Rhinovirusinfektionen, sowohl bei der Entstehung als auch beim Auslösen akuter Asthmaanfälle eine Rolle.26
- Adipositas
- Übergewicht ist mit der Entstehung der Erkrankung, einem schwereren Verlauf und schlechterem Therapieansprechen assoziiert.27
- Assoziation zu atopischen Erkrankungen28-31
- Medikamente
- Es wird empfohlen, Paracetamol und Breitbandantibiotika in der Schwangerschaft und ersten Lebensphase nur bei klarer Indikation einzusetzen.4
- Eine Metaanalyse zeigt Hinweise, dass die Exposition gegenüber Paracetamol früh im Leben mit einer Entwicklung von Asthma assoziiert ist.32
- Bei einer prospektiven Untersuchung einer Geburtskohorte aus 620 Kindern mit Allergieerkrankungen in der Familie wurde kein Zusammenhang zwischen einer Paracetamol-Einnahme und der Entwicklung von Asthma gefunden.33
- Eine Behandlung mit Breitbandantibiotika während der fetalen Entwicklung und in der frühen Lebensphase ist möglicherweise mit vermehrtem Auftreten von Asthma assoziiert. Eindeutige Belege fehlen aber bisher.34-35
- Es wird empfohlen, Paracetamol und Breitbandantibiotika in der Schwangerschaft und ersten Lebensphase nur bei klarer Indikation einzusetzen.4
Pathogenese
- Der Krankheitsprozess ist bei Asthma sehr variabel.
- Die Einteilung der Asthmaformen in Phänotypen folgt der Annahme, dass die Erkrankung bestimmter Patientengruppen sowohl durch eine ähnliche Pathophysiologie als auch durch ähnliche klinische Merkmale gekennzeichnet ist.2
- Man unterscheidet folgende Phänotypen:2
- allergisches (extrinsisches) Asthma
- atopische Disposition
- häufig begleitet von Allergien
- Nachweis spezifischer IgE im Serum
- saisonaler (z. B. Gräserpollen) oder perennialer (z. B. Hausstaubmilben) Verlauf
- nichtallergisches (intrinsisches) Asthma
- ohne Nachweis einer Sensibilisierung
- oft Atemwegsinfektion als Trigger
- weitere Sonderformen (siehe nächster Abschnitt)
- allergisches (extrinsisches) Asthma
- Asthma kann auf verschiedenen Wegen Einfluss auf die Atemwege haben:
- Veränderungen der Schleimhäute
- Veränderungen der Immunantwort
- Veränderungen der neuromuskulären Antwort
- Veränderungen der Gefäßversorgung.
- Meist kommt es zu einem erhöhten Aufkommen von eosinophilen Granulozyten, Mastzellen, T-Lymphozyten und Entzündungsmediatoren und anderen Zytokinen in den Atemwegen.
- Die Entzündungs- und Wachstumsfaktoren führen zu einer Hypertrophie und Hyperplasie der glatten Muskulatur und dadurch zur Obstruktion.
- Die Reflexaktivität und Sensibilität der Bronchialwand ist verändert, was zu der bronchialen Hyperreagibilität beiträgt.
Sonderformen des Asthmas4
- „Type-2
"“- bzw. „Type-2-High"“-Asthma- Beruht auf der Erkenntnis, dass bestimmte Zytokine wie IL-5 und IL-13 nicht nur von Allergen-spezifischen T-Helfer-Zellen, sondern auch von Allergen-unspezifischen „Innate Lymphoid Cells
"“ (ILC2) freigesetzt werden können. - Klinisch bedeutsam könnte der Phänotyp eines „Type-2-High
"“-Asthmas für das Ansprechen auf eine Therapie mit inhalativen Glukokortikosteroiden oder bestimmten Anti-Interleukin-Biologika sein. - Umstritten ist jedoch, welcher klinische Biomarker (wie z. B. exhaliertes NO oder Periostin) ein „Type-2-High
"“-Asthma am besten identifiziert.
- Beruht auf der Erkenntnis, dass bestimmte Zytokine wie IL-5 und IL-13 nicht nur von Allergen-spezifischen T-Helfer-Zellen, sondern auch von Allergen-unspezifischen „Innate Lymphoid Cells
- Eosinophiles versus nicht-Eosinophiles Asthma
- Die Unterscheidung der Subtypen erfolgt vor allem anhand von Sputum- Untersuchungen und anhand des Differenzialblutbildes.
- Ab welchem Grenzwert der Bluteosinophilen-Konzentration von einer „Blut-Eosinophilie
"“ gesprochen werden kann, ist noch nicht abschließend geklärt.- Würde man einen Grenzwert von 150 Eosinophilen/μl postulieren, wäre die Mehrheit „eosinophil
"“, würde man einen Grenzwert von 300 Eosinophilen/μl postulieren, wäre die Mehrheit „nicht-eosinophil"“. - Definition laut NVL: 2-maliger Nachweis ≥ 300 Eosinophilen/μl Blut außerhalb von Exazerbationen in den vergangenen 2 Jahren2
- Würde man einen Grenzwert von 150 Eosinophilen/μl postulieren, wäre die Mehrheit „eosinophil
- Therapeutisch bedeutsam ist, dass sich die Patient*innen mit eosinophilem und nicht-eosinophilem Asthma in ihrem Ansprechen auf ICS deutlich unterscheiden.
- Desweiteren gewinnt diese Klassifikation eine zunehmende Bedeutung für die Indikationsstellung einer Biologikatherapie, da eine Eosinophilenvermehrung das Ansprechen auf bestimmte Biologika wahrscheinlicher macht (wie Anti-IgE, Omalizumab oder Anti-IL-4-Rezeptor alpha, Dupilumab) oder überhaupt erst ein Ansprechen voraussagt (wie bei den Anti-IL-5-Biologika Mepolizumab, Reslizumab und Benralizumab).
- „Cough Variant Asthma“
- Patient*innen leiden unter chronischem, trockenem Husten aufgrund einer unspezifischen bronchialen Hyperreagibilität ohne weitere typische Asthmasymptome.
- Die Lungenfunktion und die Röntgenaufnahme der Thoraxorgane sind normal.
- 1/3 der Patient*innen mit Cough-Variant-Asthma entwickelt im weiteren Verlauf ein klassisches Asthma.
- Patient*innen mit Cough-Variant-Asthma sprechen gut auf klassische antiasthmatische Therapieoptionen an, eine frühzeitige Therapie kann den Übergang in ein klassisches Asthma verhindern.
- Aspirin Exacerbated Airway Disease (AERD)
- früher: „Asthma bei Aspirinintoleranz
"“ - Intoleranz gegenüber Hemmern der Cyclooxygenase-1 (COX-1) wie Acetylsalicylsäure (ASS) oder Ibuprofen
- Es wird vermutet, dass diese pharmakologische Intoleranz eine vorbestehende Schädigung der Atemwege lediglich aggraviert, nicht jedoch auslöst.
- Die genaue Prävalenz ist unklar, Angaben schwanken zwischen 5,5 % und 12,4 % der Asthma-Patient*innen.
Klassischerweiseklassischerweise begleitet von Nasenpolypen und chronischer Sinusitis (Samter-Trias)
- früher: „Asthma bei Aspirinintoleranz
- Asthma bei älteren Patient*innen
- häufig unterdiagnostiziert, u. a. da im fortgeschrittenen Alter seltener
- Unterscheidung zur COPD bei Älteren schwieriger
- Hinweise sind: erhöhtes Gesamt-IgE, Eosinophilie, nächtliche Zunahme.
- Anstrengungsinduzierte Bronchokonstriktion
- früher: „Anstrengungsasthma
"“ - Körperliche Belastung führt zur Atemwegsobstruktion.
- Als Ursache wird eine wiederholte Austrocknung der Schleimhäute, die ein Remodeling der Atemwege und die Entwicklung einer bronchialen Hyperreagibilität fördert, postuliert.
- Tritt gehäuft bei Ausdauersportarten (vermehrte Atemleistung) auf.
- Cave bei Sportler*innen: Behandlung mit Beta-2-Sympathomimetika unterliegt den Regularien der WADA (World Anti-Doping Association)!
- früher: „Anstrengungsasthma
Prädisponierende Faktoren
Faktoren, die die Entstehung und Ausprägung von Asthma beeinflussen
- Genetische Prädisposition
- Kinder mit genetischer Vorbelastung (sog. Risikokindern) sind dadurch definiert, dass mindestens ein Elternteil oder Geschwister unter einer atopischen Erkrankung leidet.23
- Allergenexposition
- Umweltbedingungen
- Atemwegsinfektionen
- Tabakrauch
- Berufliche Exposition
- Psychosozialen Belastungen
- Geschlecht
- Körpergewicht
- Sonnenexposition (Vitamin D)
- Ernährung
- Medikamente
Auslösende Faktoren
- Siehe auch die Artikel Asthmaanfall bei Erwachsenen und Asthmaanfall bei Kindern und Jugendlichen.
- Es gibt zahlreiche Faktoren, die einen akuten Asthmaanfall auslösen können:
- Atemwegsinfektionen, v. a. viraler Genese36
- Allergenexposition
- Exposition gegenüber (Tabak-)Rauch
- kalte Luft
- körperliche Belastung
- psychische Belastung (Angst)
- Medikamente (z. B. Betablocker oder ASS).
- Eine Metaanalyse kommt zu dem Ergebnis, dass bei 7 % der erwachsenen Asthma-Patient*innen und bei 15 % der Patient*innen mit schwerem Asthma Acetylsalicylsäure als auslösender Faktor infrage kommt.37
ICPC-2
- R96 Asthma
ICD-10
- J45 Asthma
- J45.0 Vorwiegend allergisches Asthma bronchiale
- J45.1 Nichtallergisches Asthma bronchiale
- J45.8 Mischformen des Asthma bronchiale
- J45.9 Asthma bronchiale, nicht näher bezeichnet
- J46 Status asthmaticus, inkl. akutes schweres Asthma bronchiale
Diagnostik
Diagnostische Kriterien
- Die Diagnose des Asthmas stützt sich auf:2
- eingehende Anamnese einschließlich Familienanamnese
- charakteristische körperliche Befunde
- Lungenfunktionsprüfung
- Nachweis einer variablen, meist reversiblen Atemwegsobstruktion
- Nachweis einer bronchialen Hyperreagibilität
- Ein Beschwerdebeginn im Erwachsenenalter spricht nicht gegen ein Asthma.
- Das eosinophile Asthma scheint sich im Gegensatz zum allergischen Asthma bevorzugt in der 2. Lebenshälfte zu manifestieren.2
- Häufig kann die Diagnose nicht bei der ersten Vorstellung gestellt werden.
- Die Verlaufsbeobachtung ist wichtiger Bestandteil der Diagnostik.
- Die wichtigste Differenzialdiagnose im Erwachsenenalter ist die chronische obstruktive Lungenerkrankung (COPD).
- Diagnostik und Therapie des Asthmas bei älteren Menschen bedarf besonderer Aufmerksamkeit.
- Komorbiditäten, verminderte Symptomwahrnehmung, Akzeptanz der Atemnot als Alterserscheinung2
Exazerbationen
- Zur Diagnostik und Therapie des akuten Asthmaanfalls siehe auch:
Leitlinien zur Diagnostik
- In Deutschland existieren sowohl eine Leitlinie von der Deutschen Gesellschaft für Pneumologie und Beatmungsmedizin (DGP)4 als auch eine Nationale Versorgungsleitlinie Asthma (NVL).2
.Zudem existiert die internationale Leitlinie Global Initiative for Asthma (GINA).3 Der folgende Leitlinienkasten fasst die gemeinsamen Aussagen der Leitlinien zusammen. - Deutliche Abweichungen voneinander sind kursiv gekennzeichnet.
Leitlinie: Diagnostik2-4
Die 4 Säulen der Diagnose Asthma
- Anamnese, Beschwerden und körperliche Untersuchung
- Reversible Atemwegsobstruktion
- Chronisch entzündliche Veränderung der Atemwege
- Bronchiale Hyperreagibilität
Kriterien für die Diagnose Asthma
- Diagnose gilt als gesichert bei:
- nachgewiesenem Vorliegen typischer Anamnese und Beschwerden
- nachgewiesener Obstruktion (FEV1/FVC < LLN [Lower Limit of Normal])
- nachgewiesener Reversibilität (Normalisierung der Lungenfunktion).
- Diagnose gilt als wahrscheinlich bei:
- nachgewiesenem Vorliegen typischer Anamnese und Beschwerden
- nachgewiesener Obstruktion (FEV1/FVC < LLN) und Teilreversibilität
- weitere Kriterien
- Therapieansprechen bzgl. Lungenfunktion und Symptome
- FEV1-Abfall durch körperliche Belastung (indirekte Provokation)
- bronchiale Hyperreagibilität im direkten Provokationstest oder PEF-Variabilität > 10 %
- teilreversible Obstruktion ohne Normalisierung der Lungenfunktion, aber mit klinischer Besserung unter Therapie.
- Diagnose gilt als unwahrscheinlich bei:
- untypischen Symptomen
- nichtreversibler Obstruktion
- fehlendem Nachweis einer Obstruktion
- fehlendem Nachweis einer bronchialen Hyperreagibilität.
Anamnese
- Klassische Symptome (variabel, ggf. episodenhaft mit zwischenzeitlicher Beschwerdefreiheit)
- Asthmaspezifische Anamnese
- Auslösefaktoren
- z. B. Atemwegsreize, Tages- und Jahreszeit, Aufenthaltsort und Tätigkeit
- bei Kindern oft körperliche Belastung (z. B. Spielen)
- Risikofaktoren
- Komorbiditäten
- z. B. Erkrankungen der oberen Atemwege, Adipositas, COPD
- Auslösefaktoren
- Gegen die Diagnose Asthma sprechen:
Klinische Untersuchung
- Zielt auf den Nachweis von Zeichen einer Atemwegsobstruktion ab.
- Der Untersuchungsbefund kann im Intervall unauffällig sein.
- Mögliche Befunde in der Untersuchung:
- angestrengte Atmung, Atemnot
- exspiratorischer Stridor
- Giemen oder pfeifendes Atemgeräusch
- erhöhte Atemfrequenz
- Einsatz der Atemhilfsmuskulatur
- im schweren Asthmaanfall fehlendes Atemgeräusch durch Überblähung („stille Lunge“), Zyanose, Blutdruckabfall, Erschöpfung, Verwirrtheit.
- Bei Kindern sollte zusätzlich geachtet werden auf:
- Atopie-Zeichen, z. B. atopisches Ekzem
- Einziehungen jugulär, interkostal und epigastrisch als Zeichen von Dyspnoe
- einen erhöhten Thoraxdurchmesser durch Überblähung
- Zeichen eines minderwüchsigen und dystrophen Kindes (erhöhte Atemarbeit)
- Differenzialdiagnosen ausschließen (z. B. Mukoviszidose, Immundefekt, Ziliendysfunktion etc.).
Lungenfunktionsdiagnostik
- Um die Diagnose eines Asthmas zu erhärten, soll eine variable, (partiell) reversible Atemwegsobstruktion durch eine Lungenfunktionsprüfung, typischerweise durch Spirometrie, nachgewiesen werden.
- Normalbefund in der Lungenfunktionsdiagnostik schließt ein Asthma nicht aus.
Spirometrie
- Mit Darstellung der vollständigen Fluss-Volumen-(FV)-Kurve (ggf. in der Hausarztpraxis)
- Messung forcierte Vitalkapazität (FVC), Einsekundenkapazität (FEV1) und Verhältnis FEV1/FVC (Tiffeneau-Index)
- Bewertung der besten Werte aus 3 akzeptablen Messungen ohne ausgeprägte Differenz (bis 5 %) der Ergebnisse
- Bild einer obstruktiven Ventilationsstörung
- Reduktion des altersabhängigen Quotienten aus FEV1 und FVC (Tiffeneau-Index)
- Reduktion der absoluten Einsekundenkapazität
- Reduktion der maximalen endexpiratorischen Atemstromstärke
- Zur Interpretation der Ergebnisse verweist die NVL auf die DGP-Leitlinie Spirometrie.38
- Bewertung anhand der altersspezifischen Referenzwerte der Global Lung Initiative (GLI)3-4
- altersspezifische Grenze für unteren Normwert (5. Perzentile)
- Unterer Normwert wird als LLN („Lower Limit of Normal“) bezeichnet.
- Im Erwachsenenalter Einteilung der Obstruktion in 3 Schweregrade:
- Eine Obstruktion liegt vor, wenn FEV1/FVC < LLN.
- leichte Obstruktion: FEV1 ≥ 85 % LLN (> 60 % Soll)
- mittelschwere Obstruktion: FEV1 55–84 % LLN (40–60 % Soll)
- schwere Obstruktion bei FEV1 < 55 % LLN (< 40 % Soll).
- Eine Obstruktion liegt vor, wenn FEV1/FVC < LLN.
- Im Kindesalter keine Einteilung in Schweregerade entsprechend FEV1/FVC wie bei Erwachsenen
- stattdessen Angabe z-Werte (Standardabweichungen, die ein Messwert vom Soll-Mittelwert abweicht)
Reversibilitätstestung
- Bei Patient*innen mit nachgewiesener Atemwegsobstruktion ist zur Bestätigung ein Reversibilitätstest mit SABA empfohlen.
- Reversible Obstruktion spricht eher für Asthma, „fixierte“ Obstruktion eher dagegen.
- Eine Reversibilitätstestung kann auch bei einer „normalen" Lungenfunktion sinnvoll sein, da der persönliche Bestwert trotz des im Normbereich liegenden Wertes deutlich höher sein kann.
- Spirometrie vor und 15
Minutenmin nach Inhalation von Bronchodilatatoren - Bei Erwachsenen Inhalation eines kurzwirksamen Beta-2-Sympathomimetikums (z. B. bis zu 400 μg Salbutamol in 4 separaten Dosen)
- alternativ kurzwirksames Anticholinergikum (SAMA, 160 μg Ipratropiumbromid)
- alternativ erneute Spirometrie nach 2-mal täglicher Inhalation einer hohen ICS-Dosis über mindestens 4 Wochen
- alternativ erneute Spirometrie nach 7 bis
maximalmax. 14 Tagen oraler Einnahme von 20–40 mg Prednisolon pro Tag
- Bei Kindern ebenfalls Inhalation eines kurzwirksamen Beta-2-Sympathomimetikums (SABA) bis zu 4 Hübe eines Dosieraerosols (z. B. Salbutamol à 100 μg)
- FEV1-Zunahme um > 12 % bzw. um 200 ml (bei Erwachsenen) gilt als positiv.
- Fehlende Reversibilität in einem Reversibilitätstest schließt Asthma jedoch nicht aus.
Messung der Hyperreagibilität (Provokationstest)
- Sofern die Lungenfunktion nicht eingeschränkt ist, aber die Anamnese für ein Asthma spricht, sollte die Diagnose durch den Nachweis einer unspezifischen bronchialen Hyperreagibilität erhärtet werden.
- Voraussetzungen: Beachtung von Kontraindikationen und Erfahrung der Anwender*innen
- Überlegenheit der Ganzkörper-Bodyplethysmografie zur Interpretation der Bronchoprovokation auf der Basis des spezifischen Atemwegswiderstands (flächendeckende Verfügbarkeit in pneumologischen Praxen)
- Methoden der Provokationstestung
- unspezifische inhalative Provokation mit Pharmaka (z. B. Methacholin)
- standardisierte Belastung (mittels Laufband, „Free-Running-Test" besonders bei Kleinkindern oder – eher weniger geeignet – Fahrradergometer)
- Kaltluftprovokation
- Im klinischen Alltag häufig direkte Stimulation mit Methacholin und Messung der Hyperreagibilität
- Bei Kindern mit Beschwerden bei körperlicher Anstrengung wird ein Lauf-Belastungstest empfohlen.
- Test wird als positiv gewertet bei:
- FEV1-Abfall ≥ 20 %
- Verdopplung des spezifischen Atemwegswiderstandes ≥ 2,0 kPa x sec
- Abfall der FEV1 um 10 % bei rein körperlicher Belastung ohne pharmakologische Provokation (10–15 % bei Kindern)
Ganzkörper-Plethysmografie (bei Lungenfachärzt*innen)
- Beurteilung des intrathorakalen Gasvolumens (Überblähung?) und der Atemwegswiderstände
- bei fraglicher spirometrischer Obstruktion oder mangelhafter Mitarbeit hilfreich
- insbesondere zur Differenzialdiagnose zwischen Asthma und COPD empfohlen
- Erlaubt im Gegensatz zur Spirometrie die Beurteilung einer Lungenüberblähung.
- Eine Alternative stellen Oszillations- oder Okklusionsverfahren zur Bestimmung des Atemwiderstandes dar.
Diffusionskapazität für Kohlenmonoxid (DLCO; bei Pneumolog*innen)
- Messung des intrapulmonalen Gasaustausches
- Bei Asthma üblicherweise nicht verändert
- Abgrenzung zu COPD
Messung des exspiratorischen Spitzenfluss (Peak Expiratory Flow, PEF) (in der Hausarztpraxis, ggf. Selbstmessung)
- Entsprechend der aktuellen NVL kein Stellenwert in der Primärdiagnostik
- Die Diagnose des Asthmas soll nicht ausschließlich durch Anwendung der Peak-Flow-Messung (PEF) gestellt werden.
- in Deutschland breite Verfügbarkeit der Provokationstestung
- Die häusliche Messung des PEF-Wertes ist jedoch für die Beurteilung des Verlaufs der Erkrankung und der Beurteilung der Asthmakontrolle hilfreich.
- Ergänzende häusliche Messung 2 x tgl., Bestimmung der PEF-Variabilität
- ggf. zur Verlaufsbeobachtung und Beurteilung der Asthmakontrolle
- Bei Kindern nicht generell empfohlen
Weitere Untersuchungen
Fraktion von Stickstoffmonoxid (FeNO) in der Ausatemluft
- Kann zur Diagnosesicherung eingesetzt werden.
- Diagnostischer Zusatznutzen von FeNO in der Primärdiagnostik ist Gegenstand der aktuellen Forschung.
- Hohe FeNO-Werten erhöhen die Wahrscheinlichkeit für die Diagnose Asthma und für das Ansprechen auf ICS.
- Ein niedriger FeNO-Wert schließt die Diagnose Asthma nicht aus.
- Der empfohlene Grenzwert (laut der American Thoracic Society) liegt für Kinder bei FeNO < 20 ppb (< 25 ppb bei Erwachsenen).
- Bei erhöhten Werten Therapie-Adhärenz prüfen, ggf. ICS-Dosis erhöhen.
- Cave: Während die DGP die FeNO-Bestimmung als „wertvollen Baustein im Rahmen von Diagnostik und Management" bezeichnet, sieht die NVL „die Anwendung von FeNO in der Diagnostik als nicht ausreichend im Nutzen belegt, da konfirmatorische Studien fehlen, die den diagnostischen Zusatznutzen abschließend klären würden."
Röntgenuntersuchung
- Laut NVL keine Indikation für den routinemäßigen Einsatz
- Laut DGP bei Erwachsenen bei Erstdiagnose Röntgen des Thorax in 2 Ebenen empfohlen
- zum Ausschluss von Differenzialdiagnosen
- ggf. CT für weitere pulmonale Differenzialdiagnosen
- Bei Kindern und Jugendlichen nicht generell empfohlen
Labordiagnostik
- Bei fehlendem Ansprechen auf die Therapie, häufigen Bronchialinfekten, Lungeninfiltraten oder bei schwerem Asthma sollte aus differenzialdiagnostischen Gründen eine ergänzende Labordiagnostik erfolgen.
- Leukozytenzahl und CRP bei V. a. Infektexazerbation
- absolute Eosinophilenzahl (Eosinophile/μl) als Marker für eosinophile Atemwegsentzündung und die Wirksamkeit einer Anti-IL-5-Therapie
- Gesamt-IgE im Blut
- bei Werten über 100 kU/l Hinweis auf allergische Genese des Asthmas
- bei Werten > 1 000 kU/l und kompliziertem Verlauf Hinweis auf eine andere Genese der Probleme, wie das Churg-Strauss-Syndrom oder die allergische bronchopulmonale Aspergillose
Allergologische Stufendiagnostik
- Sollte laut NVL nur bei Patient*innen mit V. a. allergisches Asthma durchgeführt werden.
- Sollte laut DGP bei jeder Erstdiagnose durchgeführt werden.
- Stufendiagnostik
- Allergieanamnese einschließlich Berufsanamnese (ggf. Fragebogen)
- Allergie-Hauttestung (z. B. Prick-Test)
- Bestimmung von spezifischem und Gesamt-IgE
- ggf. allergenspezifischen Organprovokationstests
- diagnostische Expositionskarenz
Überprüfung der Diagnose
- Die Diagnose Asthma soll laut NVL überprüft bzw. infrage gestellt werden:
- bei unzureichender Kontrolle trotz leitliniengerechter Therapie – oder –
- nach einem mehrmonatigen Auslassversuch unter Berücksichtigung saisonaler Triggerfaktoren.
- Ziel ist die Vermeidung von Fehldiagnosen und einer Über- bzw. Fehlversorgung.
- Die DGP weist zudem darauf hin, dass die Diagnose Asthma nicht immer bereits bei der Eingangsuntersuchung gestellt werden kann. Daher sind Verlaufsbeobachtungen sinnvoll, da sie Aufschluss über die spontanen und/oder medikamentös verursachten Schwankungen des Krankheitsbildes erlauben.
Algorithmus für die Diagnostik des Asthmas
- Die NVL bietet ein
FlußschemaFlussschema für die Diagnostik des Asthmas.
Kriterien für schweres Asthma2
- Bei Erwachsenen
- Therapie mit inhalativen Kortikosteroiden (ICS) in Höchstdosis und mindestens 1 zusätzlichen Langzeitmedikament (langwirkendes Beta-2-Sympathomimetikum oder Montelukast) oder oralen Kortikosteroiden (OCS) > 6 Monate/Jahr
- Einer der folgenden Punkte trifft zu bzw. würde bei Reduktion der Therapie zutreffen:
- Atemwegsobstruktion: FEV1 < 80 % des Sollwertes (FEV1/FVC < LLN)
- häufige Exazerbationen: ≥ 2 kortikoidsteroidpflichtige Exazerbationen in den letzten 12 Monaten
- schwere Exazerbationen: ≥ 1 Exazerbation mit stationärer Behandlung oder Beatmung in den letzten 12 Monaten
- teilweise kontrolliertes oder unkontrolliertes Asthma
- Bei Kindern und Jugendlichen
- sachgerechte und adäquat durchgeführte Therapie mit dem Ziel einer guten Asthmakontrolle
- dauerhafter (> 6 Monate) Bedarf einer Add-on-Therapie mit einem LAMA oder einem monoklonalen Antikörper und/oder einer hohen ICS-Tagesdosis
Differenzialdiagnosen
Erwachsene
- Chronisch obstruktive Lungenerkrankung (COPD)
- Chronische Bronchitis (persistierender Husten mit Auswurf)
- Dysfunktionale Atmung, z. B. Hyperventilationssyndrom
- Bronchiektasen
- Asthma cardiale (Herzinsuffizienz)
- Mukoviszidose (zystische Fibrose)
- Stimmbanddysfunktion (Vocal Cord Dysfunction, VCD)
- Fremdkörperaspiration
- Tumor (Kehlkopf, Trachea, Lunge)
- Hyperventilation
- Adipositas
- Pneumonie
- Keuchhusten (Pertussis)
- Pneumothorax
- Lungenembolie
- Lungenfibrose
- Gastroösophagealer Reflux
Kinder und Jugendliche
- Virale Bronchitis
- Bronchiolitis (RS-Virus)
- Angeborene Herzfehler
- Kongenitale Anomalien, z. B. Tracheo-Bronchomalazie
- Fremdkörperaspiration
- Mukoviszidose (zystische Fibrose)
- Pseudokrupp
- Epiglottitis
- Keuchhusten
- Diabetische Ketoazidose
- Pneumonie
- Pneumothorax
- Hyperventilation
- Stimmbanddysfunktion (Vocal Cord Dysfunction, VCD)
Differenzialdiagnostische Abgrenzung Asthma und COPD
- Siehe Tabelle Abgrenzung Asthma/COPD.
Anamnese
- Folgende Besonderheiten sollten bei Erwachsenen in der Anamnese beachtet werden:
- Medikamente
- Die NVL empfiehlt eine ausführliche Medikamentenanamnese in der Diagnostik.2
- Sowohl ASS und NSAR als auch Betarezeptorenblocker können das Morbiditätsrisiko bei vorhandenem Asthma beeinflussen.
- Berufsanamnese
- Bei ca. 15 % (9–25 %) der neu diagnostizierten Fälle ist die arbeitsbezogene Exposition für die Krankheitsentstehung von zentraler Bedeutung.4,39
- Einem berufsbezogenen Asthma gehen häufig Rhinitis-Symptome voraus.40
- Siehe auch den Artikel Berufsbedingte allergische Atemwegserkrankungen.
- Bei Kleinkindern sind folgende Besonderheiten in der Anamnese zu beachten:
Klinische Untersuchung
- Siehe Leitlinienkasten.
Ergänzende Untersuchungen in der Hausarztpraxis
Lungenfunktionsdiagnostik
- In den Leitlinien wird die Durchführung einer Lungenfunktionsdiagnostik (typischerweise Spirometrie) zur Diagnosesicherung und differenzialdiagnostischen Abgrenzung empfohlen.2,4
- Wiederholungen der Lungenfunktionstestung zur Verlaufs- und Therapiekontrolle
- Für weitere Informationen zur Lungenfunktionsdiagnostik siehe Leitlinienkasten.
Labordiagnostik
- Zur Diagnosestellung sind keine Laboruntersuchungen erforderlich, jedoch zur Differenzialdiagnostik geeignet.2
- Siehe Leitlinienkasten.
- Absolute Eosinophilenzahl (Eosinophile/μl)
- Marker für eosinophile Atemwegsentzündung und Wirksamkeit einer Anti-IL-5-Therapie
- Assoziation zwischen einer erhöhten Eosinophilenzahl (> 400/µl) und der Anzahl an Exazerbationen, einer verminderten Asthmakontrolle und dem Risiko für akute respiratorische Ereignisse41
Diagnostik bei Spezialist*innen
- Für weitere apparative Untersuchungen siehe Leitlinienkasten.
- Für allergologische Stufendiagnostik siehe Leitlinienkasten.
Indikationen zur Überweisung/Klinikeinweisung
- Indikation zur Überweisung zur (pädiatrischen) Pneumologie bzw. einer spezialisierten Einrichtung2,4
- Zweifel an der Diagnose
- unzureichende Asthmakontrolle trotz intensivierter Behandlung
- vorausgegangene Notfallbehandlung
- Indikation zur Behandlung mit monoklonalen Antikörpern
- Ggf. bei Begleiterkrankungen, die die Asthmakontrolle negativ beeinflussen (z. B. COPD, chronische Sinusitis).
- Alle Kinder und Jugendlichen, deren Asthma eine Behandlung der Therapiestufe 4 oder höher erfordert.
- Betreuung in der Schwangerschaft2,4
- Beratungsgespräch zu Beginn einer Schwangerschaft über die Therapie während der Schwangerschaft mit dem Ziel einer guten Asthmakontrolle
- Schwangere Frauen mit unzureichender Asthmakontrolle sollten von Pneumolog*innen und Gynäkolog*innen gemeinsam in enger Abstimmung betreut werden.
- Indikationen zur Krankenhauseinweisung2,4
- schwere bronchopulmonale Infektionen
- an Asthma erkrankte Schwangere mit Verdacht auf Gefährdung des ungeborenen Kindes
- Bei einem schweren oder lebensbedrohlichen Asthmaanfall sollte nach der Initialtherapie die sofortige Einweisung in ein Krankenhaus organisiert werden, ggf. mit notärztlicher Begleitung (bei lebensbedrohlichem Anfall).
- Zeigt sich 30–60 Minuten nach der initialen Versorgung eines leichten bis mittelschweren Asthmaanfalls keine nachhaltige Besserung, empfiehlt die Leitliniengruppe die umgehende Einweisung in das Krankenhaus bzw. die weitergehende Behandlung in der Notaufnahme.
Therapie
Therapieziele
- Ziel der Asthmabehandlung ist es, über einen langen Zeitraum eine gute Asthmakontrolle zu erreichen.2,4
- Therapieziele in Abhängigkeit von Alter und Begleiterkrankungen der Patient*innen2
- Vermeidung von:
- akuten und chronischen Krankheitserscheinungen (z. B. Symptome, Asthmaanfälle)
- Beeinträchtigung der physischen, psychischen und geistigen Entwicklung
- Beeinträchtigung der körperlichen und sozialen Aktivitäten im Alltag
- Komplikationen und Folgeschäden
- unerwünschten Wirkungen der Therapie.
- Verbesserung der gesundheits- und asthmabezogenen Lebensqualität
Allgemeines zur Therapie
Grundsätze in der Behandlung von Asthma
- Grundlage der Therapie ist der Grad der Asthmakontrolle.2-4
- Es werden 3 Grade der Asthmakontrolle definiert:
- kontrolliertes Asthma
- teilweise kontrolliertes Asthma
- unkontrolliertes Asthma.
- Verlaufsbeobachtung und wiederholte Beurteilung der Asthmakontrolle
- Beurteilung der Therapieziele und ggf. Anpassung (Intensivierung/Reduktion)
- Es werden 3 Grade der Asthmakontrolle definiert:
- Meidung der auslösenden Faktoren (z. B. Allergenexposition)
- Stufenbasierte, medikamentöse Langzeittherapie
- Verbrauch an Bedarfsmedikation durch langfristige antientzündliche Therapie möglichst minimieren.
- Information und Patientenschulung von Betroffenen und Angehörigen
- Bei allergischem Asthma ggf. Versuch der frühzeitigen Hyposensibilisierung
- Zur Behandlung bei Kindern und Jugendlichen siehe auch:
- Zur Akuttherapie im Asthmaanfall siehe auch:
Medikamentöse Therapie
- Ziel der medikamentösen Therapie ist eine gute Asthmakontrolle.
- Man unterscheidet eine Bedarfs- und Langzeitmedikation.
- Die Bedarfsmedikation wird akut eingesetzt und wirkt in kurzer Zeit antiobstruktiv.
- Wichtigste Vertreter dieser Gruppe sind kurzwirkende Beta-2-Sympathomimetika (SABA).
- Die Langzeittherapie soll in erster Linie die Entzündung der Atemwege reduzieren und so Symptomen vorbeugen.
- Die Grundlage dieser Therapie bilden in den meisten Fällen inhalative Kortikosteroide (ICS).
- Die Bedarfsmedikation wird akut eingesetzt und wirkt in kurzer Zeit antiobstruktiv.
- Wahl und Erklärung des Inhalationssystems ist eine wichtige Besonderheit in der Behandlung.
- Therapieadhärenz und korrekte Anwendung des Inhalationssystems sind für den Therapieerfolg entscheidend.
Medikamentöse Stufentherapie bei Erwachsenen
- Siehe Tabelle Grade der Asthmakontrolle bei Erwachsenen.
- Siehe Tabelle Medikamentöses Stufenschema bei Asthma (Empfehlung der NVL)2
- Cave: Seit 2020 empfiehlt auch die NVL als „Reliever" ICS + Formoterol im Off-Label-Use. Die GINA hatte bereits 2019 sich für die bevorzugte Gabe von ICS + Formoterol gegenüber SABA als Bedarfsmedikation ausgesprochen.3
- Grund ist die vermutliche Risikoerhöhung für Exazerbationen durch eine Monotherapie mit SABA und die bessere Langzeitkontrolle bei Einsatz von ICS.
- Siehe Vergleichstabelle der Dosierungen inhalativer Kortikosteroide (ICS) für Erwachsene.
Medikamentöse Stufentherapie bei Kindern und Jugendlichen
- Siehe auch Artikel Asthma bei Kindern und Jugendlichen.
- Siehe Tabelle Grade der Asthmakontrolle bei Kindern und Jugendlichen.
- Siehe Tabelle Medikamentöses Stufenschema Asthma bei Kindern und Jugendlichen.
- Siehe Vergleichstabelle der Dosierungen inhalativer Kortikosteroide (ICS) für Kinder und Jugendliche.
Medikamentöse Behandlung im akuten Asthmaanfall
- Siehe die Artikel:
Klimabewusste Verordnung von inhalativen Arzneimitteln
- Die Angaben zu diesem Abschnitt beziehen sich auf die entsprechende Leitlinie der DEGAM.42
- Dosieraerosole (DA) benutzen Treibmittel, um den Wirkstoff in tiefe Lungenabschnitte zu transportieren.
- Diese schädigen zwar die Ozonschicht nicht, sind aber starke Treibhausgase.
- Dadurch haben DA im Vergleich zu Pulverinhalatoren ein vielfach höheres Schädigungspotenzial für die Atmosphäre.
- Nichtsdestotrotz sind DA in folgenden Fällen indiziert:
- bei Kindern < 5 Jahre für die Inhalation von Beta-2-Sympathomimetika oder Glukokortikosteroiden
- bei akutem Asthmaanfall.
- Verschreibende, Apotheker*innen und Patient*innen sollten berücksichtigen, dass zwischen den einzelnen DA beträchtliche Unterschiede in ihrem Global Warming Potential bestehen, und das DA mit einem möglichst niedrigen GWP bevorzugen, wenn sie klinisch vergleichbar wirksam sind.
- Bei stabilem Asthma ab einem Alter von 5 Jahren sind andere inhalative Arzneimittel genauso effektiv wie ein DA.
Übersicht Medikamentengruppen
- Akutmedikation („Reliever“)
- kurzwirkende Beta-2-Sympathomimetika (SABA)
- z. B. Salbutamol, Terbutalin
- Fixkombination aus niedrig dosiertem ICS und LABA
- (Single Inhaler) Maintenance And Reliever Therapy ((S)MART)4
- Kann zur Bedarfs- und Langzeittherapie eingesetzt werden.
- weitere Medikamente im akuten Asthmaanfall
- kurzwirksame Anticholinergika (Ipratropiumbromid)
- parenterale Beta-2-Sympathomimetika
- Magnesiumsulfat
- systemische Kortikosteroide
- kurzwirkende Beta-2-Sympathomimetika (SABA)
- Langzeittherapeutika („Controller“)
- inhalative Kortikosteroide (ICS)
- z. B. Budesonid, Fluticason
- langwirksame Beta-2-Sympathomimetika (LABA)
- z. B. Formoterol, Salmeterol
- Leukotrienrezeptorantagonisten (LTRA)
- Montelukast
- langwirkende Anticholinergika (LAMA)
- Tiotropium für die Behandlung des Asthmas zugelassen2
- weitere Medikamente
- Anti-IgE-Antikörper: Omalizumab
- Anti-IL5-Antikörper: Mepolizumab und Reslizumab
- orale Kortikosteroide (OCS)
- inhalative Kortikosteroide (ICS)
Leitlinie: Medikamentöse Therapie des Asthmas2-4
- Deutliche Abweichungen der Leitlinien voneinander sind kursiv gekennzeichnet.
Allgemeines zur medikamentösen Therapie
- Therapieziele
- Optimale Asthmakontrolle erreichen.
- Atemwegsobstruktion vermeiden.
- Bronchiale Hyperreagibilität reduzieren.
- Asthmabedingte Atemwegsentzündung unterdrücken.
- Die medikamentöse Asthmatherapie zielt darauf ab, den Status eines kontrollierten Asthmas nach dem Prinzip „so viel wie nötig, jedoch so wenig wie möglich" zu erreichen und diesen aufrechtzuerhalten.
- Ergänzung der Pharmakotherapie durch nichtmedikamentöse Maßnahmen
- Bestmögliches Wissen der Patient*innen über ihre Erkrankung und das Selbstmanagement ist anzustreben.
- Insbesondere komplexe Therapieschema führen oft zu mangelnder Therapieadhärenz.
- Bestmögliches Wissen der Patient*innen über ihre Erkrankung und das Selbstmanagement ist anzustreben.
- Die Medikamente werden in 2 Klassen eingeteilt:
- Langzeittherapeutika („Controller“)
- Langzeittherapie von erwachsenen Patient*innen empfohlen, wenn > 2 x/Woche Bedarfsmedikation angewendet wird.
- ICS: Die Therapie mit inhalativen Kortikosteroiden (ICS) bildet die Grundlage der Langzeittherapie.
- keine Monotherapie mit langwirkendem Beta-2-Sympathomimetikum (LABA) oder langwirkenden Anticholinergikum (LAMA) empfohlen
- Bedarfsmedikamente („Reliever“)
- SABA: Kurzwirksame Beta-2-Sympathomimetika (SABA) sind in jeder Therapiestufe als Bedarfsmedikation einsetzbar.
- Ein geringer Bedarf an SABA ist ein wichtiges Ziel und ein Kriterium für den Erfolg der Therapie.
- Eine Alternative stellt eine Fixkombination aus ICS und Formoterol (ab 12 Jahren) dar, wenn diese auch die Langzeittherapie darstellt.
- Von der NVL als gleichwertig erachtet, von GINA als bevorzugt gegenüber SABA angesehen.
- Langzeittherapeutika („Controller“)
- Verschiedene Applikationsformen der Medikamente (inhalativ, oral, parenteral)
- Die inhalative Applikation soll bevorzugt werden.
- höhere lokale Konzentrationen, schneller Wirkeintritt und weniger systemischen Nebenwirkungen
- Die inhalative Applikation soll bevorzugt werden.
- Patient*innen mit diagnostiziertem Asthma sollen gemäß eines medikamentösen Stufenschemas behandelt werden.
- Die Therapie orientiert sich am Grad der Asthmakontrolle.
- Trotz adäquater Therapie und Therapieadhärenz gibt es Fälle, in denen keine gute Asthmakontrolle erreicht wird.
- Intensivierung der Therapie, wenn weiterhin Symptome und Exazerbationen auftreten (s. u.).
- Vor Behandlung in einer höheren Therapiestufe Inhalationstechnik und Therapieadhärenz prüfen.
- Bei Patient*innen mit saisonalem Asthma sollte die Therapie an die saisonale Pollenexposition angepasst werden.
- Die Therapie orientiert sich am Grad der Asthmakontrolle.
Verlaufsbeurteilung: Asthmakontrolle
- Die Beurteilung der Asthmakontrolle bildet die Grundlage für die langfristige Verlaufsbeurteilung und das Therapiekonzept.
- Asthmakontrolle soll mit der geringstmöglichen Anzahl von Antiasthmatika in der niedrigstmöglichen Dosis aufrechterhalten werden.
- Einteilung in 3 Grade entsprechend den Beschwerden, der Einschränkungen im Alltag und dem Gebrauch der Bedarfsmedikation:
- kontrolliertes Asthma
- teilweise kontrolliertes Asthma
- unkontrolliertes Asthma.
- Siehe Tabelle Grade der Asthmakontrolle bei Erwachsenen.
- Siehe Tabelle Grade der Asthmakontrolle bei Kindern und Jugendlichen.
Therapieanpassung orientiert an der Asthmakontrolle
- Kontrolliertes Asthma
- Therapiereduktion erwägen (siehe Stufenschema).
- Vor einer möglichen Reduktion der Therapie mit ICS soll das Asthma für mindestens 3 Monate kontrolliert sein.
- Davon ausgenommen sind Patient*innen mit saisonalem Asthma. Hier orientiert sich die Therapie an der saisonalen Pollenexposition, sodass eine Reduktion bereits nach kürzeren Zeiträumen möglich wird
- Da die Vermeidung einer Übertherapie im Kindesalter besonders relevant ist, kann ggf. versucht werden, die Therapie bereits nach 2 Monaten mit stabiler Asthmakontrolle zu reduzieren.
- bei Absetzen einer Therapie mit Kortikosteroiden oder monoklonalen Antikörpern engmaschige Überwachung empfohlen
- Teilweise kontrolliertes oder unkontrolliertes Asthma
- Überprüfung der Inhalationstechnik (Vorführung durch die Patient*innen) und Therapieadhärenz
- Überprüfung des Schulungsbedarfes
- Allergie- und Umweltkontrolle
- Beachtung von Komorbiditäten und aggravierenden Faktoren
- Überprüfung der Diagnose Asthma
- Teilweise kontrolliertes Asthma
- Therapieintensivierung erwägen (anhand Stufenschema).
- Unkontrolliertes Asthma
- Therapieintensivierung empfehlen (anhand Stufenschema).
- Beobachtung, Wiedervorstellung (nach Intensivierung innerhalb von 3 Monaten)
Medikamentöse Stufentherapie
- Die NVL aus dem Jahr 2020 empfiehlt bei Erwachsenen eine Stufentherapie mit 5 Stufen.
- Hinweise zum „Off-Label-Use“
- In der NVL Asthma und der GINA empfohlene Therapieoptionen sind nicht für alle adressierten Patientengruppen oder Indikationen zugelassen.
- Die Dosisangaben in der NVL weichen teilweise von den Fachinformationen ab.
- Kriterien für „Off-Label-Use“ (zulassungsüberschreitender Einsatz eines Arzneimittels)
- nachgewiesene Wirksamkeit
- günstiges Nutzen-Risikoprofil
- fehlende Alternativen – Heilversuch
- Initiale Behandlung bei Erwachsenen
- bei bisher unbehandelten Patient*innen mit Kriterien eines teilweise kontrollierten Asthmas:
- Beginn der Langzeittherapie in der Regel auf Stufe 2.
- bei bisher unbehandelten Patient*innen mit Kriterien eines unkontrollierten Asthmas:
- Beginn der Langzeittherapie mindestens auf Stufe 3.
- bei bisher unbehandelten Patient*innen mit Kriterien eines teilweise kontrollierten Asthmas:
- Für die medikamentöse Stufentherapie bei Kindern siehe Artikel Asthma bei Kindern und Jugendlichen.
- Siehe Tabelle Medikamentöses Stufenschema bei Asthma (Empfehlung der NVL)2
- Siehe Tabelle Medikamentöses Stufenschema Asthma bei Kindern und Jugendlichen.
Therapiestufe 1 bei Erwachsenen
- Bedarfstherapie: Inhalation eines kurzwirksamen inhalativen Beta-2-Sympathomimetikums (SABA)
- alleinige SABA-Therapie insbesondere für Patient*innen mit nur leichten oder seltenen Beschwerden (< 2 x/Monat)
- Nach GINA besteht unter alleiniger SABA-Therapie ein erhöhtes Risiko für Exazerbationen.
- Deshalb sollte dies für Jugendliche und Erwachsene nicht mehr durchgeführt werden.
- Laut GINA soll die hierzulande nicht zugelassene bedarfsweise Inhalation eines ICS zusammen mit einem schnell- aber dennoch langwirkenden LABA erfolgen (Budesonid plus Formoterol).3
- z. B. Salbutamol 1–2 Hübe als Dosieraeorosol (max. 10–12 Hübe pro Tag bei Erwachsenen)
- alleinige SABA-Therapie insbesondere für Patient*innen mit nur leichten oder seltenen Beschwerden (< 2 x/Monat)
- Inzwischen geht man davon aus, dass die auch in Stufe 1 bestehende inflammatorische Komponente des Asthmas durch die Anwendung von niedrigdosierten ICS in Langzeittherapie behandelt werden kann.
- Daher hat die NVL 2020 die Empfehlungen von GINA bezüglich der Gabe von ICS + Formoterol als Alternative zur SABA-Gabe übernommen.
- Alternativen in begründeten Fällen
- Anwendung von niedrigdosierten ICS in Langzeittherapie (z. B. Budesonid 200–400 μg/d) + Bedarfstherapie mit SABA
Therapiestufe 2 bei Erwachsenen
- Bedarfstherapie
- inhalatives SABA
- z. B. Salbutamol 1–2 Hübe als Dosieraeorosol (max. 10–12 Hübe pro Tag bei Erwachsenen)
- alternativ Inhalation eines ICS zusammen mit einem schnell-, aber dennoch langwirkenden LABA (Budesonid + Formoterol, off label)
- inhalatives SABA
- Langzeittherapie
- niedrigdosiertes inhalatives Kortikosteroid (ICS)
- z. B. Budesonid 200–400 μg/d
- Gabe als Einmaldosis oder aufgeteilt auf 2 tägliche Dosen
- ggf. Verwendung von Inhalierhilfen (Spacer)
- niedrigdosiertes inhalatives Kortikosteroid (ICS)
- Alternativen in begründeten Fällen
- Leukotrienrezeptorantagonist Montelukast (LTRA) als Monotherapie
- bei Nebenwirkungen oder Kontraindikationen für ICS
- in Deutschland nur für Kinder zugelassen
- Bei Patient*innen über 15 Jahren nicht empfohlen, außer wenn sie nicht zur Inhalation von ICS in der Lage sind oder inakzeptable Nebenwirkungen auftreten.
- temporäre ICS-Dauertherapie bei lediglich saisonal auftretendem allergischem Asthma
- Leukotrienrezeptorantagonist Montelukast (LTRA) als Monotherapie
Therapiestufe 3 bei Erwachsenen
- Bedarfstherapie
- inhalatives SABA
- z. B. Salbutamol 1–2 Hübe als Dosieraeorosol (max. 10–12 Hübe pro Tag bei Erwachsenen)
- Alternativ Fixkombination aus ICS und LABA, wenn dies auch die Langzeittherapie darstellt.
- z. B. Budesonid oder Beclometason mit Formoterol als Bedarfs- und Langzeitmedikation
- Laut GINA ist bei Patient*innen ab 12 Jahren bevorzugt das SMART-Regime (Single Maintenance and Reliever Therapy) anzuwenden: Fixkombination aus ICS und LABA sowohl zur Erhaltungstherapie als auch im Bedarfsfall.3
- inhalatives SABA
- Langzeittherapie
- bevorzugt Kombination aus niedrigdosiertem ICS und langwirkendem Beta-2-Sympathomimetikum (LABA)
- z. B. Budesonid/Formoterol, Fluticasonpropionat/Formoterol, Beclometason/Formoterol
- Einsatz in Form einer Fixkombination empfohlen
- alternativ ICS in mittlerer Dosis
- bevorzugt Kombination aus niedrigdosiertem ICS und langwirkendem Beta-2-Sympathomimetikum (LABA)
- Alternativen in begründeten Fällen
- Kombination aus niedrigdosiertem ICS und langwirkendem Anticholinergikum (LAMA)2
- Tiotropium ist als LAMA für die Behandlung des Asthmas zugelassen.
- in der DGP-Leitlinie nicht Teil der Therapiestufe 34
- Kombination aus niedrigdosiertem ICS und Leukotrienrezeptorantagonist (LTRA)
- Die Leitlinie der DGP nennt hier ein ICS in hoher Dosis als weitere Alternative.4
- Diese Alternative sei jedoch seltener effektiv.
- Bei Erwachsenen sei daher in den meisten Fällen die
Addition eines 2. Wirkstoffes der Erhöhung der Dosis bei Monotherapie vorzuziehen.
- Kombination aus niedrigdosiertem ICS und langwirkendem Anticholinergikum (LAMA)2
Therapiestufe 4 bei Erwachsenen
- Bedarfstherapie
- inhalatives SABA
- z. B. Salbutamol 1–2 Hübe als Dosieraeorosol (max. 10–12 Hübe pro Tag bei Erwachsenen)
- Alternativ Fixkombination aus ICS und LABA, wenn dies auch Langzeittherapie darstellt.
- z. B. Budesonid oder Beclometason mit Formoterol als Bedarfs- und Langzeitmedikation
- Laut GINA ist bei Patient*innen ab 12 Jahren bevorzugt das SMART-Regime (Single Maintenance and Reliever Therapy) anzuwenden: Fixkombination aus ICS und LABA sowohl zur Erhaltungstherapie als auch im Bedarfsfall.
- inhalatives SABA
- Langzeittherapie
- bevorzugt Kombination aus einem ICS im mittleren oder hohen Dosisbereich und einem LABA
- Kombination aus mittelhochdosiertem ICS und LABA am häufigsten wirksam
- z. B. Budesonid/Formoterol, Fluticasonpropionat/Formoterol, Beclometason/Formoterol
- alternativ ICS im mittleren oder hohen Dosisbereich mit LABA und additiv LAMA
- bevorzugt Kombination aus einem ICS im mittleren oder hohen Dosisbereich und einem LABA
- Ausreizung aller verfügbaren Therapieoptionen, bevor die Therapie zur Stufe 5 eskaliert wird.
- Beispielsweise ICS-Dosis erhöhen oder Dreifachkombination (ICS + LABA + LAMA).
- Alternativen in begründeten Fällen
- Kombination aus ICS mittel- bis hochdosiert, LABA und LTRA
- Kombination aus ICS mittel- bis hochdosiert und LAMA2
Therapiestufe 5 bei Erwachsenen
- Vorstellung bei Pneumolog*in mit Erfahrung in der Behandlung des schweren Asthmas
- Vor Behandlung Indikation zu einer Rehabilitation prüfen.
- engmaschigere Beobachtung, Adhärenz, Umsetzung
- Bedarfstherapie
- inhalatives SABA
- z. B. Salbutamol 1–2 Hübe als Dosieraeorosol (max. 10–12 Hübe pro Tag bei Erwachsenen)
- Alternativ Fixkombination aus ICS und LABA, wenn dies auch die Langzeittherapie darstellt.
- z. B. Budesonid oder Beclometason mit Formoterol als Bedarfs- und Langzeitmedikation
- inhalatives SABA
- Langzeittherapie
- Kombination aus einem ICS in Höchstdosis, einem LABA und einem LAMA (Tiotropium)
- Monoklonale Antikörper
- Erst, wenn selbst unter 3-monatiger maximaler inhalativer Kombinationstherapie keine Asthmakontrolle erreicht wird.
- Indikationsstellung und Behandlungsbeginn durch erfahrene pneumologische Fachärzt*in
- Beurteilung des Therapieerfolgs durch erfahrene Spezialist*innen nach 4 und 12 Monaten, dann jährlich
- Langzeittherapie zunächst beibehalten (nach klinischem Ansprechen unter engmaschiger Kontrolle reduzieren).
- Anti-IgE-Antikörper (Omalizumab)
- für Erwachsene mit schwerem IgE-vermitteltem, allergischem Asthma Therapieversuch über 4 Monate empfohlen
- Voraussetzungen
- schweres IgE-vermitteltes allergisches Asthma und
- positiver Hauttest oder in-vitro Reaktivität gegen ein ganzjährig auftretendes Aeroallergen und
- IgE-Serumkonzentration unter Berücksichtigung des Körpergewichts im therapierbaren Bereich und
- erfolgte Eliminierung vermeidbarer Allergenexpositionen.
- Anti-IL5-Antikörper (Mepolizumab, Reslizumab, Benralizumab)
- Therapieversuch für mind. 4 Monate bei Erwachsenen in Stufe 5 mit schwerem eosinophilem Asthma
- Definition des eosinophilen Asthmas: 2-maliger Nachweis ≥ 300 Eosinophilen/μl Blut außerhalb von Exazerbationen in den vergangenen 2 Jahren
- z. B. Mepolizumab 100 mg s. c. 1 x monatlich oder Reslizumab 3 mg/kg KG i. v. 1 x monatlich
- Anti-IL4-Antikörper (Dupilumab)
- Therapieversuch für mind. 4 Monate bei Erwachsenen in Stufe 5
- Voraussetzungen
- schweres eosinophiles Asthma und 2-maliger Nachweis einer Konzentration von > 300 Eosinophilen pro μl Blut außerhalb von Exazerbationen in den vergangenen 2 Jahren oder
- 2-maliger Nachweis einer erhöhten FeNO-Konzentration (> 25 ppb)
- Orale Kortikosteroide (OCS)
- Langzeittherapie mit systemischen Kortikosteroiden nachrangige Therapieoption für die Langzeittherapie in Stufe 5 (Gefahr schwerer Nebenwirkungen)
- Indikation, falls unzureichende Asthmakontrolle trotz maximaler Kombinationstherapie und zusätzlich monoklonaler Antikörper
- intermittierende oder dauerhafte Therapie mit niedriger Dosis (≤ 7,5 mg Prednison oder Äquivalent)
- Gabe in niedrigster noch effektiver Dosis
- Risiko von Nebenwirkungen (Blutdrucksteigerung, Diabetes mellitus, Osteoporose)
- genaue Aufklärung und Verlaufsbeurteilung
- Osteoporose-Prophylaxe bei Dauerbehandlung (≥ 3 Monate)
- Langzeittherapie mit systemischen Kortikosteroiden nachrangige Therapieoption für die Langzeittherapie in Stufe 5 (Gefahr schwerer Nebenwirkungen)
Spezifische (Allergen-)Immuntherapie (SIT) bei allergischem Asthma
- Bei Patient*innen mit allergischem Asthma soll die Indikation zu einer spezifischen Immuntherapie (SIT) geprüft werden, wenn die allergische Komponente der asthmatischen Beschwerden gut dokumentiert ist (nachgewiesene spezifische Sensibilisierung und eindeutige klinische Symptomatik nach Allergenexposition).
- Indikationsstellung und Auswahl der Antigene und der Applikationsform durch allergologisch qualifizierte Ärzt*in
- Sondervotum der DEGAM: Die Indikationsstellung sowie die Auswahl der Antigene und der Applikationsform sollen von allergologisch erfahrenen Ärzt*innen vorgenommen werden.
- Kein Ersatz für antiasthmatische Therapie
- Indikationsstellung restriktiver als bei der allergischen Rhinokonjunktivitis
- Zwei Formen:
- subkutane Immuntherapie (SCIT)
- sublinguale Immuntherapie (SLIT).
- Kontraindikation: unkontrolliertes Asthma
- Siehe Artikel Allergenspezifische Immuntherapie (SIT).
SMART (Single Maintenance and Reliever Therapy)
- GINA empfiehlt SMART: Fixkombination aus ICS uns LABA sowohl als Erhaltungstherapie als auch im Bedarfsfall (z. B. Budesonid und Formoterol, off label bei Bedarf: Fluticason und Formoterol, Fluticason und Salmeterol, Fluticason und Vilanterol).3
- Arzneitelegramm zum Einsatz in Stufe 1 und 2:
4243- „Jugendlichen und erwachsenen Patient*innen mit guter Symptomkontrolle auf Stufe 1, aber erhöhtem Exazerbationsrisiko, sowie Patient*innen auf Stufe 2, die die tägliche ICS-Inhalation nicht akzeptieren, kann als Alternative zu den Standardregimen auf diesen Stufen die Kombination aus ICS plus Formoterol bei Bedarf angeboten werden.
- Es muss dann eine Fixkombination verschrieben werden. Die Patient*innen müssen darüber aufgeklärt werden, dass die Therapie hierzulande nicht zugelassen ist.
- Patient*innen auf Therapiestufe 2 müssen zudem wissen, dass sich die Symptomkontrolle unter dem Regime verschlechtern kann.“
- Arzneitelegramm zum Einsatz in Stufe 3 und 4:
4344- „Nach mehreren systematischen Übersichten treten schwere Asthmaexazerbationen unter dem SMART-Regime seltener auf, insbesondere Exazerbationen, die systemische Glukokortikoide erfordern. Dieser Vorteil zeigt sich auch im Vergleich mit einer höher dosierten ICS-Erhaltungsdosis plus LABA und einem kurzwirkenden Betamimetikum (SABA) bei Bedarf.
- In Bezug auf Asthmasymptome, Lebensqualität und Lungenfunktion ist eine klinisch relevante Überlegenheit des SMART-Konzeptes nicht hinreichend belegt.
- Unseres Erachtens ist SMART vor allem bei Patient*innen ab 12 Jahren zu erwägen, die mit einem niedrig- bis mitteldosierten ICS plus LABA unzureichend kontrolliert sind oder trotz guter Symptomkontrolle auf Therapiestufe 3 oder 4 ein erhöhtes Exazerbationsrisiko haben.
- Bei Patient*innen, die eine hochdosierte ICS-Erhaltungstherapie benötigen, raten wir von SMART ab.“
- Arzneitelegramm zum Einsatz in Stufe 1 und 2:
Inhalationstechnik und Wahl des Inhalationssystems
- Aktuell gibt es noch eine hohe Fehlerquote bei der Anwendung von Inhalationssystemen.
- Eine Ursache ist die große Zahl unterschiedlicher Applikationsformen.
- Auswahl des Inhalationssystems2
- Anpassung an die kognitiven und motorischen Fähigkeiten der Patient*innen
- in Absprache mit den Patient*innen (Präferenzen)
- Altersgruppe der Patient*innen
- nach Möglichkeit nur ein einheitliches Inhalationssystem (nur ein Typ Dosieraerosol oder Pulverinhalator)
- Wechsel des Inhalationssystems im Behandlungsverlauf vermeiden (Gefahr von Handhabungsfehlern).
- nach Wechsel Neueinweisung der Patient*innen in die Handhabung
- Schulung der Patient*innen im Gebrauch der Inhalationssysteme2-4
- alleiniger Hinweis auf Beipackzettel meist nicht ausreichend
- Demonstration der Funktionsweise und ggf. Anweisungen mit Bildern
- regelmäßige Überprüfung der Inhalationstechnik (insbesondere bei unzureichender Asthmakontrolle)
- Die Deutsche Atemwegsliga e. V. bietet Hinweise, Anleitungen und Videos zur korrekten Inhalation auf ihrer Internetpräsenz: Deutsche Atemwegsliga – Richtig inhalieren.
- Auf der Seite der NVL gibt es Patientenblätter, u. a.:
- Asthma – Unterschiede bei Inhalier-Geräten
- Asthma – Wechsel des Inhalier-Gerätes.
- Allgemeinen Prinzipien der Anwendung von Inhalationssystemen:2
- vor der Inhalation
- tiefe Ausatmung (Ausnahme Vernebler)
- Dosieraerosole vor der Anwendung schütteln.
- bei der Inhalation
- Das optimale Atemmanöver ist abhängig von der Art des Inhalationssystems.
- Dosieraerosol und Vernebler: möglichst langsame und tiefe Inspiration
- Pulverinhalator: forcierte Inhalation mit möglichst hoher Atemstromstärke (für kleine Kinder oder bei Asthmaanfall nicht geeignet)
- nach der Inhalation
- endinspiratorische Atempause von mind. 3, eher 5 sec
- Gerät absetzen (Exhalation in das Gerät vermeiden).
- vor der Inhalation
- Inhalierhilfen (Spacer)
- Können ab dem 1. Lebensjahr verwendet werden.
- Erhöhen die Deposition des Medikaments in der Lunge um 15–20 %.
- in der Langzeittherapie mit ICS bessere Wirkstoffverfügbarkeit bei Reduktion der Nebenwirkungen
4445 - Spacer haben den Gebrauch von Verneblern bei Kindern bis zum 4.–5. Lebensjahr oft ersetzt.
4546 - Inhalationstechnik: langsame tiefe Inspiration über mehrere Atemzüge
- Geeignetste Applikationssysteme bei Kindern2
- Kinder unter 5 Jahren
- bevorzugt Treibgasdosieraerosole mit Spacer
- möglichst frühzeitiger Ersatz einer Gesichtsmaske durch Mundstück (z. B. mit Erreichen des 2. Lebensjahres)
- Kinder ab 5 Jahren
- Dosieraerosol mit Spacer und Mundstück
- Kinder unter 5 Jahren
Akutmedikation2-4
- Siehe Behandlung des akuten Asthmaanfalls.
- Kurzwirksame Beta-2-Sympathomimetika (SABA)
- z. B. Salbutamol oder Terbutalin
- wichtigste Behandlung bei akuten Asthmabeschwerden in allen Therapiestufen
- Kurzwirksame Anticholinergika
- z. B. Ipratropiumbromid
- im schweren und lebensbedrohlichen Asthmaanfall sowie bei unzureichender Wirkung des SABA empfohlen
- Bewirkt in Kombination mit SABA ggf. einen besseren Effekt als separate Gabe.
4647
- Orale Kortikosteroide (OCS)
- z. B. Prednisolon
- Frühzeitige orale Kortikosteroide reduzieren die Wahrscheinlichkeit für eine Krankenhauseinweisung.
4748
- Sauerstoffgabe
- Sauerstoff wird im akuten Asthmaanfall als Gabe mit niedriger Flussrate empfohlen.
- Ziel: Sauerstoffsättigung von mindestens 95 %
- Ziel: Sauerstoffsättigung von mindestens 95 %
- Sauerstoff wird im akuten Asthmaanfall als Gabe mit niedriger Flussrate empfohlen.
- Magnesiumsulfat
- Theophyllin
- Verordnungen sind in den letzten Jahren rückläufig.2
- aus Sicht der NVL kein Stellenwert mehr in der Behandlung des Asthmas2
- geringe therapeutischen Breite, Nebenwirkungspotenzial und verfügbare Alternativen
- Gabe als Einzelfallentscheidung nur noch in lebensbedrohlicher Situation und bei fehlendem Ansprechen auf die Initialtherapie4
- Bestimmung der Serumspiegel nach erstmaliger Gabe
Langzeitbehandlung2-4
- Inhalative Kortikosteroide (ICS)
- z. B. Beclometason, Fluticason, Budesonid
- Inhalative Kortikosteroide (ICS) sind die effektivsten Präparate zur Dauermedikation, die zur Verfügung stehen.3
- Siehe Vergleichstabelle der Dosierungen inhalativer Kortikosteroide (ICS) für Erwachsene
- Siehe Vergleichstabelle der Dosierungen inhalativer Kortikosteroide (ICS) für Kinder und Jugendliche.
- Nachgewiesene Effekte umfassen:
- Eingrenzung der Schleimhautentzündung in den Atemwegen
- Reduktion der bronchialen Hyperreagibilität
- Verbesserung der Lungenfunktion
- seltenere Asthmasymptome, seltenere und leichtere Exazerbationen
- Reduktion der Krankenhauseinweisungen und Todesfälle
- Reduktion der Bedarfsmedikation.
- Nebenwirkungen
- Die regelmäßige Verwendung kann bei Kindern zu einer Reduktion des Längenwachstums führen.
5051-5152 - Langwirkende Beta-2-Sympathomimetika (LABA)
- z. B. Formoterol, Salmeterol
- LABA sollten nicht als Monotherapie, sondern nur zusammen mit ICS eingesetzt werden.2,
5253-5556- Führt bei alleiniger Gabe zu einer Verschlechterung und Zunahme von Exazerbationen.
- Fixkombination von Formoterol und Budesonid (ICS) in fester Dosierung sowohl als Langzeitbehandlung als auch als Bedarfsmedikation reduziert die Anzahl von Exazerbationen.
5657-5758- Dieser Einsatz von ICS und LABA in fester Kombination wird als
„(Single Inhaler) Maintenance and Reliever Therapy (SMART)“bezeichnet.4
- Dieser Einsatz von ICS und LABA in fester Kombination wird als
- Eine Kombination aus niedrigdosiertem ICS und LABA ist die effektivste und sicherste Behandlung, um Exazerbationen vorzubeugen und zu begrenzen.
5859- weniger Exazerbationen unter Kombinationstherapie als mit alleinigem ICS
5960
- weniger Exazerbationen unter Kombinationstherapie als mit alleinigem ICS
- Leukotrienrezeptor-Antagonisten (LTRA): Montelukast
- In Deutschland nur zur Behandlung von leichtem und mittelschwerem Asthma zugelassen.4
- Montelukast kann als Monotherapie bei Kindern von 2–14 Jahren in Therapiestufe 2 eingesetzt werden.2
- Bei erwachsenen Patient*innen ist die zusätzliche Gabe eines LABA zu einem ICS effektiver als ein LTRA, vor allem im Hinblick auf die Lungenfunktion.
6061 - Die FDA warnt vor einem erhöhten Risiko für neuropsychiatrische Nebenwirkungen und empfiehlt eine strenge Indikationsstellung.
6162
- Langwirksame Anticholinergika (LAMA): Tiotropium
- LAMA sollten nicht als Monotherapie eingesetzt werden, ggf. additiv in der Langzeittherapie in Stufe 3–5.2
- Anti-IgE-Antikörper: Omalizumab
- in Deutschland zugelassen für Kinder ab 6 Jahren, Jugendliche und Erwachsene in der höchsten Therapiestufe2,4
- Der monoklonale Antikörper bindet an im Körper zirkulierende Antikörper vom Typ IgE.
- Kann bei schwerem Asthma, das trotz optimaler Behandlung unkontrolliert ist, eingesetzt werden.
6465-6566 - Omalizumab reduzierte die Anzahl und Schwere von Exazerbationen bei Patient*innen, die bereits mit ICS und LABA behandelt werden.
6667-6768 - Sehr kostenintensive Behandlung, sollte von Spezialist*innen verschrieben werden.4
- Anti-IL5-Antikörper: Mepolizumab, Reslizumab und Benralizumab
- für erwachsene Patient*innen in Therapiestufe 5 mit schwergradigem eosinophilem Asthma2,4
- Anti-IL-5-Antikörper als Zusatztherapie reduzieren die Anzahl der Exazerbationen bei Patient*innen mit schwerem, schlecht kontrolliertem eosinophilem Asthma um ca. 50 %.
6869 - Gabe je 1 x monatlich: Mepolizumab 100 mg s. c. bzw. Reslizumab 3 mg/kg KG i. v. bzw. Benralizumab 30 mg s. c.
- Orale Kortikosteroide (OCS)
- aufgrund möglicher schwerer Nebenwirkungen nur nachrangige Therapieoption in Stufe 52
- Nur indiziert, sofern die Asthmakontrolle trotz des kombinierten Einsatzes der verschiedenen Therapieoptionen der vorherigen Stufe sowie zusätzlich monoklonaler Antikörper unzureichend ist.2
- Bei Beendigung einer Therapie mit Kortikosteroiden, insbesondere bei systemischer Gabe, besteht das Risiko einer Nebenniereninsuffizienz.
6970 - Spezifische Immuntherapie (SIT)
- Siehe Leitlinienkasten.
Überprüfung der Asthmakontrolle und Therapieanpassung
- Siehe Leitlinienkasten.
Weitere Therapien
- Die medikamentöse Therapie des Asthmas sollte durch nichtmedikamentöse Therapiemaßnahmen ergänzt werden.2-4
- Ziel ist u. a. eine Stärkung der Krankheitsbewältigung und des Selbstmanagements.
- Die nichtmedikamentösen Maßnahmen bei Asthma umfassen:
- Patientenschulung und Informationsangebote
- Physiotherapie und Atemphysiotherapie
- körperliche Aktivität
- Vermeidung der Allergenexposition oder anderer Auslöser
- Gewichtsreduktion bei Adipositas
- ggf. Raucherentwöhnung
- ggf. Sozial- und Berufsberatung
- Unterstützung durch das familiäre und soziale Umfeld.
Informationsangebote und Patientenschulung
- Allen Patient*innen mit Asthma und medikamentöser Langzeittherapie soll ein strukturiertes, verhaltensbezogenes Schulungsprogramm und empfohlen und ermöglicht werden.2,4,
7071-7172- Bei Kindern und Jugendlichen nach Möglichkeit die Eltern einbeziehen.
- Regelmäßige Nachschulungen anbieten.2
- Nachgewiesene Wirkungen
7071,7273
- Verbesserung der Asthmakontrolle mit weniger Asthmaanfällen
- Verbesserung der Lebensqualität
- Reduktion der Krankenhaus-, Arbeitsunfähigkeits- bzw. Schulfehltage
- aktive Teilnahme der Patient*innen (bei Kindern und Jugendlichen auch deren Familien) an der Krankheitsbewältigung
- Inhalte von Schulungsprogrammen
- Pathophysiologie und Auslöser der Erkrankung
- Behandlungsgrundsätze
- Inhalationstechniken
- Therapieadhärenz
- Fähigkeit zum Selbstmanagement
- individueller Asthma-Aktionsplan bzw. Selbstmanagementplan2,
7374 - z. B. Symptomtagebuch, häusliche PEF-Messungen
- individueller Asthma-Aktionsplan bzw. Selbstmanagementplan2,
Vermeidung der Auslöser
- Identifizierte Auslöser, z. B. kalte Luft oder Luftschadstoffe, so weit wie möglich meiden.
- Allergenkarenz
- wesentlicher Bestandteil der Behandlung des allergischen Asthmas2
- Bei nachgewiesener Tierallergie mit Symptomen bei Exposition Vermeidung des direkten und indirekten Tierkontaktes anstreben.
- Keine potenziell anfallsauslösenden Medikamente (ASS, NSAR oder Betablocker)
- Anpassung des beruflichen Umfeldes, falls Zusammenhang mit Asthmasymptomen besteht.
- Anpassung der häuslichen Umgebung
- Feuchtes Innenraumklima und Schimmelbefall vermeiden.
- Maßnahmen zur Reduktion der Allergenexposition, z. B. spezielle Bettbezüge gegen Hausstaubmilben oder Luftfilter
7475-7576
- Die NVL bewertet milbendichte Matratzenschoner als Maßnahme, die potenziell zur Allergenreduktion beitragen kann.2
Physiotherapie
- Atemphysiotherapie
- Mobilisation der Atemmuskulatur und Erlernen und Stärken von physiologische Atemmustern4
- Soll allen Patient*innen mit Koinzidenz von Asthma und dysfunktionaler Atmung (auch VCD) angeboten werden.2
- Sollte Patient*innen mit Asthma und zusätzlichem Behandlungsbedarf oder bei durch die Atemnot ausgelöster Angst empfohlen werden.2
- Ziel ist eine Kontrolle von Atemnot, Hustenreiz und Angst.
- Auch Atemtraining mit Relaxationstraining oder Biofeedbackmethoden können zu einer Verbesserung von Symptomen und Lebensqualität führen.
7677 - Aus klinischer Erfahrung sind Atemübungen förderlich, eindeutig gesichert ist der Effekt jedoch nicht.
7778
Körperliche Aktivität
- Allen Patient*innen mit Asthma
sollten Maßnahmen dessollte körperlichenrperlichesTrainingsTraining- Anstrengungsinduzierte Symptome sind oft Ausdruck einer unzureichenden Asthmakontrolle.
- ggf. Intensivierung der Langzeittherapie entsprechend der Stufentherapie
- Effekte von regelmäßiger sportlicher Aktivität sind:
7879- Verringerung der Asthmasymptomatik
- Besserung der Belastbarkeit
- Verbesserung der Lebensqualität
- Verringerung der Morbidität
- Vermeidung einer Stigmatisierung.
- Eine Gewichtsreduktion bei Übergewicht wirkt sich positiv auf den Krankheitsverlauf aus.
- Bei Asthma und Adipositas ist eine Gewichtsreduktion empfohlen.2
- Regelmäßiges körperliches Training
7980
Tabakentwöhnung
- Rauchverzicht
- Allen Patient*innen mit Asthma soll ein Rauchverzicht empfohlen werden.2
- Patient*innen mit Bereitschaft sollen bezüglich der Tabakentwöhnung ärztlich beraten werden.
- Angebot nichtmedikamentöser und medikamentöser Hilfen
- Patient*innen sollen in einer rauchfreien Umgebung leben können.2
Rehabilitation
- Soll Patient*innen mit beeinträchtigenden körperlichen, sozialen oder psychischen Krankheitsfolgen trotz adäquater ambulanter Betreuung angeboten werden.2
- Die Krankheitsfolgen behindern die Möglichkeiten von normalen Aktivitäten bzw. der Teilhabe am normalen beruflichen und privaten Leben.
- z. B. bei Gefährdung der Berufs- und Erwerbsfähigkeit, drohender Pflege- und Hilfsbedürftigkeit oder Komorbiditäten mit multiprofessionellem Therapieansatz
- Insbesondere nach stationär behandelten Asthmaanfällen sollten rehabilitative Maßnahmen in Betracht gezogen werden. Der multimodale Ansatz umfasst u. a.:
- personalisierte Diagnostik
- Prüfung der Auslöser und Allergenexposition
- Optimierung der Behandlung
- Patientenschulung
- Physiotherapie und Trainingstherapie
- psychologische Beratung und Psychotherapie
- Raucherentwöhnung
- Ernährungsberatung
- Berufsberatung.
Asthma und Begleiterkrankungen
- Rhinitis
- Asthma ist mit chronisch-entzündlichen Erkrankungen der oberen Atemwege assoziiert.
- Einige Autor*innen betrachten entzündliche Erkrankungen gleicher Pathogenese in den oberen und unteren Atemwegen als einheitliches Krankheitsbild (Hypothese der „United Airways").
- Chronisch-entzündliche Erkrankungen der oberen Atemwege sollten zuverlässig diagnostiziert und behandelt werden, um der Entstehung oder Verschlechterung des Asthma bronchiale vorzubeugen.4
- Reflux
- Ein gastroösophagealer Reflux tritt bei Patient*innen mit Asthma deutlich häufiger auf als in der Normalbevölkerung.4
- Symptomatische Patient*innen berichteten eine Auswirkung auf die Lebensqualität, die Asthmasymptome schienen jedoch unbeeinflusst durch die Refluxerkrankung.
8081 - Eine symptomatische Refluxerkrankung sollte wie gewohnt behandelt werden.
- Psychische Erkrankungen
- Die psychische Situation und das soziale Umfeld in der Behandlung und Verlaufsbeurteilung berücksichtigen.2
- Psychosoziale Beeinträchtigungen durch Asthma sind im privaten und beruflichen Bereich bei Patient*innen häufig und unterdiagnostiziert.2,4
- Können Behandlung und Selbstmanagement erschweren.
- Vor allem Angsterkrankungen und Depressionen treten häufig begleitend mit Asthma auf.
- Bei Kindern und Jugendlichen kann durch psychische Komorbiditäten die körperliche, seelische und schulische Entwicklung beeinträchtigt sein.4
- Psychosoziale und psychotherapeutische Behandlungen sind häufig Bestandteil einer pneumologischen Rehabilitation.
8182
Komplementäre Therapie
- Patient*innen (und bei Kindern deren Eltern) sollen gefragt werden, ob sie für die Behandlung des Asthmas alternative oder komplementäre Verfahren anwenden und ggf. über damit einhergehende Risiken aufgeklärt werden.2
- Für die folgenden Maßnahmen kann aufgrund einer unzureichenden Datenlage keine gesicherte Aussage oder wegen unzureichender bzw. fehlender Wirksamkeit in unterschiedlichen Studien keine Empfehlung ausgesprochen werden:2,4
- Akupunktur
8283 - Homöopathie
- Chiropraxis
8384 - Ernährungsmaßnahmen (Fischöl, Salzrestriktion, Vitamin-C-Gabe, Mineralstoffsupplementation bzw. -restriktion)
- Hypnose oder Relaxationstechniken
- in Einzelfällen Besserung des subjektiven Befindens oder der Lungenfunktion
- Ionisierer der Raumluft (Air Ionisers)
- Sollen in der Asthmatherapie nicht eingesetzt werden.4
- Luftfeuchtigkeitskontrolle
- Speläotherapie
- Traditionelle Chinesische Medizin (TCM)
- Phytotherapeutika
- Kräutergemische können das Asthma positiv beeinflussende Bestandteile enthalten.
- bronchiale Thermoplastie
- bronchoskopisches Verfahren der alternativen Behandlung des Asthmas: Durchführung in spezialisierten Zentren
- Verfahren, in dem die Atemwege per Radiofrequenz-Puls-Behandlung mit Wärme behandelt werden.
- Die Leitlinien stufen die Evidenz bezüglich Wirkung und Langzeiteffekt als unzureichend ein.2,4
- Nach GINA bei schweren Fällen als Zusatzbehandlung zu erwägen.3
- möglicher Einsatz bei fehlender Verbesserung der Asthmakontrolle mit leitliniengerechten medikamentösen Maßnahmen.2
- Akupunktur
- Bei Patient*innen mit unkontrolliertem Asthma und häufigen Exazerbationen sollte der Vitamin-D-Spiegel bestimmt und, wenn notwendig, Vitamin D substituiert werden.2
- Bei bestimmten Patient*innen mit niedrigen Vitamin-D-Spiegeln und häufigen Asthmaanfällen, die mit systemischen Kortikosteroiden behandelt werden mussten, könnte ein präventiver Effekt für weitere Asthmaanfälle vorliegen.
- Zudem bestehen keine Hinweise für schwere unerwünschte Wirkungen.
Asthma in der Schwangerschaft
- Primärversorger*innen sollen Patientinnen im gebärfähigen Alter präkonzeptionell über die Wichtigkeit einer guten Asthmakontrolle bei Eintritt in die Schwangerschaft beraten.2
- Bei Frauen mit gut kontrolliertem Asthma besteht weniger Risiko für Graviditäts- und Geburtskomplikationen.
- Bei Frauen mit unkontrolliertem Asthma zeigt sich ein erhöhtes Auftreten von Komplikationen.
8485- erhöhtes Risiko für Präeklampsie, Schwangerschaftsdiabetes, Plazentaablösung, Placenta praevia und Frühgeburten
- Frauen in der Schwangerschaft mit unzureichender Asthmakontrolle sollen von Pneumolog*innen und Gynäkolog*innen gemeinsam in enger Abstimmung betreut werden.2
- Asthma ist keine primäre Indikation für eine Sectio und soll nicht als Begründung für diese herangezogen werden.2
- Verlaufsuntersuchungen bezüglich der Schwangerschaft sollten auch eine Beurteilung der Asthmakontrolle beinhalten.
- Raucherinnen sollten über die Gefahren des Tabakrauchens für die eigene Gesundheit und die des ungeborenen Kindes aufgeklärt werden. Hier können Maßnahmen zur Raucherentwöhnung angeboten werden.
- Medikamentöse Therapie in der Schwangerschaft
- Aus der klinischen Erfahrung ist bekannt, dass die medikamentöse Therapie, die zum Erhalt der Asthmakontrolle notwendig wäre, häufig von den Patientinnen oder Ärzt*innen aus Angst vor unerwünschten Wirkungen reduziert oder abgesetzt wird.2
- Die Reduktion bzw. das Absetzen der Medikation birgt das Risiko der Verschlechterung der Asthmakontrolle. Die daraus resultierende Gefahr für den Schwangerschaftsverlauf wird als schwerwiegender eingeschätzt, als die, die von den potenziellen unerwünschten Wirkungen der Medikamente ausgeht.2
- Zur Risikoeinschätzung der medikamentösen Therapie des Asthmas in der Schwangerschaft siehe auch Embryotox.
- Asthmaanfall in der Schwangerschaft
- Bei Patientinnen in der Schwangerschaft mit einem Asthmaanfall soll eine Sauerstoffbehandlung frühzeitig eingeleitet werden (Zielsättigung: > 95 %) und eine Überwachung des Feten erfolgen.2
- Geburtseinleitung und Behandlung der postpartalen Uterusatonie
- Falls eine medikamentöse Geburtseinleitung oder Behandlung der postpartalen Uterusatonie erfolgt, sollte bei Frauen mit Asthma Oxytocin als Mittel der 1. Wahl eingesetzt werden.4
Arbeitsbedingtes Asthma
- Der gesamte Abschnitt basiert auf dieser Referenz.4
- Es sind über 550 verschiedene Auslöser des Berufsasthmas bekannt.
- Es werden 2 Formen des berufsbedingten Asthmas unterschieden:
- allergische (IgE-vermittelte) Form
- irritative Form.
- In etwa 9–25 % der Fälle von erwachsenen Patienten*innen mit Asthma sind berufliche Auslöser an der Entstehung der Erkrankung beteiligt.
- Die Arbeitsanamnese ist ein wichtiger Bestandteil in der Diagnostik bei Erwachsenen mit Asthma.
- Empfohlen sind regelmäßige arbeitsmedizinische Vorsorgeuntersuchungen bei typischerweise gefährdeten Arbeitnehmergruppen (Surveillance).
- Die wichtigste Maßnahme in der Behandlung des Berufsasthmas ist die konsequente Meidung des auslösenden Stoffes.
- Dies kann mit der Notwendigkeit eines Arbeitsplatzwechsels oder sogar einer Umschulung einhergehen.
- Siehe Artikel Berufsbedingte allergische Atemwegserkrankungen.
Prävention
Allgemeines
- Siehe auch den Artikel Allergieprävention.
- Die DGP-Leitlinie trifft folgende Aussagen zur Prävention bei Asthma:4
- Das vulnerable Fenster (Window of Opportunity) für die Entwicklung eines Asthmas liegt in utero und im sehr frühen Kindesalter.
- Daher sollten primäre präventive Interventionsmaßnahmen ebenfalls früh, möglicherweise schon während der Schwangerschaft begonnen werden, um eine Chance auf Erfolg zu haben.
- Im Wesentlichen erstrecken sich diese Maßnahmen auf die Reduktion von Passivrauchexposition und auf die Stärkung natürlicher Schutzfaktoren, die als Folge der modernen Zivilisation zugunsten von Risikofaktoren abgenommen haben.
- Empfehlungen
- Neugeborene sollten 4 Monate ausschließlich gestillt werden.
- Nach dem vollendeten 4. Lebensmonat soll Beikost eingeführt werden; es soll keine Verzögerung der Beikosteinführung erfolgen.
- Kinder mit Allergierisiko sollten keine Fell- und Federtiere anschaffen bzw. halten. Katzenhaltung ist bei diesen Kindern generell nicht zu empfehlen.
- Hohe Luftfeuchtigkeit und mangelnde Ventilation in Räumen, flüchtige organische Verbindungen (z. B. Formaldehyd), aktive und passive Tabakrauchexposition sowie KfZ-Abgasexposition sollen vermieden werden.
- Auch Säuglinge und Kinder mit erhöhtem Asthmarisiko sollen nach den allgemeinen Empfehlungen geimpft werden.
- Übergewicht und Adipositas sind mit Asthma positiv assoziiert und sollten bei Kindern vermieden werden.
- Stellungnahmen/Statements, jedoch keine Empfehlungen
- Es gibt keinen Anhalt dafür, dass der Einsatz partiell oder extensiv hydrolisierter Säuglingsnahrungen der Asthmaprävention dient.
- Es sind keine diätetischen Restriktionen im Hinblick auf die Ernährung der Mutter während der Schwangerschaft und Stillzeit erforderlich.
- Kinder ohne Allergierisiko müssen nicht auf Haustiere verzichten.
- Eine Hausstaubmilbensanierung ist zur Primärprävention nicht zu empfehlen, zur Sekundär- und Tertiärprävention jedoch ratsam.
- Eine höhere Anzahl älterer Geschwister, der Besuch einer Kindertagesstätte, das Aufwachsen auf einem Bauernhof mit Tieren sowie Wurminfektionen sind negativ mit Asthma assoziiert.
- Aktive Tabakrauchvermeidung und striktes Meiden von Environmental Tobacco Smoke (ETS) ist die wichtigste Präventionsmaßnahme in der Schwangerschaft.
- Telemedizin2
- Laut NVL könnten telemedizinische Maßnahmen in der Versorgung von Patient*innen mit Asthma an Bedeutung gewinnen.
- bisher unzureichende Evidenz für eine Empfehlung telemedizinischer Verfahren
- Beispiele sind SMS-Erinnerungssysteme, Smartphone- und Tablet-Apps oder Gaming-basierte Interventionen bei Jugendlichen.
- Laut NVL könnten telemedizinische Maßnahmen in der Versorgung von Patient*innen mit Asthma an Bedeutung gewinnen.
Spezifische Immuntherapie
- Kein Ersatz für eine Asthmatherapie, kann jedoch frühzeitig in der Behandlung des allergischen Asthmas eingesetzt werden.
- Allergenspezifische Immuntherapie (SIT, Hyposensibilisierung) reduziert die Asthmasymptome, den Medikamentenbedarf und die allergenspezifische bronchiale Hyperreagibilität.
8586 - Hinweise für präventive Wirkung
- Bei Patient*innen mit allergischer Rhinitis konnte die Entstehung von Asthmasymptomen (Etagenwechsel) durch eine subkutane Immuntherapie bis zu 7 Jahre nach Beendigung der 3-jährigen Therapie reduziert werden.
8687 - Von Kindern mit allergischer Rhinitis, die mit Hyposensibilisierung behandelt wurden, hatten nach 3 Jahren nur halb so viele ein Asthma entwickelt wie in der Kontrollgruppe.
8788
- Bei Patient*innen mit allergischer Rhinitis konnte die Entstehung von Asthmasymptomen (Etagenwechsel) durch eine subkutane Immuntherapie bis zu 7 Jahre nach Beendigung der 3-jährigen Therapie reduziert werden.
Impfungen
- Der gesamte Abschnitt basiert auf dieser Referenz.2
- Asthma erhöht, wie andere chronische Erkrankungen, das Risiko, an Grippe und Pneumokokken-Infektionen zu erkranken.
- Patient*innen mit Asthma sollen daher Impfungen gemäß den Empfehlungen der STIKO angeboten werden.
Verlauf, Komplikationen und Prognose
Verlauf
- Die Atemwegsentzündung verursacht wiederkehrende Episoden mit Atemnot, Engegefühl in der Brust und Husten.
- Der Verlauf der Erkrankung kann sehr fluktuieren, v. a. bei saisonaler allergischer Komponente.
- Die Anzahl an Krankenhauseinweisungen aufgrund von Asthmaanfällen ist heutzutage deutlich rückläufig (Effekt der ICS-Langzeittherapie).
8889
- Kindern mit viralen Atemwegsinfektionen als Auslöser der Asthmasymptome geht es im Sommer aufgrund der selteneren Infekte meist besser.
Komplikationen
- Schwerer und lebensbedrohlicher akuter Asthmaanfall
- Übergang in eine Mischform mit chronisch obstruktiver Lungenkrankheit (Asthma-COPD-Overlap-Syndrom, ACOS)
- Sekundäre Nebennierenrindeninsuffizienz
6970- Bei Patient*innen mit hochdosierten inhalativen Kortikosteroiden (insbesondere Fluticason) über einen längeren Zeitraum und möglicherweise systemischen Kortikosteroiden berücksichtigen.
- Warnzeichen sind Gewichtsabnahme, Müdigkeit, Übelkeit und Erbrechen.
- Mögliche Gefährdungssituation bei Beendigung einer Langzeittherapie mit entweder oralen oder inhalativen Kortikosteroiden2
- Erhöhtes Risiko, an Influenza und Pneumokokken-Infektionen zu erkranken.2
- Impfungen gemäß den Empfehlungen der STIKO
Erhöhtes Mortalitätsrisiko im Asthmaanfall2,4
- Folgende Faktoren weisen auf ein erhöhtes Mortalitätsrisiko im schweren Asthmaanfall hin:
- unzureichende Therapieadhärenz
- exzessiver Gebrauch von Beta-2-Sympathomimetika
- systemische Kortikosteroide in der Medikation
Beinahebeinahe tödlicher Asthmaanfall („Near-fatal Asthma“) in der Vorgeschichte- Intubation mit mechanischer Beatmung im Rahmen eines vorherigen Asthmaanfalls
- stationäre Behandlung wegen des Asthmas im zurückliegenden Jahr.
Prognose
- Bei einem großen Anteil von Kindern und Jugendlichen mit Asthma verschwinden die Beschwerden im Laufe des Lebens.
- Während der Pubertät kommt es insbesondere bei Jungen zu einer Verbesserung der Symptome.15
- Bei 30–50 % der Kinder verschwindet das Asthma in der Pubertät, die Krankheit kann jedoch im Erwachsenenalter erneut auftreten.
- Bei älteren Kindern gibt es eine Tendenz zu abnehmenden Beschwerden mit zunehmendem Alter, jedoch treten oft noch Symptome im Erwachsenenalter auf.
8990- Prädiktoren für anhaltendes Asthma sind Atopie, reduzierte Lungenfunktion und bronchiale Hyperreagibilität.
- Bei manchen erwachsenen Patient*innen, insbesondere Raucher*innen, kann es im Laufe der Zeit zu irreversiblen Veränderungen mit permanenter Obstruktion im Sinne einer COPD kommen.
- Alter bei Krankheitsbeginn
- Die Prognose scheint mit dem Alter bei Krankheitsbeginn assoziiert zu sein. Insbesondere bei spätem Beginn im Erwachsenenalter ist das Risiko für Lungenfunktionseinschränkungen und Exazerbationen erhöht.
9091
- Die Prognose scheint mit dem Alter bei Krankheitsbeginn assoziiert zu sein. Insbesondere bei spätem Beginn im Erwachsenenalter ist das Risiko für Lungenfunktionseinschränkungen und Exazerbationen erhöht.
- Die Auswirkungen auf das soziale und berufliche Leben bei kindlichem Asthma sind gering. Die Krankheit scheint die Ausbildung oder das Ausüben des Berufs nicht zu beeinträchtigen.
8990
Verlaufskontrolle
- Kontinuierliche Verlaufskontrolle und -beurteilung
- Langfristige Asthmakontrolle sichern und niedrigste effektive Therapiestufe wählen.
- Für die Anpassung der Stufentherapie siehe Leitlinienkasten Abschnitt Therapieanpassung.
- Eine Verlaufskontrolle ist auch bei kontrolliertem Asthma sinnvoll, da die Erkrankung fluktuieren kann.
- Langfristige Asthmakontrolle sichern und niedrigste effektive Therapiestufe wählen.
- Kontrolle des Wachstums bei Kindern und Jugendlichen anhand des Perzentilenschemas während einer ICS-Dauertherapie
- Impfungen anhand STIKO-Empfehlungen
- Bei jeder Verlaufskontrolle sollen folgende Parameter erhoben werden:2
- Asthmasymptome tagsüber, nachts und bei körperlicher Belastung
- Häufigkeit des Einsatzes von Bedarfsmedikation
- Einschränkungen der Aktivitäten des Alltags
- Therapieadhärenz und Inhalationstechnik
- Häufigkeit des Auftretens und Auslöser von Exazerbationen
- Wirksamkeit und Verträglichkeit der medikamentösen Therapie.
Versorgungskoordination
- Der gesamte Abschnitt basiert auf dieser Referenz.2
- Die NVL empfiehlt Langzeitbetreuung und Dokumentation im Rahmen eines strukturierten Behandlungsprogramms.
- in der Regel durch Hausärzt*innen oder Kinder- und Jugendärzt*innen
- in besonderen Fällen (dauerhaft hohe Instabilität oder schwerer Krankheitsverlauf) durch (pädiatrische) Pneumolog*innen
- bei Stabilisierung des Zustands ggf. Weiterbehandlung durch die Hausärzt*innen oder Kinder- und Jugendärzt*innen
- Für Indikationen zur Überweisung bzw. Einweisung in ein Krankenhaus siehe Abschnitt Indikationen zur Überweisung/
KklinikeinweisungKlinikeinweisung.- Ziel einer Überweisung ist nicht primär die Übergabe der Langzeitbehandlung, sondern Beurteilung und ggf. Anpassung der Behandlung.
- Nach einem Krankenhausaufenthalt: Indikation für eine sich direkt anschließende Rehabilitationsmaßnahme bei Kindern und Jugendlichen prüfen.
- Empfohlene Konsultationshäufigkeit
- Die NVL verzichtet auf eine Festlegung genauer Frequenzen für durchzuführende Untersuchungen: Krankheitsverlauf und Einschätzung der Notwendigkeit durch die behandelnden Ärzt*innen entscheidend.
- Nach einem Asthmaanfall sollte eine zeitnahe Wiedervorstellung mit folgenden Maßnahmen erfolgen:
- Risikofaktoren für Verschlechterung der Asthmakontrolle identifizieren.
- Asthmaaktionsplan aushändigen bzw. überarbeiten.
- Schulung bzw. Nachschulung anregen.
- Notwendigkeit einer Intensivierung der Langzeittherapie prüfen.
- Indikation zu einer Rehabilitation prüfen.
- Laut GINA ist die Lungenfunktionsdiagnostik der wichtigste Parameter für das Langzeitrisiko. Diese sollte bei Diagnosestellung, 3–6 Monate nach Therapiebeginn und danach in regelmäßigen Abständen, mindestens jährlich, wiederholt werden.3
Disease-Management-Programm (DMP) Asthma9192
- Laut DMP soll die Langzeitbetreuung der Patient*innen mit Asthma und deren Dokumentation im Rahmen des strukturierten Behandlungsprogramms grundsätzlich durch die Hausärztin oder den Hausarzt erfolgen.
- in Ausnahmefällen auch durch qualifizierte Fachärzt*innen oder qualifizierte Einrichtungen
- Eine gleichzeitige Einschreibung in das DMP Asthma bronchiale und das DMP COPD ist nicht möglich.
- Neben dem Asthma bronchiale kann eine COPD bestehen. In Abhängigkeit des Krankheitsverlaufs sollten die behandelnden Ärzt*innen abwägen, welche der beiden Diagnosen als vorrangig einzustufen ist.
- Die Frequenz der Kontrolluntersuchungen ist abhängig von der medizinischen Notwendigkeit und der Schwere des Krankheitsbildes.
- Untersuchungen und Maßnahmen bei jedem Patientenkontakt
- Anamnese und Abschätzung des Kontrollgrades
- ggf. mit Prüfung der Asthmatagebücher/PEF-Protokolle („Peak Expiratory Flow“)
- körperliche Untersuchung (Auskultation)
- Prüfung der Medikation und Begleitmedikation, Medikamenten- und Notfallplan
- Prüfung der Inhalationstechnik, ggf. Einleitung von Schulungsmaßnahmen
- Entscheidung über Weiterführung, Steigerung oder Absenkung der Dosis inhalativer Glukokortikosteroide
- Entscheidung über evtl. notwendige weitere diagnostische oder therapeutische Maßnahmen
- Entscheidung über das zukünftige Kontrollintervall
- Anamnese und Abschätzung des Kontrollgrades
- Dokumentation in Absprache mit den Patient*innen vierteljährlich oder halbjährlich
- Unabhängig vom Kontrollintervall soll ab der Vollendung des 5. Lebensjahres mind. 1 x/Jahr eine Lungenfunktionsmessung erfolgen.
Patienteninformationen
Worüber sollten Sie die Patient*innen informieren?
- Selbstmanagement, auch bei akuten Beschwerden
- individueller Asthma-Aktionsplan bzw. Selbstmanagementplan2
- ggf. PEF-Messungen und Tagebucheintragungen
- Empfehlen Sie eine Schulung und Informationsangebote für die Patient*innen und ihre Angehörigen im Rahmen einer Asthmaschule.
- Geben Sie Anleitungen zur korrekten Inhalationstechnik.
- Siehe auch die Deutsche Atemwegsliga – Richtig inhalieren.
- Möglichkeit der Unterstützung durch eine Patientenselbsthilfeorganisation
Informationsmaterial
- Nationale VersorgungsLeitlinie (NVL) Asthma: Patientenblätter
- Langzeitbehandlung mit Kortisonspray bei Asthma
- Unterschiedliche Inhaliergeräte bei Asthma
- Wechsel des Inhaliergerätes bei Asthma
- Asthma: Warum es hilft, aufs Rauchen zu verzichten.
- allergisches Asthma und Tierallergie
- Kinderwunsch, Schwangerschaft und Geburt
- Deutsche Atemwegsliga e. V.: Informationen zu Asthma
Patienteninformationen in Deximed
Asthma
- Asthma
Wie wird Asthma diagnostiziert?Wie kann ein Asthmaanfall vermieden werden?- Erste Hilfe bei Asthma
- Asthmaanfall bei Erwachsenen
- Anstrengungsasthma
Asthma, Ursachen und auslösende FaktorenAsthma und AllergieAsthma und Rauchen- Warum sollten Sie das Rauchen aufgeben, und wie gelingt es?
- Asthma und Schwangerschaft
Berufsbedingtes AsthmaAsthma bei Sportler*innenAsthma und TierallergieAsthma, Wechsel des InhaliergerätesLangzeitbehandlung bei Asthma, KortisonsprayAsthma, InhaliergerätePEF-MessungenSpirometrie
Asthma bei Kindern und Jugendlichen
- Asthma bei Kindern
- Asthmabehandlung bei Kindern
- Asthmaanfall bei Kindern
- Gesundheitsinformation.de: Asthma – Informationen für Eltern
Patientenorganisationen
- Deutsche Patientenliga Atemwegserkrankungen e. V.
-
Deutscher Allergie und Asthmabund e. V.: Wie können wir Ihnen helfen?
- Deutsche Atemwegsliga e. V.: Informationsmaterial Asthma
-
Arbeitsgemeinschaft Lungensport in Deutschland e. V.: Fit zum Atmen
Weitere Informationen
- Siehe Artikel Beurteilung der Fahreignung.
Illustrationen
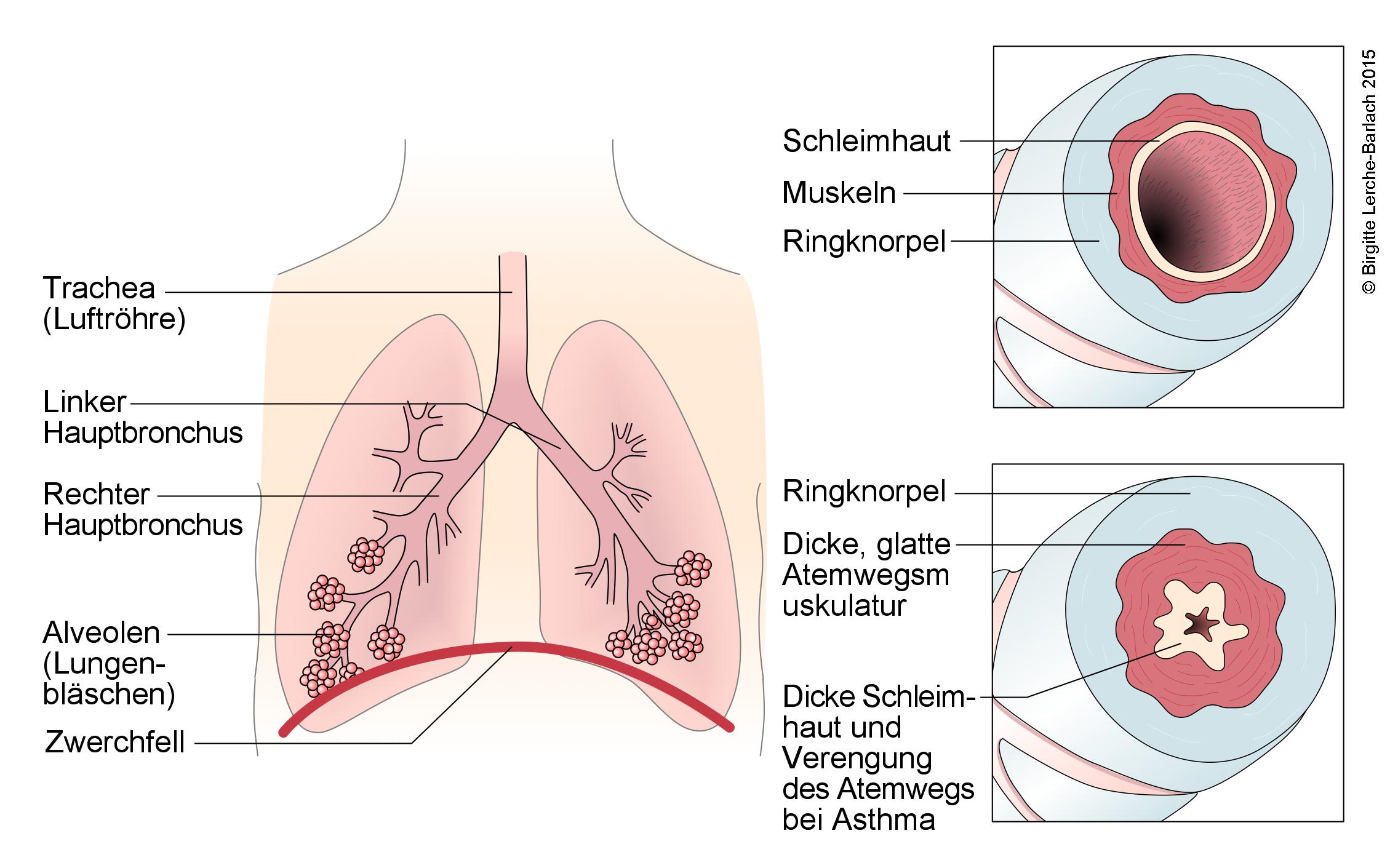
Atemwege und Veränderungen bei Asthma
CME-Punkte
Quellen
Leitlinien
- Deutsche Gesellschaft für Allgemeinmedizin und Familienmedizin. Klimabewusste Verordnung von inhalativen Arzneimitteln. S1, AWMF-Nr. 053-059. Stand 2022. www.degam.de
- Ärztliches Zentrum für Qualität in der Medizin (ÄZQ). Nationale Versorgungsleitline Asthma. 4. Auflage, Stand 2020. www.leitlinien.de
- Deutsche Gesellschaft für Pneumologie und Beatmungsmedizin (DGP). Diagnostik und Therapie von Patienten mit Asthma. AWMF-Leitlinie Nr. 020-009. S2k, Stand 2017. www.awmf.org
- Global Initiative for Asthma. Pocket Guide for Asthma Management and Prevention. Stand 2020. www.ginasthma.com
- Deutsche Gesellschaft für Pneumologie und Beatmungsmedizin (DGP). Spirometrie. AWMF-Leitlinie Nr. 020-017. S2k, Stand 2015. www.awmf.org
- Deutsche Gesellschaft für Allergologie und klinische Immunologie. Allergieprävention. AWMF-Leitlinie Nr. 061-016. S3, Stand 2014 (in Überarbeitung). www.awmf.org
Literatur
- Lohnstein M, Eras J, Hammerbacher C. Der Prüfungsguide Allgemeinmedizin - Aktualisierte und erweiterte 3. Auflage. Augsburg: Wißner-Verlag, 2018.
- Ärztliches Zentrum für Qualität in der Medizin (ÄZQ). Nationale Versorgungsleitline Asthma. 4. Auflage, Stand 2020. www.leitlinien.de
- Global Initiative for Asthma. Pocket Guide for Asthma Management and Prevention. Stand 2020. ginasthma.org
- Deutsche Gesellschaft für Pneumologie und Beatmungsmedizin (DGP). Diagnostik und Therapie von Patienten mit Asthma. AWMF-Leitlinie Nr. 020-009, Stand 2017. www.awmf.org
- GBD 2015 Chronic Respiratory Disease Collaborators. Global, regional, and national deaths, prevalence, disability-adjusted life years, and years lived with disability for chronic obstructive pulmonary disease and asthma, 1990-2015: a systematic analysis for the Global Burden of Disease Study 2015. Lancet Respir Med. 2017 Sep;5(9):691-706. doi: 10.1016/S2213-2600(17)30293-X Epub 2017 Aug 16. PubMed PMID: 28822787 www.ncbi.nlm.nih.gov
- Schmitz R et al. Verbreitung häufiger Allergien bei Kindern und Jugendlichen in Deutschland. Ergebnisse der KiGGS Studie – Erste Folgebefragung (KiGGS Welle 1) Bundesgesundheitsbl 2014 · 57:771–778 edoc.rki.de
- Moorman JE, Akinbami LJ, Bailey CM, Zahran HS, King ME, Johnson CA, Liu X. National surveillance of asthma: United States, 2001-2010. Vital Health Stat 3. 2012 Nov;(35):1-58. PubMed PMID: 24252609 www.ncbi.nlm.nih.gov
- Ramsey CD, Celedón JC. The hygiene hypothesis and asthma. Curr Opin Pulm Med. 2005 Jan;11(1):14-20. Review. PubMed PMID: 15591883 www.ncbi.nlm.nih.gov
- Dietert RR. Maternal and childhood asthma: risk factors, interactions, and ramifications. Reprod Toxicol. 2011 Sep;32(2):198-204. doi: 10.1016/j.reprotox.2011.04.007 Epub 2011 May 6. Review. PubMed PMID: 21575714 www.ncbi.nlm.nih.gov
- Halapi, E; Bjornsdottir, US (January 2009). "Overview on the current status of asthma genetics". The clinical respiratory journal. 3 (1): 2–7. doi:10.1111/j.1752-699X.2008.00119.x PMID 20298365. www.ncbi.nlm.nih.gov
- Kelly FJ, Fussell JC. Air pollution and airway disease. Clin Exp Allergy. 2011 Aug;41(8):1059-71. doi: 10.1111/j.1365 2222.2011.03776.x Epub 2011 May 30. Review. PubMed PMID: 21623970 www.ncbi.nlm.nih.gov
- Sears MR. Trends in the prevalence of asthma. Chest. 2014 Feb;145(2):219-225. doi: 10.1378/chest.13-2059 PubMed PMID: 24493506 www.ncbi.nlm.nih.gov
- Steppuhn H, Kuhnert R, Scheidt-Nave C. 12-Monats-Prävalenz von Asthma bronchiale bei Erwachsenen in Deutschland. Journal of Health Monitoring 2017; 2(3): 36-45. www.rki.de
- Robert Koch-Institut (Hrsg) (2014) Asthma bronchiale. Faktenblatt zu GEDA 2012: Ergebnisse der Studie »Gesundheit in Deutschland aktuell 2012«. RKI, Berlin www.rki.de/geda (Stand: 08.04.2015) www.rki.de
- Gibson GJ, Loddenkemper R, Sibille Y et al. (Hrsg) (2013) The European lung white book. Respiratory health and disease in Europe. European Respiratory Society, Sheffield www.ncbi.nlm.nih.gov
- Upton MN, McConnachie A, McSharry C, Hart CL, et al. Intergenerational 20 year trends in the prevalence of asthma and hay fever in adults: the Midspan family study surveys of parents and offspring. BMJ 2000; 321: 88-92. www.ncbi.nlm.nih.gov
- McCreanor J, Cullinan P, Nieuwenhuijsen MJ, et al. Respiratory effects of exposure to diesel traffic in persons with asthma.. NEJM 2007; 357: 2348-2358. www.nejm.org
- Ahluwalia SK, Matsui EC. The indoor environment and its effects on childhood asthma. Curr Opin Allergy Clin Immunol. 2011 Apr;11(2):137-43. doi: 10.1097/ACI.0b013e3283445921 Review. PubMed PMID: 21301330 www.ncbi.nlm.nih.gov
- Mackay D, Haw S, Ayres JG, et al. Smoke-free legislation and hospitalizations for childhood asthma. N Engl J Med 2010; 363: 1139-45. www.nejm.org
- Riedler J, Braun-Fahrländer C, Eder W, Schreuer M, et al. Exposure to farming in early life and development of asthma and allergy: a cross-sectional survey . Lancet 2001; 358: 1129-33. www.ncbi.nlm.nih.gov
- Mutius E, Vercelli D. Farm living: effects on childhood asthma and allergy. Nat Rev Immunol. 2010 Dec;10(12):861-8. doi: 10.1038/nri2871 Epub 2010 Nov 9. Review. PubMed PMID: 21060319 www.ncbi.nlm.nih.gov
- Lau S, Illi S, Sommerfeld C, Niggeman B, et al. . Early exposure to house dust mite and cat allergens and development of childhood asthma: a cohort study. Lancet 2000; 356: 1392-7. www.ncbi.nlm.nih.gov
- Deutsche Gesellschaft für Allergologie und klinische Immunologie. Allergieprävention. AWMF-Leitlinie Nr. 061-016, Stand 2014. www.awmf.org
- Platts-Mills T, Vaughan J, Squillace S, Woodfolk J, Sporik J. Sensitisation, asthma, and a modified Th2 response in children exposed to cat allergen: a population-based cross-sectional study. Lancet 2001; 357: 752-6. www.ncbi.nlm.nih.gov
- Illi S, von Mutius E, Lau S, Bergmann R, Niggemann B, Sommerfeld C, Wahn U. Early childhood infectious diseases and the development of asthma up to school age: a birth cohort study. BMJ 2001; 322: 390-5. www.ncbi.nlm.nih.gov
- Clark CE, Coote JM, Silver DAT, Halpin DMG. Asthma after childhood pneumonia: six year follow up study. BMJ 2000; 320:1514-6. www.bmj.com
- Beuther DA. Obesity and asthma. Clin Chest Med. 2009 Sep;30(3):479-88, viii. doi: 10.1016/j.ccm.2009.05.002Review PubMed PMID:19700046. www.ncbi.nlm.nih.gov
- van der Hulst AE, Klip H, Brand PL. Risk of developing asthma in young children with atopic eczema: A systematic review. J Allergy Clin Immunol 2007; 120: 565-9. www.ncbi.nlm.nih.gov
- Bergmann RL, Edenharter G, Bergmann KE, Forster J, Bauer CP, Wahn V, et al. Atopic dermatitis in early infancy predicts allergic airway disease at 5 years. Clin Exp Allergy 1998; 28: 965-70. www.ncbi.nlm.nih.gov
- Russell G, Ninan TK. Respiratory symptoms and atopy in Aberdeen school children: evidence from two surveys 25 years apart. BMJ 1992; 304: 873-5. www.ncbi.nlm.nih.gov
- Goksör E, Loid P, Alm B, et al.. The allergic march comprises the coexistence of related patterns of allergic disease not just the progressive development of one disease. Acta Paediatr 2016 Dec; 105(12): 1472-1479. pmid:27381249. www.ncbi.nlm.nih.gov
- Etminan M, Sadatsafavi M, Jafari S, et al. Acetaminophen use and the risk of asthma in children and adults: a sytematic review and metaanalysis. Chest 2009; 136: 1316-23. www.ncbi.nlm.nih.gov
- Lowe AJ, Carlin JB, Bennett CM, et al. Paracetamol use in early life and asthma: prospective birth cohort study. BMJ 2010; 341: c4616. dx.doi.org
- Warner JO, ETAC Study Group. Early treatment of the atopic child. A double-blinded, randomized, placebo-controlled trial of cetirizine in preventing the onset of asthma in children with atopic dermatitis: 18 months' treatment and 18 months' posttreatment follow-up. J Allergy Clin Immunol 2001; 108: 929-37. www.ncbi.nlm.nih.gov
- Örtqvist AK, Lundholm C, Kieler H, et al. Antibiotics in fetal and early life and subsequent childhood asthma: nationwide population based study with sibling analysis. BMJ 2014; 349: g6979. dx.doi.org
- Hershenson MB. Rhinovirus-Induced Exacerbations of Asthma and COPD. Scientifica (Cairo). 2013;2013:405876. doi: 10.1155/2013/405876 Epub 2013 Feb 21. Review. PubMed PMID: 24278777 PMID:24278777. www.ncbi.nlm.nih.gov
- Rajan P, Wineinger NE, Stevenson DD, White AA. Prevalence of aspirin-exacerbated respiratory disease among asthmatic patients: A meta-analysis of the literature . J Allergy Clin Immunol 2015; 135: 676-681. doi:10.1016/j.jaci.2014.08.020 DOI
- Deutsche Gesellschaft für Pneumologie und Beatmungsmedizin (DGP). Spirometrie. AWMF-Leitlinie Nr. 020 – 017. Stand 2015. www.awmf.org
- Eagan TM, Gulsvik A, Eide GE, et al. Occupational airborne exposure and the incidence of respiratory symptoms and asthma. Am J Respir Crit Care Med 2002; 1665: 933-938. www.ncbi.nlm.nih.gov
- EAACI Task Force on Occupational Rhinitis, Moscato G, Vandenplas O, Gerth Van Wijk R, Malo JL, Quirce S, Walusiak J, Castano R, De Groot H, Folletti I, Gautrin D, Yacoub MR, Perfetti L, Siracusa A. Occupational rhinitis. Allergy. 2008 Aug;63(8):969-80. doi: 10.1111/j.1398-9995.2008.01801.x PubMed PMID: 18691299. www.ncbi.nlm.nih.gov
- Price DB, Rigazio A, Campbell JD, et al. Blood eosinophil count and prospective annual asthma disease burden: A UK cohort study. Lancet Respir Med 2015; 3(11): 849-58. pubmed.ncbi.nlm.nih.gov
- Deutsche Gesellschaft für Allgemeinmedizin und Familienmedizin. Klimabewusste Verordnung von inhalativen Arzneimitteln. S1, AWMF-Nr. 053-059. Stand 2022. www.degam.de
- arzneitelegramm: Therapiekritik MILDES ASTHMA – GRUNDLEGENDER WANDEL DER STUFENTHERAPIE? a-t 2020; 51: 1-5 www.arznei-telegramm.de
- arzneitelegramm: Therapiekritik – Ein Inhalator zur Erhaltungs- und Bedarfstherapie – eine smarte Idee? a-t 2020; 51: 2-3. www.arznei-telegramm.de
- Leach CL, Colice GL. A pilot study to assess lung deposition of HFA-beclomethasone and CFC-beclomethasone from a pressurized metered dose inhaler with and without add-on spacers and using varying breathhold times. J Aerosol Med Pulm Drug Deliv. 2010 Dec;23(6):355-61. doi: 10.1089/jamp.2009.0783 Epub 2010 Jun 24. PubMed PMID: 20575669 www.ncbi.nlm.nih.gov
- Cates CJ, Welsh EJ, Rowe BH. Holding chambers versus nebulisers for beta-agonist treatment of acute asthma. Cochrane Database Syst Rev 2013; 9: CD000052. PMID: 24037768 PubMed
- Rodrigo GJ, Castro-Rodriguez JA. Anticholinergics in the treatment of children and adults with acute asthma: a systematic review with meta-analysis. Thorax 2005; 60: 740-6. PubMed
- Rowe BH, Spooner C, Ducharme FM, Bretzlaff JA, Bota GW. Early emergency department treatment of acute asthma with systemic corticosteroids. CochranenDatabase Syst Rev. 2001;(1):CD002178. Review. PubMed PMID: 11279756 www.ncbi.nlm.nih.gov
- Currie GP, Devereux GS, Lee DKC, Ayres JG. Recent developments in asthma management. BMJ 2005; 330: 585-589. www.ncbi.nlm.nih.gov
- Brozek JL, Kraft M, Krishnan JA, et al. Long-acting beta2-agonist step-off in patients with controlled asthma: systematic review with meta-analysis. Arch Intern Med 2012: 1-11 . pmid:22928176. PubMed
- Zhang L, Prietsch SOM, Ducharme FM. Inhaled corticosteroids in children with persistent asthma: effects on growth. Cochrane Database of Systematic Reviews 2014, Issue 7. Art. No.: CD009471. DOI: 10.1002/14651858.CD009471.pub2 www.ncbi.nlm.nih.gov
- Jones A, Fay JK, Burr ML, Stone M, Hood K, Roberts G. Inhaled corticosteroid effects on bone metabolism in asthma and mild chronic obstructive pulmonary disease. Cochrane Database of Systematic Reviews 2002, Issue 1. Art. No.: CD003537 Cochrane (DOI)
- Walters EH, Gibson PG, Lasserson TJ, Walters JAE. Long-acting beta2-agonists for chronic asthma in adults and children where background therapy contains varied or no inhaled corticosteroid. Cochrane Database of Systematic Reviews 2007, Issue 1. Art. No.: CD001385 Cochrane (DOI)
- Salpeter SR, Buckley NS, Ormiston TM, Salpeter EE. Meta-analysis: effect of long-acting beta-agonists on severe asthma exacerbations and asthma-related deaths. Ann Intern Med. 2006; 144: 904-12. PubMed
- Salpeter SR, Wall AJ, Buckley NS. Long-acting beta-agonists with and without inhaled corticostreoids and catastrophic asthma events. Am J Med 2010; 123: 322-8. PubMed
- Cates CJ, Jaeschke R, Schmidt S, et al. Regular treatment with formoterol and inhaled steroids for chronic asthma: serious adverse events. Cochrane Database Syst Rev 2013; 6: CD006924. pmid:23744625 PubMed
- Kew KM, Karner C, Mindus SM, et al. Combination formoterol and budesonide as maintenance and reliever therapy versus combination inhaler maintenance for chronic asthma in adults and children. Cochrane Database Syst Rev. 2013 Dec 16;12:CD009019. doi: 10.1002/14651858.CD009019.pub2. DOI
- Cates CJ, Karner C. Combination formoterol and budesonide as maintenance and reliever therapy versus current best practice (including inhaled steroid maintenance), for chronic asthma in adults and children. Cochrane Database Syst Rev 2013; 4: CD007313. pmid:23633340 PubMed
- Loymans RJ, Gemperli A, Cohen J, et al. Comparative effectiveness of long term drug treatment strategies to prevent asthma exacerbations: network meta-analysis. BMJ. 2014 May 13;348:g3009. doi: 10.1136/bmj.g3009 DOI
- Busse WW, Bateman ED, Caplan AL, et al.
.Combined Analysis of Asthma Safety Trials of Long-Acting β2-Agonists. N Engl J Med 2018; 378(26): 2497-2505. pmid:29949492 www.ncbinejm.nlm.nih.govorg - Chauhan BF, Ducharme FM. Addition to inhaled corticosteroids of long-acting beta2-agonists versus anti-leukotrienes for chronic asthma. Cochrane Database Syst Rev. 2014 Jan 24;1:CD003137. Cochrane (DOI)
- FDA. Press Announcements. FDA Requires Stronger Warning About Risk of Neuropsychiatric Events Associated with Asthma and Allergy Medication Singulair and Generic Montelukast. March 2020. www.fda.gov
- Peterrs SP, Kunselman SJ, Icitovic N, et al. Tiotropium bromide step-up therapy for adults with uncontrolled asthma. N Eng J Med 2010; : doi:10.1056/NEJMoa1008770. DOI
- Kerstjens HA, Engel M, Dahl R, et al. Tiotropium in asthma poorly controlled with standard combination therapy. N Engl J Med. 2012 Sep 2. pmid:22938706 PubMed
- Welsh EJ, Bara A, Barley E, Cates CJ. Caffeine for asthma. Cochrane Database of Systematic Reviews 2010. doi:10.1002/14651858.CD001112.pub2 DOI
- Humbert M, Beasley R, Ayres J, et al. Benefits og omalizumab as add-on therapy in patients with severe pesistent asthma who are inadequately controlled despite best available therapy. Allergy 2005; 60: 309-16. PubMed
- Normansell R, Walker S, Milan SJ, et al. Omalizumab for asthma in adults and children. Cochrane Database Syst Rev 2014; 1: CD003559. pmid:24414989 PubMed
- Norman G, Faria R, Paton F, et al. Omalizumab for the treatment of severe persistent allergic asthma: a systematic review and economic evaluation. Health Technol Assess 2013; 17: 1-342. pmid:24267198 PubMed
- Farne HA, Wilson A, Powell C, Bax L, Milan SJ. Anti-IL5 therapies for asthma. Cochrane Database of Systematic Reviews 2017; Issue 9. Art: No.: CD010834. pmid:10.1002/14651858.CD010834.pub3 Cochrane (DOI)
- Sannarangappa V, Jalleh R . Inhaled Corticosteroids and Secondary Adrenal Insufficiency. The Open Respiratory Medicine Journal 2014; 8: 93-100. doi: 10.2174/1874306401408010093
dxwww.doincbi.orgnlm.nih.gov - Wolf FM, Guevara JP, Grum CM, Clark NM, Cates CJ. Educational interventions for asthma in children (Cochrane review). Cochrane Database Syst Rev 2004;(4):CD000326. dx.doi.org
- Gibson PG, Powell H, Coughlan J, Wilson AJ, Abramson M, Haywood P, et al. Self-management education and regular practitioner review for adults with asthma (Cochrane Review). In: The Cochrane Library, issue 1, 2004. pubmed.ncbi.nlm.nih.gov
- Guevara JP, Wolf FM, Grum CM, Clark NM. Effects of educational interventions for self management of asthma in children and adolescents: systematic review and meta-analysis. BMJ 2003; 326: 1308-9. pubmed.ncbi.nlm.nih.gov
- Reddel HK, Barnes DJ. Pharmacological strategies for self-management of asthma exacerbations. Eur Respir J 2006; 28: 182-99. PubMed
- Gøtzsche PC, Johansen HK. House dust mite control measures for asthma. Cochrane Database of Systematic Reviews 2008, Issue 2. Art. No.: CD001187 Cochrane (DOI)
- Woodcock A, Forster L, Matthews E, et al. Control of exposure to mite allergen and allergen-impermeable bed covers for adults with asthma. N Engl J Med 2003; 349: 225-36. PubMed
- Lehrer PM, Vaschillo E, Vaschillo B, Lu SE, Scardella A, Siddique M, Habib RH. Biofeedback treatment for asthma. Chest. 2004 Aug;126(2):352-61. PubMed PMID:15302717 www.ncbi.nlm.nih.gov
- Freitas DA, Holloway EA, Bruno SS, et al. Breathing exercises for adults with asthma. Cochrane Database Syst Rev. 2013 Oct 1;10:CD001277.
doi: 10pubmed.1002/14651858ncbi.CD001277nlm.pub3nih.DOIgov - Eichenberger PA, Diener SN, Kofmehl R, et al. Effects of exercise training on airway hyperreactivity in asthma: a systematic review and meta-analysis. Sports Med. 2013 ;43(11):1157-70. doi: 10.1007/s40279-013-0077-2. www.ncbi.nlm.nih.gov
- Carson KV, Chandratilleke MG, Picot J, Brinn MP, Esterman AJ, Smith BJ. Physical training for asthma. Cochrane Database Syst Rev. 2013 Sep 30;(9):CD001116. doi: 10.1002/14651858.CD001116.pub4 Review. PubMed PMID: 24085631. www.ncbi.nlm.nih.gov
- DiMango E, Holbrook JT, Simpson E, et al. Effects of asymptomatic proximal and distal gastroesophageal reflux on asthma severity. Am J Respir Crit Care Med 2009; 180: 8090-16. www.ncbi.nlm.nih.gov
- Ahnert J, Löffler S, Müller J, Vogel H. [Systematic literature review on interventions in rehabilitation for children and adolescents with asthma bronchiale]. Rehabilitation (Stuttg). 2010 Jun;49(3):147-59. doi:10.1055/s-0030-1254081. Epub 2010 Jun 8. Review. German. PubMed PMID: 20533145 www.ncbi.nlm.nih.gov
- McCarney RW, Brinkhaus BG, Lasserson TJ, Linde K. Acupuncture for chronic asthma. Cochrane Database of Systematic Reviews 2003; 3: CD000008. Cochrane (DOI)
- Hondras MA, Linde K, Jones AP. Manual therapy for asthma (Cochrane Review). In: The Cochrane Library, Issue 4 2002. Oxford: Update Software. pubmed.ncbi.nlm.nih.gov
- Nelson-Piercy C. Asthma in pregnancy. Thorax 2001;56:325–328 doi: 10.1136/thorax.56.4.325. thorax.bmj.com
- Abramson MJ, Puy RM, Weiner JM. Injection allergen immunotherapy for asthma. Cochrane Database of Systematic Reviews 2010, Issue 8. Art. No.: CD001186. Cochrane (DOI)
- Jacobsen L, Niggemann B, Dreborg S, Ferdousi HA, Halken S, Høst A, Koivikko A, Norberg LA, Valovirta E, Wahn U, Möller C; (The PAT investigator group). Specific immunotherapy has long-term preventive effect of seasonal and perennial asthma: 10-year follow-up on the PAT study. Allergy. 2007 Aug;62(8):943-8. PubMed PMID: 17620073. www.ncbi.nlm.nih.gov
- Möller C, Derborg S, Ferdousi HA, et al. Pollen immunotherapy reduces the development of asthma in children with seasonal rhinoconjunctivitis (the PAT-study). J ALlergy Clin Immunol 2002; 109: 251-6. PubMed
- Gesundheitsberichterstattung des Bundes. Gemeinsam getragen von RKI und Destatis. Diagnosedaten der Krankenhäuser. Jahr 2018 (letzter Zugriff 08.10.2020). www.gbe-bund.de
- Kjellman B, Gustafsson PM. Children with asthma followed up for 21 years; severity improved, but patients seldom grow out of asthma by adulthood. Läkartidningen 2000; 97: 4572-7. www.ncbi.nlm.nih.gov
- Lange P, Çolak Y, Ingebrigtsen TS, Vestbo J, Marott JL. Long term prognosis of asthma, chronic obstructive pulmonary disease, and asthma-chronic obstructive pulmonary disease overlap in the Copenhagen City Heart study: a prospective population-based analysis. Lancet Respir Med. 2016 Jun;4(6):454-62. doi: 10.1016/S2213-2600(16)00098-9 Epub 2016 Apr 6. PubMed PMID: 27061878 www.ncbi.nlm.nih.gov
- Gemeinsamer Bundesausschuss (GBA). DMP-Anforderungen-Richtlinie: Anforderungen an das strukturierte Behandlungsprogramm für Patientinnen und Patienten mit Asthma bronchiale (ab dem vollendeten 1. Lebensjahr). Abgerufen am 08.10.2020. www.g-ba.de
Autor*innen
- Lino Witte, Dr. med., Arzt in Weiterbildung, Innere Medizin, Frankfurt
- Marlies Karsch-Völk, Dr. med., Fachärztin für Allgemeinmedizin, München
- Monika Lenz, Fachärztin für Allgemeinmedizin, Neustadt am Rübenberge
- Jonas Klaus, Arzt, Freiburg im Breisgau
- Die ursprüngliche Version dieses Artikels basiert auf einem entsprechenden Artikel im norwegischen hausärztlichen Online-Handbuch Norsk Elektronisk Legehåndbok (NEL, https://legehandboka.no/).