Prüfungsrelevant für die Facharztprüfung Allgemeinmedizin1
Allgemeine Informationen
Definition
- Langsam fortschreitende Zerstörung der Läppchen- und Gefäßstruktur der Leber mit Ausbildung von portoportalen und portozentralen bindegewebigen Brücken sowie Regeneratknoten
- Funktionelle Folgen der Zirrhose sind die Leberinsuffizienz und die portale Hypertension mit den daraus resultierenden Komplikationen.
Häufigkeit
- Die Inzidenz liegt in Europa und den USA bei ca. 250/100.000/Jahr.
- Männer sind doppelt so häufig betroffen wie Frauen.
- Die alkoholische Lebererkrankung zählt zu den 20 häufigsten Todesursachen der deutschen Allgemeinbevölkerung.2
- In Deutschland ist übermäßiger Alkoholkonsum die häufigste Ursache für eine Leberzirrhose (50–60
Ätiologie und Pathogenese
- Eine Leberzirrhose kann auf dem Boden eines exogen-toxischen, infektiösen, toxisch-allergischen, autoimmunen, vaskulären oder endogen-metabolischen (hereditären) Prozesses entstehen.2
- Fettlebererkrankungen (alkoholisch und nicht-alkoholisch)
- Virushepatiden B, C, D
- Autoimmunerkrankungen (Autoimmunhepatitis, primär biliäre Zirrhose, primär sklerosierende Cholangitis, IgG4-Cholangiopathie)
- chronische Gallenwegserkrankungen (rezidivierende bakterielle Cholangitiden, Gallenwegsstenosen)
- kardiovaskuläre Ursachen (Budd-Chiari-Syndrom, chronische Rechtsherzinsuffizienz, Morbus Osler)
- Speichererkrankungen (Hämochromatose, Morbus Wilson, Alpha-1-Antitrypsinmangel, Mukoviszidose)
- infektiöse Erkrankungen (Echinokokkose, Bilharziose, Syphilis, Brucellose)
- andere seltene Ursachen (Medikamente, Porphyrien)
- Die Fettlebererkrankungen auf dem Boden der „Volkskrankheiten“ Adipositas, Diabetes mellitus und Alkoholabusus bedürfen einer erhöhten Wachsamkeit in der Hausarztpraxis.
Pathophysiologie
- Die Leber spielt eine wichtige Rolle im Stoffwechsel (Verwertung der Nahrungsbestandteile, Glykogenspeicher, Glukoneogenese, Synthese von Galle und Cholesterin), bei der Bildung von Proteinen (Gerinnungsfaktoren, Transportproteine) sowie bei der Metabolisierung körpereigener und -fremder Toxine (z.
- Im Zuge der zunehmenden Fibrose erhöht sich der Druck im Portalkreislauf (portale Hypertension), was zur Ausbildung von portokavalen Anastomosen mit Ausbildung von Ösophagusvarizen, Aszites, Splenomegalie, Thrombozytopenie, Blutungsneigung und hepatischer Enzephalopathie führen kann.
ICPC-2
- D97 Lebererkrankung NNB
ICD-10
- Nach ICD-10-GM Version
202120234- K70 Alkoholische Leberkrankheit
- K70.2 Alkoholische Fibrose und Sklerose der Leber
- K70.3 Alkoholische Leberzirrhose
- K70.4 Alkoholisches Leberversagen
- K71 Toxische Leberkrankheit
- K71.7 Toxische Leberkrankheit mit Fibrose und Zirrhose der Leber
- K72 Leberversagen, anderenorts nicht klassifiziert
- K72.0 Akutes und subakutes Leberversagen
- K72.1 Chronisches Leberversagen
- K72.9 Leberversagen, nicht näher bezeichnet
- K74 Fibrose und Zirrhose der Leber
- K74.0 Leberfibrose
- K74.1 Lebersklerose
- K74.2 Leberfibrose mit Lebersklerose
- K74.3 Primäre biliäre Zirrhose
- K74.4 Sekundäre biliäre Zirrhose
- K74.5 Biliäre Zirrhose, nicht näher bezeichnet
- K74.6 Sonstige und nicht näher bezeichnete Zirrhose der Leber
- K76 Sonstige Krankheiten der Leber
- K76.0 Fettleber [fettige Degeneration], anderenorts nicht klassifiziert
- K76.1 Chronische Stauungsleber
- K76.2 Zentrale hämorrhagische Lebernekrose
- K76.3 Leberinfarkt
- K76.4 Peliosis hepatis
- K76.5 Venöse okklusive Leberkrankheit
- K76.6 Portale Hypertonie
- K76.7 Hepatorenales Syndrom
- K76.8 Sonstige näher bezeichnete Krankheiten der Leber
- K76.9 Leberkrankheit, nicht näher bezeichnet
- K70 Alkoholische Leberkrankheit
Diagnostik
Allgemeines zur Diagnostik
ScreeningmaßnahmenBasisdiagnostikfürzurchronischeErkennung chronischer Lebererkrankungenkönnen einfach und kostengünstig mittels2- Anamnese
, Transaminasenbestimmung, einer - Serum-Transaminasen
- Oberbauch-Sonografie
und - ggf.
einer transiententransiente Elastografiedurchgeführt werden.2
- Anamnese
Anamnese
Allgemeine Anamnese
EineFrühstadiumZirrhose bleibt oft langemeist asymptomatisch, da zum einen die Symptome eher unspezifischer Natur sind und zum anderen die symptomatische Funktionsstörung der Leber erst bei einer Schädigung von ca. 80–90 % des Parenchyms auffällt.DieMöglicheBetroffenen berichtenFrüberhsymptome- Müdigkeit, Abgeschlagenheit
,- Druckgefühl im rechten Oberbauch, Völlegefühl, Meteorismus, Übelkeit
,Gewichtsverlust,Juckreiz. Wichtig sind Fragen nach Menge,Gewichtsverlust- Juckreiz
- Häufigkeit und Dauer
des(NäheresAlkoholkonsumssieheundArtikel ÜbermäßigernachAlkoholkonsum)
- endemisches Risiko,
intravenös verabreichtei. v. Drogen, sexuelle Risikokontakte, Bluttransfusionen, Familienanamnese).
metabolischemmetabolisches Syndrom,chronischem Alkoholabusus,- Zufuhr
andererhepatotoxischer Substanzen inkl. Medikamenteerhöhen das Risiko einer Leberzirrhose. DieChild-Pugh-Kriteriendienen zur einheitlichen Beschreibung und Einteilung der Leberzirrhose nach dem Schweregrad der Symptome in unterschiedliche Stadien.Die Stadienzuteilung erlaubt eine bessere Therapieanpassung und das Erstellen einer zutreffenderen Prognose.Die Kriterien beinhaltenSerumalbumin,Bilirubin,Quick-Wert oderINR,Aszitesund Enzephalopathie.Je nach Punktzahl wird in die Stadien A, B und C eingeteilt.
Da die Mehrzahl allerhepatozellulären Karzinomeauf dem Boden einer Zirrhose entsteht, kommt die Prävention einer Zirrhose einer Prävention des HCC gleich.2
Child-Pugh-Kriterien
- Siehe Tabelle Child-Pugh-Score
. - Scorerechner auf www.mdcalc.com
MELD-Score5
- Steht für Model for Endstage Liver Disease.
- Wird in der Eurotransplant-Region eingesetzt, um die Organzuteilung zu regeln.
- Berechnet die 3-Monats-Mortalität (von 1
- Eine rasch fortschreitende Erkrankung erfordert eine häufige Neuberechnung.
Beinhaltet die ParameterKreatinin(max. 4 mg/dl [353 µmol/l]),BilirubinundINRBerechnungsformel: 10 {0,957 × Loge(Kreatinin in mg/dl) + 0,378 × Loge(Bilirubin in mg/dl) + 1,120 × Loge(INR) + 0,643}- Scorerechner auf www.mdcalc.com
Zeichen einer Dekompensation
- Kachexie, Mangelernährung mit Vitamin- und Spurenelementmangel
- Ikterus und Pruritus als Cholestasefolgen
- Blutungsneigung und hämorrhagische Diathese bei Einschränkung der Synthese von Gerinnungsfaktoren und Thrombozytopenie
- Portokavale Anastomosen mit Caput medusae, Ösophagus- und Fundusvarizen sowie anorektalen Varizen
- Blutung aus gastrointestinalen Varizen
- Aszites
- Splenomegalie
- Foetor hepaticus (süßlich-scharfer Mundgeruch)
- Hepatische Enzephalopathie mit Bewusstseinsstörung, Verwirrtheit und Wesensveränderung bis hin zum Leberkoma durch die Ansammlung hirntoxischer Substanzen bei verringertem Abbau durch die geschädigte Leber
- Durch eingeschränkte Metabolisierung in der Leber:
Erherhöhte Vulnerabilität gegenüber Toxinen, erhöhte Toxizität von Medikamenten
Klinische Untersuchung
- Leberpalpation, Perkussion und Kratzauskultation
- Lebergröße und -konsistenz?
Palmar-Aszites
-
- Dämpfung bei Perkussion der Flanken erst ab ca. 1.500 ml Aszites (für den sonografischen Nachweis reichen bereits ca. 50 ml)
- Inspektion der Haut und
Plantarerythem,Dupuytren-Kontraktur,Schleimhäute- Lacklippen, Lackzunge
, - Mundwinkelrhagaden
, - Kratzeffloreszenzen bei Pruritus
, - Ikterus
; - bei Männern: Rückgang der Körperbehaarung („Bauchglatze“)
,Gynäkomastie AszitesPalmar- und PlantarerythemDämpfung bei Perkussion der FlankenEs müssen sich ca. 1.500 ml Flüssigkeit gebildet haben, damit eine Dämpfung bei der körperlichen Untersuchung nachgewiesen werden kann, für den sonografischen Nachweis reichen bereits ca. 50 ml aus.Hautveränderungen- Spider-Angiome und Spider-Teleangiektasien
sind vaskuläre Veränderungen, die -
- am Rumpf, im Gesicht und an den oberen Extremitäten
auftreten. VaskuläreunspezifischSpider sind nicht spezifisch für die Zirrhose, sie kommen(auch in der Schwangerschaft, bei schwerer Mangelernährung und gelegentlich auch bei gesunden Personenvor.)Zwischen derAnzahl und der Größederkorrelierenvaskulären Spider undmit dem Schweregrad einer chronischen Lebererkrankungbesteht ein Zusammenhang.
- am Rumpf, im Gesicht und an den oberen Extremitäten
- Bei zahlreichen vaskulären Spidern besteht ein erhöhtes Risiko für gastrointestinale Varizenblutungen.
- Lacklippen, Lackzunge
- Dupuytren-Kontraktur
- Gynäkomastie bei Männern
Ergänzende Untersuchungen in der Hausarztpraxis
Die Wahl spezifischerUrsachensuche- Spezifische Untersuchungen
zur Feststellung der Ursache der Zirrhose sollteauf Grundlage der Anamnese,derundklinischenbisherigen Befundesowie der Labor- und der bildgebenden Befunde getroffen werdenauswählen.
- Spezifische Untersuchungen
- Laborparameter
- Blutbild, Gerinnung (Quick, PTT), Elektrolyte (Na, K, ggf. Ca), Transaminasen (GOT, GPT), Cholinesterase, Cholestase
. - ggf. Eiweiß-Elektrophorese
- GPT gilt als der kostengünstigste Screeningparameter zur Identifizierung metabolischer oder medikamenteninduzierter Leberschäden, hat aber genau wie die anderen Leberfunktionstests einen begrenzten prädiktiven Wert im Verhältnis zum Grad der Entzündung, und ist für die Einschätzung des Fibrosegrads ungeeignet.
- Der De-Ritis-Quotient ergibt sich aus dem Verhältnis GOT zu GPT und kann zur groben Einschätzung der Schwere einer Lebererkrankung verwendet werden.6
- Blutbild, Gerinnung (Quick, PTT), Elektrolyte (Na, K, ggf. Ca), Transaminasen (GOT, GPT), Cholinesterase, Cholestase
Ultraschall
DerAdomen-Ultraschallmit Doppler ist eine nichtinvasive, leicht zugängliche Untersuchung, die wertvolle Informationen über den makroskopischen Zustand der Leber und des Blutstroms in den Portal- und Lebervenen gibt.Zirrhosezeichen
Unregelmunregelmäßige, wellige Oberfläche, stumpfer Leberrand, inhomogenes Parenchym, rarefizierte Lebervenen, Zeichen portaler Hypertonie, erhöhte Echogenität und Atrophiesind die sonografischen Kennzeichen einer Zirrhose.
- Leber klein und multinodulär
, - Aszites
kann - Doppler:
nachgewiesen werden, die Doppler-Untersuchung kann einen reduziertenreduzierter Blutstrom in der portalen Zirkulationzeigen.
- Benigne und maligne Knoten sind im Ultraschall nicht zu unterscheiden
sind(weitere Untersuchungen!).
Diagnostik bei Spezialist*innen
- Transiente Elastometrie/Elastografie
Die transiente Elastografie(Fibroscan, Echosense)ist eine nichtinvasive Technik, die auf der sonografischen- sonografische Messung der Leberelastizität
beruht. Je mehr Bindegewebe in der Leber vorhanden ist, desto steifer ist das Gewebe. Je steifer das Gewebe ist, desto schneller ist die gemessene elastische Welle und desto höher ist der ermittelte Wert (angegeben in kPa).- Die Untersuchung erfordert keine Nahrungskarenz der untersuchten Person, ist nicht schmerzhaft und dauert etwa 10
Minutenmin. Kannauch zur Verlaufskontrolleeingesetzt werden.geeignet
- sonografische Messung der Leberelastizität
- Ösophagogastroduodenoskopie
- Varizen des Ösophagus oder Magenfundus? Schweregrad und Blutungsrisiko?
- Stauungsgastritis?
- Ulzera?
- CT und MRT
Aufgrund der guten diagnostischen Eigenschaften des Ultraschalls in der Primärdiagnostik nur begrenzt eingesetzt- Verlaufskontrollen und spezielle Fragestellungen
- Leberbiopsie
Eine Biopsie wird nur durchgeführt,Nur wenn sich daraus Therapieoptionen ableiten lassen, oder wenn die Diagnose unklar bleibt.In der Regel erfolgt die Biopsiemeist transkutan Ultraschall- oder CT-gesteuert.
DifferenzialdiagnosenDie verschiedenen Symptome können auch Zeichen anderer zugrunde liegender Erkrankungen sein.
Indikationen zur Überweisung
Wenn Bedarf für eine erweiterteErweiterte Diagnostik, individuelle Therapieplanung (Gastroenterologie undTherapie sowie stationäre Behandlung besteht.Hepatologie)
ChecklisteIndikationen zur
Überweisung
KrankenhauseinweisungLeberzirrhose und chronische LeberinsuffizienzZweckNotfalleinweisungderbeiÜberweisunglebensbedrohlichen Komplikationen, z. B.:weiterführendeoberebzw. bestätigende Diagnostik und TherapieGastrointestinalblutungEinweisunghepatischeszur stationären AufnahmeKoma beidekompensierterLeberversagen- Sepsis
- hepatorenales
ErkrankungSyndrom.
AnamneseDauer, VerlaufSymptomeWeitere Abklärung und Therapieplanung,Risikofaktorenrelevantez. B.Komorbiditäten,beiregelmäßige MedikamenteTumorverdacht
Klinische UntersuchungAnzeichen einer Lebererkrankung bzw. einer DekompensationErgänzende UntersuchungenUltraschall, transiente Elastometrie/Elastografie, CT, MRTÖsophago-Gastro-Duodenoskopie
Andere Untersuchungenggf. LeberbiopsieEvaluierung einer Lebertransplantation
Therapie
Therapieziele
- Die zugrunde liegende Erkrankung behandeln.
- Progression verzögern oder beenden.
- Komplikationen vorbeugen und sie ggf. behandeln.
- In fortgeschrittenen Stadien Lebensqualität erhalten.
- Notwendigkeit einer Lebertransplantation abklären.
Allgemeines zur Therapie
DieAlleZirrhosepotenziellist in vielen Fällen irreversibel.In frühen Stadien kann jedoch durch eine Therapie der Grunderkrankung eine weitere Progression verhindert und sogar eine Teilregeneration erreicht werden. Dies ist z. B. beiHepatitis BundC,Autoimmunhepatitiden,HämochromatoseundMorbus Wilsonsowie der alkoholbedingten Zirrhose möglich.Weitere Schädigungen vermeiden.Von Zirrhose Betroffene sollten allehepatotoxischen Substanzen vermeiden,die weitere Leberschäden verursachen könnenz. B.:- Alkohol
HierzuMedikamentegehören Alkohol,wie Paracetamol,Medikamente mit hepatotoxischer Wirkung sowieoder bestimmte pflanzliche Arzneimittel.
- Regelmäßige Kontrolluntersuchungen zur Früherkennung und ggf. Behandlung von Komplikationen
- Arzneimittelsicherheit
- Einige Arzneimittel werden bei Leberzirrhose anders verstoffwechselt als bei erhaltener Leberfunktion. Bei der Einschätzung, welche Medikamente ggf. in der Dosierung anzupassen oder ganz zu vermeiden sind, ist die von einer niederländischen Expertengruppe entwickelte und von der Arzneimittelkommission der deutschen Ärzteschaft (AKdÄ) in deutscher Sprache herausgegebene Handreichung Niederländischen Empfehlungen zur sicheren Anwendung von Arzneimitteln bei Leberzirrhose7 hilfreich.
Medikamentöse Therapie
- Es existiert keine kausale medikamentöse Therapie des bindegewebigen Umbaus der Leber.
- Die medikamentöse Therapie
istbeschränkteinesichTherapieauf die Behandlung der Komplikationender(sieheLeberzirrhosedort).3,8Siehe unter den jeweiligen Abschnitten zu den Komplikationen.
Lebertransplantation
- Die Lebertransplantation ist die einzige kausale und etablierte Therapie eines irreversiblen chronischen oder akuten Leberversagens.9-10
Es besteht ein Missverhältnis zwischen der Anzahl der Kandidat*innen für eine Lebertransplantation und der Anzahl der Spender*innen.Das Überleben nach einer Lebertransplantation hat sich seit den ersten Transplantationen dank einer besseren Immunsuppression sowie zunehmender medizinischer und chirurgischer Erfahrung deutlich verbessert.DerMELD-Scorewird in der Eurotransplant-Region eingesetzt, um die Organzuteilung zu regeln.Die Indikation zur Lebertransplantation istIst in allen Fällen einer fortgeschrittenen Lebererkrankung mit irreversibler Schädigung des Leberparenchyms im Sinne einer Zirrhose zu erwägen.109- Weitere etablierte Indikationen:
bestehen beim akutenakutes Leberversagen,bestimmtenbestimmteMalignomen sowieMalignome, genetischbedingtenbedingteStoffwechseldefektenStoffwechseldefekte der Leber.109 - Organzuteilung anhand des MELD-Scores
Komplikationen
Aszites
- Pathologische Ansammlung von Flüssigkeit in der Peritonealhöhle
- Wesentlich für die Differenzialdiagnostik des Aszites ist die diagnostische Punktion.
- Sekundärkomplikationen sind die spontan bakterielle Peritonitis (SBP) und das hepatorenale Syndrom (HRS).
Leitlinie: Therapie des Aszites bei Leberzirrhose11
NichtmedikamentöseAszitespunktionTherapie(abdominelle Parazentese)- Diagnostisch und ggf. therapeutisch
- Sollte ultraschallassistiert erfolgen.
- Soll bei neu aufgetretenem Aszites erfolgen.
- Soll bei allen Patient*innen mit Leberzirrhose und Komplikationen sowie bei nicht elektiver stationärer Aufnahme durchgeführt werden.
Proteinzufuhr
- Patient*innen mit Leberzirrhose und Aszites sollen eine ausreichend eiweißhaltige Ernährung (empfohlene Eiweißzufuhr: 1,2–1,5
Natrium- und Flüssigkeitsrestriktion
- Alle Betroffenen sollen aufgeklärt werden, dass eine zusätzliche Salzzufuhr zu einer Verschlechterung des Krankheitsbildes führen kann.
- Wenn eine diuretische Therapie konsequent durchgeführt wird, ist der Nutzen einer diätetischen Kochsalzrestriktion nicht erwiesen. Bei refraktärem oder schwierig zu behandelndem Aszites ist eine diätetische Kochsalzrestriktion (max. 5
- Bei einem Serum-Natrium >
Medikamentöse Therapie
- Der orale Aldosteronantagonist Spironolacton (initial 100
- Die Kombinationstherapie aus Spironolacton und einem Schleifendiuretikum kann bei ausgeprägtem oder länger bestehendem Aszites auch initial erfolgen.
- Die zusätzliche Gabe von Clonidin und/oder Midodrin kann vor allem bei refraktärem Aszites ein verbessertes Ansprechen bewirken.
- Bei ausgeprägter Hyponatriämie (<
- Die Anwendung von Vaptanen zur Langzeitbehandlung des Aszites ist kontraindiziert. Ferner sollte die Gabe von Prostaglandin-Inhibitoren, ACE-Inhibitoren, Alpha-1-Rezeptor-Blockern und Aminoglykosiden bei einer Leberzirrhose mit Aszites vermieden werden.
- Die Indikation einer nichtselektiven Betablocker-Therapie bei refraktärem Aszites und gleichzeitig bestehenden gastrointestinalen Varizen sollte sorgfältig überprüft werden, insbesondere bei spontan bakterieller Peritonitis. Bei Anzeichen einer zunehmenden Nierenfunktionsstörung, ausgeprägten Hypotonie oder Hyponatriämie sollten Betablocker abgesetzt oder deren Dosis reduziert werden.
Therapierefraktärer und rezidivierender Aszites
- Definitionen
- Als therapierefraktär wird ein Aszites bezeichnet, der nicht auf die medikamentöse Therapie, u.
- Beim intraktablen Aszites bestehen Komplikationen wie hepatische Enzephalopathie, prärenales Nierenversagen oder ausgeprägte Hyponatriämie, die eine adäquate diuretische Therapie verhindern.
- Rezidivierender Aszites ist definiert als Aszites, der trotz Empfehlung zur Natriumrestriktion und Diuretikagabe in adäquater Dosierung mindestens 3-mal in einem Zeitraum von 1 Jahr wieder auftritt.
- Als therapierefraktär wird ein Aszites bezeichnet, der nicht auf die medikamentöse Therapie, u.
- Transjugulärer intrahepatisch portosystemischer Shunt (TIPS)?
- Bei therapierefraktärem oder rezidivierendem Aszites soll immer die Lebertransplantation erwogen werden, und die Anlage eines TIPS bei fehlenden Kontraindikationen wiederholten großvolumigen Parazentesen (Punktion und Drainage) vorgezogen werden.
- Eine TIPS-Anlage zur Aszitestherapie ist in der Regel kontraindiziert bei vorbestehender chronischer hepatischer Enzephalopathie ≥
. Für die TIPS-Anlage sollte prinzipiell ein PTFE-beschichteter Stent (Stentgraft) eingesetzt werden. Eine Empfehlung für die optimale Antikoagulation nach TIPS-Anlage kann bislang nicht ausgesprochen werden.- Die Anpassung der Medikation (v.
- Peritoneo-vesikale Aszitespumpe
Kann: Implantation in einem erfahrenenZentren als Alternative der großvolumigen Parazentese in Erwägung gezogen werden.
ParazenteseAszitespunktion und i. v. Albumin
- Bei Durchführung einer großvolumigen
ParazenteseAszitespunktion (>erfolgen. Die Parazentese sollte ultraschallassistierterfolgen.
- Bei Durchführung einer großvolumigen
Spontan bakterielle Peritonitis (SBP)
- Spontan bakterielle Peritonitis = bakterielle Entzündung der Peritonealhöhle ohne Hinweis auf eine andere intraperitoneale Ursache
- Seltener im ambulanten Bereich als bei hospitalisierten Patient*innen
Leitlinie: Therapie der SBP bei Leberzirrhose11
- Primärprophylaxe
- Bei Vorliegen eines Aszites mit erniedrigtem Gesamteiweißgehalt (<
- Ist eines der beiden Kriterien (1. schwere Leberinsuffizienz, d.
- Bei einer gastrointestinalen Blutung bei Leberzirrhose (mit oder ohne Aszites) soll immer eine antibiotische Primärprophylaxe erfolgen.
- Eine Primärprophylaxe sollte mit Norfloxacin erfolgen und kontinuierlich täglich durchgeführt werden.
- Rifaximin kann als Alternative in begründeten Fällen eingesetzt werden.
- Bei Vorliegen eines Aszites mit erniedrigtem Gesamteiweißgehalt (<
- Behandlung
- Unmittelbar nach Diagnosestellung einer SBP soll eine empirische Antibiotikatherapie eingeleitet werden. Eine ambulant erworbene unkomplizierte SBP soll mittels Cephalosporinen der Gruppe 3a behandelt werden.
- Bei nosokomial erworbener SBP und/oder Vorliegen von Risikofaktoren für ein Therapieversagen (lokale Resistenzlage, antibiotische Vorbehandlung in letzten 12 Wochen) und zusätzlichen individuellen Faktoren (klinischer Schweregrad, MRE-Trägerstatus) kann eine empirische Therapie mit Carbapenemen durchgeführt werden.
- Der Erfolg der Antibiotikatherapie der SBP sollte klinisch sowie mittels diagnostischer Kontrollpunktion des Aszites ca. 48
- Begleitend zur antibiotischen Therapie soll die Gabe von Albumin intravenös am Tag der Diagnosestellung und am 3. Tag nach Diagnosestellung durchgeführt werden.
- Sekundärprophylaxe
- Nach erfolgreicher Therapie einer SBP soll eine Sekundärprophylaxe mittels Norfloxacin 400
- Alternativen zu Norfloxacin in der Sekundärprophylaxe stellen Rifaximin, Trimethoprim / Sulfamethoxazol oder Ciprofloxacin dar.
- Nach durchgemachter SBP sollte die Indikation zur Lebertransplantation geprüft werden.
- Nach erfolgreicher Therapie einer SBP soll eine Sekundärprophylaxe mittels Norfloxacin 400
Hepatische Enzephalopathie (HE)
- Die hepatische Enzephalopathie ist eine potenziell reversible Hirnleistungsstörung.8
- Aufgrund der Leberinsuffizienz kommt es zur Akkumulation neurotoxischer Substanzen, in erster Linie Ammoniak.
- Die klinische Symptomatik ist vielfältig und reicht von geringen neurologischen Veränderungen bis zum Leberkoma.
Leitlinie: Therapie der HE bei Leberzirrhose11
Auslöser
- Einer HE-Episode können eine oder mehrere mögliche auslösende Ursachen zugrunde liegen. Diese sollen bei allen von Leberzirrhose und HE Betroffenen gesucht und spezifisch therapiert werden.
- Infektionen: SBP, Harnwegsinfekt, Pneumonie etc.
- GI-Blutung: Blutung aus Varizen des Ösophagus oder Magenfundus,
Ulkus-BlutungUlkusblutung etc. - Elektrolytentgleisung: Hypokaliämie, Hyponatriämie
- Medikamente: Diuretika, Sedativa (Benzodiazepine), PPI, Regarofinib
- Exsikkose: Diuretika, Parazentese, abführende Maßnahmen, reduzierte Flüssigkeitsaufnahme
- Obstipation
- Operation/Trauma
- Azidose
- Eiweißexzess >
Ernährung
- Die Energiezufuhr bei Leberzirrhose und hepatischer Enzephalopathie sollte 30–35
- Viele Patient*innen mit Leberzirrhose sind mangelernährt.
- Die tägliche Eiweißzufuhr sollte bei 1,2–1,5
- Eine regelhafte Proteinrestriktion soll nicht durchgeführt werden.
- Die Nahrungsaufnahme sollte in häufigeren kleinen Mahlzeiten mit einem abendlichen zusätzlichen Imbiss vor dem Schlafengehen erfolgen. Nüchternphasen über 4–6 Stunden sollten vermieden werden.
- Bei Intoleranz von tierischen Eiweißen sollte auf Milchprodukte, pflanzliche Eiweiße oder selten auf eine Nahrungsergänzung mit verzweigtkettigen Aminosäure-Präparaten umgestellt werden.
- Die vorübergehende Gabe von Multivitamin- oder Zinkpräparaten kann bei HE aufgrund einer Leberzirrhose erfolgen.
Medikamentöse Therapie
- Laktulose
*(Dosierungen nach Fachinformation: einschleichende Dosierung, beginnend mit 3- bis 4-mal tgl. 5–10 g, steigend auf 3- bis 4-mal tgl. 20–30 g) soll als Medikament der 1. Wahl zur Therapie einer HE-Episode eingesetzt werden. - Zusätzlich zur oralen Gabe oder bei nicht möglicher oraler Zufuhr kann Laktulose als Einlauf (300
- In Einzelfällen kann eine Kombinationstherapie mit Rifaximin
*(Dosierungen nach Fachinformation: 2-mal tgl. 550 mg)12- Rifaximin als Monotherapie nur bei Unverträglichkeit von Laktulose
.
- Rifaximin als Monotherapie nur bei Unverträglichkeit von Laktulose
- Die intravenöse Gabe von verzweigtkettigen Aminosäuren (Valin, Leuzin und Isoleuzin) kann zusätzlich oder alternativ in der Akuttherapie der HE eingesetzt werden, wenn diese nicht auf Lactulose allein angesprochen hat.
- Intravenös appliziertes L-Ornithin-L-Aspartat kann zusätzlich oder alternativ bei einer akuten HE-Episode eingesetzt werden, die nicht auf Laktulose angesprochen hat.
- Flumazenil kann bei HE zur Klärung der HE-Auslösung nach möglicher Exposition mit Benzodiazepinen zusätzlich zu einer Standardtherapie eingesetzt werden.
- Bei HE kann in Einzelfällen die Verabreichung von 4
Rezidivprophylaxe
- Bei Zirrhose und durchgemachter HE soll eine Rezidivprophylaxe erfolgen.
- Laktulose
*(Dosierungen nach Fachinformation: einschleichende Dosierung, beginnend mit 3- bis 4-mal tgl. 5–10 g, steigend auf 3- bis 4-mal tgl. 20–30 g) sollte als Medikament zur Sekundärprophylaxe eingesetzt werden. - Rifaximin
*(Dosierungen nach Fachinformation: 2-mal tgl. 550 mg) sollte additiv zur Laktulose in der Sekundärprophylaxe der HE ohne Auslöser eingesetzt werden, wenn unter alleiniger Gabe von Laktulose ein Rezidiv aufgetreten ist. Eine Monotherapie mit Rifaximin sollte nur erfolgen, wenn eine Therapie mit Laktulose nicht möglich ist. - Bei durchgemachter HE-Episode soll auf eine ausreichende Kalorien- und Eiweißzufuhr und einen abendlichen Imbiss geachtet werden.
- Bei Besserung der Leberfunktion oder des Ernährungszustandes nach durchgemachter HE-Episode kann die Sekundärprävention beendet werden.
- Bei Patient*innen mit und ohne Leberzirrhose und therapierefraktärer HE soll nach dominanten portosystemischen Shunts mittels Sonografie, Angio-CT oder MRT gesucht werden.
- Bei Vorliegen einer Leberzirrhose mit therapierefraktärer HE und Nachweis eines großen dominanten portosystemischen Shunts kann die Indikation zu einem interventionellen oder operativen Verschluss gestellt werden.
Therapie der HE nachTIPSDie medikamentöse Therapie einer akuten HE-Episode nach TIPS-Anlage entspricht der bei HE und Leberzirrhose.Bei fehlendem Ansprechen der HE nach TIPS sind Stentreduktionsverfahren und/oder eineLebertransplantationindiziert.Vor einer TIPS-Implantation soll eine gründliche Selektion der Patient*innen erfolgen, da dies die wirksamste Maßnahme zur Prophylaxe einer HE nach TIPS darstellt.Die medikamentöse Primärprävention einer HE nach TIPS-Implantation sollte nicht durchgeführt werden.
Primärprophylaxe bei Leberzirrhose ohne HE
- Eine Primärprophylaxe der HE soll bei Leberzirrhose und oberer gastrointestinaler Blutung durchgeführt werden.
- Bei Leberzirrhose und akuter Ösophagusvarizenblutung sollte Laktulose
*in derPrimärprophylaxe eingesetzt werden.
*(Dosierungen nach FachinformationLaktulose:Laktulose, steigend auf 3- bis 4-maltäglichtgl. 20–30 g) ingder PrimärprophylaxeLaktuloseRifaximin: 2-maleingesetzttglwerden.550 mg RifaximinPfortaderthrombose
- Der gesamte Abschnitt basiert auf diesen Referenzen.8,13
- Im Stadium der kompensierten Zirrhose ist das Vorliegen einer Pfortaderthrombose äußerst selten, auch weil eine Thrombosierung meist zu einer Dekompensation führt.
- Mit zunehmender Schwere der Lebererkrankung steigt die Inzidenz.
- Bei Stenosen <
AntikoagulationGgf. in spezialisiertem Zentrum klären:Bisherige Studien bei Patient*innen mit Pfortaderthrombose und Leberzirrhose ergaben vorläufige Hinweise auf erhöhte Rekanalisierungsraten unter niedrigmolekularen Heparinen.
Dosierungsbeispiel: Enoxaparin 200 IU/kg/d (bei eingeschränkter Nierenfunktion ggf. Dosisanpassung erforderlich!)Für die Langzeittherapie kommen evtl. Vitamin-K-Antagonisten infrage. Allerdings können erkrankungsbedingteINRAntikoagulation-Abweichungen die Einstellung erschweren.Zu den direkten oralen Antikoagulanzien (DOAC) fehlen bislang ausreichende Studien. Sie sind daher für diese Indikation nicht zu empfehlen.
- Transjugulärer intrahepatischer portosystemischer Shunt (TIPS)
: nur in erfahrenen Zentren? - Kontraindikation zur Lebertransplantation
: Eine Pfortaderthrombose erhöht die perioperative Mortalität. Vor dem Eingriff sollte die Pfortader möglichst frei sein.?
Portale Hypertension/Varizenblutung
- Im Verlauf einer chronischen Lebererkrankung ist die Entwicklung einer portalen Hypertension die häufigste und gleichzeitig auch die mit der höchsten Letalität behaftete Störung.
Pathogenese
- Durch den Rückstau des Blutes, das nicht mehr frei durch die Leber fließen kann, kommt es zu einem Anstieg des Druckes in der Pfortader und in den zufließenden venösen Gefäßen.
- Steigt der Druck über ein bestimmtes Maß an, kann es an diesen Gefäßen zu Wandschädigungen und Blutungen kommen.
- Obere Gastrointestinalblutung
Ist eine schwerwiegende Komplikation der Leberzirrhose.3- In mehr als 80
Varizen entstehen auf dem Boden einer zunehmenden portalen Hypertension.Eine Blutung aus Ösophagusvarizen stellt eine lebensbedrohliche Komplikation dar.
Verhinderung Primärprävention der ersten BlutungVarizenblutung3
GabeNichtselektivereines nichtselektiven BetablockersBetablocker zur Senkung des Herzminutenvolumens und direkten Drosselung der Splanchnikusdurchblutung (z.)- ; beides off label
- Endoskopische Therapie von Varizen durch Ligatur oder Sklerosierung
Medikamentöse Akutbehandlung bei Varizenblutung3
EineSofortigefrKrankenhauseinweisung zur Notfallendoskopie- Bei starkem Blutverlust ggf. i. v. Volumenersatz
- Frühe gleichzeitige Behandlung mit vasoaktiven Substanzen
sowieundeine zusätzliche antibiotische Therapie sind Standard.Antibiotika - Vasoaktive Substanzen
- Angewendet werden Medikamente zur Senkung des portalen Druckes, z.
on labelzugelassen). - Einleitend werden 1–2 mg Terlipressindiacetat 5
. Abhängig vom Körpergewicht der behandelten Person kann die Dosis wie folgt angepasst werden:Körpergewicht unter 50 kg: 1 mgKörpergewicht zwischen 50 kg und 70 kg: 1,5 mgKörpergewicht über 70 kg: 2 mgbeihepatorenalem Syndromggf. höhere Dosierung (siehe dort).
Alternativen sind Ocreotid i. v. (on label bei Leberzirrhose), Somatostatin i. v. (off label).Die frühe medikamentöse Behandlung mit vasoaktiven Substanzen soll die Blutung idealerweise schon vor der Endoskopie stoppen. Wird die Diagnose bestätigt, werden die Medikamente für 3–5 Tage weiter gegeben.Terlipressin allein wird angewendet, wenn keine endoskopische Behandlung möglich ist.
- Angewendet werden Medikamente zur Senkung des portalen Druckes, z.
- Antibiotika
- Die frühe Gabe von Antibiotika soll Infektionen verhindern, die die Prognose deutlich verschlechtern.
Eine i. v. begonnene Behandlung kann ggf. nach 2–3 Tagen auf p. o. umgestellt werden. - Folgende Antibioseschemata werden empfohlen:14
- Ciprofloxacin 400
- Ceftriaxon 2
- Norfloxazin 400
- Ciprofloxacin 400
- Die frühe Gabe von Antibiotika soll Infektionen verhindern, die die Prognose deutlich verschlechtern.
- Laktulose
Zurzur Prophylaxe einer hepatischen Enzephalopathie nach Varizenblutungerfolgt die Gabe von Laktulose.- einschleichende Dosierung, beginnend mit 3- bis 4-mal
täglichtgl. 5–10täglichtgl. 20–30
Hepatorenales Syndrom (HRS)
- Das hepatorenale Syndrom ist eine potenziell reversible Nierenfunktionsstörung bei Patient*innen mit Leberzirrhose und Aszites oder mit alkoholischer Steatohepatitis (Fettleber).
- Zwei Formen werden unterschieden:
- HRS Typ I: rasches Nierenversagen, definiert als Verdoppelung des Serumkreatinins auf über 2,5
. - HRS Typ II: moderates Nierenversagen mit Serumkreatinin-Werten zwischen 1,5 und 2,5
bis–226
- HRS Typ I: rasches Nierenversagen, definiert als Verdoppelung des Serumkreatinins auf über 2,5
- Nierenversagen ist die häufigste Manifestation (>
chronischeschronischen Leberversagens. - Bei akuter Dekompensation einer chronischen Lebererkrankung kann Cystatin C im Serum oder Plasma zur Beurteilung der Prognose bestimmt werden.
Leitlinie
Albumingabe
Die intravenösei. v. Albumingabezum Ausschluss eines Volumenmangels bzw. zur Sicherung der Diagnose eines hepatorenalen Syndroms sollte in einer Dosierung- Gabe von
1Vasokonstriktorengwiepro kg Körpergewicht, bis max. 100 g/d über 2 Tage erfolgen.Terlipressin Die Kombinationsbehandlung aus Albumininfusion 20–40 g/d und Vasokonstriktortherapie ist Therapie der 1. Wahl beim hepatorenalen Syndrom.TIPSDieNieren-fortgesetzteundalleinige Albumininfusion soll nicht durchgeführt werden.LeberersatzverfahrenAndere Plasmaexpander können in dieser Indikation aufgrund der unzureichenden Datenlage auch weiterhin nicht empfohlen werden.
Vasokonstriktoren
Sofern keine Kontraindikationen vorliegen, sollen Patient*innen mit einem hepatorenalen Syndrom Typ I mitTerlipressinund Albumin behandelt werden, da dies das kurzfristige Überleben signifikant verbessert.Diese Therapie soll mit einer Terlipressindosis von 2–4 mg/d begonnen werden und über einen Zeitraum von mindestens 3 Tagen durchgeführt werden. Terlipressin soll max. in einer Dosis von 12 mg/d eingesetzt werden.Ein Nutzen dieser Therapie bei HRS Typ II ist bislang nicht klar belegt, deswegen sollten diese Patient*innen analog zu Patient*innen mit refraktärem Aszites behandelt werden.Unter intensivmedizinischem Monitoring kann bei einem hepatorenalen Syndrom auch zunächst versuchsweiseNoradrenalinkontinuierlich infundiert werden.Für andere Vasokonstriktoren ist ein Nutzen beim hepatorenalen Syndrom nicht belegtLebertransplantation.
Wird aus anderer Indikation eine kontinuierliche Noradrenalin-Behandlung durchgeführt, soll keine additive Terlipressingabe erfolgen.
TIPS bei HRS
Die Anlage eines transjugulären intrahepatischen portosystemischen Shunts (TIPS) sollte bei allen Patient*innen mit HRS erwogen werden.
Nieren- und Leberersatzverfahren bei HRS
Da Nierenersatzverfahren allein die Prognose bei HRS nicht verbessern, können sie bei Vorliegen von Dialysekriterien vor allem als Überbrückung bis zur Lebertransplantation eingesetzt werden.Die extrakorporale Albumindialyse hat keinen Einfluss auf Nierenfunktion und Überleben bei HRS. Leberersatzverfahren sollten daher bei HRS nur im Rahmen kontrollierter Studien zum Einsatz kommen.
Lebertransplantation bei HRS
Die Lebertransplantation ist die einzige potenziell kurative Therapie des HRS und soll bei geeigneten Patient*innen angestrebt werden.Auch bei geplanter Lebertransplantation sollten Albumin und Terlipressin verabreicht werden, da Patient*nnen mitNiereninsuffizienzbei Transplantation eine deutlich schlechtere postoperative Prognose haben.Bei Patient*innen mit HRS und einer länger dauernden Dialyseindikation sollte eine kombinierte Leber- und Nierentransplantation erwogen werden.
Hepatozelluläres Karzinom
Zirrhoseprävention ist HCC-Prävention
- Da die Mehrzahl aller hepatozellulären Karzinome (HCC) auf dem Boden einer Zirrhose entsteht, kommt die Prävention einer Zirrhose einer Prävention des HCC gleich.2
Leitlinie:Therapieindikationen Therapieund des-einschränkungen hepatozellulärennach KarzinomsZirrhosegrad15
Resektion
- Chirurgische
beim hepatozellulären Karzinom ohne Leberzirrhose
Therapie
Eine Resektion eines Leberzellkarzinoms ohne Leberzirrhose soll erfolgen, wenn eine komplette Resektion (R0-Resektion) möglich ist.
Resektion beim hepatozellulären Karzinom mit Leberzirrhose
Tumorresektion
- Bei einem singulären Tumor in Leberzirrhose mit funktioneller Resektabilität sollte eine Leberresektion erfolgen. Dies trifft insbesondere
fürauf Tumoren > - Bei multiplen Tumoren in Leberzirrhose innerhalb der Mailand-Kriterien
(solitärer Tumor ≤ 5 cm oder maximal 3 Herde ≤ 3 cm)kann eine Leberresektion durchgeführt werden.
Patient*innen mit einem kurativ behandelbaren Leberzellkarzinom sollten in einem Lebertransplantationszentrum vorgestellt werden.- Geeignete Patient*innen mit Leberzirrhose und irresektabler Tumorerkrankung innerhalb der Mailand-Kriterien (Tumorstadium BCLC A) sollen für eine Lebertransplantation evaluiert werden.
- Auch bei formal resektablen oder grenzwertig resektablen HCC-Befunden in Zirrhose kann innerhalb der
Mailand-Kriterien eine Indikation zur Transplantation bestehen.
Lokoregionäre Therapieverfahren
Perkutane AblationBei Tumoren bis 3 cm sind die Resektion und die Ablation äquivalente Verfahren.Bei Tumoren < 3 cm in für die Resektion ungünstiger Lokalisation oder mit eingeschränkter Leberfunktion sollprimär eine Thermoablation des Tumors angeboten werden.Die perkutane Ablation soll mittels Radiofrequenz-Ablation (RFA) oder Mikrowellen-Ablation (MWA) durchgeführt werden.Bei erhaltener Leberfunktion und gering- oder mäßiggradiger portaler Hypertension soll, bei einemTumor > 3 cm und < 5 cm, vor einer Thermoablation chemoembolisiert werden.
TransarterielleSystemischeChemoembolisation (TACE)TherapieSoll Patient*innen mit Leberzellkarzinom im intermediären Stadium angeboten werden, wenn keine kurativen Therapieoptionen vorliegen.Setzt eine erhaltene Leberfunktion voraus.Sollte mehrfach durchgeführt werden, solange ein Ansprechen hierauf nachweisbar ist und behandelbare hypervaskularisierte Tumoranteile verbleiben.Die Indikation zur Fortführung der TACE soll nach zwei Behandlungszyklen im Tumorboard überprüft werden.
Transarterielle Radioembolisation (TARE)Kann nach Beschluss des Tumorboards bei erhaltener Leberfunktion und intermediärem Stadium der Tumorerkrankung anstelle einer TACE eingesetzt werden.
StereotaxieEine Hochpräzisionsradiotherapie (Stereotactic Body Radiotherapy; SBRT) kann in Betracht gezogen werden, wenn andere lokale Therapieverfahren nicht möglich sind (z. B. hohe Wahrscheinlichkeit für ein Therapieversagen, eingeschränkte Leberfunktion, technische Hindernisse).
Systemische Pharmakotherapie
ErstlinientherapieDie Kombination Atezolizumab und Bevacizumab (A+B) soll angeboten werden beiChild-Pugh-StadiumAB:und BCLC B oder C, Fernmetastasen oder einer Tumorlokalisation, die lokoregionär nicht kontrolliert oder reseziert werden kann (II/A).Bei Kontraindikationen für A+B soll eine Therapie mit einem der beiden Tyrosinkinase-Inhibitoren Lenvatinib oder Sorafenib angeboten werden (II/A).
Nach Versagen, Unverträglichkeit oder bei Kontraindikationen der ErstlinientherapieEine Systemtherapie mit einem zugelassenen Tyrosinkinaseinhibitor soll nach Progress oder bei Unverträglichkeit von A + B angeboten werden bei Patient*innenimChild-Pugh-Stadium A und BCLC B oder Cmit Fernmetastasen odereiner Tumorlokalisation, die lokoregionär nicht kontrolliert oder reseziert werden kann.
Bei Tumorprogress unter einer Therapie mit Sorafenib, Child-Pugh-Stadium A und ECOG 0–1, soll eine weitere Systemtherapie angeboten werden (II/A).Hierfür stehen die beiden Tyrosinkinase-Inhibitoren Regorafenib und Cabozantinib oder bei einem Alpha-Fetoprotein-Wert von ≥ 400 ng/ml der VEGFR2-Antikörper Ramucirumab zur Verfügung.
Bei Child-Pugh-Stadium A und ECOG 0–1 mit Tumorprogress unter einer Therapie mit Lenvatinib soll eine weitere tumorspezifische Therapie angeboten werden.Die laufende Systemtherapie sollte nicht über einen radiologischen Progress hinaus fortgesetzt werden.Die Toxizität der Therapie sollte engmaschig überwacht und berücksichtigt werden.
Bei Leberzirrhose Child-Pugh B/C- Für einzelne Patient*innen im Child-Pugh-Stadium B (bis 8 Punkte), mit Fernmetastasen oder einer Tumorlokalisation, die lokoregionär nicht kontrolliert oder reseziert werden kann und mit einem ECOG-Status von 0–1
- kann eine Systemtherapie mit Sorafenib angeboten werden (II/C).
- kann eine Immuntherapie mit einem
antiAnti-PD-1-Antikörper angeboten werden.
Bei Patient*innen im StadiumChild-Pugh Csollte: keine Systemtherapiedurchgeführt werden.
- Für einzelne Patient*innen im Child-Pugh-Stadium B (bis 8 Punkte), mit Fernmetastasen oder einer Tumorlokalisation, die lokoregionär nicht kontrolliert oder reseziert werden kann und mit einem ECOG-Status von 0–1
Prognose
- Die Zirrhose ist in vielen Fällen irreversibel.
- In frühen Stadien kann jedoch durch eine Therapie der Grunderkrankung eine weitere Progression verhindert und sogar eine Teilregeneration erreicht werden. Dies ist z. B. bei Hepatitis B und C, Autoimmunhepatitiden, Hämochromatose und Morbus Wilson sowie der alkoholbedingten Zirrhose möglich.
- Prognostische Einschätzungen sind
bei Leberzirrhoseschwierig, da die Prognose von einer Reihe unterschiedlicher Faktoren wie Ursache, Schweregrad, Auftreten von Komplikationen und Komorbiditäten abhängt. - Die Mortalität von Patient*innen mit alkoholischen Lebererkrankungen ist deutlich höher als von Patient*innen mit anderen Zirrhoseformen.
- Wenn Patient*innen Komplikationen in Zusammenhang mit der Zirrhose entwickeln, wird davon ausgegangen, dass sie eine dekompensierte Erkrankung haben. Die hohe Morbidität und Mortalität in Zusammenhang mit Zirrhose ist eine Folge der Komplikationen.
Patienteninformationen
Patienteninformationen in Deximed
Illustrationen

Sonografie: Leberzirrhose mit höckeriger Oberfläche, inhomogenem Binnenmuster, Aszites (mit freundlicher Genehmigung von sonographiebilder.de ©Albertinen-Diakoniewerk e. V., Hamburg).
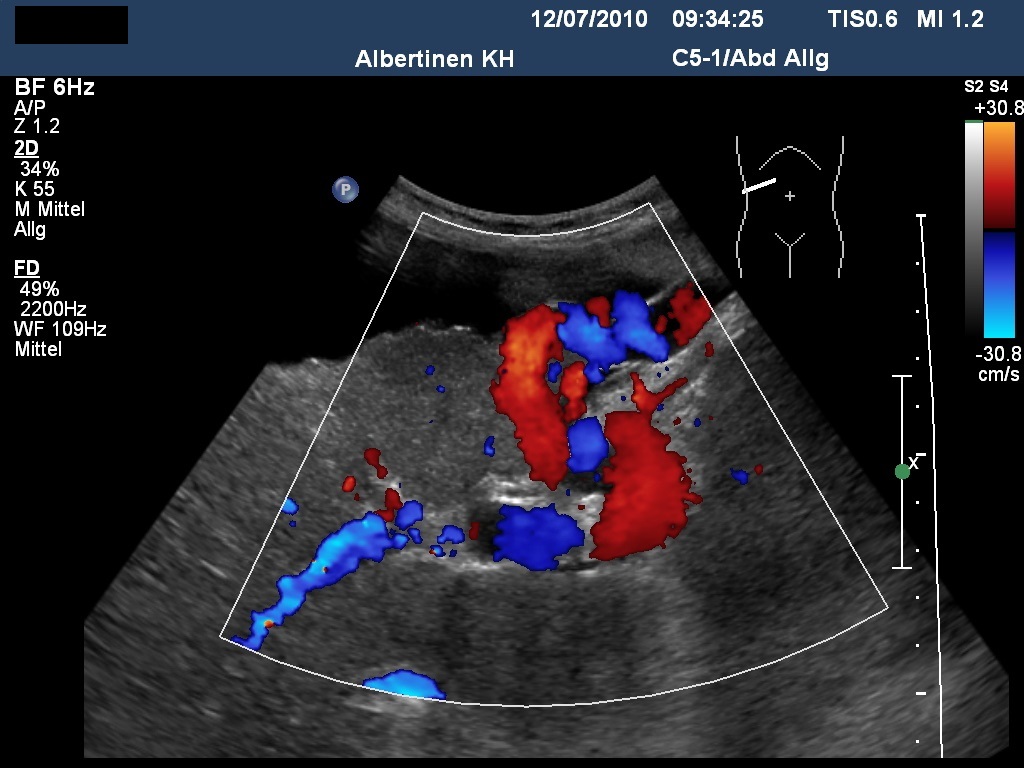
Sonografie: Leberzirrhose mit Umgehungskreisläufen (mit freundlicher Genehmigung von sonographiebilder.de ©Albertinen-Diakoniewerk e. V., Hamburg).

Sonografie: Leberzirrhose mit HCC und Aszites (mit freundlicher Genehmigung von sonographiebilder.de ©Albertinen-Diakoniewerk e. V., Hamburg).
Quellen
Leitlinien
- Deutsche Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten (DGVS). Komplikationen der Leberzirrhose. AWMF-Leitlinie Nr. 021-017. S2k, Stand 2018. www.awmf.org
- Deutsche Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten (DGVS)
, Deutsche Krebsgesellschaft (DKG).S3-LeitlinieDiagnostikHepatozellulund Therapie des hepatozelluläresrenKarzinomKarzinoms und biliärerer Karzinome. AWMF-Leitlinie Nr. 032–053OL.Stand 2021.www.awmf.org Deutsche Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten (DGVS). Gastrointestinale Blutung. AWMF-Leitlinie Nr. 021-028. S2kS3, Stand20172022.
Empfehlungen
- AkdÄ: Niederländische Empfehlungen zur sicheren Anwendung von Arzneimitteln bei Leberzirrhose (Stand 2020)
Literatur
- Lohnstein M, Eras J, Hammerbacher C. Der Prüfungsguide Allgemeinmedizin - Aktualisierte und erweiterte 3. Auflage. Augsburg: Wißner-Verlag, 2018.
- Wiegand J, Berg T
:. The etiology, diagnosis and prevention of liver cirrhosis—part 1 of a series on liver cirrhosis. Dtsch Arztebl Int 2013; 110(6): 85–91. DOI: 0.3238/arztebl.2013.0085 www.aerzteblatt.de - Sauerbruch T, Appenrodt B, Schmitz V, Spengler U
:. Conservative and interventional treatments for liver cirrhosis—part 2 of a series on liver chirrhosis. Dtsch Arztebl Int 2013; 110(8): 126−32. DOI: 10.3238/arztebl.2013.0126 www.aerzteblatt.de - Deutsches Institut für Medizinische Dokumentation und Information (DIMDI)
:. ICD-10-GM Version2021.2023, Stand1816.09.20202022. www.dimdi.de - Kaiser T, Zeuzem S, Thiery J. Lebertransplantationen: Laborwerte - das Zünglein an der Waage . Deutsches Ärzteblatt 2013. www.aerzteblatt.de
- Gressner AM, Gressner OA. De-Ritis-Quotient. In: Gressner
A.M.AM, Arndt T. (Hrsg.):. Lexikon der Medizinischen Laboratoriumsdiagnostik. Springer Reference Medizin. Berlin, Heidelberg: Springer 2019. doi.org - AKdÄ. Drug Safety Mail 2020-06. Niederländische Empfehlungen zur sicheren Anwendung von Arzneimitteln bei Leberzirrhose. 2020 www.akdae.de
- Gerbes A, Gülberg V. Aszites, Pfortaderthrombose und hepatische Enzephalopathie bei Leberzirrhose: Aktuelle Therapieempfehlungen. Viszeralmedizin 2012. core.ac.uk
Manns, Michael P. Liver Cirrhosis, Transplantation and Organ Shortage. Dtsch Arztebl Int 2013; 110(6): 83-4; DOI: 10.3238/arztebl.2013.0083www.aerzteblatt.de- Pascher A, Nebrig M, Neuhaus P
:. Irreversible liver failure: treatment by transplantation. Part 3 of a series on liver chirrhosis. Dtsch Arztebl Int 2013; 110(10): 167–73. DOI: 10.3238/arztebl.2013.0167 www.aerzteblatt.de - Manns, Michael P. Liver Cirrhosis, Transplantation and Organ Shortage. Dtsch Arztebl Int 2013; 110(6): 83-4; DOI: 10.3238/arztebl.2013.0083 www.aerzteblatt.de
- Deutsche Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten e.V. (DGVS). Komplikationen der Leberzirrhose. AWMF-Leitlinie Nr. 021 - 017. S2k. Stand 2018. www.awmf.org
- Rifaximin (Xifaxan) zur Prophylaxe der Hepatischen Enzephalopathie. a-t 2013; 44: 49-51. www.arznei-telegramm.de
- Senzolo M, Garcia-Tsao G, García-Pagán JC. Current knowledge and management of portal vein thrombosis in cirrhosis. J Hepatol 2021; 75: 442-53. pubmed.ncbi.nlm.nih.gov
- Deutsche Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten (DGVS). Gastrointestinale Blutung. AWMF-Leitlinie Nr. 021-028. S2k, Stand 2017 (abgelaufen). www.awmf.org
- Deutsche Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten
,Deutsche Krebsgesellschaft(DGVS). S3-LeitlinieHepatozellulDiagnostik und Therapie des hepatozelluläresrenKarzinomKarzinoms und biliärerer Karzinome. AWMF-Leitlinie Nr. 032–053OL. Stand20212022. www.awmf.org
Autor*innen
- Thomas M. Heim, Dr. med., Wissenschaftsjournalist, Freiburg
Caroline Beier, Dr. med., Fachärztin für Allgemeinmedizin, Hamburg- Die ursprüngliche Version dieses Artikels basiert auf einem entsprechenden Artikel im norwegischen hausärztlichen Online-Handbuch Norsk Elektronisk Legehåndbok (NEL, https://legehandboka.no/).