Allgemeine Informationen
- Sofern nicht anders gekennzeichnet basiert der gesamte Abschnitt auf diesen Referenzen.1-4
Definition
BeimDas Leberzellkarzinom oder hepatozellulärenre Karzinomhandelt(HCC)es sich um ein primäres Leberkarzinom, dashat seinen Ursprung in den Leberzellenhat und sich in der Regel aus einer bestehendenLeberzirrhose(ausgelöst z. B. durch Virushepatitiden) entwickelt.DieMeistUrsachen können jedoch nach geografischer Lage variieren.Häufig wird die Diagnose erst spät gestellt. Da es sich beim hepatozellulären Karzinom (HCC) um einen invasiven Tumor handelt, ist die Prognose häufig schlecht.Engmaschige Kontrollen bei Patient*innen mitHepatitis Cund/oder Leberzirrhose haben zu einer Verbesserunggeht derFrüherkennungErkrankunggeführteine chronische Leberschädigung voraus.
Häufigkeit
- Weltweit5-6
- Das HCC ist weltweit das fünfthäufigste Karzinom und verursacht mehr als 800.000 Todesfälle pro Jahr,
vordieallemmeisten davon in Asien und Afrika. Pro Jahr werden über 800> 900.000neueNeuerkrankungenFälleprodiagnostiziertJahr- altersstandardisierte Inzidenz: > 9/100.
Die altersgruppenrelevante000 - steigende Inzidenz
beträgt 5,5–14,9 Fälle pro 100.000 Einw. und Jahr. Inin Europa und den USAist eine steigende Inzidenz zu beobachten.- In den letzten Jahrzehnten nahm die Leberkarzinom-assoziierte Mortalität in einigen europäischen Ländern zu.
- z.
- In anderen europäischen Ländern ist die krankheitsassoziierte Mortalität rückläufig, z.
- z.
- In Europa stellt die Erkrankung die häufigste Todesursache unter Patient*innen mit Leberzirrhose dar.
- Das HCC ist weltweit das fünfthäufigste Karzinom und verursacht mehr als 800.000 Todesfälle pro Jahr,
- Deutschland – Inzidenz im Jahr
201720197 - Frauen: 3,6/100.000
- Männer: 9,
48/100.000 - In tropischen Regionen bis zu 1/1.000
AlterIn Ländern mit niedrigem ökonomischen Standard erkranken vor allem jüngere Menschen (Hepatitis B).In den Industrieländern sind vor allem Personen über 50 Jahre betroffen (Hepatitis C).
Ätiologie und Pathogenese
- Multifaktorielle
UrsachenGenese - In 80 % der Fälle entwickelt sich das hepatozelluläre Karzinom aus einer zirrhotischen Leber.
- Das Risiko ist bei einer Zirrhose 50-fach erhöht und besonders ausgeprägt bei chronischer Infektion mit Hepatitis B und C, Hämochromatose sowie Alpha-1-Antitrypsin-Mangel.
- zunehmend auch infolge nicht-alkoholischer Fettleber und Steatohepatitis (betroffen sind Personen mit Adipositas, Typ-2-Diabetes, Dyslipidämie und Hypertonie)
- Alkohol
- Wenn die Zirrhose durch Alkohol verursacht ist, erhöht der Konsum auch das Risiko eines hepatozellulären Karzinoms.
- Ein Leberkarzinom kann sich aber wahrscheinlich auch ohne Vorliegen einer Leberzirrhose entwickeln, wenn Patient*innen Aflatoxinen ausgesetzt waren (die mit Mutationen des p53-Gens in Verbindung gebracht werden), chronisch mit dem Hepatitis-B- und Hepatitis-C-Virus infiziert sind oder eine Hämochromatose aufweisen
.
Chronische Virusinfektion
Häufig entwickelt sich das hepatozelluläre Karzinom aus einer chronischen Virusinfektion mit Ausbildung einerZirrhose.Hepatitis BIn Ländern mit niedrigem ökonomischem Standard tritt die Erkrankung vor allem bei jüngeren Personen mit Hepatitis B auf.Weltweit sind 380 Mio. Menschen mit Hepatitis B infiziert.Im Vergleich zu Personen, die nicht mit dem Hepatitis-B-Virus infiziert sind, haben Träger*innen des Virus ein relatives Risiko von 100, wobei das Risiko niedriger liegt, wenn die Ansteckung erst im Erwachsenenalter erfolgt ist.Patient*innen mit Zirrhose haben ein noch höheres Risiko (Inzidenz pro Jahr: 2,0–6,6 %), wohingegen die Inzidenz unter Personen ohne Zirrhose lediglich 0,4 % beträgt.Hepatitis CIn Industrieländern tritt die Erkrankung häufig bei älteren Personen mit einer Zirrhose durch Hepatitis C auf.Weltweit sind 170 Mio. Menschen mit Hepatitis C infiziert.
Prädisponierende Faktoren
Hauptrisikofaktoren
- Die Erkrankung gehört zu den wenigen Karzinomen mit klar definierten Hauptrisikofaktoren. Dazu zählen:
DerLeberzirrhosewichtigste prädisponierende(der Faktor,istfürdasdenVorliegeneineinerZirrhose.Nichtzirrhotische Patient*innenZusammenhang mitfortgeschrittenereinemLeberfibroseerhöhten(F3HCC-Risiko am besten belegt ist)AsienchronischeundInfektionAfrikamit Hepatitis-B-Virus (HBV)- fortgeschrittene Leberfibrose infolge einer chronischen Infektion mit Hepatitis-C-Virus oder einer nichtalkoholischen Steatohepatitis
- seltenere Erkrankungen wie:
DaakuteHepatitisintermittierendeBPorphyrie (AIP)- Glykogenspeicherkrankheit
- Morbus
eineGaucher - Tyrosinämie
verbreiteteTypErkrankung ist, ist das Ansteckungsrisiko um das Dreifache erhöht. Weiterer Risikofaktor: Nahrungsmittel, die aufgrund hygienischer Missstände Aflatoxin enthaltenI.
Westliche Länder und JapanNebenübermäßigem AlkoholkonsumundHämochromatoseistHepatitis Cder wichtigste Risikofaktor für die Entstehung einerLeberzirrhose.
- Zur Ermittlung des Leberkarzinomrisikos bei Patient*innen mit chronischer HBV-Infektion ohne Leberzirrhose
- Domänen
PlPlättchen (Thrombozyten)- ≥
- 100.000–199.999/µl = 1
- <
llµl = 2
- ≥
AlterAlter- 16–29 = 0
- 30–39 = 2
- 40–49 = 4
- 50–59 = 6
- 60–69 = 8
- ≥
GenderGeschlecht- m = 6
- w = 0
- Risikostrata nach Gesamtscorewert
- ≤
- 10–17 = intermediäres Risiko (3
≥18 = hohes Risiko (17
- ≤
- Das Barcelona-Clinic-Liver-Cancer-Stagingsystem (BCLC-System) wurde mehrfach klinisch validiert und wird für die Prognose und Therapieplanung empfohlen.
- Sehr frühes Stadium (0)
- solitärer Tumor <
- erhaltene Leberfunktion
- ECOG-Performance-Status 0 (keine Beeinträchtigung)
- solitärer Tumor <
- Frühes Stadium (A)
- bis zu 3 Tumoren <
- erhaltene Leberfunktion
- ECOG-Performance-Status 0 (keine Beeinträchtigung)
- bis zu 3 Tumoren <
- Intermediäres Stadium (B)
- multinodulär
- nicht resezierbar
- erhaltene Leberfunktion
- ECOG-Performance-Status 0 (keine Beeinträchtigung)
- Fortgeschrittenes Stadium (C)
- portale Invasion
- extrahepatische Ausbreitung
- erhaltene Leberfunktion
- ECOG-Performance-Status 1–2
- Endstadium (D)
- terminales Leberversagen
- ECOG-Performance-Status 1–2
- D77 Bösartige Neubild. Verdauungstrakt
- Nach ICD-10-GM Version
202120239- C22.- Bösartige Neubildung der Leber und der intrahepatischen Gallengänge
- C22.0 Leberzellkarzinom
- C22.- Bösartige Neubildung der Leber und der intrahepatischen Gallengänge
- Häufig wird das Leberzellkarzinom bei Routineuntersuchungen oder aufgrund von Symptomen, die infolge seiner Größe und Lokalisation entstehen, entdeckt.
- Bei allen Personen mit hohem Risiko, z.
- Die Bestimmung bestimmter Marker im Serum ist unzureichend evaluiert. Eine allgemeine Empfehlung ist derzeit nicht möglich.
- Leberadenom
- Fokal-noduläre und noduläre regenerative Hyperplasie der Leber
- Hämangiom
- Zystenleber
- Lebermetastase
- Die Patient*innen zeigen in der Regel Symptome der zugrunde liegenden chronischen Lebererkrankung.
- Typisch sind Schmerzen unter dem rechten Rippenbogen, Appetitlosigkeit, Gewichtsabnahme und erhöhte Temperatur.
- Verdacht auf die Diagnose besteht insbesondere, wenn sich der Zustand von Patient*innen mit Zirrhose rasch und unerwartet verschlechtert.
- Mögliche Zeichen der Grunderkrankung (Zirrhose/Leberversagen): Splenomegalie, Aszites, Ikterus, Spidernävi, Gynäkomastie.
- Aufgrund der Zirrhose ist die Leber unter dem Rippenbogen ggf. unregelmäßig tastbar.
- Der eigentliche Tumor ist nur selten tastbar.
- In Verbindung mit dem hepatozellulären Karzinom wurden verschiedene kutane Manifestationen beschrieben, die aber nicht spezifisch für die Diagnose sind.
- Die Laborbefunde sind unspezifisch.
Es werden die gleichenBlutuntersuchungen wie zurFeststellungDiagnostik der Zirrhosevorgenommen.
- GPT (ALAT), AP, Gamma-GT, Bilirubin, INR erhöht; CHE, Albumin, Thrombozyten niedrig
- Bei 2/3 der Patient*innen ist der AFP-Wert (Alpha-1-Fetoprotein) erhöht. Die Serumwerte lassen keine zuverlässigen Schlussfolgerungen in Bezug auf Tumorgröße, Stadium oder Prognose zu. Die Werte können auch bei einer chronischen Erkrankung der Leber ohne Vorliegen des hepatozellulären Karzinoms erhöht sein.
- Hämoglobin
- Der Wert ist unauffällig oder erhöht, weil der Tumor Erythropoietin absondert.
- Hepatitis-Serologie
- Hepatitis-B-Ag, Hepatitis-C-Antikörper
- Paraneoplastisches Syndrom
- Manche Patient*innen mit hepatozellulärem Karzinom entwickeln ein paraneoplastisches Syndrom, das sich in Hypoglykämie, Polyglobulie, Hyperkalzämie und starker, wässriger Diarrhö äußern kann.
- Farbduplex- und Kontrastmittelsonografie: Feststellung der Hypervaskularisation
- MRT mit Kontrastmittel
- bei Patient*innen mit Leberzirrhose: Unterscheidung von Personen mit und ohne Leberzellkarzinom mit einer Genauigkeit von über 80 %
11 - Bei unklarem MRT-Befund oder bei Kontraindikationen für das MRT: triphasisches CT und/oder kontrastverstärkte Sonografie (Contrast-Enhanced Ultrasound, CEUS)
- bei Patient*innen mit Leberzirrhose: Unterscheidung von Personen mit und ohne Leberzellkarzinom mit einer Genauigkeit von über 80 %
- Staging: kontrastverstärktes CT des Thorax und des Abdomens
- Perkutane Biopsie
InNurdeninmeistenbesonderenFällenklinischenkannSituationendieerforderlich,Diagnose bereits aufgrund der Bildgebung erfolgenz.Die pathohistologische Untersuchung erfolgt dann aus dem ResektatB.Besondersbei Patient*innen ohne Leberzirrhoseist die Verlässlichkeit der Bildgebung in der Erkennung eines Leberzellkarzinoms jedoch begrenzt.Besondersoder beiHochrisikopatient*innenhohemsollte eine Biopsie in Erwägung gezogen werden, wenn die Läsion nicht das typische hypervaskularisierte Muster zeigt und größer als 1 cm istHCC-Risiko.10- Das Risiko für eine
VerschleppungTumorzellverschleppungvon Tumorzellen wird als soist geringeingeschätzt, dass es kein Grund ist, von einer notwendigen diagnostischen Biopsie abzusehen.
- Bei
VerdachtTumorverdachtaufzurRaumforderungenweiteren Abklärung, Staging und Therapieplanung - Bei kurativ behandelbarem HCC: Vorstellung in
dereinemLeber, festgestellt z. B. in der SonografieLebertransplantationszentrum - Je nach Stadium und Histologie des Karzinoms kurative oder palliative Therapie11-12
-13 - Wenn eine Zirrhose oder große bzw. multifokale Tumoren vorliegen, ist es in der Regel wenig erfolgversprechend, die Tumoren oder Teile des Lebergewebes chirurgisch zu entfernen.
InDanndiesen Fällen stelltist eine Lebertransplantation diealleinigeeinzige kurative Optiondar.1413
- Kurative Therapie
- Resektion, Lebertransplantation, Tumorablation
- Wahl der Therapie nach BCLC-Stadium
- Stadium 0: Ablation oder Resektion
- Stadium A:
Jeje nach Tumorlage und -ausbreitung Ablation, Resektion oder Transplantation - Stadium B: Chemo- oder Radioembolisation, ggf. Sterotaxie
- Stadium C: systemische Therapie mit molekular zielgerichteten Substanzen
- Stadium D: supportive/palliative Therapie
.
- Weitere Therapieoptionen
- ablative
sind Tumorablation undVerfahren, transarterielle Chemoembolisation (TACE),sowieevtl. in Kombination - bei fortgeschrittener Erkrankung
dieorale Therapie mit Sorafenib oder Lenvatinib (molekular zielgerichtete Therapie). - Andere molekular zielgerichtete Substanzen kommen als Zweitlinientherapie infrage.
Die Wirksamkeit einer Bestrahlung ist – mit Ausnahme der Stereotaxie – nicht belegt. Dasselbe gilt für die systemische Anwendung von Zytostatika. Daher werden diese Therapieformen nicht empfohlen.
- ablative
- Kommt bei lokalisierten, scharf abgegrenzten und nichtmetastasierenden Tumoren infrage, was aber nur für rund 1/4 aller Fälle gilt. Bei gleichzeitig vorliegender Zirrhose ist außerdem die postoperative Letalität sehr viel höher.
- Patient*innen mit Leberzellkarzinom, die die folgenden Kriterien erfüllen, haben nach Lebertransplantation eine 5-Jahres-Überlebensrate über 70
- Mailand-Kriterien
- solitärer Tumor ≤
- solitärer Tumor ≤
- Up-to-7-Kriterien
- solitärer Tumor ≤
- Summe aus Durchmesser des größten Tumors (cm)
+ Anzahl der Tumorknoten ≤
- solitärer Tumor ≤
- UCSF(University of California San Francisco)-Kriterien
- solitärer Tumor <
- weniger als 3 Herde, größter Durchmesser <
- maximale Summe aller Tumordurchmesser <
- solitärer Tumor <
- Mailand-Kriterien
- Indikation
- Kommt aufgrund der begrenzten Verfügbarkeit von Spenderlebern nur für einen kleinen Teil der an einem Leberzellkarzinom Erkrankten infrage.
1413 Bei einem kurativ behandelbaren Leberzellkarzinom sollte die betroffene Person in einem Lebertransplantationszentrum vorgestellt werden.Personen mitLeberzirrhoseund einem irresektablen Leberzellkarzinom innerhalb der Mailandkriterien (Stadium BCLC A) sollen für eine Lebertransplantation evaluiert werden.Auch bei geeigneten Personen mit einem Leberzellkarzinom außerhalb der Mailand-Kriterien und innerhalb der UCSF-Kriterien kann eine Lebertransplantation erfolgen, insbesondere dann, wenn ein Downstaging bis innerhalb der Mailand-Kriterien gelingt.Das Downstaging kann transarteriell, ablativ oder resektiv erfolgen.
- Kommt aufgrund der begrenzten Verfügbarkeit von Spenderlebern nur für einen kleinen Teil der an einem Leberzellkarzinom Erkrankten infrage.
- Zerstörung der neoplastischen Zellen mithilfe chemischer Substanzen
wie Alkohol oder Essigsäure oder, hyper-bzw.oder hypothermischer Verfahrenwie Strahlen oder Mikrowellen - Radiofrequenz-Ablation (RFA) oder Mikrowellen-Ablation (MWA)
- Bei Tumoren ≤
- Therapie der Wahl bei:
- Tumoren <
- Tumoren <
Bei erhaltener Leberfunktion und gering- bis mäßiggradiger portaler Hypertension soll, bei einem Tumorherd > 3 cm und < 5 cm, vor einer Thermoablation chemoembolisiert werden.- Bei Leberzellkarzinomen im intermediären Stadium ohne kurative Therapieoptionen
- Erfordert eine erhaltene Leberfunktion.
- Auswahl des geeigneten Verfahrens durch interdisziplinäre Tumorkonferenz
Nach Ansprechen und bei hypervaskularisierten Residuen sollte TACE wiederholt werden. Nach zwei Zyklen: Entscheidung der interdisziplinären Tumorkonferenz über Fortführung.- Wenn andere lokale Therapien nicht durchführbar sind, etwa bei geringer Chance auf ein Ansprechen, eingeschränkter Leberfunktion oder technischen Hindernissen.
- Bei erhaltener Leberfunktion (im Child-Pugh-Stadium A), mit Fernmetastasen und/oder einer Tumorlokalisation, die lokoregionär nicht kontrolliert oder reseziert werden kann, liegen für folgende Therapieregimes Phase-III-Studien mit Wirksamkeitsnachweis vor:
- Kombinationstherapie mit den Antikörpern Atezolizumab gegen PD-L1 und Bevacizumab gegen VEGF
- Tyrosinkinase-Inhibitoren
- Sorafenib und Lenvatinib
- Regorafenib und Cabozantinib nach einer Vortherapie mit Sorafenib
- VEGF-R2 Antikörper Ramucirumab nach Sorafenib und bei Alpha-Fetoprotein ≥
Die Kombination Atezolizumab und Bevacizumab (A + B) soll angeboten werden bei Child-Pugh-Stadium A und BCLC B oder C, Fernmetastasen oder einer Tumorlokalisation, die lokoregionär nicht kontrolliert oder reseziert werden kann (II/A).Bei Kontraindikationen für A+B soll eine Therapie mit einem der beiden Tyrosinkinase-Inhibitoren Lenvatinib oder Sorafenib angeboten werden (II/A).Eine Systemtherapie mit einem zugelassenen Tyrosinkinaseinhibitor soll nach Progress oder bei Unverträglichkeit von A + B angeboten werden bei Patient*innenim Child-Pugh-Stadium A und BCLC B oder Cmit Fernmetastasen odereiner Tumorlokalisation, die lokoregionär nicht kontrolliert oder reseziert werden kann.
Bei Tumorprogress unter einer Therapie mit Sorafenib, Child-Pugh-Stadium A und ECOG 0–1, soll eine weitere Systemtherapie angeboten werden (II/A).Hierfür stehen die beiden Tyrosinkinase-Inhibitoren Regorafenib und Cabozantinib oder bei einem Alpha-Fetoprotein-Wert von ≥ 400 ng/ml der VEGFR2-Antikörper Ramucirumab zur Verfügung.
Bei Child-Pugh-Stadium A und ECOG 0–1 mit Tumorprogress unter einer Therapie mit Lenvatinib soll eine weitere tumorspezifische Therapie angeboten werden.Die laufende Systemtherapie sollte nicht über einen radiologischen Progress hinaus fortgesetzt werden.Die Toxizität der Therapie sollte engmaschig überwacht und berücksichtigt werden.Für einzelne Patient*innen im Child-Pugh-Stadium B (bis 8 Punkte), mit Fernmetastasen oder einer Tumorlokalisation, die lokoregionär nicht kontrolliert oder reseziert werden kann und mit einem ECOG-Status von 0–1kann eine Systemtherapie mit Sorafenib angeboten werden (II/C).kann eine Immuntherapie mit einem anti-PD-1-Antikörper angeboten werden.
Bei Patient*innen im Stadium Child-Pugh C sollte keine Systemtherapie durchgeführt werden.- Schmerzen
- Übelkeit und Erbrechen
- Obstipation
- Maligne gastrointestinale Obstruktion
- Orale Beschwerden
- Mangelernährung und Dehydration
- Dyspnoe
- Depression
- Angst
- Delir
- Impfung
- Länder mit niedrigem ö
konomischenkonomischem Versorgungsstatus: Impfung gegen Hepatitis B – wird aber aus Kostengründen kaum umgesetzt. - Ein Impfstoff gegen Hepatitis C steht nicht zur Verfügung.
- Länder mit niedrigem ö
- Einer Hepatitis-C-Infektion kann mit sorgfältigen Kontrollen von Blutprodukten,
geschVermeidung von ungeschütztem Geschlechtsverkehr und Vorsichtsmaßnahmen beim Gebrauch von intravenösen Drogen vorgebeugt werden. - Der Tumor wächst und metastasiert innerhalb und außerhalb der Leber und infiltriert Gefäßstrukturen.
- Der Zustand der Patient*innen verschlechtert sich rasch; es treten Aszites und
ggfevtl. andere Zeichen einer Leberzirrhose oder eines Leberversagens auf. - Eine seltene histologische Sonderform ist das fibrolamelläre hepatozelluläre Karzinom: Tritt in erster Linie bei jungen Frauen ohne besondere Risikofaktoren auf und nimmt einen länger dauernden Verlauf.
- Aszites
- Ösophagusvarizenblutung
- Leberabszess
- Cholestase
- Häufig führt die Erkrankung innerhalb eines Jahres zum Tod, wobei in den Industrieländern 30–40 % der Fälle früh festgestellt werden, und die Prognose dann deutlich besser ist.
- Große Tumoren, vaskuläre Invasion, schlechter funktionaler Zustand und noduläre Metastasen verschlechtern die Prognose.
- 5-Jahres-Überlebensrate insgesamt: 15
- Die 5-Jahres-Überlebensrate der Patient*innen mit Karzinom im Frühstadium oder lokalisiertem, resektierbarem Tumor liegt über 70
- Bei palliativer Therapie beträgt die Überlebenszeit 6–12 Monate.
- Prognose nach BCLC-Stadium
- Stadium A: 50–70
- Stadium B: (unbehandelt): 50
- Stadium C: 50
- Stadium D: 50
- Stadium A: 50–70
- Leberkrebs (primäres Leberzellkarzinom)
- Leberzirrhose und chronisches Leberversagen
Krebstherapie, MedikamenteWas ist Palliativmedizin?AngstbehandlungÜbelkeit und ErbrechenVerstopfungMundtrockenheitAtembeschwerdenGewichtsverlust bei KrebsDepressionDelir- Deutsche Krebshilfe: Blaue Ratgeber Krebserkrankungen
- Deutsches Krebsforschungszentrum: Schmerzen bei Krebs
- Deutsche Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten
,Deutsche(DGVS).Krebsgesellschaft. S3-LeitlinieDiagnostikHepatozellulund Therapie des hepatozelluläresrenKarzinomKarzinoms und biliärerer Karzinome. AWMF-Leitlinie Nr. 032–053OL. S3, Stand20212022. - Deutsche Krebsgesellschaft. Psychoonkologische Diagnostik, Beratung und Behandlung von erwachsenen Krebspatienten. AWMF-Leitlinie Nr. 032-051OL. S3, Stand 2014 (abgelaufen). www.awmf.org
- Deutsche Gesellschaft für Palliativmedizin. Palliativmedizin für Patienten mit einer nicht heilbaren Krebserkrankung. AWMF-Leitlinie Nr. 128-001OL. S3, Stand 2019. www.awmf.org
- Bundesärztekammer. Bekanntmachungen. Richtlinien zur Organtransplantation gem. § 16 TPG. Richtlinie gemäß § 16 Abs. 1 S. 1 Nrn. 2 u. 5 TPG für die Wartelistenführung und Organvermittlung zur Lebertransplantation. März 2018. www.bundesaerztekammer.de
- Forner A, Llovet JM, Bruix J. Hepatocellular carcinoma. Lancet 2012; 379: 1245. pmid:22353262 PubMed
- Deutsche Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten
,Deutsche Krebsgesellschaft(DGVS). S3-LeitlinieHepatozellulDiagnostik und Therapie des hepatozelluläresrenKarzinomKarzinoms und biliärerer Karzinome. AWMF-Leitlinie Nr. 032–053OL. Stand20212022. www.awmf.org - European Society for Medical Oncology. Hepatocellular Carcinoma: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up, Stand 2018. www.esmo.org
- European Association for the Study of the Liver. EASL Clinical Practice Guidelines. Stand 2018. easl.eu
Jemal A, Bray F, Center MM, et al. Global cancer statistics. CA Cancer J Clin 2011; 61:69.PubMed- Ryerson AB, Eheman CR, Altekruse SF, et al. Annual Report to the Nation on the Status of Cancer, 1975-2012, featuring the increasing incidence of liver cancer. Cancer 2016; 122: 1312. pmid:26959385 PubMed
- Rumgay H, Arnold M, Ferlay J, et al. Global burden of primary liver cancer in 2020 and predictions to 2040. J Hepatol 2022: S0168-8278(22)03022-7. Epub ahead of print. PMID: 36208844 PubMed
- Robert
-Koch-Institut. Zentrum für Krebsregisterdaten. Leberkrebs ICD-10 C22. Stand1330.0409.20212022. www.krebsdaten.de - Papatheodoridis G, Dalekos G, Sypsa V, et al. PAGE-B predicts the risk of developing hepatocellular carcinoma in Caucasians with chronic hepatitis B on 5-year antiviral therapy. J Hepatol. 2016;64(4):800-806. doi:10.1016/j.jhep.2015.11.035 DOI
- Deutsches Institut für Medizinische Dokumentation und Information (DIMDI): ICD-10-GM Version
2021.2023, Stand1816.09.20202022. www.dimdi.de TanHuangPSQDetandalTeng MLP. Hepatocellular carcinoma. BMJ Best Practice.LondonLast2019reviewed: 14 Oct 2022, last updated: 26 Oct 2022. bestpractice.bmj.comYu NC, Chaudhari V, Raman SS, et al. CT and MRI improve detection of hepatocellular carcinoma, compared with ultrasound alone, in patients with cirrhosis. Clin Gastroenterol Hepatol 2011; 9: 161. pmid:20920597PubMed- Deutsche Krebsgesellschaft. Psychoonkologische Diagnostik, Beratung und Behandlung von erwachsenen Krebspatienten. AWMF-Leitlinie Nr. 032-051OL. S3, Stand 2014 (abgelaufen). www.awmf.org
- Deutsche Gesellschaft für Palliativmedizin. Palliativmedizin für Patienten mit einer nicht heilbaren Krebserkrankung. AWMF-Leitlinie Nr. 128-001OL. S3, Stand 2019. www.awmf.org
- Bundesärztekammer. Bekanntmachungen. Richtlinien zur Organtransplantation gem. § 16 TPG. Richtlinie gemäß § 16 Abs. 1 S. 1 Nrn. 2 u. 5 TPG für die Wartelistenführung und Organvermittlung zur Lebertransplantation. März 2018 www.bundesaerztekammer.de
- Thomas M. Heim, Dr. med., Wissenschaftsjournalist, Freiburg
- Die ursprüngliche Version dieses Artikels basiert auf einem entsprechenden Artikel im norwegischen hausärztlichen Online-Handbuch Norsk Elektronisk Legehåndbok (NEL, https://legehandboka.no/).
Risikoassessment bei Hepatitis B mittels PAGE-B-Score8
Stadieneinteilung
BCLC-Stadien
ICPC-2
ICD-10
Diagnostik
Früherkennung
Differenzialdiagnosen
Anamnese
Klinische Untersuchung
Ergänzende Untersuchungen in der Hausarztpraxis
Diagnostik bei Spezialist*innen
Indikationen zur ÜberweisungKrankenhauseinweisung
Therapie
Therapieziele
Allgemeines zur Therapie
Operative Therapie
Leberresektion
Lebertransplantation
Lokoregionäre Verfahren
Perkutane Ablation
Transarterielle Chemoembolisation (TACE) oder Transarterielle Radioembolisation (TARE)
Stereotaxie (Stereotactic Body Radiotherapy – SBRT)
Systemische medikamentöse Therapie
Substanzen mit Wirksamkeitsnachweis
Leitlinie: Medikamentöse Therapie des Leberzellkarzinoms2
Erstlinientherapie
Nach Versagen, Unverträglichkeit oder bei Kontraindikationen der Erstlinientherapie
Bei Leberzirrhose CHILD-Pugh B/C
Supportive und palliative Therapie
Prävention
Verlauf, Komplikationen und Prognose
Verlauf
Komplikationen
Prognose
Patienteninformationen
Patienteninformationen in Deximed
Palliativtherapie bei weit fortgeschrittener Krebserkrankung12-13
Weitere Informationen
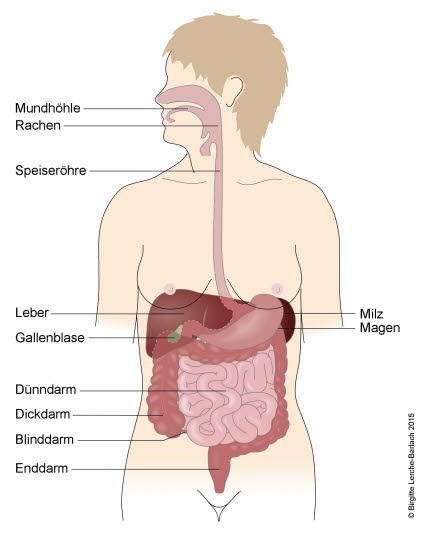
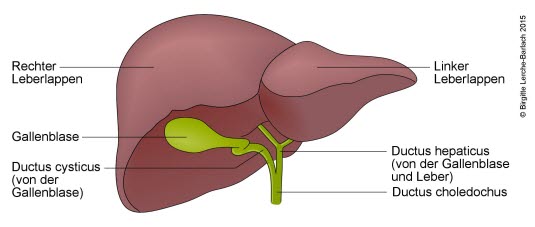
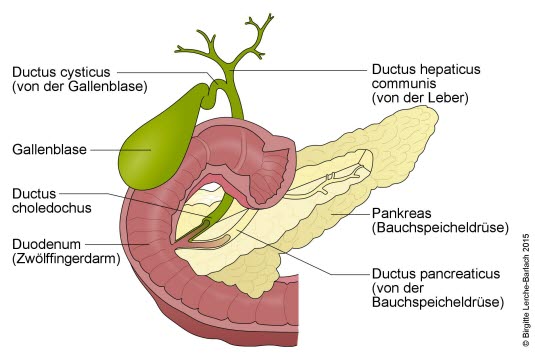
Illustrationen
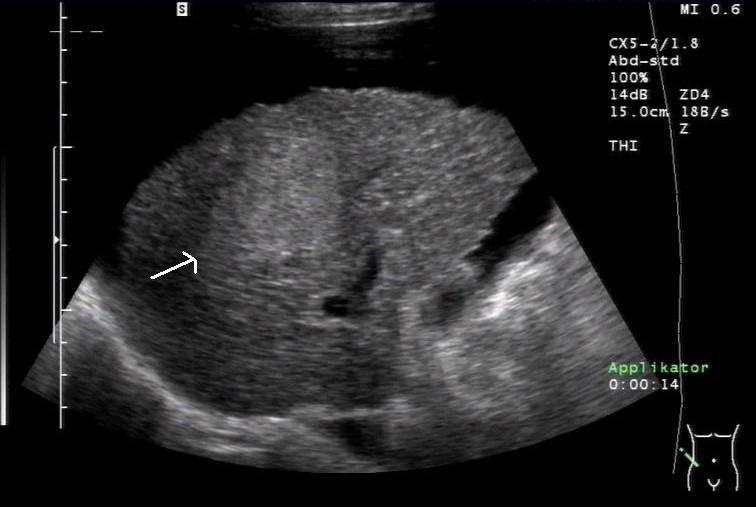
Sonografie: Leberzellkarzinom (HCC), solitär (mit freundlicher Genehmigung von sonographiebilder.de ©Albertinen-Diakoniewerk e. V., Hamburg).
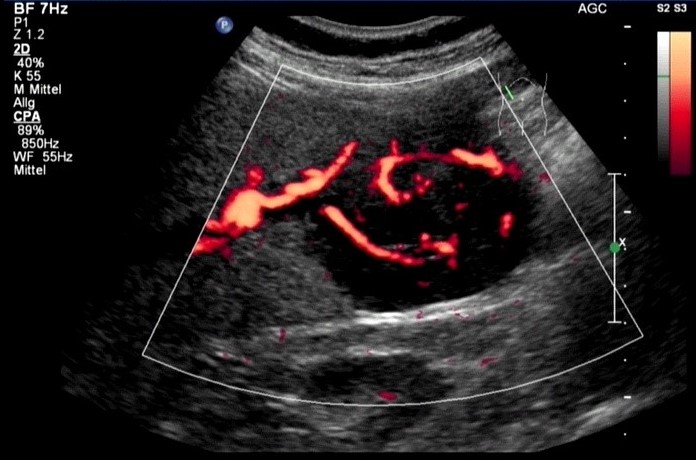
Duplexsonografie: Leberzellkarzinom (HCC), solitär mit Vaskularisation (mit freundlicher Genehmigung von sonographiebilder.de ©Albertinen-Diakoniewerk e. V., Hamburg).