Allgemeine Informationen
Definition
- Alkoholkonsum während der Schwangerschaft wirkt sich schädlich auf das Kind im Mutterleib aus und manifestiert sich bei ihm nach der Geburt auf vielfältige Weise.
- Der Oberbegriff FASD (Fetal Alcohol Spectrum Disorders) oder fetale Alkoholspektrumstörungen umfasst ein Kontinuum, das von leichteren kognitiven und verhaltensbezogenen Schwierigkeiten bis hin zu extremen Ausprägungen reicht, die meist zum vorzeitigen Tod des Fetus oder zu schweren Funktionsstörungen führen.1
- FASD ist selbst keine Diagnose, sondern beschreibt eine Gruppe spezifischer Erkrankungen:
- fetales Alkoholsyndrom – FAS2
- Diese Bezeichnung3 wird für die am schwersten betroffenen Kinder verwendet. Das Syndrom ist gekennzeichnet durch die Trias charakteristische faziale Auffälligkeiten, Wachstumsretardierung und eingeschränkte Entwicklung des ZNS.
- Wenn alle 3 Kriterien zutreffen, muss keine Alkoholexposition während der Schwangerschaft nachgewiesen worden sein, um die Diagnose stellen zu können.
- partielles fetales Alkoholsyndrom – pFAS2
- ZNS-Auffälligkeiten, 2 faziale Auffälligkeiten und bestätigte oder wahrscheinliche intrauterine Alkoholexposition
- neurologische Entwicklungsstörung durch pränatale Alkoholexposition1-2
- engl. Neurodevelopmental Disorder associated with Prenatal Alcohol Exposure (ND-PAE)
-
ZNS-Auffälligkeiten und bestätigte Alkoholexposition während der Schwangerschaft
- fetales Alkoholsyndrom – FAS2
Häufigkeit
Alkoholkonsum während der Schwangerschaft4-5
- Moderater Alkoholkonsum: ca. 20 % der schwangeren Frauen
- Riskanter Alkoholkonsum: ca. 8 % der schwangeren Frauen
- Rauschtrinken (Binge Drinking)
- < 1 pro Monat: 12 % der schwangeren Frauen
- jeden Monat: fast 4 % der schwangeren Frauen
- ≥ 1 pro Woche: 0,1 %
- Vermutlich hohe Dunkelziffer
FAS1
- Das fetale Alkoholsyndrom ist eine der häufigsten bekannten und vermeidbaren Ursachen mentaler Retardierung und mittelgradiger neurokognitiver Entwicklungsstörungen.
- Inzidenz
FASD1
- FASD zählen zu den häufigsten angeborenen Erkrankungen, ohne als solche bislang erkannt und berücksichtigt zu werden.
- Diagnose wird meist vor Ende des 10. Lebensjahres gestellt.
- Deutschland
- In 2014 lag die geschätzte Inzidenz bei 177 von 10.000 Lebendgeburten (95% KI: 135–320).6
- wahrscheinlich hohe Dunkelziffer
- Nach Einschätzung der Leitlinienkommission der Gesellschaft für Neuropädiatrie (GNP) wird die Diagnose FASD viel zu selten gestellt, da die professionellen Helfer*innen im Gesundheitssystem Hemmungen hätten, einen diesbezüglichen Verdacht auszusprechen oder zu wenig über das Krankheitsbild informiert seien.1
- USA
- 240–480 je 10.000 Geburten (2,4–4,8 %)7
Ätiologie und Pathogenese
Toxikokinetik8
- Alkohol kann die Plazentaschranke leicht überwinden, sodass im mütterlichen und kindlichen Blut schnell die gleiche Alkoholkonzentration vorherrscht.
- Da die Alkoholdehydrogenase beim Ungeborenen lediglich 10 % des Aktivitätsniveaus erreicht, das bei Erwachsenen besteht, ist das Kind auf die Leber der Mutter angewiesen, um den Alkohol zu verstoffwechseln.
- Hinzu kommt, dass das Fruchtwasser wie ein Alkoholreservoir wirkt und das Kind dem Alkohol so über längere Zeit ausgesetzt ist, wenn es Fruchtwasser schluckt.
- Schädigungsmechanismus?
- Der Schädigungsmechanismus ist nicht genau geklärt, es wird jedoch angenommen, dass der Alkohol und sein Metabolit Azetaldehyd die fetale Entwicklung stören, indem sie die Differenzierung und das Wachstum der Zellen, die DNA- und Proteinsynthese und die zelluläre Migration hemmen.
- Auch die Auswirkungen des Alkohols auf den Intermediärstoffwechsel von Fetten, Proteinen und Kohlenhydraten scheinen eine Rolle zu spielen.
- Zeitpunkt der Alkoholexposition und dessen Assoziation mit den jeweiligen Schädigungen
- 1. Trimenon: Anomalien des Gesichts und große strukturelle Anomalien, u. a. des Gehirns
- 2. Trimenon: erhöhtes Risiko einer Fehlgeburt
- 3. Trimenon: Beeinträchtigung der Gewichtszunahme, des Längenwachstums und des Wachstums des Gehirns
Alkohol und Hirnschäden1,8
- In welchem Ausmaß das Kind durch eine pränatale Alkoholexposition geschädigt wird, hängt von einer Vielzahl von Faktoren ab:
- Trinkverhalten der Mutter
- Alkoholabbau bei der Mutter
- genetische Vulnerabilität
- Zu welchem Zeitpunkt in der Schwangerschaft die Mutter trinkt.
- Schwankungen der Vulnerabilität des Gehirns im Laufe der Embyonalentwicklung.
- Alkohol wirkt sich auf komplexe Weise auf die Entwicklung des Gehirns aus.
- Bei bestimmten Gruppen von Hirnzellen kann Alkohol vermehrt zum Zelltod durch Apoptose oder Nekrose führen. In anderen Zellen wiederum wirkt er sich direkt auf die Funktion der Zellen aus, indem er erhöhten oxidativen Stress verursacht, die mitochondriale Funktion stört, Wachstumsfaktoren beeinflusst und die Genfunktion der Zellen direkt beeinträchtigt.
- Alkohol hemmt im embryonalen Entwicklungsstadium die Produktion von Retinol (Vitamin A).
- Retinol ist wichtig für die Entwicklung bestimmter Zellen und Organe, u. a. der Neuralleiste, aus der die Knorpel- und Knochenstrukturen des Gesichts gebildet werden. Wird dieser Mechanismus gestört, kann es zu den typischen Auffälligkeiten des Gesichts kommen.
- Neuropathologische Untersuchungen von Kindern mit dem fetalen Alkoholsyndrom haben gezeigt, dass Alkohol sämtliche Entwicklungsstadien des Gehirns beeinträchtigt und ausgeprägte Anomalien hervorrufen kann.
- Eine Exposition im frühen Stadium der Schwangerschaft kann zu einer Mikrozephalie, Migrationsstörungen, Mittellinienanomalien (Corpus-callosum-Agenesie, septo-optische Dysplasie) und Anomalien des Hirnstamms und Kleinhirns führen.
- Durch eine Exposition im letzten Teil der Schwangerschaft kann es zu einer verminderten und anomalen Dendritenentwicklung und einer Hemmung des Myelinisierungsprozesses kommen, was die kognitiven Schwierigkeiten und Verhaltensstörungen erklärt, die viele Kinder aufweisen.
Prädisponierende Faktoren
- Der gesamte Abschnitt basiert auf diesen Referenzen.1,9
- Alkoholkonsum während der Schwangerschaft
- Eine pränatale Alkoholexposition kann grundsätzlich zu alkoholbedingten Schädigungen des Kindes führen.
- Möglicherweise kann bereits ein moderater Alkoholkonsum während der Schwangerschaft beim Kind Störungen der kognitiven Entwicklung verursachen (Näheres zur Definition der Alkoholkonsumklassen siehe Artikel Übermäßiger Alkoholkonsum).
- Es scheint ein direkter Zusammenhang zwischen der Höhe des Alkoholkonsums der Mutter und dem Ausmaß der Schädigung des Kindes zu bestehen.
- Der vereinzelte Konsum großer Mengen Alkohol (Rauschtrinken, Näheres siehe Artikel Übermäßiger Alkoholkonsum) kann vermutlich ebenso schädlich sein wie ein geringer oder mäßiger, dafür aber regelmäßiger Konsum. Das Ungeborene kann in sämtlichen Phasen der Schwangerschaft alkoholbedingte Schädigungen erleiden.10
- Es ist keine gesicherte Untergrenze bekannt, unter der Alkohol keine schädliche Wirkung hat, sodass während der gesamten Schwangerschaft der vollständige Verzicht auf Alkohol empfohlen wird.
- Ist ein vollständiger Verzicht auf Alkohol nicht erreichbar, sollte berücksichtigt werden, dass auch jede Verringerung des Alkoholkonsums das Risiko von Schädigungen des Kindes im Mutterleib senkt.
- Auch der Zeitpunkt des Alkoholkonsums spielt eine Rolle. Das Gesicht wird in der 6.–8. Woche ausgebildet, sodass eine Alkoholexposition in diesem Zeitraum zu fazialen Auffälligkeiten führen kann.
- Eine genetisch bedingte Vulnerabilität des Kindes sowie Vulnerabilitäts- und Schutzfaktoren scheinen zu existieren, über die jedoch wenig bekannt ist.
ICPC-2
- A90 Angeborene Anomalie NNB
ICD-10
- Nach ICD-10-GM Version 202111
- Q86 Angeborene Fehlbildungssyndrome durch bekannte äußere Ursachen, anderenorts nicht klassifiziert
- Q86.0 Alkohol-Embryopathie (mit Dysmorphien)
Diagnostik
Diagnostische Kriterien
- Der gesamte Abschnitt basiert auf diesen Referenzen.1,12
- Die Diagnose fetales Alkoholsyndrom wird bei Vorliegen der typischen fazialen Auffälligkeiten, einer Wachstumsretardierung und einer gestörten Entwicklung des ZNS gestellt.13
- faziale Auffälligkeiten: kurze Lidspalte, flaches Philtrum (Furche zwischen Nase und Oberlippe) und dünne Oberlippe mit schmalem Lippenrot
- prä- und postnatale Wachstumsverzögerung: in der Regel als Körpergröße und/oder -gewicht unter der 10. Perzentile definiert
- Schädigung des ZNS
- Wird mitunter erst deutlich, wenn das Kind das Schulalter erreicht.
Leitlinie: Diagnose eines fetalen Alkoholsyndroms (FAS)1
Diagnostische Säulen
- Zur Diagnose eines FAS bei Kindern und Jugendlichen sollten alle Kriterien 1–4 zutreffen (B):
- Wachstumsauffälligkeiten
- faziale Auffälligkeiten
- ZNS Auffälligkeiten
- bestätigte oder nicht bestätigte intrauterine Alkohol-Exposition.
- Bei Kontakt zum Gesundheits-/Hilfesystem sollten, wenn ein Kind Auffälligkeiten in einer der 4 diagnostischen Säulen zeigt, die 3 anderen diagnostischen Säulen beurteilt oder ihre Beurteilung veranlasst werden.
- Wenn faziale Auffälligkeiten, Wachstumsauffälligkeiten und Mikrozephalie vorhanden sind, ist eine bildgebende Diagnostik zur Diagnose des FAS nicht erforderlich.
- Spezifische Auffälligkeiten, durch Bildgebung ersichtlich, sind bisher bei Kindern mit FAS nicht bekannt.
1. Wachstumsauffälligkeiten
- Zur Erfüllung des Kriteriums „Wachstumsauffälligkeiten“ soll mindestens 1 der folgenden Auffälligkeiten – adaptiert an Gestationsalter, Alter, Geschlecht – dokumentiert zu einem beliebigen Zeitpunkt, zutreffen (A):
- Geburts- oder Körpergewicht ≤ 10. Perzentile
- Geburts- oder Körperlänge ≤ 10. Perzentile
- Body-Mass-Index ≤ 10. Perzentile.
- Da Kinder mit FAS typischerweise Wachstumsauffälligkeiten aufzeigen (IIc), das Messen der Körpermaße ein nichtinvasives Verfahren darstellt und keine Nebenwirkungen auf das Kind hat, sollen das Körpergewicht und die Körperlänge bei Verdacht auf FAS immer erhoben werden (A).
- Die Ergebnisse der vorangegangenen Messungen sollen berücksichtigt und Wachstumskurven angelegt werden.
- Auffälligkeiten des Wachstums reichen als alleiniges diagnostisches Kriterium nicht für die Diagnose FAS aus.
- Es sollte ausgeschlossen werden, dass die Wachstumsstörung allein durch andere Ursachen erklärt werden kann, wie:
- familiärer Kleinwuchs
- konstitutionelle Entwicklungsverzögerung
- pränatale Mangelzustände
- Skelettdysplasien
- hormonelle Störungen
- genetische Syndrome
- chronische Erkrankungen
- Malabsorption
- Mangelernährung
- Vernachlässigung.
2. Faziale Auffälligkeiten
- Zur Erfüllung des Kriteriums „faziale Auffälligkeiten“ sollen alle 3 fazialen Anomalien vorhanden sein (A):
- kurze Lidspalten (≤ 3. Perzentile)
- verstrichenes Philtrum (Rang 4 oder 5 auf dem Lip-Philtrum-Guide12,14)
- schmale Oberlippe (Rang 4 oder 5 auf dem Lip-Philtrum-Guide12,14).
- Da das gemeinsame Auftreten der 3 fazialen Auffälligkeiten typisch für das FAS ist (Ib), diese Auffälligkeiten anhand der Perzentilenkurven für Lidspalten sowie des Lip-Philtrum-
GuideGuides12,14 objektiv messbar sind (Ib−IIb) und das Messen der fazialen Merkmale ein nichtinvasives Verfahren darstellt und somit keine Nebenwirkungen für das Kind hat, sollen die Lidspaltenlänge, das Philtrum und die Oberlippe bei Verdacht auf FAS mithilfe der Perzentilenkurven und des Lip-Philtrum-GuideGuides12,14 beurteilt werden (A). - Auffälligkeiten des Gesichtes reichen als alleiniges diagnostisches Kriterium nicht für die Diagnose FAS aus. Daher soll die Diagnose FAS nicht allein anhand der fazialen Auffälligkeiten gestellt werden.
3. ZNS-Auffälligkeiten
- Zur Erfüllung des Kriteriums „ZNS-Auffälligkeiten“ sollte mindestens 1 der folgenden Auffälligkeiten zutreffen (B):
- funktionelle ZNS-Auffälligkeiten
- strukturelle ZNS-Auffälligkeit (Mikrozephalie).
- Auffälligkeiten des ZNS reichen als alleiniges diagnostisches Kriterium nicht für die Diagnose FAS aus.
Funktionelle ZNS-Auffälligkeiten
- Zur Erfüllung des Kriteriums „funktionelle ZNS-Auffälligkeiten“ sollte mindestens 1 der folgenden Auffälligkeiten zutreffen, die nicht adäquat für das Alter ist und nicht allein durch den familiären Hintergrund oder das soziale Umfeld erklärt werden kann (B):
- globale Intelligenzminderung mindestens 2 Standardabweichungen unterhalb der Norm oder signifikante kombinierte Entwicklungsverzögerung bei Kindern unter 2 Jahren
- Leistung mindestens 2 Standardabweichungen unterhalb der Norm entweder in mindestens 3 der folgenden Bereiche oder in mindestens 2 der folgenden Bereiche in Kombination mit Epilepsie:
- Sprache
- Feinmotorik
- räumlich-visuelle Wahrnehmung oder räumlich-konstruktive Fähigkeiten
- Lern- oder Merkfähigkeit
- exekutive Funktionen
- Rechenfertigkeiten
- Aufmerksamkeit
- soziale Fertigkeiten oder Verhalten.
- Wenn faziale Auffälligkeiten und Wachstumsauffälligkeiten, jedoch keine Mikrozephalie, vorhanden sind, soll eine psychologische Diagnostik zur Diagnose FAS eingesetzt werden.
- Funktionelle ZNS-Auffälligkeiten sollen anhand standardisierter, gut normierter psychologischer Testverfahren und einer psychologischen oder ärztlichen Verhaltenseinschätzung des Kindes für die Diagnose FASD evaluiert werden.
- Bei der psychologischen Diagnostik sollen vor allem die bei Kindern mit FASD typischerweise betroffenen Bereiche beurteilt werden.
- Welche psychologischen Testverfahren eingesetzt werden sollen, kann aufgrund der inkonsistenten Literaturlage nicht abschließend geklärt werden.
Strukturelle ZNS-Auffälligkeit (Mikrozephalie)
- Zur Erfüllung des Kriteriums „strukturelle ZNS-Auffälligkeit“ sollte folgende Auffälligkeit, adaptiert an Gestationsalter, Alter, Geschlecht, dokumentiert zu einem beliebigen Zeitpunkt, zutreffen (B):
- Mikrozephalie (≤ 10. Perzentile/≤ 3. Perzentile)
- Da das Messen des Kopfumfanges ein nichtinvasives Verfahren darstellt und keine Nebenwirkungen für das Kind hat, soll der Kopfumfang bei Verdacht auf FASD immer erhoben werden.
- Die Ergebnisse der vorangegangenen Messungen sollen berücksichtigt und Kopfumfangskurven angelegt werden.
- Es sollte ausgeschlossen werden, dass die Mikrozephalie allein durch andere Ursachen bedingt ist wie:
- familiäre Mikrozephalie
- genetisches Syndrom
- Stoffwechselerkrankung
- pränatale Mangelversorgung
- andere toxische Schädigung
- Infektion
- maternale Erkrankungen
- chronische Erkrankungen des Kindes.
4. Bestätigte oder nicht bestätigte intrauterine Alkohol-Exposition
- Der Alkoholkonsum der leiblichen Mutter während der Schwangerschaft sollte bei der Diagnosestellung eines FAS evaluiert werden.
- Wenn Auffälligkeiten in den 3 übrigen diagnostischen Säulen bestehen, soll die Diagnose eines FAS auch ohne Bestätigung eines mütterlichen Alkoholkonsums während der Schwangerschaft gestellt werden (A).
Leitlinie: Diagnose eines partiellen fetalen Alkoholsyndroms (pFAS)1
- Zur Diagnose eines pFAS bei Kindern und Jugendlichen sollen alle Kriterien 1–3 zutreffen:
- faziale Auffälligkeiten
- ZNS-Auffälligkeiten
- bestätigte oder wahrscheinliche intrauterine Alkohol-Exposition.
1. Faziale Auffälligkeiten
- Zur Erfüllung des Kriteriums „faziale Auffälligkeiten“ sollen mindestens 2 der 3 folgenden Auffälligkeiten, dokumentiert zu einem beliebigen Zeitpunkt, vorhanden sein:
- kurze Lidspalten (≤ 3. Perzentile)
- verstrichenes Philtrum (Rang 4 oder 5 Lip-Philtrum-Guide12)
- schmale Oberlippe (Rang 4 oder 5 Lip-Philtrum-Guide12).
2. ZNS-Auffälligkeiten
- Zur Erfüllung des Kriteriums „ZNS-Auffälligkeiten“ sollen mindestens 3 der folgenden Auffälligkeiten zutreffen, die nicht adäquat für das Alter sind und nicht allein durch den familiären Hintergrund oder das soziale Umfeld erklärt werden können:
- globale Intelligenzminderung (mindestens 2 Standardabweichungen unter der Norm) oder signifikante kombinierte Entwicklungsverzögerung bei Kindern ≤ 2 Jahre
- Epilepsie
- Mikrozephalie ≤ 10. Perzentile
- Leistung mindestens 2 Standardabweichungen unter der Norm in den Bereichen:
- Sprache
- Fein-/Graphomotorik oder grobmotorische Koordination
- räumlich-visuelle Wahrnehmung oder räumlich-konstruktive Fähigkeiten
- Lern- oder Merkfähigkeit
- exekutive Funktionen
- Rechenfertigkeiten
- Aufmerksamkeit
- soziale Fertigkeiten oder Verhalten.
3. Intrauterine Alkoholexposition
- Falls faziale und ZNS-Auffälligkeiten vorhanden sind und laut Fremdanamnese ein bestätigter oder wahrscheinlicher mütterlicher Alkoholkonsum während der Schwangerschaft vorliegt, sollte die Diagnose eines pFAS gestellt werden.
- Personen, die im beruflich-unterstützenden und privaten Umfeld verlässliche Auskunft über den mütterlichen Alkoholkonsum in der Schwangerschaft geben können, sollten im Rahmen der Fremdanamnese befragt werden.
- Dabei sollen rechtliche Rahmenbedingungen für die Informationseinholung und -weitergabe berücksichtigt werden.
- Bei fehlenden Informationen zum mütterlichen Alkoholkonsum in der Schwangerschaft sollte je nach Einzelfall eine fachliche Einschätzung vorgenommen werden, ob sich durch eine fehlende Diagnose FASD das Risiko einer Kindeswohlgefährdung ergibt.
- Ist dies der Fall, darf der Berufsgeheimnisträger dem Jugendamt aufgrund der Befugnis aus § 4 KKG (Gesetz zur Kooperation und Information im Kinderschutz) Informationen weitergeben, ohne gegen seine Schweigepflicht zu verstoßen.
Leitlinie: Diagnose einer alkoholbedingten entwicklungsneurologischen Störung1
- Zur Diagnose einer alkoholbedingten entwicklungsneurologischen Störung (Alcohol-Related Neurodevelopmental Disorder, ARND) bei Kindern und Jugendlichen sollen die Kriterien 1 und 2 zutreffen:
- ZNS-Auffälligkeiten
- bestätigte intrauterine Alkohol-Exposition.
- Wenn ZNS-Auffälligkeiten vorhanden sind (Diagnosekriterien wie beim pFAS, s. o.), soll die Diagnose einer ARND bei bestätigtem mütterlichem Alkoholkonsum während der Schwangerschaft gestellt werden.
Differenzialdiagnosen
- Der gesamte Abschnitt basiert auf dieser Referenz.1
- Bei der Diagnostik der FASD sollen mögliche Differenzialdiagnosen umfassend berücksichtigt werden.
- bei Unsicherheiten: Überweisung an Behandelnde mit FASD-Erfahrung1
- Im Folgenden sind häufige Differenzialdiagnosen aufgeführt.
Pränatale Wachstumsstörungen
- Fetale Pathologie (ungestörte intrauterine Versorgung)
- endogen
- Fehlbildungen
- genetische Syndrome (z. B. Turner-Syndrom, Silver-Russell-Syndrom)
- Stoffwechselerkrankungen
- exogen
- intrauterine Infektionen, z. B. Röteln, Zytomegalie, Toxoplasmose, Herpes simplex, HIV, EBV, Parvovirus B19
- Strahlenexposition
- endogen
- Gestörte intrauterine Versorgung
- präplazentar
- maternale Erkrankungen, z. B. Präeklampsie, Hypotonie, Anämie, zyanotische Vitien, Kollagenosen, chronische Nierenerkrankungen
- toxische Einflüsse, z. B. Nikotin, Drogen
- erhöhte psychosoziale Belastung der Mutter (Stress, Gewalt)
- plazentar
- Placenta praevia
- gestörte Plazentation (Uterusfehlbildung, Myome)
- auf die Plazenta beschränkte Chromosomenstörung
- präplazentar
Postnatale Wachstumsstörungen
- Familiärer Kleinwuchs
- Konstitutionelle Entwicklungsverzögerung
- Skelettdysplasien, z. B.:
- Hypochondroplasie
- Achondroplasie
- Osteogenesis imperfecta.
- Metabolische Störungen
- Renale Erkrankungen
- Hormonelle Störungen
- Genetische Syndrome, z. B. Trisomie 21
- Chronische Erkrankungen
- Malabsorption oder Mangelernährung, z. B.:
- Mangel an
- Vitamin D
- Kalzium
- Proteinen
- generelle Unterernährung.
- Mangel an
- Psychosozialer Kleinwuchs (durch Deprivation bedingter Minderwuchs)
Faziale Auffälligkeiten
- Toxische Effekte in der Schwangerschaft, z. B.:
- Antikonvulsiva (z. B. Valproat, Näheres siehe Artikel Epilepsie)
- Toluol
- maternale Phenylketonurie
- Genetisch bedingte Erkrankungen (siehe auch Artikel Untersuchung des Neugeborenen), z. B.:
- Aarskog-Syndrom
- Cornelia-de-Lange-Syndrom
- Dubowitz-Syndrom
- Noonan-Syndrom
- Williams-Beuren-Syndrom (Mikrodeletion 7q11.23)
- Di-George-Syndrom (VCFS) (Mikrodeletion 22q11)
- Blepharophimosis-Syndrom
- Hallermann-Streiff-Syndrom
- 3-M-Syndrom
- Smith-Lemli-Opitz-Syndrom
- SHORT-Syndrom
- Feingold-Syndrom (Trisomie 9)
- Kabuki-Syndrom
- Peters-Plus-Syndrom
- Rubinstein-Taybi-Syndrom
- Geleophysic dysplasia.
ZNS-Auffälligkeiten
- Funktionell
- kombinierte umschriebene Entwicklungsstörung
- Intelligenzminderung unterschiedlichen Grades
- umschriebene Entwicklungsstörung des Sprechens und der Sprache
- umschriebene Entwicklungsstörung motorischer Funktionen
- umschriebene Entwicklungsstörung schulischer Fertigkeiten
- einfache Aufmerksamkeits- und Aktivitätsstörung
- hyperkinetische Störung des Sozialverhaltens
- Störung des Sozialverhaltens mit oppositionellem aufsässigem Verhalten
- kombinierte Störung des Sozialverhaltens und der Emotionen
- Stereotypien
- Aggressivität
- Delinquenz
- Suchterkrankungen
- reaktive Bindungsstörung des Kindesalters/posttraumatische Belastungsstörung
- sexuelle Verhaltensabweichung
- Schlafstörungen
- Angststörung/Panikstörung
- affektive Störung, z. B. Depression
- Epilepsien anderer Genese
- Mikrozephalie
- familiäre Mikrozephalie
- genetische Syndrome (s. o.)
- pränatale Mangelversorgung, toxische Schädigung, Infektion
- hypoxisch-ischämische Hirnschädigung
- maternale Erkrankungen
- postnatale Mangelernährung
- Stoffwechselstörungen
- chronische Erkrankungen
Anamnese
- Der Verdacht auf das fetale Alkoholsyndrom ergibt sich häufig aufgrund der typischen morphologischen Auffälligkeiten beim Neugeborenen.
- Die fazialen Auffälligkeiten sind im weiteren Entwicklungsverlauf des Kindes häufig immer weniger deutlich zu erkennen, sodass die Diagnosestellung später schwieriger sein kann.
- Hat die Mutter in der Phase vor der Geburt regelmäßig viel Alkohol konsumiert, können beim Neugeborenen eine Hypoglykämie und eine Azidose auftreten.
- In den ersten 72 Stunden nach der Geburt sind möglicherweise neonatale Entzugserscheinungen zu beobachten.
- Agitiertheit
- Hyperaktivität
- starker Tremor
- evtl. Krampfanfälle
- in den folgenden Tagen häufig Apathie
Klinische Untersuchung
- Praktisch alle Organsysteme können durch das fetale Alkoholsyndrom geschädigt werden.
- Vollständig ausgeprägt ist das Syndrom durch eine Kombination von Minderwuchs, neurologischen und kognitiven Defiziten sowie 3 kardinalen Auffälligkeiten der Gesichtszüge gekennzeichnet.
Kraniofaziale Auffälligkeiten1
- Typische faziale Auffälligkeiten sind Voraussetzung für die Stellung der Diagnosen FAS und pFAS:
- dünne Oberlippe
- kurze Lidspalte
- glattes Philtrum (Furche zwischen Nase und Oberlippe).
- Zudem können weitere morphologische Auffälligkeiten und leichte Fehlbildungen vorliegen, die jedoch nicht Teil der diagnostischen Kriterien sind:
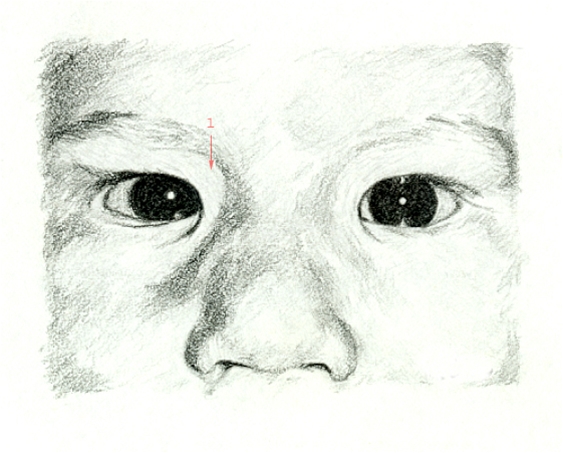 Epikanthus beim Blick nach vorn
Epikanthus beim Blick nach vorn- Epikanthus
- leichtere Ohrmuschelfehlbildungen
- Oberer Bogen des Außenohres unterentwickelt, umgestülpt oder parallel zum darunter liegenden Bogen verlaufend, sodass das Ohr einem Eisenbahngleis ähnelt („Railroad Track Ears“).
- unzureichend entwickelte Conchae und nach hinten rotierte Ohren, Mikrotie
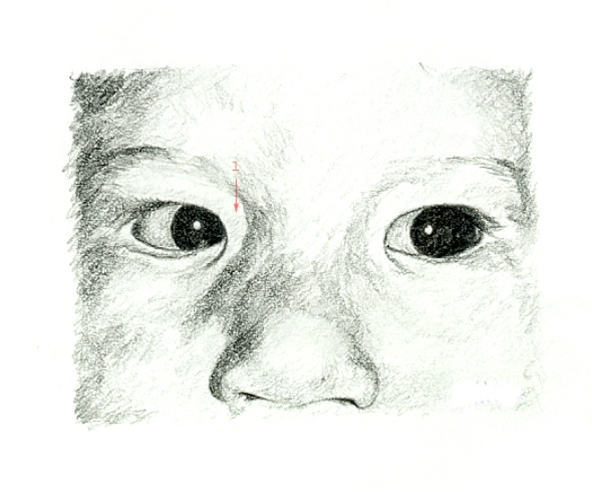 Epikanthus beim Blick zur Seite
Epikanthus beim Blick zur Seite - Mikrognathie (unterentwickelter Unterkiefer)
- leichtere Fehlbildungen der Hand
- Klinodaktylie (seitliche Abknickung der Finger)
- Gebogene obere Furche in der Handinnenfläche, die zwischen dem 2. und 3. Finger endet (ähnlich einem Hockeyschläger).
Zentralnervöse und neuropsychologische Anomalien1
- Je nach Alter
- Säuglingsalter
- reizbar
- schreckhaft, ängstlich
- autonome Instabilität
- Regulationsstörungen (Schlaf-/Wach-Regulation, Konzentration usw.)
- Kindesalter
- Hyperaktivität
- Aufmerksamkeitsstörungen
- kognitive Beeinträchtigungen
- emotionale Reaktivität
- Lernstörungen
- Hypotonie
- Hör- und Sehbehinderungen
- Anfälle
- Gedächtnis- und Lernschwäche
- Jugend- und frühes Erwachsenenalter
- primär eingeschränkte soziale Fähigkeiten sowie adaptive und exekutive Funktionen
- Säuglingsalter
- Strukturelle Anomalien
- kleiner Kopfumfang (< 10. Perzentile)
- strukturelle Abweichungen in der bildgebenden Diagnostik (z. B. Mikrozephalie)
- Neurologische Anomalien
- pathologische Reflexe, anomaler Tonus
- Hirnnervensymptome
- Koordinations- und des Gleichgewichtstörungen
- Nystagmus
- visuospatiale Störungen
- Krämpfe
- Funktionelle Anomalien
- kognitive Defizite – Störungen im Hinblick auf:
- Rechnen (besonders häufig)
- Rechtschreibung
- Lesen
- Gedächtnis
- Verarbeitungsgeschwindigkeit.
- eingeschränkte exekutive Funktionen
- Planung
- Verstehen der Konsequenzen von Handlungen
- Schwierigkeiten bei der Übertragung von Gelerntem von einer Situation auf eine andere
- eingeschränkte motorische Fähigkeiten
- Grob- und Feinmotorik
- Hypotonie
- Hyperaktivität, Aufmerksamkeits- und Konzentrationsstörungen
- eingeschränkte soziale Fähigkeiten und Anpassungsschwierigkeiten
- unzureichendes Verständnis sozialer Signale
- scheinbar fehlende Reue nach unangemessenem Verhalten
- fehlende angemessene Initiative
- fehlende gegenseitige Freundschaften
- sozialer Rückzug
- mangelnde Körperhygiene
- Gutgläubigkeit
- Bei vielen Patient*innen hohe soziale Motivation, Freundlichkeit, Zufriedenheit und sympathisches Wesen („Likeableness“), was sich in sozialer Hinsicht günstig für sie auswirkt.
- kognitive Defizite – Störungen im Hinblick auf:
- Häufig Komorbidität mit anderen psychischen Erkrankungen
Wachstumsretardierung
- Prä- oder postnatale Wachstumsretardierung ohne Aufholwachstum
- In der Regel als Körpergröße und/oder -gewicht unter der 10. Perzentile definiert
Sonstige strukturelle Fehlbildungen1
- Anomalien der Augen
- Strabismus
- Ptosis
- kleine Augen: Mikrophthalmie
- retinale Gefäßanomalien
- Hypoplasie des Sehnervs
- Refraktionsfehler: Myopie, Astigmatismus
- Gehör
- Schallleitungs- oder Schallempfindungsschwerhörigkeit
- unterentwickelte Tuba auditiva
- Kardiovaskuläre Anomalien
- Ventrikelseptumdefekte
- Atriumseptumdefekte
- Anomalien der großen Gefäße, Fallot-Tetralogie
- persistierender Ductus arteriosus
- Gastrointestinale Anomalien
- Inguinalhernien
- Abdominalhernien
- Rektusdiastase
- Gastroschisis
- extrahepatische Gallengangsatresie
- Urogenitale Anomalien
- Hydronephrose
- Nierendysplasie/-aplasie
- Hufeisenniere
- Ureter duplex
- Muskuloskelettale Anomalien
- verkürzter 5. Finger
- Beugekontrakturen und Kamptodaktylie (permanent gebeugte Finger)
- Trichterbrust (Pectus excavatum)
- Kielbrust (Pectus carinatum)
- kongenitale Halswirbelsynostose (Klippel-Feil-Syndrom)
- Klinodaktylie (Abknickung eines Fingerglieds im End- Mittel- oder Grundgelenk)
- Skoliose, z. B. aufgrund eines Halbwirbels
- radioulnare Synostose
- Sonstige Anomalien
- multiple Hämangiome
- Hirsutismus im Säuglingsalter
- anomale Fettgewebsverteilung
- möglicherweise erhöhtes Risiko bestimmter maligner Erkrankungen
Ergänzende Untersuchungen
- Neurologische Basisuntersuchung
- Größe, Gewicht, Kopfumfang
- Screeninguntersuchungen im Hinblick auf neurokognitive Symptome und psychische Störungen
Indikationen zur Überweisung
- Bei Verdacht auf ein undiagnostiziertes fetales Alkoholsyndrom sollten Hausärzt*innen das Kind und die Familie umgehend überweisen, damit schnell angemessene Förderungs- und Unterstützungsmaßnahmen ergriffen werden können.
- Da die Diagnose der ARND komplex und in ihrer Abgrenzung zu anderen Entwicklungsstörungen schwierig ist, empfiehlt die Leitliniengruppe der Gesellschaft für Neuropädiatrie (GNP) bei Verdacht auf Vorliegen einer ARND die Zuweisung an einen FASD-erfahrenen Leistungserbringer.1
- Die Erfahrung zeigt, dass eine frühzeitige Identifizierung alkoholbedingter Schädigungen bei Kindern für eine optimale Förderung von großer Bedeutung ist.
- Wenn die Diagnose FASD frühzeitig gestellt wird und das Kind in einem stabilen Umfeld aufwächst, besteht eine höhere Wahrscheinlichkeit, einen ungünstigen Lebensverlauf vermeiden zu können (Schulabbruch, Kriminalität, Suchtproblematik, unangemessenes sexuelles Verhalten, Aufenthalte in psychiatrischen Kliniken).1,7,9,12
Therapie
Therapieziel
- Optimale Bedingungen für Entwicklung und Wachstum schaffen.
Allgemeines zur Therapie
Multimodaler Ansatz5
- Es gibt keine kausale Therapie.
- Behandlung der somatischen Probleme in Kombination mit einer angemessenen Stimulation der psychischen Entwicklung
- Eine frühzeitige Stimulation kann dazu beitragen, dass das Kind seine individuellen Ressourcen optimal nutzen kann.
- Die Behandlung ist eine komplexe Aufgabe, für die eine interdisziplinäre Zusammenarbeit unerlässlich ist.
- Ggf. erforderliche Kompetenzen des Behandlungsteams, z. B. Kinder- und Jugendlichen-Psychotherapie, Pädagogik, Sozialarbeit, Physiotherapie, Allgemeinmedizin, Pädiatrie
- Es kann sinnvoll sein, eine Koordinationsgruppe zu bilden, in der das jeweils wichtigste Therapie- und Förderpersonal zusammenkommt, um die Übersicht über die verschiedenen Maßnahmen zu behalten und die Arbeit zu koordinieren.
- Eine enge Zusammenarbeit mit den Eltern ist von wesentlicher Bedeutung für eine erfolgreiche Förderung.
Medikamentöse Therapie
- Ggf. medikamentöse Therapie von Komplikationen wie hyperkinetischen Störungen, Herzfehlern usw.
Weitere Therapien
- Es gibt keine Hinweise darauf, dass bestimmte Diäten von Nutzen sind. Es werden eine normale gesunde Ernährung und ausreichend körperliche Aktivität empfohlen.
- Integration in reguläre Kindergärten und Schulen
- Ein integrativer Ansatz wirkt sich günstig auf die kognitive Entwicklung aus, sofern für die erforderlichen zusätzlichen Unterrichtsressourcen gesorgt ist.
- Bei Bedarf sollten zusätzliche Stunden z. B. mit Heilpädagog*innen, Ergotherapeut*innen, Logopäd*innen gewährleistet werden.
- Die Familien haben großen Beratungs- und Unterstützungsbedarf.
- Evtl. kann auch eine psychotherapeutische Unterstützung der Familie angezeigt sein.
Prävention
- Um eine FASD zu vermeiden, wird während der gesamten Schwangerschaft der vollständige Verzicht auf Alkohol empfohlen. Jegliche Verringerung des Alkoholkonsums bei Schwangeren scheint das Risiko derartiger Störungen zu senken.9
- Im Umfeld der Kinder sollte ein Unterstützungsnetzwerk aufgebaut werden, sodass sie weitgehend normal aufwachsen können und die psychosozialen Probleme, die häufig mit der Störung verbunden sind, so weit wie möglich verhindert werden.5
Verlauf, Komplikationen und Prognose
Verlauf
- Organschäden durch fetale Alkoholspektrumstörungen sind irreversibel.
- Der Verlauf kann sehr unterschiedlich sein und richtet sich nach dem Ausmaß der Schädigung und der Funktionsfähigkeit eines unterstützenden Netzwerks.
Komplikationen
Zahlreiche gesundheitliche Probleme15
- Praktisch alle Organsysteme können durch das fetale Alkoholsyndrom geschädigt werden.
- Kinder mit fetalem Alkoholsyndrom leiden häufig unter zahlreichen gesundheitlichen Problemen wie:16
- Fehlbildungen von Organen
- geschwächte Immunabwehr
- Wachstumsretardierung
- Verhaltensstörungen
- sozialen Problemen
- Lernschwächen.
- Durch die Umsetzung eines strukturierten Plans und ein stabiles Umfeld lässt sich die Situation für das jeweilige Kind deutlich verbessern.17
Psychosoziale Folgen im Jugend- und Erwachsenenalter
- Das FAS ist im Jugend- und Erwachsenenalter mit einem erhöhten Risiko für psychosoziale Probleme assoziiert, z. B.:18
- Erwerbsunfähigkeit
- Arbeitslosigkeit
- Alkoholmissbrauch und andere Suchterkrankungen
- psychischen Erkrankungen19
- Schulabbruch
- Kriminalität
- unangemessenes sexuelles Verhalten.
Andere Schwangerschaftskomplikationen durch Alkohol7
- Schwangerschaften mit einem hohen Alkoholkonsum der Mutter sind nicht nur mit FASD, sondern auch mit zahlreichen anderen schweren Komplikationen assoziiert, z. B.:
- Fehlgeburten
- vorzeitige Plazentalösungen (Abruptio placentae)
- Frühgeburten
- Amnionitis
- Totgeburten.
Prognose
- 95 % der FASD-Patient*innen leiden im Jugend- und Erwachsenenalter unter psychischen Störungen oder neurokognitiven Defiziten.
- Bei einem großen Teil von ihnen sind erhebliche zusätzliche Unterstützungs- und Fördermaßnahmen erforderlich, um den Schulbesuch zu ermöglichen.
Verlaufskontrolle
- Planung, Koordination und Verlaufsbeobachtung in einem interdisziplinären Team
- Die somatischen, neuropsychologischen und psychosozialen Probleme sollten alle gleichermaßen sorgfältig behandelt und beobachtet werden.
Patienteninformationen
Patienteninformationen in Deximed
Beratungs- und Selbsthilfeorganisation
- FASD Deutschland e. V.
- FAS-Beratungsstelle (Niedersachsen)
- Für Kinder in Suchtfamilien: NACOA
lllustrationen

Epikanthus beim Blick zur Seite

Epikanthus beim Blick nach vorn
Quellen
Leitlinien
- Gesellschaft für Neuropädiatrie. Fetale Alkoholspektrumstörungen, FASD - Diagnostik. AWMF-Leitlinie Nr. 022-025. S3, Stand 2016 (abgelaufen). www.awmf.org
- Deutsche Gesellschaft für Suchtforschung und Suchttherapie. Screening, Diagnostik und Behandlung alkoholbezogener Störungen. AWMF-Leitlinie Nr. 076-001. S3, Stand 2021. www.awmf.org
Literatur
- Gesellschaft für Neuropädiatrie. Fetale Alkoholspektrumstörungen, FASD - Diagnostik. AWMF-Leitlinie Nr. 022-025. S3, Stand 2016 (abgelaufen). www.awmf.org
- American Psychiatric Association. Neurobehavioral disorder associated with prenatal alcohol exposure. In: Diagnostic and Statistical Manual of Mental Disorders, Fifth Edition (DSM-5), American Psychiatric Association, Arlington, VA 2013. p.798.
- Jones KL, Smith DW
:. Recognition of the fetal alcohol syndrome in early infancy. Lancet 1973; 2: 999-1001.PubMedpubmed.ncbi.nlm.nih.gov - Deutscher Bundestag. Antwort der Bundesregierung auf die Kleine Anfrage der Abgeordneten Frank Tempel, Birgit Wöllert, Jan Korte, weiterer Abgeordneter und der Fraktion DIE LINKE. Schädigung von Föten durch Alkoholkonsum während der Schwangerschaft. Drucksache 18/3378; 18. Wahlperiode, 01.12.2014. Online-Ressource, letzter Zugriff 28.01.2018. dip21.bundestag.de
- Deutsche Hauptstelle für Suchtfragen. DHS Factsheet Alkohol in der Schwangerschaft. Dezember 2015. www.dhs.de
- Kraus L, Seitz NN, Shield KD et al. Quantifying harms to others due to alcohol consumption in Germany: a register-based study. BMC Med 2019; 17: 59. PMID: 30885214 PubMed
- May PA, Baete A, Russo J, et al. Prevalence and characteristics of fetal alcohol spectrum disorders. Pediatrics 2014; 134: 855-66. doi:10.1542/peds.2013-3319 DOI
- Feldman HS, Jones KL, Lindsay S, et al. Prenatal alcohol exposure patterns and alcohol-related birth defects and growth deficiencies: a prospective study. Alcohol Clin Exp Res 2012; 36: 670. pmid:22250768 PubMed
- Deutsche Gesellschaft für Suchtforschung und Suchttherapie. Alkoholbezogene Störungen: Screening, Diagnostik und Behandlung alkoholbezogener Störungen. AWMF-Leitlinie Nr. 076-001. S3, Stand 2021. www.awmf.org
- Alvik A, Aalen OO, Lindemann R. Early fetal binge alcohol exposure predicts high behavioral symptom scores in 5.5-year-old children. Alcohol Clin Exp Res 2013; 37: 1954-62. doi:10.1111/acer.12182 DOI
- Deutsches Institut für Medizinische Dokumentation und Information (DIMDI): ICD-10-GM Version 2021. Stand 18.09.2020; letzter Zugriff 30.03.2021. www.dimdi.de
- Landgraf MN, Nothacker M, Kopp IB, Heinen F. Diagnose des Fetalen Alkoholsyndroms. Dtsch Arztebl Int 2013; 110: 703-10. DOI: 10.3238/arztebl.2013.0703 DOI
- Fetal alcohol syndrome: Guidelines for Referral and Diagnosis. Atlanta, GA: National Center for Birth Defects and Developmental Disabilities, 2004.
- Astley SJ, FAS Diagnostic and Prevention Network, University of Washington. Diagnostic Guide forFetal Alcohol Spectrum Disorder: The 4-Digit Diagnostic Code. 3rd ed. 2004. Online-Ressource; letzer Zugriff 27.01.2018. depts.washington.edu
- Lægreid LM, Bruarøy S, Reigstad H. Fosterskade ved alkoholbruk i svangerskap. Tidsskr Nor Lægeforen 2005; 125: 445-7. PubMed
- Valborg L, Lonardson GR, Neff-Smith M et al. Characteristics of children who have full or incomplete fetal alcohol syndrome. J Pediatr 2004; 145: 635-40. PubMed
- Burd L, Cotsonas-Hassel TM, Martsolf JT et al. Recognition and management of fetal alcohol syndrome. Neurotoxicol Teratol 2003; 25: 681-8. PubMed
- Streissguth AP, Bookstein FL, Barr HM, et al. Risk factors for adverse life outcomes in fetal alcohol syndrome and fetal alcohol effects. J Dev Behav Pediatr 2004; 25: 228-38. pmid:15308923 PubMed
- Rangmar J, Hjern A, Vinnerljung B, et al. Psychosocial outcomes of fetal alcohol syndrome in adulthood. Pediatrics 2015; 135: e52-8. doi:10.1542/peds.2014-1915 DOI
Autor*innen
- Thomas M. Heim, Dr. med., Wissenschaftsjournalist, Freiburg
- Die ursprüngliche Version dieses Artikels basiert auf einem entsprechenden Artikel im norwegischen hausärztlichen Online-Handbuch Norsk Elektronisk Legehåndbok (NEL, https://legehandboka.no/).