Zusammenfassung
- Definition:Der Ventrikelseptumdefekt ist ein angeborener Herzfehler, bei dem eine Verbindung zwischen dem linken und rechten Ventrikel besteht. Der Links-Rechts-Shunt führt zu einer Volumenbelastung von dem rechten Ventrikel, den Pulmonalarterien und linken Herzhöhlen. Abhängig von der Shuntgröße kann sich eine pulmonale Hypertonie und schließlich Eisenmenger-Reaktion entwickeln.
- Häufigkeit:Häufigster angeborener Herzfehler (ca. 40 % der isolierten angeborenen Herzfehler). Zum geringeren Teil auch assoziiert mit komplexen Vitien.
- Symptome:Kleine Shunts sind asymptomatisch. Große Defekte führen bei Säuglingen vor allem zu Tachypnoe, Schwitzen, Gedeihstörung, gehäuften bronchopulmonalen Infekten. Bei Erwachsenen Dyspnoe, Leistungsschwäche.
- Befunde:Auskultatorisch Systolikum am linken unteren Sternalrand. Klinische Zeichen der Herzinsuffizienz.
- Diagnostik:Die Diagnose wird durch Echokardiografie gestellt.
- Therapie:Kleine VSD verschließen sich häufig spontan. Bei hämodynamisch relevanten VSD ist der chirurgische Verschluss die Methode der Wahl, im Einzelfall kann alternativ ein katheterinterventioneller Verschluss durchgeführt werden.
Allgemeine Informationen
Definition
- Der Ventrikelseptumdefekt (VSD) ist ein angeborener Herzfehler, bei dem eine Verbindung zwischen linkem und rechtem Ventrikel besteht.
- Ein VSD tritt isoliert oder gemeinsam mit anderen Herzfehlern auf (z. B. Fallot-Tetralogie, Transposition der großen Arterien, Univentrikuläres Herz).
Klassifikation
- Ein VSD kann an unterschiedlichen Stellen des Septums lokalisiert sein.1
- perimembranöser Defekt (ca. 80 %)
- Lokalisation im membranösen Anteil des Septums nahe Trikuspidal- und Aortenklappe
- muskulärer Defekt (ca. 15 %)
- Lokalisation im muskulären Teil des Septums, häufig multiple Defekte
- Outlet-Defekt (ca. 5 %)
- Lokalisation unterhalb der Semilunarklappen im Ausflussbereich
- Inlet-Defekt
- Lokalisation direkt unterhalb der AV-Klappen im Einflussbereich, typisch bei Down-Syndrom
- perimembranöser Defekt (ca. 80 %)
Häufigkeit
- Häufigster angeborener Herzfehler
- Anteil von ca. 40 % aller angeborenen Defekte2
- Beim weiblichen Geschlecht geringfügig häufiger3-4
- Bei systematischer echokardiografischer Untersuchung finden sich kleine muskuläre VSD bei 50/1.000 Neugeborenen.5
Ätiologie und Pathogenese
Ätiologie
- Vermutet wird eine multifaktorielle Ätiologie basierend auf der Interaktion zwischen angeborenen Dispositionen und Umweltfaktoren.6
- Gehäuft auftretend bei Chromosomendefekten wie Trisomie 13, Trisomie 18, Trisomie 216
Pathophysiologie
- Durch den Defekt entsteht aufgrund der Druckdifferenz ein Fluss vom linken zum rechten Ventrikel (Links-Rechts-Shunt)
- Das Ausmaß des Shunts hängt vorwiegend ab von:3
- der Größe des Defekts
- dem Verhältnis vom systemischen zum pulmonalen Widerstand.
- Hämodynamische Folgen sind:
- erhöhter pulmonaler Blutfluss
- erhöhter pulmonal-arterieller Druck
- Volumenbelastung des linken Ventrikels
- Dilatation und später Hypertrophie
- Erhöhung des enddiastolischen Drucks
- erniedrigter systemischer kardialer Auswurf.
- Kleine VSD wirken „restriktiv“.
- aufgrund des kleinen Defekts nur geringes Shuntvolumen mit dementsprechend geringen hämodynamischen Auswirkungen
- Druckdifferenz zwischen dem linken und rechten Ventrikel bleibt erhalten.
- häufig spontaner Verschluss kleiner, restriktiver VSD in der Postnatalperiode
- spontaner Verschluss auch noch bei 4 % der Erwachsenen mit perimembranösem VSD
- Große VSD sind nicht mehr „restriktiv“.
- Druckangleich zwischen dem linken und rechten Ventrikel
- Shuntvolumen und -richtung hängen nur noch vom Widerstandsverhältnis zwischen Lungen- und Systemkreislauf ab.3
- Bei im Verlauf zunehmender pulmonaler Hypertonie kommt es zur Shunt-Umkehr (Rechts-Links-Shunt) mit Zyanose (Eisenmenger-Reaktion).
Disponierende Faktoren
- Bei mehr als 95 % der Fälle handelt es sich um isolierte, angeborene Anomalien.
- Genetische Faktoren6
- gehäuftes Auftreten bei Eltern oder Geschwistern mit angeborenem Herzfehler
- 3-fach erhöhtes Risiko, falls ein Geschwister einen VSD aufweist.
- Bestimmte genetische Syndrome sind gehäuft mit VSD assoziiert, z. B. Trisomie 13/18/21.
- Maternale Faktoren
ICPC-2
- K73 Angeborene Anomalie Herz/Gefäßsystem
ICD-10
- Q21 Angeborene Fehlbildungen der Herzsepten
- Q21.0 Ventrikelseptumdefekt
Diagnostik
Diagnostische Kriterien
- Nachweis durch Echokardiografie
- Zielsetzung der Diagnostik:3
- Nachweis des Defekts
- Beschreibung der Lokalisation
- Abschätzen der hämodynamischen Auswirkungen
- Abschätzen des pulmonalarteriellen Drucks
- Nachweis bzw. Ausschluss von begleitenden Herz- und Gefäßfehlbildungen
- Abschätzung der Prognose
- Therapieplanung.
Differenzialdiagnosen
- Sonstige angeborene, mit einem VSD assoziierte Herzerkrankungen
- Fallot-Tetralogie
- Transposition der großen Arterien
- Persistierender Truncus arteriosus
- Persistierender Ductus arteriosus
- Univentrikuläres Herz
- Atrioventrikulärer Septumdefekt
Anamnese
- Im Rahmen der Neugeborenenuntersuchung sind auch größere Defekte häufig noch asymptomatisch.3
- Der Shunt ist noch klein aufgrund des postpartal zunächst noch hohen pulmonalarteriellen Widerstands.
- Bei abfallendem pulmonalem Widerstand gibt es bereits bei jungen Säuglingen altersentsprechende Symptome der Herzinsuffizienz:3
- Schwitzen
- Tachypnoe
- Erschöpfung beim Stillen/Gedeihstörung
- bronchopulmonale Infekte.
Klinische Untersuchung
- Die klinischen Befunde sind abhängig von der Defektgröße.
- Kleine, restriktive Defekte
- lautes Systolikum links parasternal (siehe auch Artikel Herzgeräusche bei Kindern)
- evtl. Schwirren
- bei beginnendem Spontanverschluss Abschwächung des Geräuschs
- Mittelgroße Defekte
- Systolikum links parasternal
- beginnend hebender Herzspitzenstoß (Volumenbelastung)
- leichte Tachykardie
- Große Defekte
- hyperaktives Präkordium
- Zeichen der Herzinsuffizienz
- Tritt bei Kindern im Alter von 4–8 Wochen auf: Tachykardie, Tachypnoe, Schwitzen, Hepatosplenomegalie.
- leises Systolikum, betonter 2. Herzton
- Zyanose bei Shuntumkehr nach den ersten Lebensjahren (Eisenmenger-Reaktion)
- Folge des zunehmenden pulmonalen Widerstands und Drucks
Vorgeschichte und klinische Präsentation im Erwachsenenalter
- Viele Patienten mit kleinen, evtl. auch postoperativ residuellen VSD bleiben asymptomatisch.
- Evtl. systolisches Herzgeräusch (siehe auch Artikel Herzgeräusche bei Erwachsenen)
- Bei einigen Patienten gibt es mögliche Probleme mit zunehmendem Alter:1
- Endokarditis (6-fach erhöhtes Risiko)
- Zunahme des Shunts durch ansteigenden systolischen und diastolischen LV-Druck mit Entwicklung einer Herzinsuffizienz
- bei entsprechender VSD-Lokalisation Prolaps der rechtskoronaren Aortenklappentasche mit Aortenklappeninsuffizienz
- Arrhythmien (seltener als bei anderen angeborenen Herzfehlern)
- Eine Vorstellung im hausärztlichen Bereich kann unter unterschiedlichen Umständen erfolgen:1
- VSD in der Kindheit operiert, kein residueller Shunt
- VSD in der Kindheit operiert mit residuellem Shunt
- Kleiner VSD ohne Volumenbelastung/Herzinsuffizienz, bei dem in der Kindheit keine Indikation zum Verschluss gestellt wurde.
- großer, evtl. bisher nicht bekannter VSD mit Herzinsuffizienz
- Eisenmenger-Syndrom: großer VSD mit ursprünglich großem Li-Re-Shunt, konsekutive Entwicklung einer pulmonalen Hypertonie mit Shuntumkehr/Zyanose
Ergänzende Untersuchungen in der Hausarztpraxis
- Bei Neugeborenen/Kindern weitere Abklärung durch Kinderarzt/Kinderkardiologen
- Bei Erwachsenen
- EKG (siehe auch Artikel Checkliste EKG)
- bei kleinen Defekten in der Regel unauffällig
- bei moderaten und großen Defekten mit Volumenbelastung Zeichen der linksventrikulären Hypertrophie, P-mitrale
- bei großen Defekten mit pulmonaler Hypertonie zusätzlich Zeichen der rechtsventrikulären Hypertrophie
- Rö-Thorax
- bei signifikantem Shunt Kardiomegalie, vermehrte Lungengefäßzeichnung
- Ausschluss/Nachweis von Differenzialdiagnosen bei Dyspnoe
- EKG (siehe auch Artikel Checkliste EKG)
Diagnostik beim Spezialisten
- Echokardiografie
- Nachweis eines VSD
- Lokalisation des Defekts im Verhältnis zu umgebenden Strukturen
- Bestimmung von Morphologie und Größe
- Ausmaß des Shunts – Verhältnis von pulmonalem zu systemischem Fluss (Qp:Qs)
- Größe und Funktion der Ventrikel
- Beurteilung der Klappen, insbesondere Aortenklappe
- Bestimmung des systolischen pulmonal-arteriellen Drucks
- Nachweis weiterer Fehlbildungen
- Bei 22 % der Patienten mit kongenitalem VSD gibt es bedeutsame weitere Fehlbildungen.3
- Magnetresonanztomografie (MRT)
- Alternative zur Echokardiografie bei unzureichenden Schallbedingungen
- Herzkatheteruntersuchung
- Ist für die Diagnosestellung heutzutage im Allgemeinen nicht notwendig.
- bei Patienten mit pulmonaler Hypertonie zur Bestimmung des pulmonalarteriellen Widerstands
- ggf. Testung auf Reversibilität eines erhöhten Widerstands
Schwangerschaft
- Niedriges Risiko bei asymptomatischen Patientinnen ohne LV-Dysfunktion oder pulmonale Hypertonie1
- Kontraindiziert bei Eisenmenger-Syndrom1
Indikationen zur Überweisung
- Bei klinischem/auskultatorischem Verdacht: Überweisung zur Echokardiografie
Checkliste zur Überweisung
Herzgeräusch beim Kind
- Zweck der Überweisung
- Bestätigende Diagnostik? Behandlung? Sonstiges?
- Anamnese
- Gedeihstörung, Schwindel, Synkope, Atemnot, Atemwegsinfekte, Husten, Brustschmerz, Palpitationen
- Familienanamnese: Herzfehler, plötzlicher Herztod
- Schwangerschaft: Alkohol, teratogene Medikamente, Infektionen, Diabetes mellitus
- Vor- und Begleiterkrankungen, die mit Herzfehlern assoziiert sind.
- Klinische Untersuchung
- Allgemeinzustand?
- Zyanose, Tachypnoe, Ödeme
- Blutdruckdifferenz Arme/Beine
- palpables Schwirren über Thorax, Lebervergrößerung
- Herzgeräusch: zeitliches Auftreten innerhalb des Herzzyklus, Dauer, Frequenz, Klangcharakter, Punctum maximum, Fortleitung
- Ergänzende Untersuchungen
- EKG
Therapie
Therapieziel
- Kausale Therapie: Verschluss des VSD zur Vermeidung von Komplikationen und Normalisierung der Prognose
Allgemeines zur Therapie
- Indikation zum Verschluss ist allgemein gegeben bei:3
- echokardiografisch eindeutiger Volumenbelastung (Shuntverhältnis Qp:Qs > 1,5:1)
- großem Defekt mit Ausbildung einer pulmonalen Hypertonie (solange noch nicht fixiert)
- Kleine Defekte
- Kleine, im Neugeborenenalter diagnostizierte VSD verschließen sich häufig noch spontan.
- Indikation zum Verschluss bei Entstehung einer Aortenklappeninsuffizienz (v. a. bei infundibulärem VSD)3
- Mittelgroße Defekte
- Verschluss nach dem 1. LJ bei fehlender Verkleinerung und persistierender Volumenbelastung3
- Große Defekte
- Verschluss in den ersten 6 Monaten bei (noch nicht fixierter) pulmonaler Hypertonie oder Herzinsuffizienzzeichen/Gedeihstörung3
- Nach dem 6. Lebensmonat ist die Therapieentscheidung schwieriger, daher invasive Bestimmung des pulmonalen Widerstands und Reagibilitätstestung.3
Operativer Verschluss
- Der operative Verschluss ist die Standardmethode.3
- In der Regel operativer Verschluss nach medianer Sternotomie und Rechtsatriotomie mit transtrikuspidalem Zugang3
- je nach anatomischer Lage im Einzelfall auch Aortotomie oder Ventrikulotomie (bei Ventrikulotomie höheres Risiko späterer Rhythmusstörungen) als Zugang3
- Alternativ minimalinvasive Verfahren (partielle inferiore Sternotomie, anterolaterale oder mittaxilläre Thorakotomie)3
- Verschluss durch Patch, im Einzelfall auch durch direkte Naht3
- Sehr geringes operatives Mortalitätsrisiko (sofern noch keine fixierte pulmonale Hypertonie)9
Katheterinterventioneller Verschluss
- Ein interventioneller Verschluss mit Schirmchen oder Spiralen ist technisch grundsätzlich möglich.
- Ein Verschluss perimembranöser Defekte wegen der Nähe zu Reizleitungssystem und Aortenklappe ist allerdings problematisch.3
- Die Erfolgschancen steigen mit Körpergröße und Entfernung des Verschlusses von der Aortenklappe.3
- Ein interventioneller Verschluss ist eine Option v. a. bei muskulären Defekten.10
Medikamentöse Therapie
- Bei fixierter pulmonaler Hypertonie und dadurch zu großem Verschlussrisiko drucksenkende Therapie mit Endothelinrezeptor-Antagonisten oder Phosphodiesterasehemmern3
- Symptomatische medikamentöse Therapie einer Herzinsuffizienz3
Endokarditis-Prophylaxe
- Eine Endokarditis-Prophylaxe wird in den ersten 6 Monaten nach Verschluss verabreicht, später nur bei Restshunt.11
- Ansonsten wird keine Endokarditis-Prophylaxe empfohlen.11
Indikationsstellung zum Verschluss bei Erwachsenen mit Ventrikelseptumdefekt
- Die Indikationsstellung bei Erwachsenen erfolgt ähnlich wie bei Kindern auf der Basis der hämodynamischen Wirksamkeit des VSD.
- Ein chirurgischer Verschluss ist die Methode der Wahl mit niedriger operativer Mortalität und guten Langzeitergebnissen.1
- Ein katheterinterventioneller Verschluss kann erwogen werden bei:1
- erhöhtem Operationsrisiko
- herzchirurgischen Voroperationen
- ungünstiger Lage des VSD für eine Operation.
- Ein katheterinterventioneller Verschluss ist die Alternative zur Chirurgie v. a. bei muskulären, zentral im Septum gelegenen Defekten.1
Leitlinie: Indikation zum VSD-Verschluss bei Erwachsenen1
- Bei Patienten mit Symptomen, die auf den Li-Re-Shunt durch den (residuellen) ASD zurückgeführt werden können und die keine pulmonale Hypertonie aufweisen, sollte ein chirurgischer ASD-Verschluss durchgeführt werden (I/C).
- Bei asymptomatischen Patienten mit linksventrikulärer Volumenbelastung durch den VSD sollte ein chirurgischer Verschluss durchgeführt werden (I/C).
- Bei Patienten mit einer infektiösen Endokarditis in der Vorgeschichte sollte ein chirurgischer Verschluss erwogen werden (IIa/C).
- Bei Patienten mit VSD-bedingtem Prolaps einer Aortenklappentasche und progredienter Aortenklappeninsuffizienz sollte eine Operation erwogen werden (IIa/C).
- Bei Eisenmenger-Syndrom sollte kein Verschluss durchgeführt werden (III/C).
- Bei kleinem VSD ohne Volumenbelastung/pulmonale Hypertonie/St. n. infektiöser Endokarditis sollte kein Verschluss durchgeführt werden (III/C).
Verlauf, Komplikationen und Prognose
Komplikationen
- Langfristig
- pulmonale Hypertonie
- Eisenmenger-Reaktion
- Herzinsuffizienz
- Aortenklappeninsuffizienz
- infektiöse Endokarditis
- Herzrhythmusstörungen
- plötzlicher Herztod selten12
- Kurzfristig nach Verschluss
Verlauf und Prognose
- Kleine, restriktive VSD ohne Einfluss auf Lebenserwartung und Belastbarkeit3
- Häufig spontaner Verschluss kleiner Defekte innerhalb der ersten 1–2 Lebensjahre14-15
- spontaner Verschluss am häufigsten bei muskulären Defekten6
- Spontane Verschlüsse sind nach dem 2. Lebensjahr selten.16
- Bei einigen Patienten im Verlauf Zunahme des Shunts und Behandlung im Erwachsenenalter notwendig17
- Bei großen unbehandelten Defekten erhebliches Risiko für Entstehung eines Eisenmenger-Syndroms
- Nach chirurgischer Korrektur gute Prognose, auch bei großen Defekten18-19
- bei rechtzeitiger, erfolgreicher und unkomplizierter Therapie: normale kardiopulmonale Belastbarkeit und normale Lebenserwartung3
Verlaufskontrolle
- Kinder und Jugendliche
- nach VSD-Verschluss im Kindesalter bis zum Abschluss der Wachstumsperiode regelmäßige kinderkardiologische Nachkontrollen3
- jenseits der Pubertät keine regelmäßigen Kontrollen mehr notwendig, sofern:3
- kein Restshunt
- Sinusrhythmus mit normaler AV-Überleitung
- normale Herzgröße und -funktion
- regelrechte Klappenfunktion.
- bei restriktiven VSD ohne Verschluss lebenslange Verlaufskontrollen
- Erwachsene
- jährliche Verlaufskontrollen in spezialisierten EMAH-Zentren (EMAH = Erwachsene mit angeborenen Herzfehlern) bei:1
- Restshunt
- LV-Dysfunktion
- pulmonaler Hypertonie
- Aortenklappeninsuffizienz
- Ausflusstraktobstruktion.
- Verlaufskontrollen alle 3–5 Jahre bei:
- kleinem VSD
- asymptomatisch
- keine LV-Dysfunktion, keine pulmonale Hypertonie.
- jährliche Verlaufskontrollen in spezialisierten EMAH-Zentren (EMAH = Erwachsene mit angeborenen Herzfehlern) bei:1
- Eine gute Zusammenarbeit zwischen Hausärzten und EMAH-Spezialisten ist für das langfristige Wohlergehen der Patienten wichtig.20
Patienteninformationen
Patienteninformationen in Deximed
- Septumdefekte bei Kindern: Atriumseptumdefekt (ASD) und Ventrikelseptumdefekt (VSD)
- Herzkatheteruntersuchung bei Kindern
- Echokardiografie
- Endokarditis-Prophylaxe
Patientenorganisationen
- Bundesverband herzkranke Kinder e. V.
- Interessengemeinschaft Das herzkranke Kind e. V.
- Elterninitiative Herzkranke Kinder Südbaden e. V.: Herzklopfen
- Kinderherzstiftung e. V.
Weitere Informationen
- Broschüre der Kinderherzstiftung für Patienten und Ärzte nichtkardiologischer Fachrichtungen wie Hausärzte, Internisten und Allgemeinmediziner. www.aerzteblatt.de
- Enthält eine Adressliste aller pädiatrischen und internistischen Kardiologen mit der Zusatzqualifikation EMAH.
Illustrationen


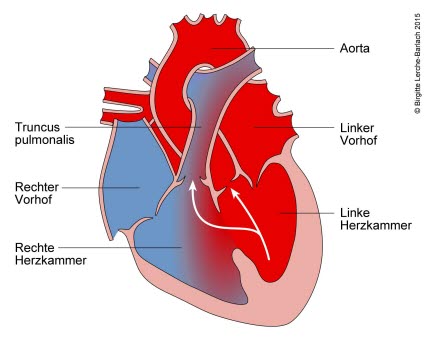
Ventrikelseptumdefekt
Quellen
Leitlinien
- Deutsche Gesellschaft für Pädiatrische Kardiologie. Ventrikelseptumdefekt im Kindes- und Jugendalter. AWMF-Nr. 023-012. S2k, Stand 2013. www.awmf.org
- Deutsche Gesellschaft für pädiatrische Kardiologie. Infektiöse Endokarditis und Endokarditisprophylaxe im Kindes- und Jugendalter. AWMF-Nr. 023-24. S2k, Stand 2014. www.awmf.org
- European Society of Cardiology. Guidelines for the management of grown-up congenital heart disease. Stand 2010. www.escardio.org
Literatur
- Baumgartner H, BonhoefferP, De Groot N, et al. ESC Guidelines for the management of grown-up congenital heart disease (new version 2010). Eur Heart J 2010; 31: 2915–2957. doi:10.1093/eurheartj/ehq249 DOI
- Penny D, Vick G. Ventricular septal defect. Lancet 2011; 377: 1103-1112. doi:10.1016/S0140-6736(10)61339-6 DOI
- Deutsche Gesellschaft für Pädiatrische Kardiologie. Ventrikelseptumdefekt im Kindes- und Jugendalter. AWMF-Nr. 023-012. Stand 2013. www.awmf.org
- Spicer D, Hsu H, Co-Vu J, et al. Ventricular septal defect. Orphanet J Rare Dis 2014; 9: 144. www.ncbi.nlm.nih.gov
- Roguin N, Du ZD, Barak M, et al. High prevalence of muscular ventricular septal defect in neonates. J Am Coll Cardiol 1995; 26: 1545-1548. doi:10.1016/0735-1097(95)00358-4 DOI
- Ramaswamy P. Ventricular septal defects. Medscape, updated Dec 10, 2015. Zugriff 21.10.18. emedicine.medscape.com
- Narchi H, Kulaylat N. Heart disease in infants of diabetic mothers. Images Paediatr Cardiol 2000; 2: 17-23. www.ncbi.nlm.nih.gov
- Yang J, Qiu H, Pengfei Q, et al. Prenatal Alcohol Exposure and Congenital Heart Defects: A Meta-Analysis. PLoS One 2015;10: e0130681. doi:10.1371/journal.pone.0130681 DOI
- Roos-Hesselink JW, Meijboom FJ, Spitaels SEC et al. Outcome of patients after surgical closure of ventricular septal defect at young age: longitudinal follow-up of 22-34 years. Eur Heart J 2004;25:1057-62. European Heart Journal
- Zartner P, Christians C, Stelter J, e al. Transvascular closure of single and multiple muscular ventricular septal defects in neonates and infants < 20 kg.. Catheter Cardiovasc Interv 2014; 83: 564-570. pmid:23996896 PubMed
- Knirsch W, Mackenzie C, Schäfers H, et al. für die Deutsche Gesellschaft für pädiatrische Kardiologie. Infektiöse Endokarditis und Endokarditisprophylaxe im Kindes- und Jugendalter. Stand 2014. www.awmf.org
- Khairy P, Balaji S. Cardiac Arrhythmias In Congenital Heart Diseases. Indian Pacing Electrophysiol J 2009; 9: 299–317. pmid:19898654 PubMed
- Schipper M, Slieker M, Schoof P, et al. Surgical Repair of Ventricular Septal Defect; Contemporary Results and Risk Factors for a Complicated Course. Pediatr Cardiol 2017; 38: 264-270. pmid:27872996 PubMed
- Gabriel HM, Heger M, Innerhofer P, et al. Long-term outcome of patients with ventricular septal defect considered not to require surgical closure during childhood. J Am Coll Cardiol 2002;39:1066-1071. PMID: 11897452 PubMed
- Sologashvili T, Prêtre R, Ponti A. Was Allgemeinärzte über Herzoperationen bei Kindern wissen müssen - Fehlbildungen des Herzens. Schweiz Med Forum 2017; 17: 570-578. doi:10.4414/smf.2017.02954 DOI
- Miyake T, Shinohara T, Fukuda T, Ikeoka M, Takemura T. Spontaneous closure of perimembranous ventricular septal defect after school age. Pediatr Int 2008; 50: 632-635 PMID: 19261109 PubMed
- Soufflet V, Van de BA, Troost E, et al. Behavior of unrepaired perimembranous ventricular septal defect in young adults. Am J Cardiol 2010;105:404-407. PMID: 20102957 PubMed
- Scully BB, Morales DL, Zafar F, et al. Current expectations for surgical repair of isolated ventricular septal defects. Ann Thorac Surg 2010; 89: 544-9. PubMed
- Moller JH, Patton C, Varco RL, Lillehei CW. Late results (30 to 35 years) after operative closure of isolated ventricular septal defect from 1954 to 1960. Am J Cardiol 1991; 68: 1491-7. PubMed
- Tutarel O, Bauer U, Diller G. Erwachsene mit angeborenen Herzfehlern: Was zu beachten ist. Dtsch Arztebl 2018; 115: 26-32. doi:10.3238/PersKardio.2018.03.30.05 DOI
Autoren
- Michael Handke, Prof. Dr. med., Facharzt für Innere Medizin, Kardiologie und Intensivmedizin, Freiburg i. Br.
- Bjørnar Grenne, PhD, konst. overlege, Klinikk for hjertemedisin, St. Olavs-Hospital, Trondheim