Allgemeine Informationen
Definition
- Maligne Raumforderungen, die Absiedelungen extrahepatischer Malignome darstellen.
- Häufige Primärtumoren:
Häufigkeit
- Lebermetastasen stellen die häufigste Form der bösartigen Lebertumoren dar.1
- Besonders verbreitet sind Metastasen von Primärtumoren im Verdauungstrakt, in der Brust und in der Lunge.
- Etwa die Hälfte aller Patient*innen mit kolorektalem Karzinom weist entweder bereits bei Diagnosestellung synchrone Lebermetastasen auf oder entwickelt im Verlauf sog. metachrone Lebermetastasen (> 3 Monate nach Diagnosestellung des Primarius).2
Ätiologie und Pathogenese
- Am häufigsten hämatogene Metastasierung vom Primärtumor in die Leber
- Eine Metastasierung durch Überschreitung der Organgrenzen oder Ausbreitung über Lymphsystem ist dagegen selten.
ICPC-2
- D77 Bösartige Neubild. Verdauungstrakt
ICD-10
- C78.7 Sekundäre bösartige Neubildung der Leber und der intrahepatischen Gallengänge
Diagnostik
Diagnostische Kriterien
- Die Diagnose erfolgt durch bildgebende Verfahren bei bekannter maligner Grunderkrankung und/oder Biopsie der Leber.
Differenzialdiagnosen
- Leberzellkarzinom
- Cholangiokarzinom
- Leberadenom
- Fokal-noduläre und noduläre regenerative Hyperplasie der Leber
- Hämangiom
- Zystenleber
Anamnese
- Die Erkrankung verläuft häufig über längere Zeit asymptomatisch.
- Im weiteren Verlauf können jedoch die Metastasen oder der Primärtumor selbst Symptome verursachen.
- Hierzu gehören Müdigkeit, Krankheitsgefühl, schlechter Allgemeinzustand, Thrombosen.
Klinische Untersuchung
- Ikterus
- Leber vergrößert palpabel und von unregelmäßiger Struktur
- Aszites
- Bei unbekanntem Primärtumor darüber hinaus Tumorsuche
- Hautläsionen (malignes Melanom)
- Lymphknotenstatus
- evtl. digital-rektale Untersuchung3
- bei Frauen: Tastbefund Brust
Ergänzende Untersuchungen
- Die Blut- und Leberwerte können unauffällig sein.
- Erhöhte Leberwerte liegen erst bei bereits ausgeprägter Metastasierung vor.
- CEA
- Häufig ist der CEA-Wert (CEA = karzinoembryonales Antigen) erhöht.
- Klassisch beim kolorektalen Karzinom, aber u. a. auch bei Mamma-, Lungen- oder Pankreas-Ca Erhöhung möglich.
- Dient nicht zur Diagnostik, sondern als Verlaufsparameter zur Kontrolle der Therapie.
- Steigt z. B. der Wert nach erfolgter Tumor- bzw. Metastasenresektion an, legt dies den Verdacht auf Lebermetastasen nahe.4-5
- Häufig ist der CEA-Wert (CEA = karzinoembryonales Antigen) erhöht.
- AFP
- diagnostischer Parameter
- Sensitivität der Früherkennung eines HCC wird durch die AFP-Bestimmung erhöht.3
- Bildgebende Methode der Wahl: Ultraschall (evtl. mit Kontrastmittelgabe bei Spezialist*in)3-4,6-8
- In der Regel sind Läsionen erkennbar, die größer als 0,5 cm sind.
- typisches Merkmal der Lebermetastase: Halo (echoarmer Randsaum)
- generell aber variables Erscheinungsbild
- ggf. multiple Herde
- ggf. Suche nach intraabdominellem Primärtumor
Diagnostik bei Spezialist*innen
- CT und/oder MRT (ggf. MR-Angiografie) sind in folgenden Fällen indiziert:
- bei unklarem Ultraschallbefund
- bei unerwartet unauffälligem Ultraschallbefund
- zur Bestimmung des Stadiums (Staging)
- Wenn eine Leberresektion geplant ist.
- Ultraschallgesteuerte Biopsie
- Suche nach Primärtumor: ÖGD, Koloskopie, MRT/CT von Lunge, Pankreas, Mammografie, Mammasonografie
Präoperative Untersuchungen
- Hb, Leukozyten, Thrombozyten, Na, K, Cl, Ca, Kreatinin, Harnstoff, Amylasen, Albumin, GOT (ASAT), GPT (ALAT), AP, Bilirubin, LDH, TSH
- EKG, Röntgenthorax, CT von Thorax, Abdomen (Zweiphasen-Spiral-CT) und Becken, MRT, Kontrastmittel-Sonografie
- Für die Beurteilung der Operabilität sind präoperativ Ultraschall, CT und MRT die entscheidenden Verfahren.
- PET-Untersuchung bei kolorektalem Karzinom?4
- nicht empfohlen zur primären Ausbreitungsdiagnostik bei kolorektalem Karzinom
- ggf. bei resektablen Rezidivmetastasen eines kolorektalen Karzinoms zur Vermeidung einer unnötigen Laparotomie
Indikationen zur Überweisung
- Bei Verdacht auf Lebermetastasen eines bislang unbekannten Primärtumors
- Bei Verdacht auf neu aufgetretene Lebermetastasen eines bekannten Primärtumors
- Bei Verdacht auf ein Tumorrezidiv eines kurativ behandelten Tumors
Therapie
Therapieziele
- Je nach Stadium und Histologie der Erkrankung besteht das Therapieziel in einer Heilung oder Linderung der Symptome.9-10
Allgemeines zur Therapie
- Die Therapie richtet sich nach dem zugrunde liegenden Primärtumor.
- Prinzipiell können einzelne Lebermetastasen kurativ entfernt werden.
- Wichtig ist gute präoperative Diagnostik, um weitere Metastasierung auszuschließen.
Kolorektales Karzinom
Magenkarzinom
Malignes Melanom
Mammakarzinom
Ösophaguskarzinom
- Bei präoperativem Nachweis einer Fernmetastasierung soll keine Operation erfolgen.8
- in der Regel dann palliative Chemotherapie
Exokrines Pankreaskarzinom
- Bei Vorliegen von Lebermetastasen in der Regel palliative Chemotherapie7
Medikamentöse Therapie
- Je nach zugrunde liegendem Tumor kann eine Chemotherapie infrage kommen.
Operative Therapie
- Kontraindikationen4,13-15
- Schlechter Allgemeinzustand, der eine Operation nicht erlaubt.
- extensive extrahepatische Metastasierung
- relativ: nicht-resektabler Primärtumor
- Dank der modernen bildgebenden Diagnoseverfahren lässt sich die Operabilität einschätzen und eine extrahepatische Metastasierung ausschließen.
- Leberresektionen werden in atypische oder Keilresektionen einerseits und anatomische Resektionen andererseits unterteilt.
- Onkologisch betrachtet führen anatomische Resektionen zu besseren Ergebnissen als atypische Resektionen.16-17
- Bei normaler Funktion der Leberzellen können bis zu 75 % der Leber entfernt werden. Bei herabgesetzter Leberfunktion, z. B. bei Patient*innen mit Zirrhose, kann auch eine weniger umfassende Teilresektion der Leber zu Leberversagen und Tod führen.
- Da sich die Leber selbst regenerieren kann, ist bei einer Resektion die Entnahme von Lebergewebe bis hin zur Überlebensgrenze möglich. Die Leber wächst innerhalb einiger Wochen bis zur normalen Größe nach und ist nach einigen Monaten wieder normal funktionsfähig.
Indikationen für einen chirurgischen Eingriff4,6,11-15
- Abhängig vom Primärtumor
- In der Regel kommen nur einzelne Lebermetastasen infrage bei darüber hinaus stabiler Erkrankung.
- Der Allgemeinzustand erlaubt eine Operation.
Chirurgischer Eingriff
- Standardeingriff bei Lebermetastasen, die über 1 cm groß sind oder tief im Gewebe liegen.
- Dissektion des Hilus mit Identifizierung von Ductus choledochus, Ductus hepaticus und dessen zweier Äste, Leberarterien und Vena portae mit Ästen
- danach Teilung des jeweiligen Hauptzweigs von Ductus hepaticus, Arteria hepatica und Vena portae
- Inzision der Leberkapsel, danach Resektion gemäß der anatomischen
- Aufteilung des Leberparenchyms
- Drainage des Operationsgebietes
- Kleine (< 1 cm), vereinzelte, oberflächliche Lebermetastasen
- in erster Linie Keilresektion
Prä- und postoperative Therapie
- Infektions- und Thromboseprophylaxe
- Leberwerte 2-mal wöchentlich bis zur Entlassung
- Bei Fieberanstieg
- Kontrolle auf ggf. nicht drainierte Hohlräume im Umfeld des Resektionsgebiets mittels Ultraschall des Bauchs
- Ein postoperativer Ikterus geht in der Regel vorüber und stellt meist keine ernste Komplikation dar.
Weitere onkologische Therapie und palliative Behandlung
- Bei nicht resektablen Metastasen können Bestrahlung, Chemotherapie und lokal ablative Verfahren infrage kommen.
- Dies wird nach klinischer Beurteilung durch die behandelnden Onkolog*innen entschieden.
- Kombinationstherapien aus Kryochirurgie, verschiedenen Chemotherapien und laparoskopisch gesteuerten Eingriffen befinden sich in der Erprobung und können bei bestimmten Patient*innen infrage kommen.
Palliativtherapie
- Schmerzen
- Übelkeit und Erbrechen
- Obstipation
- Maligne gastrointestinale Obstruktion
- Mundtrockenheit
- Mangelernährung und Dehydratation
- Atembeschwerden
- Depression
- Angst
- Delir
Verlauf, Komplikationen und Prognose
Verlauf
- Abhängig von Grunderkrankung
Komplikationen
- Aszites
- Gastrointestinale Blutungen
- Cholangitis
- Leberabszess
- Cholestase
- Thrombosen
Prognose
Kolorektales Karzinom
- Bei vollständiger (R0) Resektion gute Prognose mit Heilung in bis zu 20–50 % der Fälle4-5
- Synchrone Metastasierung, d. h. der Nachweis von Lebermetastasen zum Diagnosezeitpunkt, gilt als prognostisch ungünstig.
- Metachrone Metasierung, d. h. der Nachweis von Lebermetastasen im Verlauf, ist mit einer besseren Prognose als synchrone Metastasen verbunden, insbesondere bei einem langen krankheitsfreien Intervall (> 6 Monate).4
- Indikatoren für eine schlechte Prognose (Fong-Score):19
- Lymphknotenmetastasen des Primärtumors
- Krankheitsfreies Intervall zwischen Diagnose des Primärtumors und Auftreten von Lebermetastasen < 12 Monate
- > 1 Lebermetastase
- Metastasengröße > 5 cm
- Erhöhtes karzinoembryonales Antigen (CEA > 200 mg/ml)
- Je höher der Score, desto niedriger das Langzeitüberleben. Bei ≥ 3 Punkten ist eine chirurgische Resektion von Lebermetastasen zurückhaltend zu beurteilen.
Verlaufskontrolle
- Gemäß der Grunderkrankung
Patienteninformationen
Patienteninformationen in Deximed
Weitere Informationen
- Deutsche Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten (DGVS): Patientenleitlinien Darmkrebs
- Früherkennung von Darmkrebs
- Darmkrebs im frühen Stadium
- Darmkrebs im fortgeschrittenen Stadium
Illustrationen
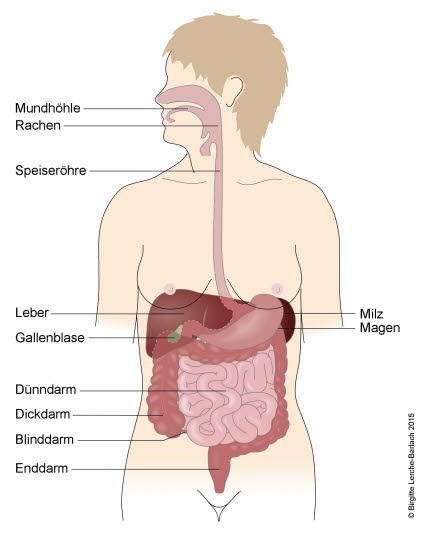
Übersicht Verdauungsorgane
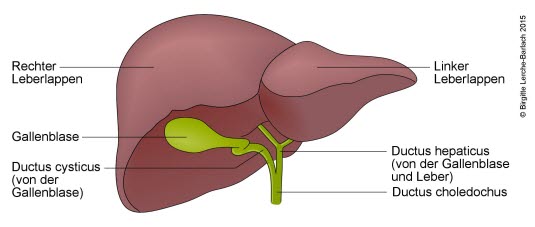
Leber und Gallenblase
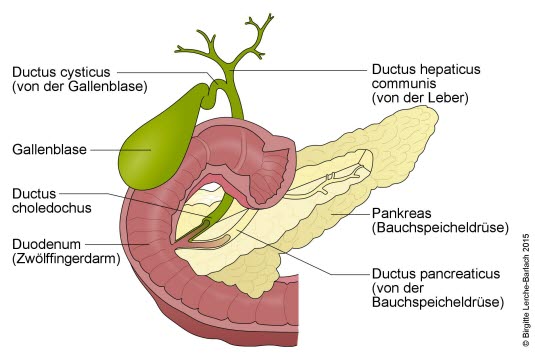
Gallenblase und Bauchspeicheldrüse
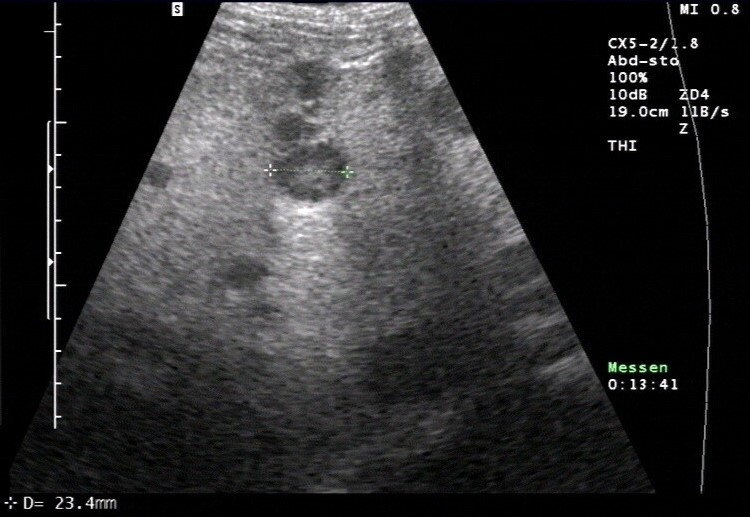
Sonografie: Lebermetastase mit typischem Halo und dorsaler Schallverstärkung (mit freundlicher Genehmigung von sonographiebilder.de ©Albertinen-Diakoniewerk e.V., Hamburg)

Sonografie: Echoarme Metastasen eines Mammakarzinoms in einer Fettleber (mit freundlicher Genehmigung von sonographiebilder.de ©Albertinen-Diakoniewerk e.V., Hamburg)
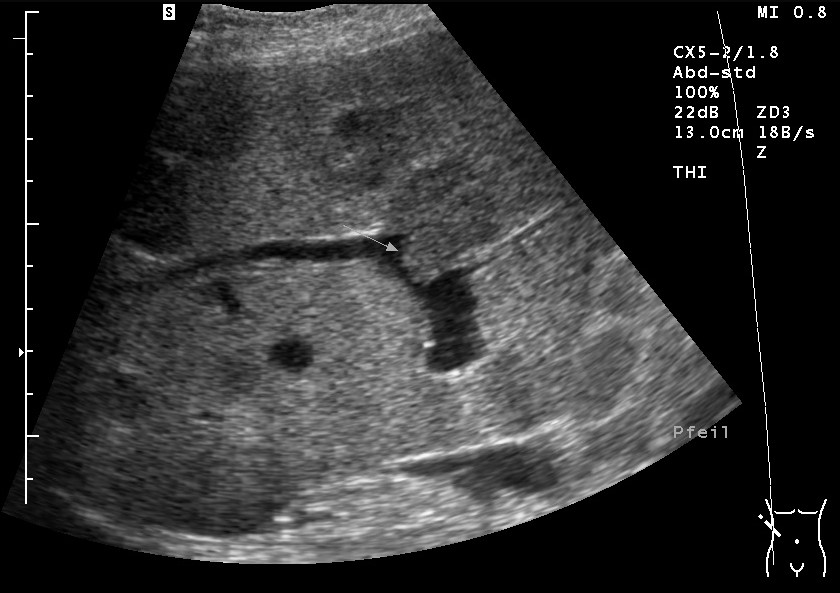
Sonografie: Lebermetastase eines Ovarialkarzinoms mit Gefäßinvasion (mit freundlicher Genehmigung von sonographiebilder.de ©Albertinen-Diakoniewerk e.V., Hamburg)
Quellen
Leitlinien
- Deutsche Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten (DGVS), Deutsche Krebsgesellschaft (DKG). Hepatozelluläres Karzinom und biliäre Karzinome. AWMF-Leitlinie Nr. 032-053OL. S3, Stand 2021. www.awmf.org
- Deutsche Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten (DGVS), Deutsche Krebsgesellschaft (DKG). Magenkarzinom – Diagnostik und Therapie der Adenokarzinome des Magens und ösophagogastralen Übergangs. AWMF-Leitlinie Nr. 032-009OL. S3, Stand 2019. www.awmf.org
- Deutsche Gesellschaft für Palliativmedizin. Palliativmedizin für Patienten mit einer nicht heilbaren Krebserkrankung. AWMF-Leitlinie Nr. 128-001OL. S3, Stand 2019. www.awmf.org
- Deutsche Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten (DGVS). Plattenepithelkarzinome und Adenokarzinome des Ösophagus, Diagnostik und Therapie. AWMF-Leitlinie Nr. 021-023OL. S3, Stand 2018. www.awmf.org
- Deutsche Krebsgesellschaft (DKG), Deutsche Dermatologische Gesellschaft (DDG). Diagnostik, Therapie und Nachsorge des Melanoms. AWMF-Leitlinie Nr. 032-024OL. S3, Stand 2018. www.awmf.org
- Deutsche Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten. Kolorektales Karzinom. AWMF-Leitlinie Nr. 021-007OL. S3, Stand 2017. www.awmf.org
- Deutsche Krebsgesellschaft (DKG), Deutsche Gesellschaft für Gynäkologie und Geburtshilfe (DGGG). Früherkennung, Diagnostik, Therapie und Nachsorge des Mammakarzinoms. AWMF-Leitlinie Nr. 032-045OL. S3, Stand 2017. www.awmf.org
- Deutsche Krebsgesellschaft. Psychoonkologische Diagnostik, Beratung und Behandlung von erwachsenen Krebspatienten. AWMF-Leitlinie Nr. 032-051OL. S3, Stand 2014 (abgelaufen). www.awmf.org
- Deutsche Krebsgesellschaft (DKG), Deutsche Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten (DGVS). Exokrines Pankreaskarzinom. AWMF-Leitlinie Nr. 032-010OL. S3, Stand 2013 (abgelaufen). www.awmf.org
Literatur
- Namasivayam S, Martin DR, Saini S. Imaging of liver metastases: MRI. Cancer Imaging. 2007;7 : 2-9. doi:10.1102/1470-7330.2007.0002. DOI
- Zimmermann TM. Versorgungsabläufe bei kolorektalen Lebermetastasen - Ergebnisse einer standardisierten Patienten-Erhebung. Stand 25.11.2020. Letzter Zugriff 13.07.2021. epub.uni-regensburg.de
- Deutsche Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten (DGVS), Deutsche Krebsgesellschaft (DKG). Hepatozelluläres Karzinom und biliäre Karzinome. AWMF-Leitlinie Nr. 032-053OL. S3, Stand 2021. www.awmf.org
- Deutsche Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten. Kolorektales Karzinom. AWMF-Leitlinie Nr. 021-007OL. S3, Stand 2017. www.awmf.org
- Van Cutsem E, Cervantes A et al. ESMO consensus guidelines for the management of patients with metastatic colorectal cancer. Ann Oncol. 2016 Aug;27(8):1386-422. PubMed PMID: 27380959. PubMed
- Deutsche Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten (DGVS), Deutsche Krebsgesellschaft (DKG). Magenkarzinom - Diagnostik und Therapie der Adenokarzinome des Magens und ösophagogastralen Übergangs. S3 Leitlinie, Registernummer 032 - 009OL, Stand 31.08.2019. www.awmf.org www.awmf.org
- Deutsche Krebsgesellschaft (DKG), Deutsche Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten (DGVS). Exokrines Pankreaskarzinom. AWMF-Leitlinie Nr. 032-010OL. S3, Stand 2013. www.awmf.org
- Deutsche Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten (DGVS). Plattenepithelkarzinome und Adenokarzinome des Ösophagus, Diagnostik und Therapie. AWMF-Leitlinie Nr. 021-023OL. S3, Stand 2018. www.awmf.org
- Deutsche Krebsgesellschaft.Psychoonkologische Diagnostik, Beratung und Behandlung von erwachsenen Krebspatienten. AWMF-Leitlinie Nr. 032-051OL, Stand 2014. www.awmf.org
- Deutsche Gesellschaft für Palliativmedizin.Palliativmedizin für Patienten mit einer nicht heilbaren Krebserkrankung. AWMF-Leitlinie Nr. 128-001OL, Stand 2019. www.awmf.org
- Deutsche Krebsgesellschaft (DKG), Deutsche Dermatologische Gesellschaft (DDG). Diagnostik, Therapie und Nachsorge des Melanoms. AWMF-Leitlinie Nr. 032-024OL. S3, Stand 2018. www.awmf.org
- Deutsche Krebsgesellschaft (DKG), Deutsche Gesellschaft für Gynäkologie und Geburtshilfe (DGGG). Früherkennung, Diagnostik, Therapie und Nachsorge des Mammakarzinoms. www.awmf.org
- Fong Y, Fortner J, Sun RL et al. Clinical score for predicting recurrence after hepatic resection for metastatic colorectal cancer. Ann Surg 1999; 230: 309-21. PubMed
- Berri RN, Abdalla EK. Curable metastatic colorectal cancer: recommended paradigms. Curr Oncol Rep 2009; 11:200. PubMed
- Adam R, de Haas RJ, Wicherts DA, et al. Is hepatic resection justified after chemotherapy in patients with colorectal liver metastases and lymph node involvement? J Clin Oncol 2008; 26:3672. PubMed
- Nagakura S, Shirai Y, Yokoyama N et al. Major hepatic resection reduces the probability of intrahepatic recurrences following resection of colorectal carcinoma liver metastasis. Hepatogastroenterology 2003; 50: 779-83. PubMed
- DeMatteo RP, Palese C, Jarnagin WR et al. Anatomical segmental hepatic resection is superior to wedge resection as an oncological operation for colorectal liver metastasis. J Gastrointest Surg 2000; 4: 178-84. PubMed
- Morris EJ, Forman D, Thomas JD, et al. Surgical management and outcomes of colorectal cancer liver metastases. Br J Surg 2010; 97:1110. PubMed
- Fong Y, Fortner J, Sun RL, Brennan MF, Blumgart LH. Clinical score for predicting recurrence after hepatic resection for metastatic colorectal cancer. Ann Surg 1999; 230: 309-21. PubMed
Autor*innen
- Lino Witte, Dr. med., Arzt in Weiterbildung, Allgemeinmedizin, Frankfurt
- Dietrich August, Dr. med., Arzt in Weiterbildung Innere Medizin, Freiburg
- Die ursprüngliche Version dieses Artikels basiert auf einem entsprechenden Artikel im norwegischen hausärztlichen Online-Handbuch Norsk Elektronisk Legehåndbok (NEL, https://legehandboka.no/).