Prüfungsrelevant für die Facharztprüfung Allgemeinmedizin1
Allgemeine Informationen
Definition
- Synonym: Schilddrüsenüberfunktion
- Die Genese ist vielgestaltig.2-4
- Morbus Basedow, häufigste Ursache bei jüngeren Patient*innen
- autonomes Adenom, häufigste Ursache bei älteren Patient*innen
- jod- bzw. medikamentös induziert (Kontrastmittel, Amiodaron)
- Frühphase einer Autoimmunthyreoiditis Hashimoto, transient
- TSH-produzierende Hypophysenadenome (selten)
- Hyperthyreosis factitia, durch Einnahme größerer Mengen L-Thyroxin
- bei Kindern zudem: G-Protein-assoziierte Schilddrüsendefekte, konstitutiv aktivierende Mutationen des TSH-Rezeptors (häufig familiär)
- Manifeste Hyperthyreose
- Latente Hyperthyreose
Häufigkeit
- Angaben für Europa aus einer Metaanalyse (subklinische und manifeste Hyperthyreosen)7
- jährliche Inzidenz: 51 Fälle pro 100.000 Personen
- Prävalenz: 0,75–1,72 %
- Angaben für Deutschland aus einer Stichprobe von 3.941 asymptomatischen Personen8
- Prävalenz manifeste Hyperthyreose: 0,4 %
- Prävalenz subklinische Hyperthyreose: 1,8 %
- Alter und Geschlecht
- Vor allem jüngere Frauen sind betroffen.
- Häufigste Ursachen
- Schilddrüsenautonomie und M. Basedow9
Ätiologie und Pathogenese
Physiologie
- Die Schilddrüsenhormone Thyroxin (T4) und Trijodthyronin (T3) werden in den Follikelzellen der Schilddrüse produziert.
- T3 ist das aktive Hormon. T4 wird in den peripheren Geweben und Zielorganen in T3 umgewandelt (dejodiert).
- T3 aktiviert intrazelluläre Rezeptoren und reguliert die Gentranskription. Zu seinen wichtigsten Aufgaben gehören die Regulierung der Wärmeproduktion und die Steuerung des Zellstoffwechsels.
- Der größte Teil der Schilddrüsenhormone zirkuliert im Blut an Proteinen gebunden (Albumin, Thyreoglobulin).
- Im Labor wird die freie Fraktion (FT4, FT3) gemessen, da diese von äußeren Faktoren unabhängiger ist.
- Eine Hyperthyreose entsteht durch eine übermäßige Freisetzung von Schilddrüsenhormonen aus der Schilddrüse.
Autonomes Adenom
- Autonomer Schilddrüsenbereich, der nicht mehr der Regulation der Hypophyse unterliegt, sondern unabhängig vom Bedarf Schilddrüsenhormone produziert.
- Typischer Befund ist eine toxische Knotenstruma.
- Der Begriff „toxisch" steht in diesem Zusammenhang für eine Hyperthyreose.
M. Basedow
- Für die häufigste Ursache einer Hyperthyreose bei jungen Menschen siehe Artikel M. Basedow.
- Es kommt zur Schilddrüsenhormonüberproduktion durch Autoantikörper, die sich gegen den TSH-Rezeptor richten und somit zu einer Überaktivierung der Schilddrüse führen.
Thyreoiditis
- Eine Hyperthyreose (meist in milder Form) kann auch auf eine Thyreoiditis zurückzuführen sein, die oft nur vorübergehend zur Überfunktion führt und in vielen Fällen spontan abklingt.
- Der Artikel Thyreoiditis bietet eine Übersicht über die häufigsten Varianten.
Medikamenteninduzierte Hyperthyreose
- Vereinzelt können Medikamente eine Thyreoiditis und Hyperthyreose auslösen.
- Amiodaron
- Enthält 37 % Jod.
- Induziert eine Hyperthyreose vor allem bei Patient*innen mit vorbestehender Schilddrüsenkrankheit (positive Schilddrüsen-Antikörper oder Struma).
- Jod
- Überdosierung mit L-Thyroxin
- akzidentell, z. B. bei Kleinkindern oder auch Menschen mit demenziellen Syndromen
- Patient*innen, die Schilddrüsenpräparate zum Abnehmen missbrauchen.
- Medikamente, die die TSH-Produktion (bei initial normalen peripheren Hormonen) drosseln und somit eine Hyperthyreose vortäuschen können, sind u. a.:9
- Dopamin und Dopaminagonisten
- Serotoninantagonisten
- Somatostatin, Octreotide
- Morphin und Morphinderivate
- Glukokortikoide
- Heparin.
In der Schwangerschaft
- Während der Schwangerschaft kommt es zu einer physiologischen Vergrößerung der Schilddrüse.
- HCG (humanes Choriongonadotropin) hat eine schwach TSH-ähnliche Wirkung auf die Schilddrüse, was zur erhöhten T4-Produktion und TSH-Suppression führt.
- Aufgrund dieser HCG-Wirkung ist der TSH-Normbereich im ersten Trimenon niedriger als im späteren Schwangerschaftsverlauf.
- Eine Blasenmole kann aufgrund der pathologisch erhöhten HCG-Werte zu einer ausgeprägten Hyperthyreose führen.
- Schwangere Patientinnen mit einer Hyperthyreose sollten im Zweifelsfall, unabhängig von der Ursache, zur Endokrinologie überwiesen werden.
Tumoren als Ursache einer Hyperthyreose
- TSH-produzierende Hypophysentumoren
- Können vorkommen, sind aber selten.
- TSH und freie Hormone erhöht
- Weitere seltene Ursachen
- Schilddrüsenkarzinome
- Schilddrüsenhormon produzierende Ovarialtumoren
- Trophoblastentumoren, die vermehrt HCG freisetzen.
Andere Ursachen
- Aktivierende Mutationen am TSH-Rezeptor2
- familiär auftretend
- Angeborene Hyperthyreose3
- seltene Erkrankung, vorwiegend bei mütterlichem Morbus Basedow durch transplazentaren Übertritt schilddrüsenstimulierender Antikörper
- Schilddrüsenhormonresistenz (Refetoff-Syndrom)10
- Genetische, erbliche Störung, bei der die Hypophyse und die peripheren Gewebe auf die Schilddrüsenhormone nicht ansprechen.
- sehr selten, Inzidenz 1:40.000
- erhöhte freie periphere Schilddrüsenhormonspiegel mit einem nicht supprimierten Thyreotropin-Spiegel im Serum
- Die Symptome sind sehr variabel, u. a. Tachykardie, Aufmerksamkeitsstörung mit Hyperaktivität, Kleinwuchs, Schilddrüsenvergrößerung.
Prädisponierende Faktoren
- Hyperthyreose in der Familie
- Schwangerschaft
- Einnahme jodhaltiger Präparate
- Bekannte Knotenstruma
ICPC-2
- T85 Hyperthyreose / Thyreotoxische Krise
ICD-10
- E05 Hyperthyreose
- E05.0 Hyperthyreose mit diffuser Struma, inkl. M. Basedow
- E05.1 Hyperthyreose mit toxischem solitärem Schilddrüsenknoten
- E05.2 Hyperthyreose mit toxischer mehrknotiger Struma
- E05.3 Hyperthyreose durch ektopisches Schilddrüsengewebe
- E05.4 Hyperthyreosis factitia
- E05.5 Thyreotoxische Krise
- E05.8 Sonstige Hyperthyreose
- E05.9 Hyperthyreose, nicht näher bezeichnet
- E06 Thyreoiditis
- E06.0 Akute Thyreoiditis
- E06.1 Subakute Thyreoiditis
- E06.2 Chronische Thyreoiditis mit transitorischer Hyperthyreose
- E06.3 Autoimmunthyreoiditis
- E06.4 Arzneimittelinduzierte Thyreoiditis
- E06.5 Sonstige chronische Thyreoiditis
- E06.9 Thyreoiditis, nicht näher bezeichnet
Diagnostik
Diagnostische Kriterien
- Typische Anamnese und klinische Symptomatik
- Laborveränderungen: TSH-Spiegel supprimiert und FT4- und/oder FT3-Spiegel oberhalb des Referenzbereichs
- bei sekundärer Hyperthyreose aufgrund eines Hypophysen-Adenoms TSH-, FT4- und FT3-Erhöhung
- Sonografie der Schilddrüse, um Hinweise für die Ursache der Hyperthyreose zu erlangen.
Differenzialdiagnosen
- Krankheiten, die die Symptome einer Hyperthyreose imitieren können, u. a.:
- generalisierte Angststörung (Unruhe)
- Phäochromozytom (Tachykardie, vermehrtes Schwitzen).
Anamnese
- Die Symptome einer Hyperthyreose sind vielfältig und können je nach Alter der Betroffenen, der Erkrankungsdauer, der Schwere der Hormonstörung und dem Vorliegen von Komorbiditäten variieren.11
- Bei einem anamnestisch unerklärlichen Gewichtsverlust oder Anzeichen eines Vorhofflimmerns sollte als Diagnose eine Hyperthyreose in Betracht gezogen werden. Plötzlich einsetzende hyperthyreote Symptome können auf eine Thyreoiditis oder einen Morbus Basedow hindeuten.12
- Die Hyperthyreose aufgrund eines autonomen Adenoms entwickelt sich meist schleichender.
- Bei älteren Patient*innen können klassische Symptome fehlen oder erst spät im Krankheitsverlauf auftreten, sodass die klinische Diagnosestellung schwierig sein kann. Häufig sind Müdigkeit und Niedergeschlagenheit die vorherrschenden Symptome. Dies gilt vor allem bei Einnahme von Betablockern, da diese die Symptome einer Hyperthyreose vermindern bzw. verschleiern.12-13
- In der Anamnese sollte auch die Medikamenteinnahme erfragt werden.9
- Medikamente mit hohem Jodanteil: Kontrastmittel, Amiodaron, jodhaltige Nahrungsergänzungsmittel
- Medikamente, die den TSH-Wert erniedrigen können: u. a. Levothyroxin, Glukokortikoide, Dopaminagonisten, Katecholamine oder Somatostatin.
Typische Symptome einer Hyperthyreose
- Wärmeintoleranz
- Erhöhte Schweißneigung
- Palpitationen, Tachykardie
- Vorhofflimmern
- Müdigkeit, Abgeschlagenheit, Schwäche
- Nervosität, Irritabilität, Affektlabilität, Schlafstörungen
- Tremor
- Gewichtsverlust trotz gesteigerten Appetits
- Alkoholintoleranz
- Bei Kindern: Enuresis2
- Gesteigerte Stuhlfrequenz (keine Diarrhö), häufiger Harndrang
- Oligomenorrhö oder Amenorrhö
- Erektile Dysfunktion oder Gynäkomastie bei Männern
Endokrine Orbitopathie9
- Häufigste extrathyreoidale Manifestation des M. Basedow
- Subjektive Aktivitätszeichen: Schmerzen oder Druckgefühl hinter dem Augapfel oder Schmerzen bei Auf-, Ab- oder Seitenblick
- Objektive Entzündungszeichen: Rötung oder Schwellung der Augenlider, diffuse Rötung der Konjunktiva in mindestens einem Quadranten, Chemosis und Karunkelschwellung
Leichtere Symptome
- Bei leichteren Krankheitsverläufen und bei älteren Patient*innen können einige oder viele der typischen Symptome fehlen.
- Weitere Symptome, die auf einer Hyperthyreose beruhen können:
- Osteoporose, Hyperkalzämie, Herzinsuffizienz, oder ansteigender HbA1c-Wert bei Patient*innen mit Diabetes
Klinische Untersuchung
Typischer Befund
- Struma: vergrößerte Schilddrüse, evtl. Druckschmerz oder auskultatorisch erfassbares Gefäßgeräusch beim M. Basedow
- Struma diffusa: palpatorisch häufig weiche Schilddrüse
- Adenome: ein oder mehrere festere Knoten tastbar, Knoten > 1 cm können ggf. ertastet werden, kleinere Knoten sind besser sonografisch darstellbar.
- Thyreoiditis: meist geschwollene, druckschmerzhafte Schilddrüse
- Rastlosigkeit, schnelles Sprechen
- Tremor
- Tachykardie
- Feuchtwarme Haut, warme Hände, dünnes Haar
- Vorhofflimmern
- Arterielle Hypertonie
- Myopathien
Ergänzende Untersuchungen in der Hausarztpraxis
Labor
- TSH und FT4 obligat zur Diagnosestellung
- Ggfs. Auto-Antikörper der Schilddrüse
- Anti-TPO-AK bei V. a. Hashimoto-Thyreoiditis
- Anti-TSH-Rezeptor-AK bei V. a. M. Basedow
- BSG, CRP, Leukozyten
- bei V. a. infektiöse Thyreoiditis
Schilddrüsensonografie
- Beurteilung von Größe, Echogenität, Vorhandensein von Knoten
- Doppler-Sonografie zur Evaluation der Vaskularisierung (Hypervaskularisierung bei M. Basedow)
- Elastografie zur genaueren Beurteilung des Schilddrüsengewebes9
Diagnostik bei Spezialist*innen
Szintigrafie
- Die Szintigrafie eignet sich zur Darstellung des Ausmaßes der Möglichkeit der Schilddrüse bzw. lokalisierter Areale, Jod aus dem Blut aufzunehmen.14
- Gemessen wird der Radiojod- und der Tc-99m-Uptake, die als Äquivalent für die Jodid-Clearance gelten.
- Indikationen für eine Szintigrafie14
- Knoten ≥ 1 cm
- V. a. fokale oder diffuse Autonomie bei Hyperthyreose
- diagnostisch unklare Fälle in der Abklärung eines M. Basedow (DD lymphozytäre Thyreoiditis oder Marine-Lenhardt-Syndrom: M. Basedow und gleichzeitig autonomes Adenom)
- insbesondere hilfreich bei TRAK-negativem M. Basedow
- zur Dokumentation des Therapieerfolgs einer definitiven Therapie (OP, Radiojod)
- ektop gelegenes SD-Gewebe
- konnatale Hypothyreose
Indikationen zur Überweisung/Krankenhauseinweisung
- Zum Zeitpunkt der Diagnosestellung sollten Patient*innen bei Unklarheiten oder ggf. auch zur Therapieeinstellung an eine endokrinologische Praxis überwiesen werden.
- Endokrinologisch versierte Hausärzt*innen können die Behandlung und die Verlaufskontrolle einer Hyperthyreose jedoch auch selbst übernehmen und weitere Maßnahmen koordinieren.
- Bei Verdacht auf eine endokrine Orbitopathie soll an eine Augenarztpraxis überwiesen werden.
- Indikationen zur Krankenhauseinweisung sind u. a.:
- Erstdiagnose Vorhofflimmern
- V. a. thyreotoxische Krise
Überweisung im weiteren Krankheitsverlauf
- Planung einer Schwangerschaft bei Patientinnen mit Hyperthyreose
- Manifeste Hyperthyreose während oder nach einer Schwangerschaft
- Zur Indikationsstellung einer definitiven Therapie (Radiojodtherapie oder Thyreoidektomie)
- Rezidive nach abgeschlossener Radiojodtherapie oder subtotaler Thyreoidektomie
- Augenärztliche Kontrollen beim Morbus Basedow
Checkliste zur Überweisung
Hyperthyreose
- Zweck der Überweisung
- Bestätigende Diagnostik? Therapie?
- Anamnese
- Krankheitsdauer und -beginn? Verlauf?
- Symptombeschreibung, Augensymptome?
- Andere relevante Krankheiten?
- Regelmäßige Medikamente?
- Rauchen?
- Familienanamnese
- Klinische Untersuchung
- Struma oder Knoten in der Schilddrüse?
- Puls, Vorhofflimmern? Blutdruck
- Symptome einer endokrinen Augenerkrankung?
- Allgemeinzustand
- Ergänzende Untersuchungen
Therapie
Therapieziele
- Die euthyreote Stoffwechsellage einstellen.
- Symptomfreiheit erreichen.
- Komplikationen verhindern.
Allgemeines zur Therapie
- Grundsätzlich gibt es 3 Therapiemöglichkeiten:
- Radiojodtherapie und Operation werden als definitive Therapien bezeichnet.
- Die Wahl der Therapie hängt von verschiedenen Faktoren ab:
- Alter der Patient*innen
- Ursache der Hyperthyreose
- Größe der Schilddrüse bzw. Adenome
- Malignomverdacht?
- soziale Faktoren
- ggf. Kontraindikationen gegen einzelne Therapieformen
- Wunsch der Patient*innen.
- In der Regel wird beim M. Basedow mit einer medikamentösen Thyreostatikatherapie versucht, eine Remission zu erreichen.
- Bei medikamentösem Therapieversagen, Patientinnen mit Kinderwunsch oder endokriner Orbitopathie erfolgt eine definitive Therapie.
- Beim Adenom ist immer eine definitive Therapie notwendig und die medikamentöse Thyreostatikatherapie dient nur der Vorbereitung.
Therapieauswahl
- Pro thyreostatische Therapie15
- Morbus Basedow: bei geringem Rezidivrisiko (weiblich, > 40 Jahre, Schilddrüsenvolumen < 40 ml, TRAK < 10 IU/l nach 6 Monaten der konservativen Therapie)
- autonome Adenome: nur zur Herstellung einer Euthyreose bis zur definitiven Therapie
- Kontraindikationen gegen eine Operation oder Radiojodtherapie
- Pro operative Therapie15
- Malignomverdacht
- große Zysten
- Kompressionssymptome
- intrathorakale Struma
- Kindes- und Jugendalter: bei Knoten oder nach erfolgloser konservativer Therapie eines M. Basedow
- Notwendigkeit eines sofortigen Therapieeffekts
- Morbus Basedow: bei hohem Rezidivrisiko, Persistenz oder Rezidiv der Hyperthyreose nach 6–12 Monaten konservativer Therapie, insbesondere bei großer Struma
- Morbus Basedow mit florider endokriner Orbitopathie oder bei Kinderwunsch18
- Ablehnung einer Radiojodtherapie
- Pro Radiojodtherapie15
- Morbus Basedow: bei hohem Rezidivrisiko, Persistenz oder Rezidiv der Hyperthyreose nach 6–12 Monaten konservativer Therapie, insbesondere bei kleiner oder mittlerer Struma
- Schilddrüsenautonomie/Knotenstruma, bei stoffwechselrelevanter Autonomie (TSH-Spiegel ≤ 0,4 mU/l)
- Voroperationen an der Schilddrüse
- Kontraindikationen oder Ablehnung einer Operation
- Detaillierte Informationen zur Therapie der subklinischen Hyperthyreose
- Detaillierte Informationen zur Therapie des M. Basedow
- Detaillierte Informationen zur Therapie der Knotenstruma
Empfehlungen für Patient*innen
- Bei Beginn der thyreostatischen Behandlung sollten die Patient*innen über die Symptome einer Agranulozytose (Fieber, Pharyngitis oder Zystitis) und Hepatitis (Ikterus, acholischer Stuhl oder dunkler Urin) aufgeklärt werden.19
- Dabei handelt es sich um mögliche relevante Nebenwirkungen der medikamentösen Therapie.
- Bei Auftreten der Symptome sollten die Thyreostatika sofort abgesetzt und ein ärztlicher Kontakt gesucht werden.19
Medikamentöse Therapie
Thyreostatika
- Präparate
- Carbimazol/Thiamazol
- Carbimazol ist Prodrug von Thiamazol, die Umwandlung erfolgt durch die Leber.
- Hemmung der Biosynthese der Schilddrüsenhormone durch Inhibition der Thyreoperoxidase (verantwortliches Enzym für Iodierung der Schilddrüsenhormone)
- Aufgrund des günstigeren Nebenwirkungsprofils Medikamente der Wahl19
- Leberschädigung bei 0,4 % der Patient*innen im Gegensatz zu 2,7 % bei Einnahme von Propylthiouracil20
- Propylthiouracil (PTU)
- Carbimazol/Thiamazol
- Dosierung
- Carbimazol laut Fachinformation21
- Im Allgemeinen reichen bei der niedrigen Jodversorgung in Deutschland 40 bis maximal 60 mg Carbimazol aus, um die Schilddrüsenhormonsynthese zu hemmen.
- Die Dosierungsempfehlungen sind abhängig vom Therapieprinzip:
- Nach einer höher dosierten Initialtherapie (etwa in Höhe der voll blockierenden Dosis) Fortsetzung der Behandlung mit einer Erhaltungsdosis von 5–20 mg Carbimazol pro Tag; hierbei ist gewöhnlich die Supplementierung mit Schilddrüsenhormonen erforderlich.
- Monotherapie mit Tagesdosen von 2,5–10 mg Carbimazol.
Die Dosis richtet sich nach der individuell zu kontrollierenden Stoffwechsellage der Patient*innen, wobei dem Verhalten des TSH besondere Beachtung zu schenken ist.
- Es ist bisher nicht entschieden, welches Therapieverfahren bessere Resultate (im Sinne einer Dauerremission der Hyperthyreose) liefert.
- Thiamazol laut Fachinformation22
- Die Anfangsbehandlung einer Hyperthyreose (auch vor einer Schilddrüsenoperation bzw. vor und nach einer Radioiodtherapie) erfolgt je nach Schweregrad der Erkrankung mit 20–40 mg Thiamazol pro Tag, verteilt auf regelmäßige Einzelgaben von 5–20 mg.
- Nach Normalisierung der Schilddrüsenfunktionslage (in der Regel nach 3–8 Wochen) beträgt die Erhaltungsdosis zwischen 2,5 und 10 mg Thiamazol pro Tag als Einzeldosis.
- Bei Erreichen der euthyreoten Stoffwechsellage kann eine antistrumigene Zusatztherapie mit Schilddrüsenhormonen (zwischen 50 und 100 Mikrogramm Levothyroxin) einsetzen.
- Propylthiouracil laut Fachinformation23
- Anfangsdosis bei geringer klinischer Aktivität der Hyperthyreose
- 100–300 mg Propylthiouracil/d, entsprechend 2–3 Einzeldosen zu je 50–100 mg
- Anfangsdosis in schweren Fällen und nach Jodkontamination
- 300–600 mg Propylthiouracil/d, verteilt auf 4–6 Einzeldosen
- Erhaltungsdosis
- 50–150 mg Propylthiouracil/d
- Anfangsdosis bei geringer klinischer Aktivität der Hyperthyreose
- Carbimazol laut Fachinformation21
- Verlaufskontrolle
- Vor Therapiebeginn soll die Leukozytenzahl bestimmt werden.
- Cave: Nebenwirkung Agranulozytose bei thyreostatischer Therapie!
- Zur Therapieüberwachung werden FT4 (und evtl. FT3) bestimmt: Ziel ist es, FT4 im oberen Normbereich zu halten.24
- Eine Kombinationsbehandlung mit Thyroxin kann erforderlich sein, um die Stoffwechsellage zu stabilisieren, eine Hypothyreose zu vermeiden und FT4 im oberen Normbereich zu halten.
- Eine Hypothyreose unter Therapie ist zu vermeiden, da diese das Strumawachstum begünstigt und sich beim M. Basedow ungünstig auf eine endokrine Orbitopathie auswirkt.
- Vor Therapiebeginn soll die Leukozytenzahl bestimmt werden.
- Dauer
- Durch Thyreostatika lässt sich die Hyperthyreose innerhalb weniger Wochen bei 90 % der Patient*innen unter Kontrolle bringen.25
- Die optimale Behandlungsdauer scheint bei 12–18 Monaten zu liegen.26
- Eine Therapie mit Thyreostatika über Jahre ist grundsätzlich nicht zu empfehlen und beschränkt sich allenfalls auf hochbetagte, meist multimorbide Patient*innen mit begrenzter Lebenserwartung.9
- Nebenwirkungen und Komplikationen
- Pruritus, Hautexantheme, Arthralgien, Myalgien, Cholestase, Geschmacksstörungen
- Die Behandlung sollte dann abgebrochen werden.
- Nach Abklingen der Nebenwirkungen kann zu einem anderen Thyreostatikum gewechselt oder eine definitive Therapie angestrebt werden.
- Agranulozytose
- Leberschädigung
- leichte Transaminasenerhöhung bei bis zu 30 % der mit PTU behandelten Patient*innen27
- ausgeprägte Hepatotoxizität bei 2,7 % der Patient*innen20
- Aufgrund der Hepatotoxizität gilt PTU nur als Reservemedikament.2,15
- Auch Carbimazol kann zu einer reversiblen Cholestase und in seltenen Fällen zu einer akut entzündlichen Hepatitis führen.28
- Rote-Hand-Brief vom 06.02.2019: zwei Warnhinweise bezüglich Carbimazol- und Thiamazol-haltigen Arzneimitteln
- Es liegen Fallberichte über das Auftreten einer akuten Pankreatitis nach Behandlung mit Carbimazol- oder Thiamazol-haltigen Arzneimitteln bevor.
- Bei Auftreten einer akuten Pankreatitis sollte die Behandlung mit diesen Arzneimitteln sofort beendet und jede erneute Exposition vermieden werden.
- Carbimazol- und Thiamazol-haltige Arzneimittel stehen im Verdacht, angeborene Fehlbildungen zu verursachen, wenn sie während der Schwangerschaft und insbesondere im ersten Trimenon und in hoher Dosierung verabreicht wurden.
- Frauen im gebährfähigen Alter müssen während einer Behandlung mit diesen Arzneimitteln eine wirksame Methode der Kontrazeption anwenden.
- Diese Arzneimittel dürfen in der Schwangerschaft nur nach strenger individueller Nutzen-Risiko-Bewertung, in der niedrigst möglichen Dosierung und ohne zusätzliche Schilddrüsenhormone angewendet werden.
- Es liegen Fallberichte über das Auftreten einer akuten Pankreatitis nach Behandlung mit Carbimazol- oder Thiamazol-haltigen Arzneimitteln bevor.
Symptomatische Behandlung
- Indikation
- bei ausgeprägter Hyperthyreose und adrenergen Symptomen wie Tremor, Palpitationen, Wärmeintoleranz und Nervosität
- Betablocker
- Propranolol
- 3–4 x/d jeweils 10–40 mg29
- langsame Dosissteigerung bis zur Symptomkontrolle
- Propranolol
- Kalziumblocker?
- Diltiazem kann bei Unverträglichkeit von Betablockern zum Absenken der Herzfrequenz eingesetzt werden.30
- Cave: Off-Label-Einsatz!
- Loperamid
- Kann bei Diarrhö und vermutlich zu schneller Darmpassage der Thyreostatika probatorisch verwendet werden.
- Sollte nicht langfristig eingesetzt werden.
Bei Thyreoiditis
- Eine Thyreoiditis ist initial oft mit einer leichten Hyperthyreose verbunden, die mit Propranolol behandelt werden kann.
- Thyreostatika werden nicht eingesetzt.
- Im Verlauf häufig Hypothyreose, dann Einsatz von Levothyroxin
Behandlung in der Schwangerschaft
- Cave: Sowohl die maternalen TSH-Rezeptor-Antikörper (TRAK), die Thyreostatika und die Schilddrüsenhormone (FT3, FT4) sind plazentagängig.19
- Das erhöhte Risiko bei manifester maternaler Hyperthyreose für u. a. Abort und intrauterine Wachstumsstörungen macht eine konsequente Behandlung dringend erforderlich.
- Laut Bulletin zur Arzneimittelsicherheit von Dezember 2019 werden folgende Empfehlungen zur Thyreostatikagabe in der Schwangerschaft gegeben:31
- Patientinnen im gebärfähigen Alter, die mit Thiamazol (TMZ) bzw. Carbimazol (CMZ) behandelt werden, sollten für die Zeit der Behandlung eine effektive Verhütung anwenden, weil die Behandlung mit TMZ bzw. CMZ mit angeborenen Fehlbildungen assoziiert sein kann, wenn sie während der Schwangerschaft und insbesondere im ersten Trimenon der Schwangerschaft und in hoher Dosierung verabreicht werden.
- Eine routinemäßige Einstellung auf PTU sollte bei Patientinnen ohne Kinderwunsch vermieden werden, da die Anwendung von PTU mit einem höheren Risiko für akutes Leberversagen assoziiert ist.
- Patientinnen mit Morbus Basedow, die eine Schwangerschaft planen, sollte eine Beratung angeboten werden. Während dieser Beratung sind die Komplexität des Managements des Morbus Basedows während der Schwangerschaft und die vorhandenen therapeutischen Alternativen zu
diskutieren.- Grundsätzlich sollte eine Verschiebung der Empfängnis empfohlen werden, bis die mütterliche Grunderkrankung ausreichend kontrolliert ist bzw. definitiv behandelt wurde.
- Eine manifeste Hyperthyreose während der Schwangerschaft bedarf einer adäquaten Behandlung, um dem Auftreten von schweren mütterlichen und fetalen Komplikationen entgegenzuwirken.
- Wird eine Schwangerschaft unter thyreostatischer Therapie in Erwägung gezogen, sollten Patientinnen, die mit TMZ bzw. CMZ behandelt werden, nach individueller Nutzen-Risiko-Abwägung vor Empfängnis auf PTU umgestellt werden, da die derzeit vorhandene Datenlage auf ein
allenfalls gering erhöhtes Fehlbildungspotenzial von PTU hindeutet. - Die derzeitige Evidenz erlaubt keine verlässliche Aussage bezüglich des Nutzens der Umstellung von TMZ bzw. CMZ auf PTU im ersten Trimenon einer bereits bestehenden Schwangerschaft.
- Diesbezüglich sollte nach einer individuellen Nutzen-Risiko-Abwägung unter Beachtung des potenziellen Risikos für eine temporäre inadäquate Kontrolle der Schilddrüsenfunktion während der Umstellung entschieden werden.
- Die Anwendung von TMZ bzw. CMZ im ersten Trimenon der Schwangerschaft sollte auf die Fälle einer Unverträglichkeit gegenüber PTU begrenzt sein.
- Die Umstellung von PTU auf TMZ bzw. CMZ nach Vollendung der sensiblen Phase der Organogenese kann unter individueller Nutzen-Risiko-Abwägung erwogen werden, um das Risiko des mütterlichen Leberversagens zu reduzieren. Das potenzielle Risiko einer temporären Entgleisung der Schilddrüsenfunktion während der Umstellung sollte jedoch beachtet werden.
- Eine thyreostatische Therapie bei Schwangeren sollte grundsätzlich mit der niedrigsten wirksamen Dosis ohne zusätzliche Verabreichung von Schilddrüsenhormonen erfolgen.
- Ein engmaschiges Monitoring von Mutter, Fetus und Neugeborenem ist notwendig, falls eine thyreostatische Therapie bei Schwangeren angewendet wird.
Radiojodtherapie
- Indikationen
- Siehe Abschnitt Pro Radiojodtherapie.
- Durchführung
- Durchführung unter stationären Strahlenschutzbedingungen als Einzeittherapie auf einer nuklearmedizinischen Therapiestation15
- Systemische Applikation des Beta- und Gamma-Strahlers I–131 als Natriumiodid, um hohe intrathyreoidale Strahlendosen zu erreichen.15
- Verabreichung in der Regel p. o. (Kapsel oder flüssig)
- tägliche Messung von Uptake und effektiver Halbwertszeit
- bei Bedarf: Nachtherapie während des gleichen stationären Aufenthaltes
- Entlassung bei einer Dosisleistung von ≤ 3,5 μSv/h in 2 m Abstand
- Radioaktives Jod wird von den Follikelzellen aufgenommen, sodass die Strahlung ausschließlich das Schilddrüsengewebe schädigt.32-33
- Die volle Wirkung tritt im Laufe von 4–12 Wochen ein.
- Nebenwirkungen
- Infolge der Behandlung kommt es häufig zur Entwicklung einer permanenten Hypothyreose.
- Weitere Nebenwirkungen sind selten, und die Behandlung scheint das Krebsrisiko nicht zu erhöhen.34
- Mögliche Nebenwirkungen sind leichte Schmerzen im vorderen Halsbereich aufgrund einer Strahlenthyreoiditis und eine vorübergehend verstärkte Hyperthyreose (kann durch Vorbehandlung mit Thyreostatika vorgebeugt werden).
- erhöhtes Risiko für die Entwicklung eines Hyperparathyreoidismus35
- Infolge der Behandlung kommt es häufig zur Entwicklung einer permanenten Hypothyreose.
- Kontraindikationen
- Schwangerschaft und Stillzeit
- Innerhalb der ersten 6 Monate nach der Radiojodtherapie wird von einer Schwangerschaft abgeraten (gilt auch für Männer, die mit Radiojod therapiert wurden).
- Frauen, die ihre Familienplanung noch nicht abgeschlossen haben (relative Kontraindikation).
- endokrine Orbitopathie (kann sich durch die Therapie verschlimmern)30
- Wird bei bestehender Orbitopathie dennoch eine Radiojodbehandlung durchgeführt, sollten gleichzeitig Kortikosteroide in relativ hoher Dosierung verabreicht werden.15
- Schwangerschaft und Stillzeit
Operative Therapie
- Indikationen
- Siehe Abschnitt Pro operative Therapie.
- Durchführung17
- unifokale Autonomie: subtotale Lappenresektion oder Hemithyreoidektomie
- multifokale Autonomie und Morbus Basedow: Thyreoidektomie oder fast-totale Thyreoidektomie (hohes Rezidivrisiko im verbliebenen Restgewebe)
- Vorbehandlung17
- Präoperativ ist das Erreichen einer klinischen Euthyreose anzustreben.
- Wirksamkeit
- Die Thyreoidektomie ist in mehr als 90 % der Fälle kurativ.36
- Komplikationen
- Abhängig von der Menge des verbliebenen Schilddrüsengewebes entwickeln die meisten Patient*innen eine postoperative Hypothyreose.
- Hypoparathyreoidismus
- Schädigung des Nervus laryngeus recurrens
- vorübergehende Hypokalzämie
- generelle OP-Risiken wie Blutung oder Infektion
Verlauf, Komplikationen und Prognose
Verlauf
- Der Krankheitsverlauf kann je nach Ursache variieren.
- Bei einigen Patient*innen ist eine Spontanheilung zu beobachten, bei den meisten jedoch hält die Erkrankung an.
- Augen-, Herz- und psychische Komplikationen können auch bei kontrollierter Hyperthyreose fortbestehen.
Komplikationen
- Thyreotoxische Krise
- lebensbedrohliche Dekompensation einer Hyperthyreose
- Endokrine Orbitopathie
Prognose
- Bei adäquater Behandlung und regelmäßigen Verlaufskontrollen ist die Prognose günstig.
- Nach einer Radiojodtherapie oder Operation entwickeln viele der Patient*innen eine Hypothyreose. Dies macht eine lebenslange Thyroxinbehandlung erforderlich.
- Bei insuffizient behandelten Patient*innen mit Hyperthyreose ist das Risiko für einen kardiovaskulär bedingten Tod erhöht.37
Verlaufskontrolle
- In den meisten Fällen erfolgt die Therapie in Kooperation mit endokrinologischen Spezialist*innen.
- Nach Rücksprache mit Spezialist*in können die Verlaufskontrollen in der hausärztlichen Praxis erfolgen.
Thyreostatische Therapie
- Die Thyreostatikadosis wird anhand des fT4-Werts, der anfangs alle 3–4 Wochen bestimmt wird, bis zum Erreichen der Erhaltungsdosis titriert.
- Das Behandlungsziel ist, FT4 im oberen Normbereich zu halten.
- Nach Erreichen der Erhaltungsdosis sollten die Patient*innen in Abständen von 3–6 Monaten kontrolliert werden.
- Unter thyreostatischer Therapie sollen regelmäßig Blutbild (cave: Agranulozytose), und Leberwerte (cave: Hepatitis) kontrolliert werden.
Nach Radiojodtherapie oder operativer Therapie
- Kontrollen nach Maßgabe des behandelnden Zentrums
- Die meisten Patient*innen entwickeln nach einer definitiven Therapie eine Hypothyreose, die eine lebenslange Hormonsubstitution erfordert
- Steuerung der Hormonsubstitution mittels FT4 und TSH
Patienteninformationen
Patienteninformationen in Deximed
Patienteninformationen des IQWIG
- Gesundheitsinformation.de: Schilddrüsenüberfunktion
Patientenorganisationen
- Schilddrüsen-Liga Deutschland e. V.: Dachverband der Selbsthilfegruppen Deutschland
- Die Schmetterlinge e. V.: Selbsthilfeorganisation für Kinder und Erwachsene mit Schilddrüsenerkrankungen
Illustrationen
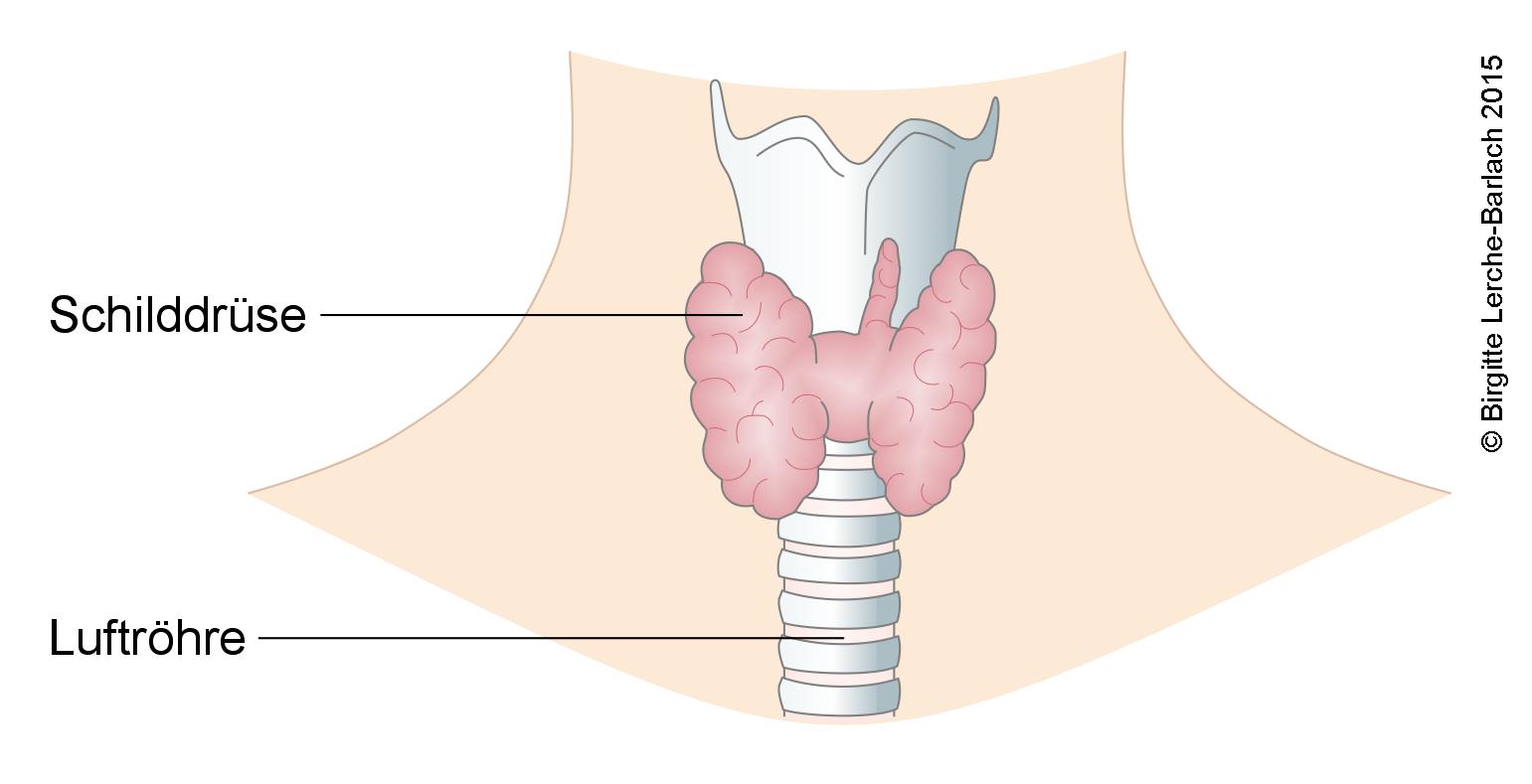
Thyreoidea, Schilddrüse
Quellen
Leitlinien
- Deutsche Gesellschaft für Kinder- und Jugendmedizin (DGKJ). Hyperthyreose. AWMF-Leitlinie Nr. 027-041. S1, Stand 2011. www.awmf.org
- Deutsche Gesellschaft für Kinder- und Jugendmedizin (DGKJ). Angeborene Hyperthyreose. AWMF-Leitlinie Nr. 027-042. S1, Stand 2011. www.awmf.org
- Deutsche Gesellschaft für Kinder- und Jugendmedizin e.V. (DGKJ). Autoimmunthyreoiditis. AWMF-Leitlinie Nr. 027 - 040. S1, Stand 2011. www.awmf.org
- Deutsche Gesellschaft für Nuklearmedizin e. V. (DGN). Schilddrüsenszintigraphie. AWMF-Leitlinie Nr. 031-011. S1, Stand 2014. www.awmf.org
- Deutsche Gesellschaft für Nuklearmedizin e. V. (DGN). Radioiodtherapie bei benignen Schilddrüsenerkrankungen. AWMF-Leitlinie Nr. 031-003. S1, Stand 2015. www.awmf.org
- Deutsche Gesellschaft für Nuklearmedizin (DGN). Radioiodtest. AWMF-Leitlinie Nr. 031-012. S1, Stand 2014. www.awmf.org
- Deutsche Gesellschaft für Allgemein- und Viszeralchirurgie e.V. (DGAV). Benigne Schilddrüsenerkrankungen, operative Therapie. AWMF-Leitlinie Nr. 088-007. S2k, Stand 2015. www.awmf.org
Literatur
- Lohnstein M, Eras J, Hammerbacher C. Der Prüfungsguide Allgemeinmedizin - Aktualisierte und erweiterte 3. Auflage. Augsburg: Wißner-Verlag, 2018.
- Deutsche Gesellschaft für Kinder- und Jugendmedizin (DGKJ). Hyperthyreose. AWMF-Leitlinie Nr. 027-041. S1, Stand 2011. www.awmf.org
- Deutsche Gesellschaft für Kinder- und Jugendmedizin (DGKJ). Angeborene Hyperthyreose. AWMF-Leitlinie Nr. 027-042. S1. Stand 2011 www.awmf.org
- Deutsche Gesellschaft für Kinder- und Jugendmedizin e.V. (DGKJ). Autoimmunthyreoiditis. AWMF-Leitlinie Nr. 027 - 040. S1. Stand 2011. www.awmf.org
- Theiler-Schwetz V, Trummer C, Pilz S. Hyperthyreose – Fokus Immunthyreopathie Basedow. Journal für Klinische Endokrinologie und Stoffwechsel volume 2020; 13: 96-105. link.springer.com
- Biondi B, Bartalena L, Cooper DS, et al. The 2015 european thyroid association guidelines on diagnosis and treatment of endogenous subclinical hyperthyroidism. Eur Thyroid J 2015; 4(3): 149-63. pubmed.ncbi.nlm.nih.gov
- Garmendia Madariaga A, Santos Palacios S, et al. The incidence and prevalence of thyroid dysfunction in Europe: a meta-analysis. J Clin Endocrinol Metab 2014; 99: 923-31. pubmed.ncbi.nlm.nih.gov
- Völzke H, Lüdemann J, Robinson DM, et al. The prevalence of undiagnosed thyroid disorders in a previously iodine-deficient area. Thyroid 2003; 13: 803-10. pubmed.ncbi.nlm.nih.gov
- Schmidt M. So erkennen und behandeln Sie die Hyperthyreose. CME 2017; 14: 9-23. link.springer.com
- Bettendorf M, Pohlenz J. Krankheiten der Schilddrüse. Berlin, Heidelberg: Springer, 2020.
- Reid JR, Wheeler SF. Hyperthyroidism: Diagnosis and treatment. Am Fam Physician 2005; 72: 623-30. PubMed
- Vaidya B, Pearce SH. Diagnosis and management of thyrotoxicosis. BMJ. 2014;349:g5128. doi: 10.1136/bmj.g5128. www.ncbi.nlm.nih.gov
- US Preventive Services Task Force. Screening for thyroid disease: Recommendation statement. Ann Intern Med 2004; 140:125-27. Helfand M. Screening for subclinical thyroid dysfunction in nonpregnant adults: A summary of the evidence for the US Preventive services task force. Ann Intern Med 2004; 140:128-41. www.ncbi.nlm.nih.gov
- Deutsche Gesellschaft für Nuklearmedizin e. V. (DGN). Schilddrüsenszintigraphie. AWMF-Leitlinie Nr. 031-011. S1. Stand 2014 www.nuklearmedizin.de
- Deutsche Gesellschaft für Nuklearmedizin e. V. (DGN). Radioiodtherapie bei benignen Schilddrüsenerkrankungen. AWMF-Leitlinie Nr. 031 - 003. S1. Stand 2015. www.awmf.org
- Deutsche Gesellschaft für Nuklearmedizin (DGN). Radioiodtest. AWMF-Leitlinie Nr. 031-012. S1, Stand 2014. www.nuklearmedizin.de
- Deutsche Gesellschaft für Allgemein- und Viszeralchirurgie e.V. (DGAV). Benigne Schilddrüsenerkrankungen, operative Therapie. AWMF-Leitlinie Nr. 088 - 007. S2k. Stand 2015 www.awmf.org
- Burch HB, Burmann KD, Cooper DS. A 2011 survey of clinical practice patterns in the management of Graves' disease. J Clin Endocrinol Metab 2012; 97: 4549. pmid:23043191 PubMed
- Allelein S, Schott M. Update Morbus Basedow. Dtsch Med Wochenschr 2019; 144(3): 152-5. www.thieme-connect.com
- Ross DS, Burch HB, Cooper DS et al. 2016 American Thyroid Association Guidelines for Diagnosis and Management of Hyperthyroidism and Other Causes of Thyrotoxicosis. Thyreoid 2016; 26: 1343-1421. pubmed.ncbi.nlm.nih.gov
- Fachinformation Carbimazol. Sanofi. Stand 2019. Letzter Zugriff 17.12.2020. mein.sanofi.de
- Fachinformation Thiamazol. Sanofi. Stand 2019. Letzter Zugriff 17.12.2020. mein.sanofi.de
- Diagnosia. Fachinformation Propylthiouracil. Zuletzt aktualisiert 09/2020. Letzter Zugriff 17.12.2020. info.diagnosia.com
- Woeber KA. Update on the management of hyperthyroidism and hypothyroidism. Arch Intern Med 2000; 160: 1067-71. PubMed
- Cooper DS. Antithyroid drugs. N Engl J Med 2005; 352: 905-17. New England Journal of Medicine
- Abraham P, Avenell A, McGeoch SC, Clark LF, Bevan JS. Antithyroid drug regimen for treating Graves' hyperthyroidism. Cochrane Database of Systematic Reviews 2010, Issue 1. Art. No.: CD003420. DOI: 10.1002/14651858.CD003420.pub4 DOI
- Liaw YF, Huang MJ, Fan KD, Li KL, Wu SS, Chen TJ. Hepatic injury during propylthiouracil therapy in patients with hyperthyroidism. A cohort study. Ann Intern Med 1993; 118: 424-8. www.ncbi.nlm.nih.gov
- Woeber KA. Methimazole-induced hepatotoxicity. Endocr Pract 2002; 8: 222-4. PubMed
- Fachinformation Propranolol. Teva GmbH. Stand 2013. Letzter Zugriff 19.12.2020. s3.eu-central-1.amazonaws.com
- Ginsberg J. Diagnosis and management of Graves' disease. CMAJ 2003; 168: 575-85. www.cmaj.ca
- Frizler M. Thyreostatische Behandlung des Morbus Basedow während der Schwangerschaft. Bulletin zur Arzneimittelsicherheit. Informationen aus BfArM und PEI 2019; 4: 14-29. www.bfarm.de
- Allahabadia A, Daykin J, Sheppard MC, Gough SC, Franklyn JA. Radioiodine treatment of hyperthyroidism-prognostic factors for outcome. J Clin Endocrinol Metab 2001; 86: 3611-7. PubMed
- Metso S, Jaatinen P, Huhtala H, Luukkaala T, Oksala H, Salmi J. Long-term follow-up study of radioiodine treatment of hyperthyroidism. Clin Endocrinol (Oxf) 2004; 61: 641-8. www.ncbi.nlm.nih.gov
- Bahn Chair RS, Burch HB, Cooper DS, et al. Hyperthyroidism and other causes of thyrotoxicosis: management guidelines of the American Thyroid Association and American Association of Clinical Endocrinologists. Thyroid 2011; 21: 593. PubMed
- Colaco SM, Si M, Reiff E, Clark OH. Hyperparathyroidism after radioactive iodine therapy. Am J Surg 2007; 194: 323-7. PubMed
- Palit TK, Miller CC 3rd, Miltenburg DM. The efficacy of thyroidectomy for Graves' disease: A meta-analysis. J Surg Res 2000; 90: 161-5. PubMed
- Lee SL. Hyperthyroidism and Thyrotoxicosis. Medscape, last updated Oct 19, 2020. emedicine.medscape.com
Autor*innen
- Lino Witte, Dr. med., Arzt in Weiterbildung, Innere Medizin, Frankfurt
- Die ursprüngliche Version dieses Artikels basiert auf einem entsprechenden Artikel im norwegischen hausärztlichen Online-Handbuch Norsk Elektronisk Legehåndbok (NEL, https://legehandboka.no/).