Allgemeine Informationen
Definition
- Inflammatorisch-proliferative Erkrankung mit teils destruierend wachsenden Granulomen um klonal vermehrte Langerhanszell-Histiozyten1-3
- Es handelt sich um ein Spektrum von Erkrankungsformen, das von lokal begrenzten Einzelherden bis zu einem lebensbedrohlichen Multiorgan-Befall reicht.3
- Es kann jedes Organ betroffen sein; am häufigsten sind Haut, Knochen, Lunge und zentrales Nervensystem (v. a. Hypophyse) befallen.3-4
- Wegweisend sind der immunhistologische oder elektronmikroskopische Nachweis von Langerhanszell-Histiozyten mit umgebender Entzündungsreaktion (lymphozytäres und eosinophiles Infiltrat).
- Es ist umstritten, ob es sich um eine neoplastische oder immunologisch vermittelte Erkrankung handelt.1-3,5
- Historische Bezeichnungen
- Histiozytosis X ‒ historische Sammelbezeichnung für histiozytär-proliferative Erkrankungen. Das X sollte einen vermuteten, damals unbekannten gemeinsamen Auslöser verdeutlichen.2
- Eosinophiles Granulom – lokal begrenzte Erkrankungsform; meist solitäre Läsionen in den Knochen1
- Abt-Letterer-Siwe-Krankheit ‒ eine akute, progressive Multisystem-Variante mit hoher Letalität, die insbesondere Säuglinge/Kleinkinder trifft.1-2
- Hand-Schüller-Christian-Krankheit – eine multifokale Form mit Exophtalmus, Knochenläsionen und Diabetes insipidus1-2
Häufigkeit
- Selten; am häufigsten sind Kinder oder junge Erwachsene betroffen,
- Geschätzte Inzidenz
- Männliche Patienten sind etwas häufiger betroffen (1,2:1).6,8
- Bei Kindern
- Systemisch-disseminierte Formen sind im Neugeborenenalter am häufigsten.5-6
- Bei Erwachsenen
- medianes Erkrankungsalter 34 Jahre8
Ätiologie und Pathogenese
- Die Pathogenese ist unzureichend verstanden.1-3
- Die Erkrankung zeigt sowohl Merkmale eines fehlregulierten Immunsystems als auch von Tumorerkrankungen. Nach wie vor ist umstritten, ob sie als Neoplasie (ähnlich z. B. dem Hodgkin-Lymphom) oder als immunvermittelte Erkrankung (ähnlich z. B. der Sarkoidose) eingeordnet werden sollte.1-2,5
- Es kommt zu einer Proliferation von mononukleären Gewebsmakrophagen (Histiozyten). Da diese mit ihren Oberflächen-Antigenen und elektronmikroskopisch den dendritischen Zellen der Haut, den Langerhans-Zellen, ähneln, wurde der Name Langerhanszell-Histiozytose gewählt.1-2
- Es ist jedoch unklar, ob die pathologischen Langerhans-Zell-Histiozyten von dendritischen Zellen der Haut oder von myeloiden Zellen aus dem Knochenmark abstammen. Möglich ist auch, dass lokal begrenzte Formen ihren Ursprung in Langerhans-Zellen der Haut haben, während disseminierte Formen aus hämatopoetischen Stammzellen des Knochenmarks entstehen.1
- Für ein Verständnis als Neoplasie spricht, dass Langerhanszell-Histiozyten klonal vermehrt sind und häufig somatische Mutationen in Proto-Onkogenen aufweisen, insbesondere im Gen BRAF. In bis zu 85 % der Fälle zeigen sich genetische Veränderungen dieser Achse RAS-RAF-MEK, die das Zellwachstum begünstigen.1,9
- Gegen eine neoplastische Erkrankung spricht die variable klinische Ausprägung, das Vorkommen von Spontanremission und hohe Überlebensraten bei Patient*innen ohne Organdysfunktion.1-2,5
- Um die Langerhanszell-Histiozyten zeigt sich ein ausgeprägtes inflammatorisches Infiltrat mit T-Lymphozyten, Eosinophilen und Granulombildung. Man nimmt an, dass lokal und systemisch vermehrte proinflammatorische Proteine zu Entzündungsreaktion und systemischen Beschwerden beitragen („Zytokinsturm“).1-2
- Für einen infektiösen Ursprung der Erkrankung fanden sich keine Belege.2
Langerhans-Zellen
- Dendritische Zellen der Epidermis, zum ersten Mal beschrieben von Langerhans (1868).
- Charakteristisch ist die Expression des Oberflächenproteins Langerin (CD207). Elektronmikroskopisch zeigen sich sog. Birbeck-Granula.1-2,5
- Langerhans-Zellen sind Teil des angeborenen Immunsystems und überwachen das Gewebe auf Gefahren. Durch Kontakt mit einem Antigen werden sie aktiviert und wandern in lokale Lymphknoten, wo sie Antigene anderen Immunzellen, insbesondere T-Lymphozyten, präsentieren. Hierdurch kann eine spezifische Immunreaktion generiert werden.10-12
Prädisponierende Faktoren
- Rauchen bei der Entwicklung einer pulmonalen Langerhanszell-Histiozytose
ICPC-2
- B99 Blut-/Lymph-/Milz-Erkrankung, andere
ICD-10
- C96 Sonstige und nicht näher bezeichnete bösartige Neubildungen des lymphatischen, blutbildenden und verwandten Gewebes
- C96.0 Multifokale und multisystemische (disseminierte) Langerhanszell-Histiozytose [Abt-Letterer-Siwe-Krankheit]
- C96.5 Multifokale und unisystemische Langerhans-Zell-Histiozytose
- C96.6 Unifokale Langerhanszell-Histiozytose
- D76 Bestimmte Krankheiten mit Beteiligung des lymphoretikulären Gewebes und des retikulohistiozytären Systems
Diagnostik
Diagnostische Kriterien
- Zusammenschau von klinischen, radiologischen und histologischen Befunden3-4
- Die Histologie mit Nachweis von Langerhanszell-Histiozyten ist zum Stellen der Diagnose zwingend erforderlich.3-4
- Ist die Diagnose gestellt, so ist eine Art Staging zur Bestimmung des Ausmaßes der Erkrankung entscheidend. Die Therapie richtet sich nach Anzahl der befallenen Organsysteme bzw. Befall von Risikoorganen.1,3,5
Differenzialdiagnosen
- Das Spektrum an Differenzialdiagnosen ist breit und entscheidend von den befallenen Organsystemen abhängig. Die Leitlinie gibt einen guten Überblick (Tabelle 4, Seite 9).3 Beispielhaft seien genannt:
- Gehirntumoren
- multiple Sklerose
- Sarkoidose
- Lymphom
- multiples Myelom
- Strahlenschäden
- andere Histiozytosen.
Anamnese
- Die Symptome variieren mit Ausmaß der Erkrankung, die von isolierten Knochenläsionen bis hin zu einem Multiorganbefall reicht. Da praktisch jedes Organ befallen sein kann, sind die Symptome vielfältig. Hervorzuheben sind:3
- Hautausschlag
- Schleimhautveränderungen
- B-Symptome wie Fieber und Gewichtsverlust/mangelnde Gewichtszunahme bei Kindern
- Polydipsie und Polyurie (bei Diabetes insipidus durch Hypophyseninsuffizienz)
- Knochenschmerzen
- Hörminderung oder Otorrhö
- Luftnot (bei Lungenbeteiligung)
- neurologische Ausfälle
Diabetes insipidus
- Eine häufige Manifestation ist ein zentraler Diabetes insipidus mit ADH-Mangel, der durch eine Beteiligung von Hypothalamus, Hypophysen-Stiel oder Hypophysenhinterlappen verursacht wird.
- Verstärkter Durst und Diurese sind Leitsymptome. Diese können anderen Symptomen vorausgehen oder verspätet auftreten.3
Klinische Formen
Haut
- Kann erste Manifestation einer Langerhans-Histiozytose sein. Die Erkrankung kann auf die Haut beschränkt sein oder andere Organsysteme können befallen sein.3,13-14
- Bis zu 50 % der Patient*innen weisen bei Erkrankungsbeginn einen Hautausschlag auf.13
- Hautmanifestationen sind variabel. Häufig sind erythematöse Makula, Papeln oder Knötchen, die verkrustet oder ulzeriert sein können. Petechien kommen begleitend vor.3,13
- Effloreszenzen können lokal begrenzt oder generalisierte Dermatosen sein. Seborrhoische Areale, insbesondere die Kopfhaut, sind vermehrt betroffen.3,13
- Juckreiz ist selten.13
- Bei Befall von Leisten, Genitalien oder perianal (intertriginöse Stellen) können sich wunde Stellen bilden, die weder mit Antibiotika- noch mit antifungaler Therapie heilen.
- Auch die Mundschleimhaut kann befallen sein, wodurch die Zahnentwicklung beeinträchtigt sein kann.3
- Bei limitiertem kutanem Befall ist die Prognose gut.14
Knochen
- Kann als asymptomatischer Zufallsbefund auffallen.
- Schmerzhafte Schwellungen sind häufig das erste Anzeichen.
- Schädel- und Kieferknochen gehören zu den am häufigsten befallenen Stellen.15
- Schmerzen im Kiefer und lockere Zähne können die ersten Symptome sein.
- Es können Spontanfrakturen entstehen.
- In der Wirbelsäule können lytische Prozesse eine Kompression und einen Kollaps von Wirbeln verursachen.
Lunge
- Häufigste Form bei Erwachsenen
- Betroffen sind in erster Linie junge Raucher.16-17
- Leitsymptome sind Husten, Dyspnoe und Brustschmerzen.
- Rund 20 % der Patient*innen mit Lungenaffektion sind symptomfrei.18
- Die Lunge ist meistens das einzige befallene Organsystem.
- Diagnostisch wichtig sind eine hochauflösende Computertomografie und eine bronchoalveoläre Lavage. In unklaren Fällen erfolgt eine Lungenbiopsie.17
- Die wichtigste therapeutische Maßnahme ist ein Rauchstopp. Die Prognose ist gut.17,19
Knochenmark
- In seltenen Fällen bei systemischen Erkrankungsformen im Kindesalter1
- Klinische Manifestation als Anämie oder Thrombozytopenie3
- Verbunden mit einer schlechten Prognose3-4
Leber und Milz
- Leber- und Milzbefall sollte bei jeder Langerhans-Zell-Histiozytose sonografisch ausgeschlossen werden.3
- Bei Leberfunktionsstörung (z. B. Hyperbilirubinämie, Hypoalbuminämie, Transaminasenerhöhung, Aszites) unklarer Ätiologie kann eine Leberbiopsie notwendig sein.3
- Gelten als Risikoorgane, deren Befall mit einer schlechteren Prognose verbunden ist.1,3
Gastrointestinaltrakt
- Das häufigste Anzeichen sind „Gedeihstörungen‟ bei einem Kind, die durch eine Malabsorption verursacht werden.
- Andere Symptome können Erbrechen, Diarrhö (mit oder ohne Blut) und enterales Eiweißverlustsyndrom sein
- Abklärung mittels Endoskopie und Biopsie3
Endokrine Ausfälle
- Hormonstörung gehören zu den häufigsten Manifestationen.3
- Diabetes insipidus3
- 15–50 % der Fälle bei Kindern
- Symptome sind Polydipsie und Polyurie.
- MRT zur Darstellung der Hypophyse
- Osmolalität des Morgenurins, Durstversuch
- Weitere häufige hormonelle Störungen, insbesondere bei Kindern, umfassen einen Wachstumshormonmangel und Hypothyreose. Es können sich Wachstumsstörungen, Galaktorrhö, eine zu frühe oder verspätete Pubertät zeigen.3
Zentrales Nervensystem
- Primärer oder sekundärer Befall; in einigen Fällen Jahre nach Erstmanifestation1,3
- Die klinische Präsentation ist vielfältig und umfasst u. a. eine zerebelläre Ataxie und Lernschwierigkeiten.3
- Die häufigste Lokalisation besteht in Hypothalamus/Hypophyse, aber auch alle anderen Teile des Gehirns können affiziert sein.20
- Ca. 50 % haben Diabetes insipidus.21
- Wenige weisen andere Dysfunktionen im vorderen Teil der Hypophyse auf.22
- Bei einigen entwickelt sich Panhypopituitarismus.22
Basisdiagnostik
- Der Abschnitt basiert auf dieser Referenz.3
- Blutbild mit Differenzialblutbild
- Elektrolyte (Na, K, Ca), Kreatinin
- Leberfunktionswerte (GOT, GPT, Gamma-GT, AP, CHE, INR, Albumin)
- CRP
- Blutgerinnung
- Sonografie Abdomen
- Röntgen Thorax
Diagnostik bei Spezialist*innen
Basisdiagnostik3
- Bildgebung des Skeletts
- Verschiedene Verfahren kommen zum Einsatz:3,5
- Röntgen-Skelett-Status
- Ganzkörper Niedrigdosis-Computertomografie
- Ganzkörper-Magnetresonanztomografie23
Spezielle Diagnostik
- Lunge3,17
- Lungenfunktionsuntersuchung
- hochauflösendes CT (HR-CT)
- Bronchioalveoläre Lavage in erster Linie zur Differenzialdiagnostik; selten können Langerhans-Zell-Histiozyten im Lavagat nachgewiesen werden.
- in unklaren Fällen: Lungenbiopsie
- Zentrales Nervensystem
- Endokrinologische Diagnostik
- Beteiligung Mastoid/Innenohr
- Hörtest 3
- Gastrointestinale Beschwerden
- Endoskopie mit Biopsien3
Histologie
- Die Biopsie mit Gewebegewinn zum Nachweis von Langerhans-Histiozyten ist die entscheidende Untersuchung.1,3,5
- Entnommen von der am besten zugänglichen Läsion3
- Lichtmikroskopische Untersuchung mit immunhistochemischen Färbungen3-4
- Entscheidend ist der Nachweis von CD1a+ und CD207+ (Langerin) Langerhanszell-Histiozyten.3-4
- Zusätzlich entzündliches Infiltrat mit Lymphozyten, Makrophagen, Eosinophilen und Granulombildung
- Eine Referenzbefundung wird empfohlen.3
Indikationen zur Überweisung
- Bei Verdacht auf die Erkrankung
Therapie
Therapieziele
- Einen lokalen und systemischen Progress der Erkrankung verhindern.
- Komplikationen der Organinfiltrationen verhindern.
Allgemeines zur Therapie
- Der Abschnitt basiert auf dieser Referenz.3
- Die Langerhanszell-Histiozytose ist eine heterogene Krankheit sowohl im Hinblick auf den Verlauf als auch auf die befallenen Organe. Es wird unterschieden zwischen:
- monosystemischen und
- multisystemischen Formen.
- Risikoorgane: Der Befall von dem hämatopoetischen System, Leber oder Milz ist mit einer schlechteren Prognose verbunden und wird deshalb wie multisystemische Formen agressiver behandelt.25
- Behandlungsstrategien umfassen beobachtendes Abwarten (Watch and Wait), Lokaltherapie sowie systemische Chemo-/Immuntherapie.26-27
Beobachtendes Abwarten
- Watch and Wait
- Bei auf die Haut beschränktem Befall und singulären Knochenläsionen3
- Bei isoliertem Lungenbefall bei jungen Rauchern (Rauchabstinenz!)3,17
- Regelmäßige Verlaufskontrollen, um einen Übergang in multisystemische Formen zu erkennen.3
Lokaltherapie
- Intraläsionale Steroidinjektionen bei singulären Knochenläsionen, z. B. 40–160 mg Depot-Methylprednisolon3
- Lokale topische Therapie bei ausgedehntem, aber auf die Haut begrenztem Befall (z. B. mit Caryolysine)3
- Prospektiv-randomisierte Studien fehlen.3
Systemische Therapie
- Indikationen3
- Multisystembefall
- Befall von Risikoorganen
- hämatopoetisches System
- Leber
- Milz
- ZNS-Befall
- multifokaler Knochenbefall
- Knochenläsionen in komplikationsträchtiger Lokalisation
- kraniofazial
- Wirbelkörperbefall mit drohender Knochenmarkskompression
- Dens axis
- orbital
- Beteiligung des Hörorgans
- ggf. Beteiligung gewichtstragender Knochen
- Möglichst Behandlung im Rahmen von prospektiven Studien3
- Erstlinientherapie: Vinblastin + Prednisolon3
- Induktionstherapie über 6–12 Wochen
- anschließend Evaluation des Therapieansprechens
- bei gutem Ansprechen dann Erhaltungstherapie
- Gesamttherapiedauer: 12 Monate
- Zweitlinientherapie3
- im Rahmen von Studien
- Chemotherapie
- Biologika
- hämatopoetische Stammzelltransplantation28-29
Verlauf, Komplikationen und Prognose
Verlauf
- Variabel
- Bei singulären Läsionen: häufige Spontanremission
- Bei multisystemischem Befall: progredient mit zunehmender Funktionseinschränkung der befallenen Organsysteme
Komplikationen
- Der gesamte Abschnitt basiert auf dieser Referenz.3
- Häufig, insbesondere bei multisystemischen Formen und Befall von Risikoorganen
- Die häufigsten Komplikationen sind orthopädische Probleme, eingeschränktes Hörvermögen, Diabetes insipidus und neuropsychologische Defekte.
- Endokrinologisch
- Substitutionstherapie
- Orthopädisch
- Physiotherapie
- Befall der Mundschleimhaut
- bei Kindern u. U. gestörte Zahnentwicklung
- zahnärztliche Beurteilung
- Erwachsene mit einer Langerhanszell-Histiozytose erhalten eine vollständige Kostenerstattung für notwendige Zahnbehandlungen.
- Neurologische Probleme
- Selten treten neurologische Komplikationen Jahre nach der Erstmanifestation auf.
- regelmäßige Testung von Lernfortschritten
- Follow-up mit Schädel-MRT
- Lungenbefall
- Wichtig ist eine Nikotinkarenz.
- Verlaufsbeobachtung mit Lungenfunktionstestung und bildgebenden Verfahren
- Hörprobleme
- Hörtest
Prognose
- Die Prognose wird vor allem von der Anzahl der betroffenen Organsysteme und deren Dysfunktion bestimmt.30-31
- Wie der Verlauf ist auch die Prognose variabel, da die Erkrankung heterogen ist.
- Bei auf die Haut oder eine Knochenläsion begrenztem Befall ist die Prognose exzellent.
- Kinder mit Multisystembefall
- 3-Jahres-Überlebensrate ca. 80 %32
- Das Alter ist ein prognostischer Faktor – je jünger, desto schlechter die Prognose.
- Erwachsene mit isoliertem Lungenbefall5,19
- bis zu 50 % Remission
Verlaufskontrolle
- Der gesamte Abschnitt basiert auf dieser Referenz.3
- Verlaufskontrollen zur frühzeitigen Erkennung von lokalem Progress, Rezidiven oder Befall weiterer Organsysteme sind wichtig.
- Nach Diagnosestellung
- im 1. Jahr 3-monatlich
- Jahr 2–5 halbjährlich
- anschließend jährlich
- Spezielle Verlaufskontrollen richten sich nach befallenen Organsystemen und Therapie, z. B.:
- zahnärztliche Kontrolluntersuchungen
- Testung von Lernfortschritten
- Schädel-MRT
- Lungenfunktionstestung5
- endokrinologische Tests
Patienteninformationen
Patienteninformationen in Deximed
- Langerhanszell-Hiystiozytose
- Rauchen schadet Ihrer Gesundheit
- Warum sollten Sie das Rauchen aufgeben, und wie gelingt es?
Illustrationen
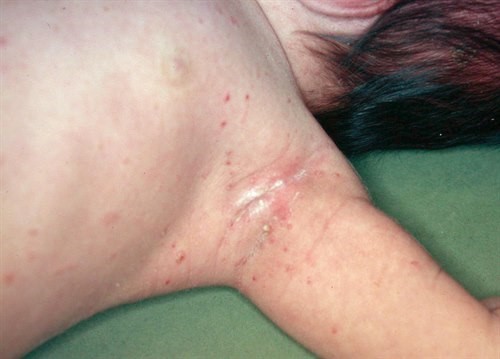
Langerhanszell-Histiozytose
Quellen
Leitlinien
- Gesellschaft für Pädiatrische Onkologie und Hämatologie: Langerhanszell-Histiozytose (LCH) im Kindes- und Jugendalter. AWMF-Registernummer 025-015. S1, Stand 2017. www.awmf.org
- Gesellschaft für Pädiatrische Radiologie: Ganzkörper-MRT im Kindesalter. S1-Leitlinie, AWMF-Registernummer 064-018. S1, Stand 2018. www.awmf.org
Kompetenzzentren
- Euro-Histio-Net: Referenznetzwerk für Langerhans-Zell-Histiozytose und assoziierte Syndrome
Literatur
- Allen CE, Merad M, McClain KL. Langerhans-Cell Histiocytosis. N Engl J Med. 2018 Aug 30;379(9):856-868. doi: 10.1056/NEJMra1607548. PMID: 30157397. PubMed
- Badalian-Very G, Vergilio JA, Fleming M, Rollins BJ. Pathogenesis of Langerhans cell histiocytosis. Annu Rev Pathol. 2013 Jan 24;8:1-20. doi: 10.1146/annurev-pathol-020712-163959. Epub 2012 Aug 6. PMID: 22906202. PubMed
- Gesellschaft für Pädiatrische Onkologie und Hämatologie: Langerhanszell-Histiozytose (LCH) im Kindes- und Jugendalter. S1-Leitlinie, AWMF-Registernummer 025 - 015, Stand 06/2017, https://www.awmf.org. www.awmf.org
- Emile JF, Abla O, Fraitag S, Horne A, Haroche J, Donadieu J, Requena-Caballero L, Jordan MB, Abdel-Wahab O, Allen CE, Charlotte F, Diamond EL, Egeler RM, Fischer A, Herrera JG, Henter JI, Janku F, Merad M, Picarsic J, Rodriguez-Galindo C, Rollins BJ, Tazi A, Vassallo R, Weiss LM; Histiocyte Society. Revised classification of histiocytoses and neoplasms of the macrophage-dendritic cell lineages. Blood. 2016 Jun 2;127(22):2672-81. doi: 10.1182/blood-2016-01-690636. Epub 2016 Mar 10. PMID: 26966089. PubMed
- Girschikofsky M, Arico M, Castillo D, Chu A, Doberauer C, Fichter J, Haroche J, Kaltsas GA, Makras P, Marzano AV, de Menthon M, Micke O, Passoni E, Seegenschmiedt HM, Tazi A, McClain KL. Management of adult patients with Langerhans cell histiocytosis: recommendations from an expert panel on behalf of Euro-Histio-Net. Orphanet J Rare Dis. 2013 May 14;8:72. doi: 10.1186/1750-1172-8-72. PMID: 23672541. PubMed
- Guyot-Goubin A, Donadieu J, Barkaoui M, Bellec S, Thomas C, Clavel J. Descriptive epidemiology of childhood Langerhans cell histiocytosis in France, 2000-2004. Pediatr Blood Cancer. 2008 Jul;51(1):71-5. doi: 10.1002/pbc.21498. PMID: 18260117. PubMed
- Kobayashi M, Tojo A. Langerhans cell histiocytosis in adults: Advances in pathophysiology and treatment. Cancer Sci. 2018 Dec;109(12):3707-3713. doi: 10.1111/cas.13817. Epub 2018 Oct 30. PMID: 30281871. PubMed
- Aricò M, Girschikofsky M, Généreau T, Klersy C, McClain K, Grois N, Emile JF, Lukina E, De Juli E, Danesino C. Langerhans cell histiocytosis in adults. Report from the International Registry of the Histiocyte Society. Eur J Cancer. 2003 Nov;39(16):2341-8. doi: 10.1016/s0959-8049(03)00672-5. PMID: 14556926. PubMed
- Chakraborty R, Burke TM, Hampton OA, Zinn DJ, Lim KP, Abhyankar H, Scull B, Kumar V, Kakkar N, Wheeler DA, Roy A, Poulikakos PI, Merad M, McClain KL, Parsons DW, Allen CE. Alternative genetic mechanisms of BRAF activation in Langerhans cell histiocytosis. Blood. 2016 Nov 24;128(21):2533-2537. doi: 10.1182/blood-2016-08-733790. Epub 2016 Oct 11. PMID: 27729324. PubMed
- de Graaf JH, Egeler RM. New insights into the pathogenesis of Langerhans cell histiocytosis. Curr Opin Pediatr 1997; 9: 46-50. PubMed
- Coppes-Zantinga A, Egeler RM. The Langerhans Cell Histiocytosis X files revealed. Br J Haematol 2002; 116: 3-9. PubMed
- Egeler RM, D'Angio GJ. Langerhans Cell Histiocytosis. J Pediatr 1992; 127: 1-11. PubMed
- Munn S, Chu AC. Langerhans cell histiocytosis of the skin. Hematol Oncol Clin North Am. 1998 Apr;12(2):269-86. doi: 10.1016/s0889-8588(05)70510-4. PMID: 9561900. PubMed
- Simko SJ, Garmezy B, Abhyankar H, Lupo PJ, Chakraborty R, Lim KP, Shih A, Hicks MJ, Wright TS, Levy ML, McClain KL, Allen CE. Differentiating skin-limited and multisystem Langerhans cell histiocytosis. J Pediatr. 2014 Nov;165(5):990-6. doi: 10.1016/j.jpeds.2014.07.063. Epub 2014 Oct 21. PMID: 25441388. PubMed
- Baumgartner I, von Hochstetter A, Baumert B, Luetolf U, Follath F. Langerhans Cell Histiocytosis in Adults. Med Ped Oncol 1997; 28: 9-14. PubMed
- Maghnie M, Cosi G, Genovese E, et. al. Central Diabetes Insipidus in Children and Young Adults. N Engl J Med 2000; 343: 998-1007. New England Journal of Medicine
- Tazi A. Adult pulmonary Langerhans' cell histiocytosis. Eur Respir J. 2006 Jun;27(6):1272-85. doi: 10.1183/09031936.06.00024004. PMID: 16772390. PubMed
- Travis WD, Borok Z, Roum JH, Zhang J, Feuerstein I, Ferrans VJ, Crystal RG. Pulmonary Langerhans Cell Granulomatosis (Histiocytosis X): A Clinicopathologic Study of 48 Cases. Am J Surg Pathol 1993; 17: 971-86. PubMed
- Delobbe A, Durieu J, Duhamel A, Walleert B. Determinants of Survival in Pulmonary Langerhans Cell Granulomatosis (Histiocytosis X). Eur Respir J 1996; 9: 2002-6. PubMed
- Grois NG, Favara BE, Mostbeck GH, Prayer D. Central nervous system disease in Langerhans cell histiocytosis. Hematol Oncol Clin North Am 1998; 12: 287-305 PubMed
- Modan-Moses D, Weintraub M, Meyerovitch J, Segal-Lieberman G, Bielora B. Hypopituitarism in langerhans cell histiocytosis: seven cases and a literature review. J Endocrinol Invest 2001; 24: 612-7. PubMed
- Kaltsas GA, Powles TB, Evanson J, et al. Hypothalamo-pituitary abnormalities in adult patients with Langerhans cell histiocytosis: clinical, endocrinological, and radiological features and response to treatment. J Clin Endocrinol Metab 2000; 85: 1370-6. PubMed
- Leitlinie: Ganzkörper-MRT im Kindesalter www.awmf.org
- Büchler T, Cervinek L, Belohlavek O, et al. Langerhans cell histiocytosis with central nervous system involvement: Follow-up by FDG-PET during treatment with cladribine. Pediatr Blood Cancer 2004; 43: 1-3. PubMed
- McClain KL. Treatment of Langerhans cell histiocytosis. UpToDate, last updated Aug 5, 2013 . UpToDate
- Egeler RM, de Kraker J, Voute PA: Cytosine-arabinoside, vincristine, and prednisolone in the treatment of children with disseminated Langerhans cell histiocytosis with organ dysfunction: Experience at a single institution. Med Pediatr Oncol 1993; 21: 265. PubMed
- Viana MB, Oliverira BM, Silva CM, Rios Leite VH: Etoposide in the treatment of six children with Langerhans cell histiocytosis (histiocytosis X). Med Pediatr Oncol 1991; 19: 289. PubMed
- Nagarajan R, Neglia J, Ramsay N, Baker KS. Successful treatment of Langerhans cell histiocytosis with unrelated cord blood transplantation. J Pediatr Hematol Oncol 2001; 23: 632-39. PubMed
- Conter V, Reciputo A, Arrigo C, Bozzato N, Sala A, Arico C. Bone marrow transplantation for refractory Langerhans cell hystiocytosis. Haematologica 1996; 81: 468-71. PubMed
- Grundy P, Ellis R: Histiocytosis X: A review of the etiology, pathology, staging, and therapy. Med Pediatr Oncol 1986; 14: 45. PubMed
- Komp DM: Concepts in staging and clinical studies for treatment of Langerhans' cell histiocytosis. Semin Oncol 1991; 18: 18. PubMed
- Gadner H, Grois N, Arico N, et al. A randomized trial of treatment for multisystem Langerhans' cell histiocytosis. J Pediatr 2001; 138: 728-34. PubMed
Autor*innen
- Dietrich August, Dr. med., Arzt in Weiterbildung Innere Medizin, Freiburg
- Die ursprüngliche Version dieses Artikel basiert auf einem entsprechenden Artikel im norwegischen hausärztlichen Online-Handbuch Norsk Elektronisk Legehåndbok (NEL, https://legehandboka.no/).