Allgemeine Informationen
- Sofern nicht anders gekennzeichnet, basiert der gesamte Artikel auf diesen Referenzen.1-5
Definition
Infektion mit dem Herpes-simplex-Virus (HSV)
- Virusinfektion, verursacht vom Herpes-simplex-Virus (HSV) Typ 1 oder 2, einem Virus der Familie der Herpesviren
- Die Krankheit führt normalerweise zu lokalisierten, schmerzhaften Vesikeln an Schleimhäuten und Haut.
- Mit der Infektion werden Betroffene zu lebenslangen Trägerinnen des Virus.
Herpes genitalis
- Durch Genital- oder Oralverkehr und/oder über anogenitale Läsionen übertragene HSV-Infektion, die lebenslang im Körper verbleibt und periodisch reaktiviert wird.6
Klinische Einteilung
- Asymptomatische Primärinfektion
- 75 % der Patientinnen, die sich mit HSV-2 anstecken.
- 90 % der Patientinnen, die sich mit HSV-1 anstecken.
- Primärerkrankung
- Bei exogener Primärinfektion mit HSV-1 oder -2, d. h. bei Infektion zu einem Zeitpunkt, zu dem die Patientin noch keine Antikörper gegen dasselbe Virus aufgrund einer früher durchgemachten Infektion gebildet hat.
- bei nicht-primärer Infektion
- exogene Infektion mit HSV-1 bei einer Patientin mit Antikörpern gegen HSV-2
- oder exogene Infektion mit HSV-2 bei einer Patientin mit Antikörpern gegen HSV-1
- Rezidiv
- endogene Reaktivierung einer latenten HSV-Infektion, unabhängig von Sexualkontakten
Häufigkeit
- Inzidenz
- 50–80 % durchlaufen eine Primärinfektion mit HSV-1 als Kind.
- Eine Primärinfektion mit HSV-2 erfolgt selten vor dem ersten Sexualkontakt.
- Prävalenz
- Frauen sind häufiger von Herpes genitalis betroffen als Männer.6
- Ende der 1990er Jahre lag die Seroprävalenz von HSV-1 bei Frauen bei 86–92 %, die von HSV-2 bei 14–22%.
- HSV-1
- asymptomatische Primärinfektion bei ca. 90 % (unabhängig von der Ansteckungsart)
- HSV-2
- In der Altersgruppe 20–40 Lj. haben 20–40 % der Bevölkerung eine Primärinfektion durchgemacht.
- Anders als in den USA, wo die HSV-2-Seroprävalenz zunahm, war diese in den alten Bundesländern Deutschlands Ende der 1990er Jahre rückläufig.
- Nur 20–30 % der Fälle von Herpes genitalis manifestieren sich klinisch eindeutig.
- 50 % verlaufen asymptomatisch.
- 20 % gehen mit Symptomen einher, die von der betroffenen oder behandelnden Person falsch gedeutet werden.
- HSV-1 und HSV-2
- Etwa 70–80 % der genitalen Herpeserkrankungen werden durch HSV-2 verursacht.
- HSV-1 liegt einem Großteil der Herpeserkrankungen im Lippen- und Gesichtsbereich und 20–30 % der genitalen Herpeserkrankungen zugrunde.
- Insbesondere bei jüngeren Frauen scheint der Anteil HSV-1-bedingter Herpes-genitalis-Fälle zuzunehmen.7
- Vermutlich besteht zwischen HSV-1 und HSV-2 eine partielle Kreuzimmunität, die die Ausbreitung von HSV-2 erschwert.
- Rezidivhäufigkeit
- Dem primären Herpes genitalis folgt in ca. 85 % der Fälle ein symptomatisches Rezidiv.
- Endogene Rezidive werden in mehr als 90 % der Fälle durch HSV-2 ausgelöst.
- Eine genitale Infektion mit HSV-1 bleibt meist ein einmaliges Ereignis.
- Eine Primärinfektion in der Schwangerschaft tritt bei rund 1 % der bisher seronegativen Schwangeren auf.
Ätiologie und Pathogenese
- HSV-1 und HSV-2
- HSV-1 ist auf sexuellem Weg übertragbar, meist erfolgt die Ansteckung jedoch über die Lippen oder Mundschleimhaut, häufig bereits in der Kindheit.
- HSV-2 wird fast nur sexuell übertragen.
- Die sexuelle Übertragung geschieht z. T. über Sekrete, z. T. über direkten Kontakt mit infizierten Schleimhäuten.
- Die Virusaussonderung hält bei den ersten Infektionen länger an (15–16 Tage).
- Die beiden Virustypen unterscheiden sich dadurch, dass sie in ihrer Hülle unterschiedliche Antigene ausbilden.
- Bei Kindern ist Herpes genitalis sehr selten.
- Schmierinfektion von der Mutter?
- Sexueller Missbrauch?
- Die Inkubationszeit beträgt bei beiden Virustypen ca. 3–7 Tage.
- Latente Infektion
- Während der aktiven Primärinfektion wandert das Virus über sensorische Nerven in sacrospinale Hinterwurzelganglien, wo es latent persistiert.
- Eine latente Virusinfektion spricht nicht auf Medikamente an und bleibt in der Regel lebenslang bestehen.
- Endogene Reaktivierung
- Durch verschiedene Stressfaktoren kann die latente Infektion zu einer virusproduktiven Infektion reaktiviert werden.
- Beispiele relevanter Stressfaktoren:
- psychische Belastung (Ärger, Erschöpfung, Schlafentzug)
- Verletzungen, Gewebeschäden
- UV-Lichtbestrahlung des mukokutanen Innervationssegmentes
- Infektionen und Fieber (Herpes febrilis).
- Bei einer Reaktivierung breitet sich das Virus vom Hinterhornganglion entlang des Spinalnervs aus und kann im entsprechenden Nervenversorgungsgebiet zu einer Haut- oder Schleimhaut-Effloreszenz führen.
- Subklinische Virusausscheidung
- Auch ohne sichtbare Läsionen können Herpesviren aus den Genitalien oder dem Mund abgesondert werden.
- bei mehr als 80 % der HSV-2-seropositiven Personen ohne Läsionen
- besonders häufig im ersten Jahr nach der Primärinfektion
- Darauf beruht die vermutlich häufigste Form der Infektionsübertragung auf die Sexualpartner*innen.
- Auch beim Petting ist eine Übertragung möglich.
- Ob Kondome einer Übertragung auf die Sexualpartner*innen wirksam vorbeugen, wurde nie systematisch untersucht. Indirekte Hinweise aus negativen Studien zu HSV-Impfstoffen legen aber nahe, dass eine konsequente Anwendung von Kondomen sehr empfehlenswert ist (IIb/B). Es ist allerdings damit zu rechnen, dass ein Kondom keinen vollständigen Schutz bietet, da es nicht den gesamten Genitalbereich bedeckt.
Prädisponierende Faktoren
- Sexueller Kontakt
- Das Risiko für eine Infektion korreliert mit der Anzahl der Sexualpartner*innen.
- Immunsuppression
- Alter (kumulatives Risiko): Die Seroprävalenz ist bei Erwachsenen am höchsten und bei Säuglingen am niedrigsten.
- Geschlecht: w > m
- Möglicherweise beruht diese Beobachtung auf einer unvollständigen Erfassung asymptomatischer Infektionsfälle bei Männern.
- Niedriger sozioökonomischer Status
ICPC-2
- X90 Herpes genitalis, Frau
ICD-10
- Nach ICD-10-GM Version 20228
- A60 Infektionen des Anogenitalbereiches durch Herpesviren [Herpes simplex]
- A60.0 Infektionen der Genitalorgane und des Urogenitaltraktes durch Herpesviren
- A60.1 Infektion der Perianalhaut und des Rektums durch Herpesviren
- A60.9 Infektion des Anogenitalbereiches durch Herpesvieren, nicht näher bezeichnet
- N77 Vulvovaginale Ulzeration und Entzündung bei anderenorts klassifizierten Krankheiten
- N77.0 Ulzeration der Vulva bei anderenorts klassifizierten infektiösen und parasitären Krankheiten
- N77.1 Vaginitis, Vulvitis oder Vulvovaginitis bei anderenorts klassifizierten infektiösen und parasitären Krankheiten
- A60 Infektionen des Anogenitalbereiches durch Herpesviren [Herpes simplex]
Diagnostik
Diagnostische Kriterien
- Klassischer Genitalherpes kann anhand der typischen Haut- oder Schleimhautläsionen und Lymphadenitis diagnostiziert werden.
- Bei rezidivierender Erkrankung können Prodromi eine Reaktivierung der Infektion anzeigen.
- Die Symptomatik weicht aber bei vielen Patientinnen stark vom klassischen Krankheitsbild ab.
- Herpetische Haut- oder Schleimhautläsionen können anderen genitalen Dermatosen oft sehr ähnlich sehen.
- Eine Diagnose nur anhand des klinischen Erscheinungsbildes sollte bei atypischer Symptomatik möglichst vermieden werden.
- Eine Diagnosesicherung durch Virusnachweis sollte in allen Verdachtsfällen angestrebt werden.
Differenzialdiagnosen
- Zervizitis
- Candida-Vaginitis und andere Pilzinfektionen
- Trichomoniasis
- Bakterielle Vaginose
- Vaginalkarzinom
- Morbus Behçet
- Syphilis (Primäraffekt)
- Ulcus molle (weicher Schanker)
- Zoster
- Pemphigus
- Mollusca contagiosa
- Impetigo contagiosa
- Urethritis anderer Genese, z. B. Chlamydien, Mykoplasmen oder Trichomonaden
- Dysurie anderer Genese, z. B. Harnwegsinfekt
- Proktitis anderer Genese, z. B. chronisch entzündliche Darmerkrankung
- Plattenepithelkarzinom der Haut
- Verletzungen, Hautirritationen durch Sex
- Kontaktekzem, z. B. durch Pflegemittel, Gleitgel, Spermizide
- Kratzeffekte bei Juckreiz, z. B. Skabies
- Neuropathische Schmerzen anderer Genese
- Somatoforme Schmerzerkrankung
Anamnese
Exogene Primärerkrankung
- Frühstadium
- Häufig treten Beschwerden in Form von lokalisiertem oder regionalem, stechendem oder brennendem Schmerz im Genitalbereich auf.
- Weil keine Bläschen oder Erosionen sichtbar sind, wird Herpes genitalis in diesem Stadium häufig mit Pilzinfektionen verwechselt.
- Allgemeine Symptome
- in mehr als 2/3 der Fälle:
- Kopfschmerzen
- allgemeines Krankheitsgefühl
- Fieber
- Muskelschmerzen, oft Rückenschmerzen.
- Diese Beschwerden sind bei Frauen stärker ausgeprägt als bei Männern.
- in mehr als 2/3 der Fälle:
- Lokale Symptome
- Typisch ist:
 Herpes genitalis
Herpes genitalis- Aussaat der Bläschen über größere Flächen des Genitales und der angrenzenden Haut
- symmetrische Verteilung der Effloreszenzen
- lange Persistenz der Hauterscheinungen, bis zu 3 Wochen.
- Die Bläschen platzen auf und hinterlassen kleine, flache Ulzera. Diese infizieren sich häufig erneut, verheilen aber mit der Zeit und hinterlassen keine Narben.
- evtl. starke Schmerzen an der Vulva mit ausgeprägter Berührungsempfindlichkeit
- Schmerzhafte lokale Lymphadenitis: Weist auf eine Primärinfektion hin.
- Brennen beim Wasserlassen
- Herpes-Urethritis mit oder ohne Ausfluss
- evtl. schwere Dysurie bis hin zum Harnverhalt
- Herpesbläschen in Urethranähe?
- evtl. auch durch Nervenbefall
- Typisch ist:
- Eine exogene Primärerkrankung kann 2–4 Wochen andauern. Während dieser Zeit kann es zu starken neuropathischen Schmerzen kommen.
Primärerkrankung bei nichtprimärer Infektion
- Exogene Infektion mit HSV-1 bei einer Patientin mit Antikörpern gegen HSV-2 oder exogene Infektion mit HSV-2 bei einer Patientin mit Antikörpern gegen HSV-1
- Kann zu denselben Symptomen führen wie bei einer Primärerkrankung ohne Vorinfektion; die Symptome sind aber oft weniger ausgeprägt.
- Fieber, geschwollene Lymphknoten, Allgemeinsymptome und neuropathische Schmerzen kommen weniger häufig vor.
- Der lokale Haut- und Schleimhautbefall ist weniger ausgedehnt.
Rezidive
- Nach HSV-2 Primärerkrankung häufige endogene Reaktivierung mit bis zu 12 Rezidiven im Jahr
- Nach genitaler HSV-1-Infektion eher selten
- Prodromi
- Hyperästhesie und neuropathische Schmerzen im Genitalbereich
- allgemeines Krankheitsgefühl
- Meist nur wenige umschriebene, gruppierte Bläschen und Erosionen
- Winzige Erosionen können oft nur mit der Lupe aufgespürt werden, geleitet von der Schmerzlokalisation.
- Bilden sich zu polyzyklischen Läsionen zurück.
- Rezidivierender Herpes kann körperlich und psychisch sehr belasten – sowohl die Patientin als auch die Partner*innen.
- Paarkonflikte und sexuelle Funktionsstörungen können dadurch ausgelöst oder verstärkt werden.
Auslösende Faktoren?
- Stressfaktoren, die eine endogene Reaktivierung von HSV begünstigen.
Ergänzende Untersuchungen
- Der Erregernachweis aus Bläschen, Erosionen oder Ulzera ist der zuverlässigste Weg der Diagnosesicherung.
- Bei unsicherer Diagnose können Abstriche aus den Herpes-Bläschen oder Ulzera untersucht werden. Dies geschieht am besten innerhalb von 2 Tagen nach Beginn der Erkrankung.
- Probengewinnung in der Regel durch Abstriche vom Grund der Läsion, z. B. von Herpesbläschen nach Öffnung mit einer Nadel oder einem Skalpell.
- Transportmedium für Viren verwenden.
- Ein negativer Test schließt eine Infektion nicht aus.
- Ein positiver Test gilt als sichere Bestätigung der Erkrankung.
Leitlinie: Labordiagnostik des Herpes genitalis2
Virusnachweis
- Direkter Virusnachweis in Proben aus dem Genitaltrakt wird bei allen Verdachtsfällen empfohlen (Ib/A).
- Da asymptomatisch Infizierte nur zeitweise HSV-Viren absondern, werden routinemäßige Abstrichuntersuchungen bei diesen Patientinnen nicht empfohlen, denn die Chance, dass man damit eine latente Infektion beweisen kann, ist gering (Ib/A).
- Typisierung in HSV-1 und -2
- bei allen Patientinnen mit erstmaligem genitalem Herpes relevant für Beratung und Behandlungsplanung (III/B)
- Der Nachweis von HSV-DNA wird mittlerweile als diagnostischer Goldstandard angesehen. Er ist sensitiver und spezifischer als der HSV-Nachweis auf Zellkulturen (Ib/A).
- Der Nachweis von HSV-DNA in mukokutanen Abstrichen mittels Echtzeit-PCR erlaubt eine um 11–71 % höhere HSV-Erkennungsrate als in der Zellkultur und ist daher als diagnostische Methode vorzuziehen (Ib/A).
- Zellkulturen können gelegentlich benötigt werden, um die Sensitivität gegenüber antiviralen Therapien zu ermitteln oder um genügend Viruskopien für Transmissionsstudien zu generieren.
- Die Probe für eine Echtzeit-PCR ist weniger lagerungs- und transportempfindlich als für eine Zellkultur und erlaubt es, HSV schnell nachzuweisen und zu typisieren, mit einem niedrigeren Kontaminationsrisiko als die klassischen PCR-Assays.
- Methoden zum Nachweis viralen Antigens – wie der direkte Immunfluoreszenz-Assay (IFA), Enzym-Immun-Assay (EIA) oder Tzanck- und Papanicolaou-Färbung – werden nicht mehr empfohlen, außer unter Bedingungen mit extrem begrenzten Ressourcen (Ib/A).
HSV-Typ-spezifische Serologie
- Nicht routinemäßig bei asymptomatischen Patientinnen (IV/C)
- Kann unter folgenden Umständen von Nutzen sein:
- bisher rezidivierender Verlauf oder atypischer Herpes genitalis und negatives Ergebnis direkter Virusnachweismethoden (III/B)
- Ersterkrankung mit Herpes genitalis, wenn die Unterscheidung zwischen Erstinfektion und latenter Infektion für Beratung und Therapieplanung relevant ist (III/B).
- Sexualpartner*innen von Patientinnen mit Herpes genitalis, wenn Fragen zu einer möglichen Ansteckung aufkommen. Serodiskordante Paare können über Strategien zur Reduktion des Infektions- und Erkrankungsrisikos aufgeklärt werden (Ib/A).
Indikationen zur Überweisung
- Normalerweise nicht indiziert
- Antikörper werden 2–3 Wochen nach einer Primärinfektion gebildet; eine dahingehende Untersuchung kann hinsichtlich einer Ansteckungsproblematik bei Schwangeren zweckmäßig sein.
- U. U. nötig, um eine evtl. Ansteckung der Partner*innen festzustellen.
- Bei indizierter Blasenkatheterisierung
- Zur Klärung der Frage, ob ein suprapubischer Katheter besser zur Symptomlinderung geeignet ist.
Indikationen zur Krankenhauseinweisung
- Eine stationäre Behandlung kann erforderlich sein bei:
- Herpes-Episode in der Schwangerschaft
- starken Schmerzen
- Immunsuppression
- besonders schweren und häufigen Episoden
- Komplikationen
- stark beeinträchtigtem Allgemeinzustand
- Harnverhalt
- Meningismus
- ungünstiger psychosozialer Situation (z. B. Obdachlosigkeit, Suchterkrankung).
Therapie
Therapieziele
- Beschwerden lindern.
- Krankheitsdauer bei Erstmanifestation verkürzen.
- Rezidivrate reduzieren.
- Ansteckungsrisiko reduzieren.
Allgemeines zur Therapie
- Bei Primärerkrankung
- Eine Behandlung mit oral verabreichten antiviralen Mitteln wird innerhalb der ersten 5 Tage nach Beginn der Episode empfohlen.
- Es gibt keine Therapie, die den natürlichen Verlauf der Virusinfektion verändert.
- Bei Rezidiven
- Meist ist keine medikamentöse Behandlung notwendig, sie kann jedoch die Dauer des Krankheitsschubs verkürzen und Beschwerden lindern und sollte deshalb bei einem schweren Schub angeboten werden.
- Suppressionsbehandlung (Langzeitbehandlung)
- Kann bei häufigen und schmerzhaften Rezidiven indiziert sein.
- Latente Virusinfektion
- Bei einer latenten Virusinfektion gibt es keine wirksame Behandlung, die Rezidivfrequenz kann nicht beeinflusst werden.
- Die Langzeitbehandlung von Personen mit HSV-2 reduziert die Gefahr der Ansteckung von zuvor nicht exponierten Partner*innen.
- Die Ansteckungsgefahr wird reduziert, die Viren jedoch werden weder durch eine Standardtherapie noch durch eine Hochdosistherapie mit Virostatika komplett eliminiert.9
- Bei einer latenten Virusinfektion gibt es keine wirksame Behandlung, die Rezidivfrequenz kann nicht beeinflusst werden.
Empfehlungen für Patientinnen
- Wundpflege: Leitungswasser in Körpertemperatur kann zum vorsichtigen Abspülen der befallenen Areale/wunden Stellen verwendet werden.
- Seifenwasser wird nicht empfohlen.
- Bei schlechter Wasserqualität kann isotone Kochsalzlösung verwendet werden.
- Keine engen Hosen tragen. Locker sitzende Kleidung ist von Vorteil.
- Den betroffenen Bereich sauber und trocken halten, um eine Sekundärinfektion zu vermeiden.
- Schmerzen lassen sich durch Lokalanästhetika, wie z. B. Lidocain, lindern.
- Läsionen möglichst nicht berühren und nach einem Kontakt immer die Hände waschen.
- Sexuelle Abstinenz während der akuten Episode
- Bei serodiskordanten Sexualpartner*innen reduzieren Kondome das Risiko einer HSV-Übertragung.
Medikamentöse Therapie
- Virostatische Behandlung mit Nukleosidanaloga wird bei akuter Primärerkrankung und bei Rezidiven empfohlen, die Beschwerden auslösen.
- Es gibt keine Therapie, die den natürlichen Verlauf der Erkrankung beeinflusst.
- Suppressionsbehandlung bei Patientinnen mit häufig rezidivierendem Herpes genitalis
- Kann die Virusabscheidung sowohl während des Rezidivs als auch während der asymptomatischen Phasen reduzieren.
- Vermindert das Risiko für eine Übertragung auf seronegativen Sexualpartner*innen (Ib/A).
Primärerkrankung2-3
- Oral verabreichte Nukleosidanaloga spätestens 5 Tage nach Auftreten der ersten Symptome
- Verkürzen die Episode um ca. 3 Tage, die Phase mit lokalen Schmerzen um ca. 2 Tage, die Virusausscheidung um ca. 7 Tage und die Zeit bis zum Abheilen der Läsionen um ca. 6 Tage.
- Empfohlene Regimes10
- Aciclovir 3 x täglich 400 mg – oder –
- Aciclovir 5 x täglich 200 mg – oder –
- Famciclovir 3 x täglich 250 mg – oder –
- Valaciclovir: 2 x täglich 500 mg
- Die Behandlung dauert 7–10 Tage, abhängig von der Symptomschwere und -persistenz.
- Eine intravenöse Behandlung ist nur dann angezeigt, wenn eine orale Applikation wegen Schluckbeschwerden oder Erbrechen nicht möglich ist.
Rezidiv2-3
- Eine medikamentöse Behandlung ist meist nicht notwendig. Wenn die Behandlung aber frühzeitig eingeleitet wird, idealerweise während der Prodromalphase, dann lässt sich die Dauer des Krankheitsschubs um einige Tage verkürzen, und die Symptome fallen milder aus.
- Eine frühzeitige Behandlung kann verhindern, dass herpetische Hautläsionen entstehen.
- Wenn bereits innerhalb 24 Stunden nach dem Auftreten der ersten Symptome behandelt wird, sind die Chancen am besten, dass die Episode schnell beendet werden kann.
- Es ist daher sinnvoll, wenn Patientinnen mit rezidivierendem Herpes genitalis eine Stand-by-Medikation vorhalten.
- Falls überhaupt Medikamente eingesetzt werden, sollte an erster Stelle eine Ultrakurzzeittherapie versucht werden (Ib/A):
- Aciclovir 3 x tgl. 800 mg über 2 Tage – oder –
- Famciclovir 2 x tgl. 1.000 mg an einem Tag – oder –
- Valaciclovir 2 x tgl. 500 mg über 3 Tage.
- Alternativ kann eine 5-tägige Behandlung erfolgen, mit:
- Aciclovir 3 x tgl. 400 mg (über 3–5 Tage) – oder –
- Aciclovir 2 x tgl. 800 mg – oder –
- Valaciclovir: 1 x tgl. 1.000 mg – oder –
- Famciclovir 2 x tgl. 125 mg.
Suppressionstherapie (Langzeitbehandlung)2-3
- Eine Langzeitbehandlung mit antiviralen Mitteln reduziert Rezidivfrequenz und Virusausscheidung.
- Bei Krankheitsverläufen mit mehr als 5 Rezidiven pro Jahr senkt die Suppressionsbehandlung die Rezidivhäufigkeit um 70–80 %.
- Bei den meisten Patientinnen werden trotz Behandlung gelegentlich Rezidive auftreten.
- Aciclovir ist die in der Suppressionstherapie am besten untersuchte Substanz.
- Mögliche Regimes
- Aciclovir 2 x tgl. 400 mg
- Valaciclovir 1 x tgl. 500 mg
- Famciclovir 2 x tgl. 250 mg
- Valaciclovir- oder Famciclovir-Dosis verdoppeln.
- bei immungeschwächten Erkrankten
- evtl. bei unzureichendem Ansprechen auf die Behandlung
- Spätestens nach 6 Monaten sollte der Behandlungszyklus beendet werden, um den weiteren Verlauf zu beobachten (siehe auch Abschnitt Verlaufskontrolle).
- Dann sollte man mindestens so lange abwarten, bis 2 Rezidive auftreten, um sich ein Bild über Rezidivfrequenz und -schwere machen zu können.
- Bei Patientinnen mit erheblichen Beschwerden ist eine Weiterbehandlung vernünftig und sicher (IV, C).
- In vielen Fällen ist eine Behandlung über mehrere Jahre notwendig.
- Eine Alternative ist, dass die Patientin ein antivirales Mittel schnell zur Hand hat und bei einem Rezidiv selbst die Behandlung beginnen kann (s. o.).
- Arzneimittelresistenzen entwickeln sich nur selten.
Sicherheit und Verträglichkeit von Nukleosidanaloga
- Aciclovir ist das Nukleosidanalogon, dessen Verträglichkeit und Sicherheit von allen zur Behandlung von HSV-Infektionen zugelassenen Wirkstoffen am besten untersucht ist.
- Aciclovir, Famciclovir und Valaciclovir sind in der Regel gut verträglich und haben ein ähnliches Nebenwirkungsprofil. Die häufigsten Nebenwirkungen sind:
- Schwindel
- Kopfschmerzen
- Übelkeit und Erbrechen
- Diarrhö
- Abdominalschmerzen
- Juckreiz
- Hautausschlag (einschl. Photosensibilitätsreaktionen)
- Anstieg der Leber-Transaminasen (Famciclovir).
- Blutbildveränderungen
- besonders bei immungeschwächten Patientinnen unter Valaciclovir gelegentlich Leukopenien oder Thrombozytopenien
- unter Famciclovir selten Thrombozytopenien
- unter Aciclovir sehr selten Anämien, Leukopenien oder Thrombozytopenien
- Arzneimittelinteraktionen
- Bei Aciclovir und Famciclovir wurden bislang keine klinisch signifikanten Wechselwirkungen mit anderen Arzneimitteln beobachtet.
- Bei Patientinnen mit eingeschränkter Nierenfunktion ist ggf. eine Dosisanpassung erforderlich.
- Valaciclovir sollte nur mit Vorsicht mit nephrotoxischen Arzneimitteln kombiniert werden, besonders bei Patientinnen mit Nierenfunktionsstörungen. Es sollte eine regelmäßige Überwachung der Nierenfunktion erfolgen. Dies gilt für die gleichzeitige Gabe von:
- Aminoglykosiden
- organischen Platinverbindungen
- jodhaltigen Kontrastmitteln
- Methotrexat
- Pentamidin
- Foscarnet
- Ciclosporin
- Tacrolismus.
- Schwangerschaft
- Aciclovir, Famciclovir oder Valaciclovir scheinen zu keiner erhöhten Inzidenz embryonaler oder fetaler Fehlbildungen zu führen (III).
Lokale Behandlung
- Topisch verabreichte Nukleosidanaloga werden nicht empfohlen, da sie weniger wirksam sind als orale, und weil sie eher zu Resistenzen führen.
- Salzbäder können Linderung verschaffen und unterstützen möglicherweise die Abheilung.
- Vaseline kommt evtl. infrage, um Juckreiz zu lindern, vor Reibung zu schützen und Krusten aufzuweichen.
Schmerztherapie
- Lokale Anwendung lidocainhaltiger Gele oder Salben
- Lindert Schmerzen.
- Kommt auch zur Vorbeugung von Schmerzen beim Wasserlassen und Stuhlgang infrage.
- Bei starken Schmerzen, evtl. mit neuropathischer Komponente (siehe Artikel Schmerzbehandlung, Grundsätze)
Leitlinie: Therapie des Herpes genitalis2-3
- Primärerkrankung
- Patientinnen, die sich innerhalb der ersten 5 Tage vom Beginn der Primärerkrankung vorstellen oder bei denen sich noch neue Läsionen bilden, sollten oral mit antiviralen Substanzen behandelt werden. Orales Aciclovir, Valaciclovir oder Famciclovir ist wirksam, d. h. es reduziert die Schwere und Dauer der aktuellen Episode (Ib/A).
- Topisch verabreichte antivirale Mittel werden nicht empfohlen, da sie weniger wirksam sind als orale, und weil sie eher zu Resistenzen führen (IV/C).
- Salzbäder und eine adäquate Analgesie werden empfohlen.
- Lokalanästhetika bergen zwar das Risiko für eine Kontaktsensibilisierung, unter Lidocain tritt diese jedoch nur selten auf. Lidocainhaltige Gels oder Salben haben sich in der Behandlung des genitalen Herpes als sicher erwiesen. Unter Benzocain ist das Risiko für eine Kontaktsensibilisierung hoch; es sollte daher nicht verwendet werden (IV/C).
- Die Patientinnen stehen oft unter einer hohen psychischen Belastung, die unter einer antiviralen Therapie zurückgehen kann (Ib/A).
- Rezidiv
- Orales Aciclovir, Valaciclovir oder Famciclovir reduziert Dauer und Schwere des Rezidivs um durchschnittlich 1–2 Tage (Ib/A).
- Suppressionsbehandlung
- In der antiviralen Suppressionsbehandlung ist Aciclovir die am besten untersuchte Substanz (Ib/A).
- Die optimale Tagesdosis für eine Suppressionsbehandlung mit Aciclovir ist 800 mg.
- 4 x 200 mg scheinen 2 x 400 mg geringfügig überlegen zu sein (IIb/B).
- Dennoch sollte sich die Verordnung daran orientieren, ob die Patientin in der Lage dazu ist, eine 4-mal tägliche Einnahme zuverlässig einzuhalten.
- Im Vergleich zwischen Valaciclovir 500 mg und Famciclovir 2 x 250 mg zeigten sich keine signifikanten Unterschiede (IV/C).
- Bei Patientinnen, die unzureichend auf Valaciclovir oder Famciclovir ansprechen, kann es erforderlich sein, die Dosis zu verdoppeln (IV/C).
Bei Immunsuppression und HIV-Infektion1-2
- Bei Immunkompromittierten, etwa bei HIV-positiven Patientinnen, ist das Risiko für Komplikationen einer HSV-Infektion erhöht. Die Behandlung erfordert daher ein spezielles Vorgehen.
- HIV-Infizierte haben ein erhöhtes Risiko für eine HSV-Infektion und umgekehrt.
- HSV-Infektionen verstärken die HIV-Replikation und können dadurch die Ansteckung der Partner*innen mit HIV begünstigen.
- Möglicherweise wirkt eine HSV-suppressive Therapie diesem entgegen.
- Das HSV-Rezidivrisiko korreliert mit dem Maß der Immunschwäche.
- Bei ausgeprägter Immunschwäche kann eine Herpeserkrankung chronisch progredient verlaufen.
- Primärerkrankung
- Nach Expertenkonsens ist bei immunkompromittierten Patientinnen zur Behandlung einer primären Herpes-genitalis-Episode ein Mehrfaches der antiviralen Standarddosis notwendig.
- Bei HIV-positiven Patientinnen orientiert sich das Vorgehen am Immunstatus.
- Bei Patientinnen mit normalen CD4-Zahlen ist eine solche Dosisanpassung nicht erforderlich.
- empfohlene Regimes bei HIV-Infektion (IV/C)
- Aciclovir 5 x tgl. 400 mg über 7–10 Tage
- Valaciclovir 2 x tgl. 500–1.000 mg über 10 Tage
- Famciclovir 3 x tgl. 250–500 mg über 10 Tage
- bei fulminantem Herpes-genitalis
- Aciclovir 5–10 mg/kg KG i. v. alle 8 Stunden über 2–7 Tage
- bei klinischer Besserung Umstellung auf orale Medikation
- Insgesamt über mindestens 10 Tage behandeln.
- Rezidiv
- Die meisten Patientinnen kommen mit einer 5-tägigen Behandlung aus.
- Bei Patientinnen mit ausreichenden CD4-Zahlen (> 500 Zellen/mm3) scheinen auch kürzere Regimes auszureichen.
- Für HIV-Positive ohne Hinweise auf Immunschwäche scheinen Standarddosierungen auszureichen (Ib/A).
- Bei Patientinnen mit fortgeschrittenem AIDS kann es erforderlich sein, die Standarddosis zu verdoppeln und länger als 5 Tage zu behandeln (Ib/B).
- Ultrakurzzeittherapien sollten nur mit Vorbehalt eingesetzt werden, denn sie wurden bislang nicht ausreichend in der Behandlung immunkompromittierter Patientinnen erprobt.
- Suppressionstherapie
- Scheint bei HIV-Positiven weniger wirksam zu sein als bei HIV-Negativen, bei ebenfalls guter Verträglichkeit.
- Kann die HI-Viruslast reduzieren, eignet sich aber nicht als alleinige Therapie einer HIV-Infektion.
- Die HSV-Suppressionstherapie sollte bei HIV-Patientinnen immer wieder probeweise unterbrochen werden, besonders wenn die CD4-Zahl ansteigt.
- Wenn die Herpes-Episoden abnehmen, kann eine Fortsetzung der suppressiven Therapie evtl. unterbleiben.
- Wenn ohne Suppressionstherapie wieder so häufige Rezidive auftreten wie vor der Behandlung, kann es notwendig sein, diese wieder aufzunehmen (IV/C).
- empfohlene Regimes
- Aciclovir 2–3 x tgl. 400 mg
- Valaciclovir 2 x tgl. 500 mg
- Bei unzureichendem Ansprechen sollte zunächst die Dosis verdoppelt werden.
- Bei anhaltendem Therapieversagen kann ein Behandlungsversuch mit Famciclovir 2 x tgl. 500 mg unternommen werden (IIa/B).
Beratung und psychosoziale Unterstützung
- Offen sprechen über:
- Risiken einer sexuellen Übertragung
- Auch in einer monogamen Beziehung eines serodiskordanten Paares können asymptomatische Infizierte sogar noch nach Jahren die seronegativen Partner*innen anstecken.
- den Verlauf der Erkrankung einschließlich häufiger subklinischer Virusausscheidung
- Behandlungsmöglichkeiten
- Möglichkeiten und Grenzen präventiver Maßnahmen
- begrenzte HSV-Schutzwirkung von Kondomen und antiviraler Therapie
- Risiken einer sexuellen Übertragung
- Die Frage, ob und wem gegenüber die Patientin ihren Infektionsstatus offenlegen soll, erfordert eine pragmatische und der individuellen Situation angepasste Beratung.
- Dabei sollte die geringe körperliche Beeinträchtigung durch eine subklinische Infektion und deren hohe Prävalenz in der Bevölkerung betont werden.
- Sehr wichtig ist eine sorgfältige Aufklärung über die Risiken einer Herpes-genitalis-Infektion während Schwangerschaft und Entbindung einschließlich des Risikos einer Übertragung auf das Neugeborene.
- Von besonderer Bedeutung ist das auch für medizinisches Personal in der Geburtshilfe.
- Die meisten Patientinnen werden mit 1–2 Beratungsgesprächen auskommen.
- Es ist allerdings schwer vorherzusagen, wie viel Zeit jemand braucht, um sich mit den Gegebenheiten zu arrangieren.
- Weitere aufmerksame Begleitung ist wichtig.
- Patientinnen, die nach 3–6 Monaten weiterhin Schwierigkeiten mit der Krankheitsbewältigung haben, benötigen intensivere psychosoziale Unterstützung.
Vorbeugung einer Virusübertragung
- Sexuelle Abstinenz
- Einzige Methode, eine Virusübertragung sicher zu vermeiden.
- Sollte zumindest während jeder akuten Episode eingehalten werden.
- Beim Oralsex kann eine Ansteckung mit HSV-1 über den Mund an die Genitalien erfolgen.
- Auch beim Petting ist eine Übertragung möglich.
- Auch die asymptomatischen Regionen der genitalen Haut und Schleimhäute können Viren absondern.
- Erhöhte Gefahr einer neonatalen Herpesinfektion bei einer Primärinfektion besteht in den letzten 5 Wochen vor der Geburt.
- hohes Risiko bei HSV-2-seronegativen Schwangeren und HSV-2-seropositiven Partner*innen
- Geringes Risiko bei Frauen, die eine Infektion bereits durchgemacht haben, auch wenn während der Schwangerschaft ein Rezidiv auftritt.
- Eine Übertragung kann auch über orale Läsionen nach der Geburt erfolgen.
- Kondome vermindern das Übertragungsrisiko, schließen eine Übertragung jedoch nicht vollständig aus.
- Evtl. Suppressionstherapie
- Bei Erstmanifestation sowie bei Rezividausbrüchen mit starken Beschwerden wird eine antivirale Behandlung empfohlen.
- Virostatika verkürzen die Zeit der Virusausscheidung und der Ansteckungsgefahr (Ib).
- Um eine Ansteckung Neugeborener zu vermeiden, sollte medizinisches Personal mit akutem Herpes nicht im Kreissaal bzw. auf der Neugeborenenstation eingesetzt werden.
- Eine Primärinfektion in der Schwangerschaft sollte unbedingt vermieden werden (siehe Abschnitt In der Schwangerschaft).
In der Schwangerschaft
- Die Gefahr der Übertragung auf das Kind ist gering, wenn es sich um keine Primärinfektion handelt.
- Eine präventive Behandlung mit antiviralen Mitteln reduziert die Gefahr des Ausbruchs bei der Geburt; das Risiko ist jedoch gering und daher von fraglicher klinischer Relevanz.
- Eine Primärinfektion in der Schwangerschaft sollte unbedingt vermieden werden.
- Läsionen im Geburtskanal können bei einem infizierten Neugeborenen zu Virämie, Hepatitis und Enzephalitis führen. Die Mortalität ist in diesen Fällen hoch.
- Das Risiko für eine Mutter-Kind-Übertragung ist bei einer Primärinfektion im 3. Trimenon besonders hoch.
- Weil während der Geburt oft große Virusmengen abgesondert werden, sollte man bei diesen Frauen einen Kaiserschnitt in Erwägung ziehen, besonders bei Patientinnen, die innerhalb von 6 Wochen vor Entbindung Symptome aufweisen (Ib/B).11
- Eine Suppressionstherapie mit 3 x tgl. 400 mg Aciclovir bis zur Entbindung sollte erwogen werden.
- Wenn die vaginale Geburt bei bestehender HSV-Läsion nicht aufzuhalten ist, sollte die Fruchtblase möglichst lange intakt bleiben, Skalp-Elektroden vermeiden, pädiatrisch-fachärztliche Mitbehandlung.
- Auch fetale Blutentnahmen, etwa für eine Mikroblutuntersuchung (MBU), sollten unterlassen werden.
- Die gegen HSV eingesetzten Medikamente scheinen zu keiner erhöhten Inzidenz embryonaler oder fetaler Fehlbildungen zu führen (III).
- Ggf. lokale Behandlung
Verlauf, Komplikationen und Prognose
Verlauf
Primärinfektion
- Die Inkubationszeit beträgt in der Regel 3–7 Tage.
- Die Symptome bei einer exogenen Primärerkrankung können bis zur Genesung 2–4 Wochen andauern.
- Bei vielen Patientinnen verläuft die Infektion asymptomatisch, sie können jedoch trotzdem andere Personen anstecken.
- Bei Personen, die an Herpes oralis (HSV-1) erkrankt waren, kann die Genitalherpes-Infektion (HSV-2) milder ausfallen.
- Beim Oralsex kann eine Ansteckung mit HSV-1 über den Mund an die Genitalien erfolgen.
Spätere Infektionen
- Rezidive verursachen meist nur leichte Schmerzen, sind von kürzerer Dauer (1–2 Wochen) und verursachen weniger wunde Stellen.
- Darüber hinaus kommt es zu einer Virusausscheidung der Genitalschleimhaut, während die subjektiven Symptome atypisch sind oder ganz fehlen.
- Bei HSV-1-Seropositiven, die sich genital mit HSV-2 infizieren (Primärerkrankung bei nichtprimärer Infektion), fällt der Krankheitsverlauf relativ mild aus.
Prodromi
- Prodromi weisen darauf hin, dass man mit einem Rezidiv aufgrund einer Reaktivierung einer latenten Infektion zu tun hat.
Komplikationen
- Schwere oder lebensbedrohliche Komplikationen sind selten und betreffen vor allem immungeschwächte, z. B. HIV-infizierte Patientinnen.
- Extragenitale Herde, meist durch eine vom Genitale ausgehende Autoinokulation, z. B. am:
- Gesäß und Anus
- Rektum (Herpes-Proktitis)
- Finger (Herpes-Paronychie)
- Auge (Keratoconjunctivitis herpetica)
- Oropharynx.
- Opportunistische Infektionen, häufig mit Pilzen
- Harnverhalt
- durch urethrale Läsionen
- neurogen: Blasenlähmung
- Spontane benigne Meningitis
- 36 % der Frauen mit Herpes genitalis
- Herpesenzephalitis
- Fieber?
- Kopfschmerzen?
- Verhaltensauffälligkeiten?
- Krampfanfall?
- Sakrale Radikulomyelopathie
- Befall sensorischer und autonomer Nerven
- meist im Verlauf einer Herpes-Proktitis
- schwere Komplikation mit günstiger Prognose
- Abheilung innerhalb von 2–4 Wochen
- Psychosoziale Folgen12
- Eczema herpaticum
- Disseminierter Virus-Befall
- Leberbefall mit fulminanter Hepatitis
- Pneumonie
- Neonatale HSV-Infektion (siehe Abschnitt In der Schwangerschaft)
- Eine HSV-2-Infektion ist mit einem erhöhten Risiko für eine Infektion mit HIV-assoziiert (siehe Abschnitt zur Immunsuppression und HIV-Infektion).
Prognose
- Die meisten Infizierten entwickeln keine Symptome, können aber zeitweise das Virus absondern.
- Rezidive bei Infektion mit HSV-1
- Wurde die primäre Episode eines Herpes genitalis exogen durch HSV-1 ausgelöst, kommt es selten zu Rezidiven.
- Die durchschnittliche Dauer bis zur nächsten Episode beträgt ca. 1 Jahr.
- Rezidive bei Infektion mit HSV-2
- Wurde die primäre Episode eines Herpes genitalis exogen durch HSV-2 ausgelöst, liegt die Wahrscheinlichkeit eines Rezidivs bei 80–90 %.
- Die durchschnittliche Anzahl von Rezidiven beträgt 4 pro Jahr, die durchschnittliche Dauer bis zum ersten Rezidiv 50 Tage.
- Häufig nimmt die Frequenz der Krankheitsschübe im Lauf der Jahre ab.
- Krankheitsverlauf
- Die klinische Manifestation ist bei beiden Typen gleich, bei HSV-2 kommt es aber deutlich häufiger zu Rezidiven.
- Bei Patientinnen mit schwerer Primärerkrankung, die z. B. länger als 35 Tage andauert, kommt es häufiger zu Rezidiven, und die Zeitabstände zwischen den Rezidiven fallen kürzer aus.
- Bei Frauen sind Rezidive seltener als bei Männern.
Verlaufskontrolle
- Nach Therapie einer akuten Episode
- bis zum Abklingen der Symptome
- So lange die Patientin Beratungsbedarf hat (siehe Abschnitt Beratung und psychosoziale Unterstützung).
- Evtl. weitere Kontrolluntersuchungen, wenn andere Ursachen genitaler Ulzera ausgeschlossen werden sollen oder begleitend vorliegen.
- Die Patientin ausdrücklich dazu einladen, sich bei Problemen mit Rezidiven jederzeit erneut vorzustellen.
- Unter Suppressionstherapie
- Therapiezyklus über maximal 6 Monate
- Danach absetzen und erneut evaluieren, wie hoch die Rezidivfrequenz ohne Medikation ist.
- Dabei sollte man mindestens so lange abwarten, bis 2 Rezidive auftreten, um sich ein Bild über Rezidivfrequenz und -schwere machen zu können.
- Wenige Patientinnen werden nach Absetzen der Medikation eine niedrigere Rezidivfrequenz erreichen als vor Beginn der Suppressionsbehandlung.
Patienteninformationen
Worüber sollten Sie die Patientinnen informieren?
- Über Ursache, Behandlung, Prognose und vorbeugende Maßnahmen (siehe Abschnitt Beratung und psychosoziale Unterstützung)
Patienteninformationen in Deximed
Illustrationen
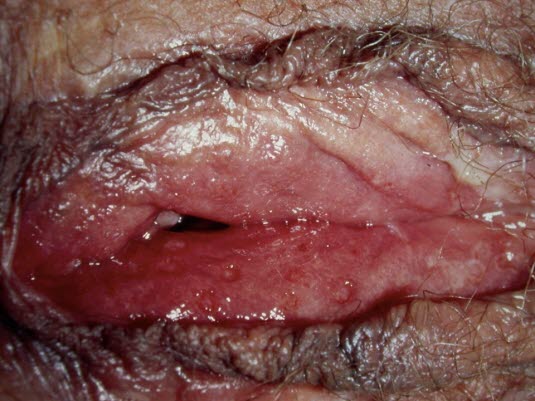
Herpes genitalis
Quellen
Leitlinien
- Deutsche STI-Gesellschaft (DSTIG). Sexuell übertragbare Infektionen (STI) – Beratung, Diagnostik und Therapie. AWMF-Leitlinie Nr. 059-006. S2k, Stand 2018. www.awmf.de
Literatur
- Centers for Disease Control and Prevention. 2015 sexually transmitted diseases treatment guidelines: genital HSV infections. Accessed February 14, 2022 www.cdc.gov
- International Union against Sexually Transmitted Infections. 2017 European guidelines for the management of genital herpes. iusti.org
- Deutsche STI-Gesellschaft (DSTIG). Sexuell übertragbare Infektionen (STI) – Beratung, Diagnostik und Therapie. AWMF-Leitlinie Nr. 059-006, Klasse S2k Stand 2018. www.awmf.org
- Sauerbrei A. Optimal management of genital herpes: current perspectives. Infect Drug Resist 2016; 9: 129-41. PMID: 27358569 PubMed
- Lorenz BD. Herpes simplex virus infection. BMJ Best Practice. Last reviewed: 14 Jan 2022; last updated: 27 Jan 2022. bestpractice.bmj.com
- Groves MJ. Genital herpes: a review. Am Fam Physician 2016; 93: 928-34. PMID:27281837 PubMed
- Bernstein DI, Bellamy AR, Hook EW III, et al. Epidemiology, clinical presentation, and antibody response to primary infection with herpes simplex virus type 1 and type 2 in young women. Clin Infect Dis. 2013; 56(3): 344–351. pmid:23087395 PubMed
- Deutsches Institut für Medizinische Dokumentation und Information (DIMDI): ICD-10-GM Version 2022. Stand 17.09.2021; letzter Zugriff 14.02.2022. www.dimdi.de
- Johnston C, Saracino M, Kuntz S, et al. Standard-dose and high-dose daily antiviral therapy for short episodes of genital HSV-2 reactivation: three randomised, open-label, cross-over trials. Lancet 2012; doi:10.1016/S0140-6736(11)61750-9. DOI
- Patel R, Kennedy O, Clarke E et al. European guideline for the management of genital herpes. IUSTI / WHO European STD guidelines Editorial Board. 201724. Stephenson-Famy A, Gardella C. Herpes simplex virus infection during pregnancy. Obstet Gynecol Clin North Am 2014; 41(4): 601–614.
wwwpubmed.iustincbi.orgnlm.nih.gov - Stephenson-Famy A, Gardella C.. Herpes simplex virus infection during pregnancy. Obstet Gynecol Clin North Am 2014; 41(4): 601–614. pubmed.ncbi.nlm.nih.gov
- Dunphy K. Herpes genitalis and the philosopher's stance. J Med Ethics 2014; 40(12): 793–797. jme.bmj.com
Autor*innen
- Thomas M. Heim, Dr. med., Wissenschaftsjournalist, Freiburg
- Die ursprüngliche Version dieses Artikels basiert auf einem entsprechenden Artikel im norwegischen hausärztlichen Online-Handbuch Norsk Elektronisk Legehåndbok (NEL, https://legehandboka.no/).