Allgemeine Informationen
Definition
- International bestehen verschiedene Definitionen der akuten Bronchiolitis.1
- In Europa wird meistens nur die erste Krankheitsmanifestation einer viralen Infektion der unteren Atemwege in den ersten 12 Lebensmonaten als akute Bronchiolitis bezeichnet.
- In Nordamerika wird jede virale Infektion der unteren Atemwege in den ersten 24 Lebensmonaten, unabhängig von der Anzahl des Auftretens, akute Bronchiolitis genannt.
- Überschneidung mit dem Begriff der obstruktiven Bronchitis im deutschsprachigen Raum2
Häufigkeit
- Prävalenz von akuten Bronchiolitiden im 1. Lebensjahr 18–32 %3
- Im 1. Lebensjahr häufigster Grund für Hospitalisierungen2
- Etwa 3 % aller Kinder werden in ihrem 1. Lebensjahr wegen einer akuten Bronchiolitis stationär behandelt.4
RS-Virus-Infektionen
- Ist der häufigste Erreger von Erkrankungen der unteren Atemwege (Bronchiolitis, Bronchitis, Pneumonie) in den ersten beiden Lebensjahren.5
- Nach aktuellen Schätzungen kommen RSV-Atemwegserkrankungen weltweit mit einer Inzidenz von 48,5 Fällen und 5,6 schweren Fällen pro 1.000 Kindern im ersten Lebensjahr vor.6
- RSV-Infektionen treten saisonal auf, in Mitteleuropa ist die Inzidenz von November bis April am höchsten (RSV-Saison); der Gipfel liegt meist im Januar und Februar.2
Ätiologie und Pathogenese
- Die Erkrankung wird in den meisten Fällen (70 %) durch das Respiratory-Syncytial-Virus (RSV) verursacht7, weitere häufige Erreger sind das Metapneumovirus (hMPV) und das Parainfluenzavirus Typ 3.8
RS-Virus-Infektionen6
- Das RS-Virus ist ein RNA-Virus aus der Familie der Paramyxoviren.
- Inkubationszeit
- 2–8 Tage (durchschnittlich 5 Tage)
- Infektionsweg
- primär durch Tröpfcheninfektion (direkte Übertragung und über Aerosole)9
- Eine indirekte Übertragung über kontaminierte Hände, Gegenstände und Oberflächen ist wahrscheinlich möglich.
- RSV kann in respiratorischem Sekret 20 min auf Händen überleben, 45 min auf Papierhandtüchern und Baumwollkitteln und bis zu mehreren Stunden auf Einmalhandschuhen, auf Stethoskopen und auf Kunststoffoberflächen.
- Jugendliche und Erwachsene spielen als asymptomatische oder symptomarme Überträger eine Rolle.
- Kontaktpersonen der Patient*innen (auch medizinisches Personal) können zu einer raschen, auch nosokomialen Ausbreitung beitragen, wenn Schutz- und Hygienemaßnahmen lückenhaft sind.
- Säuglinge in den ersten 4–6 Lebenswochen sind meistens durch diaplazentar übertragene Antikörper geschützt, Frühgeborene können wegen einer geringeren Versorgung mit maternalen Antikörpern auch in den ersten Lebenswochen bereits schwer erkranken.
- Infektiosität
- Sie beginnt einen Tag nach der Ansteckung, also noch vor Symptombeginn.
- Die Dauer beträgt 3–8 Tage bei immunkompetenten Patient*innen.
- Frühgeborene, Neugeborene, immundefiziente oder immunsupprimierte Patient*innen können das Virus über mehrere Wochen, im Einzelfall über Monate ausscheiden.
- Pathophysiologie
- Die Infektion führt zu einer reversiblen Schädigung der zilientragenden Epithelzellen der Atemwegsschleimhaut.
- Durch Zelldetritus, einwandernde unspezifische und spezifische Abwehrzellen und Mukus werden die Bronchiolen verlegt.
- Dies führt zu Obstruktion und begünstigt die Entstehung von nicht belüfteten (Atelektasen), aber auch von kompensatorisch zu stark belüfteten Lungenarealen (Überblähung).
- Das gestörte Gleichgewicht zwischen Ventilation und Perfusion führt zu Hypoxämie.8
Disponierende Faktoren
- Das Risiko einer RSV-Infektion ist erhöht für:5
- Kinder bis zum 6. Lebensmonat
- Mehrlingsgeburt
- neonatale respiratorische Komplikationen
- Kinder mit Geschwisterkindern im Kleinkindalter
- Nikotinexposition durch Eltern oder im Haushalt
- Unterernährung
- positive Familienanamnese für atopische Erkrankungen oder Asthma.
- Das Risiko einer schweren RSV-Infektion ist erhöht für:6
- Frühgeborene
- Kinder mit pulmonalen Vorerkrankungen (z. B. bronchopulmonale Dysplasie, zystische Fibrose, neurologische und muskuläre Erkrankungen mit eingeschränkter Ventilation)
- Kinder mit Herzfehlern mit vermehrter Lungendurchblutung
- Erwachsene mit kardialen oder pulmonalen Vorerkrankungen
- alle immundefizienten und immunsupprimierten Personen
- Besonders gefährdet sind Empfänger*innen hämatopoetischer Zelltransplantate, von Lungen- oder anderen Organtransplantaten sowie stark immunsupprimierte Patient*innen mit maligner hämatologischer Erkrankung.
- Kein erhöhtes Risiko weisen Kinder auf,5
- die einen hämodynamisch nicht relevanten Herzfehler haben, wie z. B. persistierendes Foramen ovale, bikuspide Aortenklappe, leichte und nicht therapiebedürftige Pulmonal-, Aorten- oder Aortenisthmusstenose, kleiner isolierter Vorhof- oder Ventrikelseptumdefekt sowie ein kleiner Ductus arteriosus.
- deren Herzfehler adäquat korrigiert wurden (Operation/Intervention), wenn sie nicht noch wegen einer Herzinsuffizienz medikamentös behandelt werden müssen oder andere Risikofaktoren haben.
ICPC-2
- R78 akute Bronchitis / Bronchiolitis
ICD-10
- J21 akute Bronchiolitis
- J21.0 Akute Bronchiolitis durch Respiratory-Syncytial-Viren [RS-Viren]
- J21.1 Akute Bronchiolitis durch humanes Metapneumovirus
- J21.8 Akute Bronchiolitis durch sonstige näher bezeichnete Erreger
- J21.9 Akute Bronchiolitis, nicht näher bezeichnet
Diagnostik
Diagnostische Kriterien
- Die Bronchiolitis ist eine klinische Diagnose, die auf Grundlage einer typischen Anamnese (Säuglinge, Auftreten in Wintermonaten) und dem klinischen Befund (obstruktive Ventilationsstörung mit reduziertem AZ) gestellt wird.
- Cave: Da die klinischen Befunde innerhalb von Minuten stark variieren können, sollten die Befunde mehrfach erhoben werden.10
- Die Bestimmung von Atemfrequenz und Sauerstoffsättigung bei Raumluft sowie die Beurteilung von thorakalen Einziehungen und der Ernährungssituation erlauben eine Einteilung der akuten Bronchiolitis in 3 Schweregrade.2
Schweregrade
- Der gesamte Abschnitt basiert auf dieser Referenz.11
Leicht
- Atemfrequenz/min: < 40
- O2-Sättigung unter Raumluft (%): > 92
- Sternale/thorakale Einziehungen: fehlend
- Ernährung: problemlos
Mittel
- Atemfrequenz/min: 40–70
- O2-Sättigung unter Raumluft (%): 88–92
- Sternale/thorakale Einziehungen: eher mild ausgeprägt
- Ernährung: schwierig
Schwer
- Atemfrequenz/min: > 70
- O2-Sättigung unter Raumluft (%): < 88
- Sternale/thorakale Einziehungen: stark ausgeprägt
- Ernährung: unmöglich
Differenzialdiagnosen
- Akute Bronchitis
- Asthma
- Asthmaanfall
- Pseudokrupp
- Fremdkörper in den Atemwegen
- Lungenentzündung
- Weitere siehe Artikel Atembeschwerden bei Kindern.
Anamnese
- Zu Beginn meist Zeichen eines unkomplizierten Atemwegsinfektes wie verstopfte Nase, Pharyngitis, leichtes Fieber und Husten.
- Bei einem Teil der Patient*innen nimmt die Erkrankung nur einen milden Verlauf, vor allem bei Kindern, die bereits eine RSV-Infektion hatten.
- Nach 1–3 Tagen wird der Husten ausgeprägter, die Atemfrequenz steigt auf > 40–50 pro min, typischerweise mit exspiratorischem Giemen.
- Es kommt häufig zu subkostalen, interkostalen oder jugulären Einziehungen (Einsatz der Atemhilfsmuskulatur).
- Es treten Schwierigkeiten bei der Nahrungsaufnahme (Trinkverweigerung, Reflux, Erbrechen, Dehydratation) auf.
- Apnoen können vorkommen und sind ein Zeichen für einen schwerwiegenderen Verlauf.
Klinische Untersuchung
- Cave: Stark variierende Symptomatik, Schweregrad kann sich innerhalb von Minuten deutlich verändern!2
- Bestimmung der Atemfrequenz, in der Regel Tachypnoe
- Fieber in etwa 1/3 der Fälle10
- In schweren Fällen Zyanose und sichtbarer Gebrauch der Atemhilfsmuskulatur (juguläre, subkostale, interkostale Einziehungen)
- Charakteristischer Auskultationsbefund ist ein vorwiegend endinspiratorisches Knisterrasseln („Crackles"), verursacht durch den erhöhten Strömungswiderstand in den mit Sekret gefüllten distalen Bronchiolen.2
- Dehydrierung als Folge von Fieber und reduzierter Flüssigkeitszufuhr
- Bei sehr jungen Säuglingen zentrale Apnoe möglich2
Ergänzende Untersuchungen in der Hausarztpraxis
- Blutuntersuchungen werden nicht routinemäßig empfohlen, da bakterielle Sekundärinfektionen selten sind.2
- Messung der Sauerstoffsättigung
- Mikrobiologie
Diagnostik bei Spezialist*innen
- Mikrobiologie
- Bei Krankenhausbehandlung ggf. zur Kohortenisolierung und Verhinderung nosokomialer Infektionen13
- Methoden6
- PCR, sehr spezifisch, schnell und hochsensitiv, zum Nachweis von RSV und anderen Erregern von Atemwegsinfektionen
- Antigennachweis durch Schnelltests, meist auf Enzym-Immunoassays (EIA) basierend, Sensitivität 50–90 % und Spezifität 75–100 %, der positive Vorhersagewert hängt stark vom Alter der Patient*innen und von der Saison ab (Vortest-Wahrscheinlichkeit).
- Röntgenthorax
Indikationen zur Klinikeinweisung
- Klinikeinweisung bei Zeichen eines schweren Verlaufs
- deutliche Atemwegsobstruktion, Apnoen, Zyanose, ausgeprägte Tachypnoe, Erschöpfung und Dehydrierung15
- Frühe Klinikeinweisung bei Risikopatient*innen
- Beachtung geografischer Faktoren (z. B. ein langer Anfahrtsweg zum Krankenhaus) und sozialer Aspekte (Adäquate Versorgung gewährleistet? Kann eine Verschlechterung des Zustands rechtzeitig erkannt werden?)2
Therapie
Therapieziele
- Hypoxie verhindern.
- Lungenfunktion verbessern.
Allgemeines zur Therapie
- Die wichtigsten Therapieansätze sind rein supportive Maßnahmen und bestehen aus minimalem Handling sowie Sicherung einer ausreichenden Hydratation und Oxygenierung.2
- NaCl-Tropfen und abschwellende Nasentropfen (cave: korrekte Dosierung bei Xylometazolin 0,025 %) für die jüngsten Kinder. Alles, was die Respirationsarbeit erleichtert, ist gut!
Schwer zu dosierende abschwellende Nasentropfen (Xylometazolin 0,025 % mit Tropfpipette, Otriven) sind erst für Kinder ab 1 Jahr zugelassen.- Folgende Behandlungen werden nicht empfohlen:
- systemische oder inhalative Glukokortikoide
- Beta-Agonisten
- Anticholinergika.16-17
- Antibiotika
- Selten indiziert, da das Risiko einer sekundären bakteriellen Infektion unter 1 % liegt.18
Medikamentöse Therapie
Sauerstoffgabe
- Sauerstoffsupplementierung bei peripherer Sättigung < 90 % (amerikanische Leitlinie)19 bzw. < 92 % (australische und britische Leitlinien)20-21
- Supplementierung bei < 90 % im Vergleich zu < 94 % genau so effektiv und sicher22
Flüssigkeitsgabe
- Bei unzureichender Trinkmenge i. v. Flüssigkeitsgabe oder über transnasale/orale Magensonde2
- Die britische Leitlinie empfiehlt bevorzugte Applikation über eine Sonde.20
Adrenalin-Inhalation
- Adrenalin reduziert die bronchotracheale Sekretion und das Schleimhautödem und sorgt bei Bronchiolitis in den ersten 24 Stunden für kurzzeitige Besserung.23
- Die Gabe von Adrenalin beeinflusst nicht den langfristigen Verlauf der Bronchiolitis.6
- Weder bei ambulant noch stationär behandelten Kindern verbessert sich das finale Outcome.24
- Die Mehrzahl der internationalen Leitlinien empfiehlt daher überhaupt keine bzw. keine routinemäßige Anwendung von Epinephrin-Inhalationen.10
Weitere Therapien (im Krankenhaus)
- CPAP oder Respiratorbehandlung kann erforderlich sein.25
Prävention
- Einhalten allgemeiner Hygieneregeln, um die Ausbreitung zu minimieren.
- regelmäßiges Händewaschen
- hygienisches Husten und Niesen
- Reinigung evtl. kontaminierter Gegenstände (Kinderspielzeug)26
- Eine gute Handhygiene ist die wichtigste, vorbeugende Maßnahme sowohl zuhause als auch im Krankenhaus.27
- Die Ansteckungsgefahr stellt auf Kinderstationen ein großes Problem dar.
- Passivrauchen vermeiden.5
- Eine medikamentöse Prophylaxe kann bei Hochrisiko-Säuglingen indiziert sein.
Impfung
- Eine aktive Impfung gegen RSV ist derzeit nicht verfügbar.5
Medikamentöse Prophylaxe mit Palivizumab5
- Humanisierter monoklonaler Antikörper gegen das F-Protein von RS-Viren
- Zugelassen für Risikokinder
- bei Frühgeborenen ≤ 35 Schwangerschaftswochen im 1. Lebensjahr bzw. zusätzlich im 2. Lebensjahr für behandlungsbedürftige Frühgeborene mit bronchopulmonaler Dysplasie
- Kinder unter 2 Jahren mit hämodynamisch signifikanten angeborenen Herzfehlern
- Halbiert bei diesen Kindern Anzahl stationärer Aufenthalte wegen RSV-Infektion im Vergleich zu Placebo.28
- Eine Reduktion harter Therapieendpunkte wie Beatmungspflichtigkeit und Sterblichkeit ist nicht gesichert.27
- Dosierung: 15 mg/kg Körpergewicht i. m. in 4-Wochen-Intervallen (5 Injektionen) während der RSV-Saison
- Die erste Palivizumab-Gabe in Deutschland sollte Anfang November eines jeden Jahres erfolgen, die letzte Dosis entsprechend zwischen Ende Februar und Anfang März.
- Anwendung unter Bereitschaft zur sofortigen Behandlung von Anaphylaxie
- Eine Behandlung ist für Risikokinder in Betracht zu ziehen.
- Eine mögliche Prophylaxe sollten Sie mit den Eltern besprechen.
- Es sollte eine individuelle Entscheidung gefällt werden, die den Wert der Vermeidung einer stationären Behandlung den Nachteilen der Prophylaxe (Aufwendungen, Injektionen für das Kind) gegenüberstellt.
Meldepflicht
- In Deutschland besteht keine krankheits- oder erregerspezifische Meldepflicht.6
Verlauf, Komplikationen und Prognose
Verlauf
- Die Bronchiolitis ist in vielen Fällen eine leichte Infektion der unteren Atemwege; in einigen Fällen sind die Kinder mehr mitgenommen, und bei einem Teil der betroffenen Kinder kommt es zu schweren Infektionsverläufen.
- Die Einweisung ins Krankenhaus ist häufig bei Risikopatient*innen erforderlich, die für einen schweren Verlauf disponiert sind.
- Im Schnitt sistieren die Symptome nach 14 Tagen, 10 % der Kinder mit akuter Bronchiolitis weisen nach 3 Wochen noch Husten auf.2
- Die Epithelien regenerieren sich innerhalb von 4–8 Wochen.6
- Eine langfristige Immunität besteht nicht. Reinfektionen sind häufig, insbesondere bei Erwachsenen mit regelmäßigem Kontakt zu Kleinkindern.29
Komplikationen6
- Komplikationen treten insbesondere bei Risikopatient*innen auf.
- RSV-bedingte Pneumonie
- Atelektasen
- Exazerbation von vorbestehenden Erkrankungen
- Die jüngsten Säuglinge (6 Wochen bis 3 Monate) entwickeln häufig eine Apnoetendenz.
- Sekundäre bakterielle Infektionen sind selten, Koinfektionen mit anderen respiratorischen Viren sind häufig.
- Eine häufige Komplikation der RSV-Infektion ist eine akute Otitis media.
- In bis zu 3/4 der Fälle einer akuten Otitis media bei Kindern unter 3 Jahren wird RSV nachgewiesen.
- Als Langzeitkomplikation sind wiederkehrende Obstruktionen und eine anhaltende Hyperreagibilität des Bronchialsystems als Folge einer akuten RSV-induzierten Bronchiolitis beschrieben.
Prognose
- Letalität schwerer RSV-bedingter Erkrankungen bei hospitalisierten Kindern ≤ 2 Jahren6
- 0,2 % der Fälle bei Kindern ohne bekanntes erhöhtes Risiko
- 1,2 % bei Frühgeborenen
- 4,1 % bei Kindern mit bronchopulmonaler Dysplasie
- 5,2 % bei Kindern mit angeborenem Herzfehler.6
- Einige Kinder entwickeln nach einer schweren RSV-Infektion eine Disposition für Asthma. Es besteht jedoch derzeit kein sicherer Zusammenhang zwischen einer RSV-Infektion und einem später auftretenden Asthma und Atopie.15
Verlaufskontrolle
- Keine spezielle Verlaufskontrolle erforderlich
Patienteninformationen
Patienteninformationen in Deximed
Weitere Informationen
- Robert Koch-Institut, BZgA: Wir gegen Viren, Hygienetipps
Illustrationen
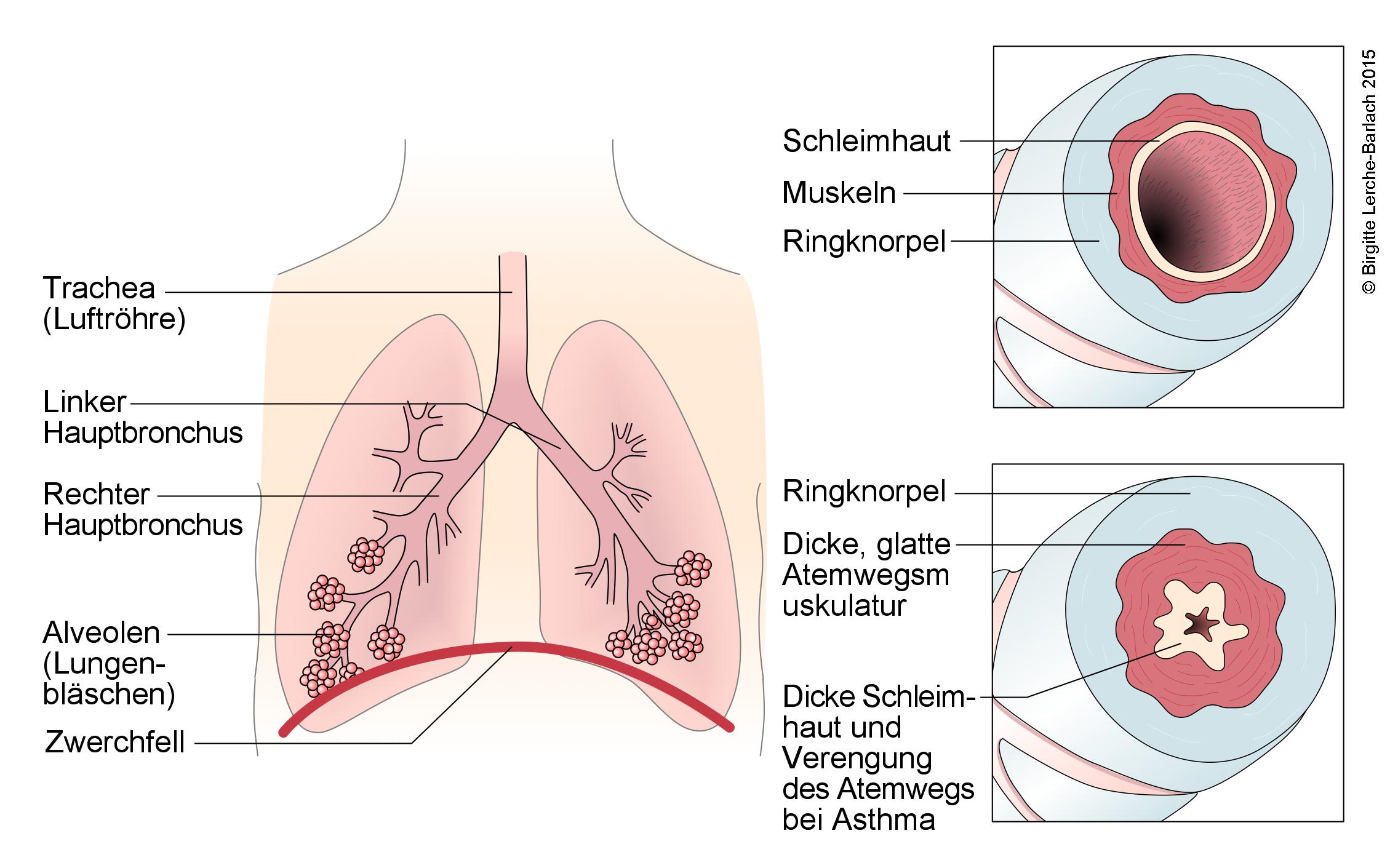
Trachea, Bronchien, Alveolen
Quellen
Leitlinien
- Deutsche Gesellschaft für Pädiatrische Infektiologie e. V. (DGPI). Prophylaxe von schweren Erkrankungen durch Respiratory Syncytial Virus (RSV) bei Risikokindern. AWMF-Leitlinie Nr. 048-012. S2k, Stand 2018. www.awmf.org
- The Royal Australasian College of Physicians. Australasian bronchiolitis guideline. Stand 2019 (Leitlinie Australien). www.pubmed.gov
- NICE Guideline. Bronchiolitis in children: diagnosis and management. Stand 2015 (Leitlinie UK). www.nice.org.uk
- American Academy of Pediatrics. Clinical practice guideline: the diagnosis, management, and prevention of bronchiolitis. Stand 2014 (Leitlinie USA). www.pediatrics.org
Literatur
- Hancock DG, Charles-Britton B, Dixon DL, et al. The heterogeneity of viral bronchiolitis: A lack of universal consensus definitions. Pediatr Pulmonol 2017; 52: 1234-40. pubmed.ncbi.nlm.nih.gov
- Schorlemer C, Eber E. Akute virale Bronchiolitis und obstruktive Bronchitis bei Kindern. Monatsschrift Kinderheilkunde 2020; 168: 1147-57. link.springer.com
- Jartti T, Smits HH, Bønnelykke K et al. Bronchiolitis needs a revisit: distinguishing between virus entities and their treatments. Allergy 2019; 74: 40-52. pubmed.ncbi.nlm.nih.gov
- Smyth RL, Openshaw PJM. Bronchiolitis. Lancet 2006; 368: 312-22. PubMed
- Deutsche Gesellschaft für Pädiatrische Infektiologie e.V. (DGPI). Prophylaxe von schweren Erkrankungen durch Respiratory Syncytial Virus (RSV) bei Risikokindern. AWMF-Leitlinie 048-012. Stand 2018. www.awmf.org
- Robert Koch-Institut. Respiratorische Synzytial-Virus-Infektionen (RSV). RKI-Ratgeber für Ärzte. 2011. www.rki.de
- Dawson-Caswell M, Muncie HL. Respiratory syncytial virus infection in children. Am Fam Physicianb 2011; 83: 141-6. PubMed
- Zorc JJ, Hall CB. Bronchiolitis: Recent Evidence on Diagnosis and Management. Pediatrics 2010; 125: 342-49. Pediatrics
- Kulkarni H, Smith CM, Lee Ddo H, et al. Evidence of respiratory syncytial virus spread by aerosol: Time to revisit infection control strategies?. Am J Respir Crit Care Med 2016 Aug 1; 194(3): 308-16. pmid:26890617 PubMed
- Florin TA, Plint AC, Zorc JJ. Viral bronchiolitis. Lancet 2017; 389: 211-24. pubmed.ncbi.nlm.nih.gov
- Frey U, Gappa M, Eber E et al. Pädiatrische Pneumologie, 3. Auflage. Obstruktive Atemwegserkrankungen. Berlin, Heidelberg: Springer, 2014.
- Nielsen LM, Halgrener J, Lühr Hansen BV. Respiratorisk syncytialvirus-infektioner hos børn i almen praksis. Ugeskr Læger 2003; 165: 2747-9. PubMed
- Kirolos A, Manti S, Blacow R et al. A systematic review of clinical practice guidelines for the diagnosis and management of bronchiolitis. J Infect Dis 2020; 222: 672-9. academic.oup.com
- Zorc JJ, Hall CB. Bronchiolitis: REcent evidence on diagnosis and management. Pediatrics 2010; 125: 342. Pediatrics
- Black CP. Systematic review of the biology and medical management of respiratory syncytial virus infection. Respir Care 2003; 48: 209-31. PubMed
- Ralston SL, Lieberthal AS, Meissner HC, et al. Clinical practice guideline: The diagnosis, management, and prevention of bronchiolitis. Pediatrics 2014. doi.10.1542/peds.2014-2742 pubmed.ncbi.nlm.nih.gov
- Gadomski AM, Scribani MB. Bronchodilators for bronchiolitis. Cochrane Database Syst Rev. 2014;6:CD001266. DOI: 10.1002/14651858.CD001266.pub4. DOI
- Purcell K, Fergie J. Concurrent serious bacterial infection in 2396 infants and children hospitalized with respiratory syncytial virus lower respiratory tract infections. Arch Pediatr Adolesc Med 2002;156:322-4. PubMed
- Ralston SL, Lieberthal AS, Meissner HC et al. Clinical practice guideline: the diagnosis, management, and prevention of bronchiolitis. Pediatrics 2014; 134: 1474-502. pediatrics.aappublications.org
- NICE Guideline. Bronchiolitis in children: diagnosis and management. Stand 2015. www.nice.org.uk
- O’Brien S, Borland ML, Cotterell E et al. Australasian bronchiolitis guideline. J Paediatr Child Health 2019; 55: 42-53. pubmed.ncbi.nlm.nih.gov
- Cunningham S, Rodriguez A, Adams T et al. Oxygen saturation targets in infants with bronchiolitis (BIDS): a double-blind, randomised, equivalence trial. Lancet 2015; 386: 1041-8. www.thelancet.com
- Hartling L, Bialy LM, Vandermeer B, et al. Epinephrine for bronchiolitis. Cochrnae Database of Systematic Reviews 2011; 6: CD003123. DOI: 10.1002/14651858.CD003123.pub3 DOI
- Meissner HC. Viral Bronchiolitis in Children. N Engl J Med 2016; 374: 1793-4. www.nejm.org
- Shah PS, Ohlsson A, Shah JP. Continuous negative extrathoracic pressure or continuous positive airway pressure compared to conventional ventilation for acute hypoxaemic respiratory failure in children. Cochrane Database of Systematic Reviews 2013, Issue 11. Art. No.: CD003699. DOI: 10.1002/14651858.CD003699.pub4 DOI
- Robert Koch Institut, Bundeszentrale für gesundheitliche Aufklärung. Wir gegen Viren www.wir-gegen-viren.de
- Grønn M, Lossius K, Brunvand L, Rudi HM, Nøkleby H et al. RSV-infeksjon og forebyggende behandling med monoklonalt antistoff - forslag til nasjonale anbefalinger. MSIS Ukerapport 42, 2000.
- Cochrane Database Syst Rev. 2013. Andabaka T, Nickerson JW et al, Monoclonal antibody for reducing the risk of respiratory syncytial virus infection in children. www.ncbi.nlm.nih.gov
- Hashem M, Hall CB. Respiratory syncytial virus in healthy adults: the cost of a cold. J Clin Virol 2003; 27: 14-21. PubMed
Autor*innen
- Lino Witte, Dr. med., Arzt in Weiterbildung, Innere Medizin, Frankfurt
- Erika Baum, Prof. Dr. med., Professorin für Allgemeinmedizin, Biebertal (Review)
- Die ursprüngliche Version dieses Artikels basiert auf einem entsprechenden Artikel im norwegischen hausärztlichen Online-Handbuch Norsk Elektronisk Legehåndbok (NEL, https://legehandboka.no/).