Allgemeine Informationen
Definition
- Insulinome gehören zu der heterogenen Gruppe der neuroendokrinen Tumoren (NET), die hauptsächlich in den Langerhans-Inselzellen des Pankreas ihren Ursprung haben.
- Häufigster neuroendokriner Pankreastumor: Ist meist gutartig (> 90 %)1, meist solitär (90 %) und oft klein (< 2 cm).2
- Insulinome produzieren vor allem Insulin, aber auch andere gastrointestinale Hormone.
- Episoden mit Nüchternhypoglykämie oder postprandialer Hypoglykämie können vorkommen.3
Häufigkeit
- Die Inzidenz liegt bei ca. 1–3/1.000.000 Personen pro Jahr.4
- Insulinome sind die häufigste Ursache für eine Nüchternhypoglykämie.
- 90 % der Insulinome sind benigne.5
- Insulinome kommen etwas häufiger bei Frauen als bei Männern vor.5
- Das mediane Alter zum Diagnosezeitpunkt liegt bei 50 Jahren.5
Ätiologie und Pathogenese
- Allen Insulinomen ist gemein, dass sie Insulin mehr oder weniger unabhängig vom Serumglukosespiegel produzieren.
- Insulin
- Wird aus dem inaktiven Vorläufer Proinsulin gebildet.
- Bei einer Spaltung von Proinsulin bilden sich äquimolare Mengen Insulin und C-Peptid.
- Bei gesunden Menschen macht das Proinsulin weniger als 20 % der gesamten Insulinmenge aus, die in den Blutkreislauf abgegeben wird.
- Sekretion
- Die Insulinfreisetzung aus den Tumorzellen kann stabil sein oder stoßweise erfolgen, sodass der Glukosespiegel plötzlich schwankt.
- Zusätzlich setzen die Insulinomzellen eine verhältnismäßig große Menge Proinsulin frei, sodass das Proinsulin 30–90 % des gesamten Insulins ausmacht.
- Risiko einer Hypoglykämie?
- Personen mit normaler Insulinproduktion tolerieren eine verhältnismäßig ausgeprägte Hypoglykämie aufgrund der kompensatorischen Ketonproduktion.
- Eine ungehemmte Insulinproduktion behindert die Ketonbildung. Patient*innen mit einem Insulinom zeigen daher schon bei einem subnormalen Glukosespiegel Symptome.
- Produktion anderer Hormone
- Ebenso wie andere neuroendokrine Tumoren können einzelne Insulinome außer Insulin auch andere Hormone produzieren.
- Am häufigsten sind Gastrin, ACTH, Glukagon, hCG und Somatostatin.
- Pathologie
- Die allermeisten Insulinome sind benigne und ohne bekannte Ursache.
- Sie scheinen vom duktalen/azinalen System im Pankreas zu entstehen.6
- Ca. 10 % sind maligne.5
- Die Dignität ist in der präoperativen Diagnostik schwierig und kann oft nur bei Lymphknoten- oder Fernmetastasen beurteilt werden.7
- Die Schweregradeinteilung ist histologisch und immunhistochemisch zu stellen, nach Differenzierungsgrad Ki67-Index.4
- Die malignen Tumoren sind normalerweise größer als die benignen.
- In ca. 10 % der Fälle findet man multiple Insulinome im Pankreas.5
- Multiple endokrine Neoplasie Typ 1 (MEN Typ 1)
- MEN Typ 1 ist eine autosomale Erbkrankheit, die durch einen Defekt im Tumor-Supressor-Gen MEN1 auf dem Chromosom 11q13 verursacht wird.
- Ca. 50 % der Patient*innen MEN Typ 1 entwickeln im Lauf des Lebens einen neuroendokrinen Tumor des Pankreas.7
- Weniger als 1 % der Insulinome sind ektopisch (am häufigsten in Magen, Duodenum, Meckel-Divertikel, Gallengängen und Omentum).
Disponierende Faktoren
- Erbliches Vorkommen von MEN Typ 1
ICPC-2
- T73 Neubild. endokrine unspez., andere
ICD-10
- D13.7 Endokriner Drüsenanteil des Pankreas inkl. Inselzelltumor/Insulinom
Diagnostik
Diagnostische Kriterien
- Ein Verdacht auf diese Diagnose stellt sich meist aufgrund der Anamnese.
- Die endgültige Diagnose setzt aber voraus, dass in der gleichen Blutprobe eine Hypoglykämie, ein erhöhter Insulin- und C-Peptid-Spiegel nachgewiesen werden.
Differenzialdiagnosen
Differenzialdiagnosen bei Hypoglykämie
- Idiopathische postprandiale Hypoglykämie
- Missbrauch von Insulin oder Sulfonylharnstoffen
- Ist nicht selten die Ursache bei Personen, bei denen Hypoglykämie festgestellt wird.
- Eine exogene Insulinzufuhr wird festgestellt, wenn in der gleichen Probe ein hoher Insulinspiegel und ein supprimiertes Plasma-C-Peptid gemessen werden (C-Peptid/Insulin-Quotient < 1).
- Der Missbrauch von Sulfonylharnstoffen lässt sich schwerer nachweisen, da in diesem Fall sowohl der Insulin- als auch der C-Peptid-Spiegel steigen.
- Psychomotorische Epilepsie
- Psychiatrische Erkrankungen
- Autoimmune Hypoglykämie
- Ist eine sehr seltene Ursache.8
- Kommt hauptsächlich bei Personen mit japanischer Abstammung vor.
- Eine autoimmune Hypoglykämie kann schwere neuroglykopene Symptome verursachen.
- Wenn diätetische Maßnahmen zur Hypoglykämievermeidung nicht ausreichen, kann eine immunsuppressive Behandlung oder die Gabe von Somatostatinanlagoga oder Dioxazid notwendig sein.8
- Andere Ursachen für Hypoglykämie können Lebererkrankungen, extrapankreatische Insulin-produzierende Tumoren und vereinzelte andere endokrine Erkrankungen sein.
Andere Pankreastumoren
- Bei 60–80 % der Tumoren der Inselzellen des Pankreas handelt es sich um Insulinome. Bei der Differenzialdiagnostik müssen auch andere endokrine Tumoren in Erwägung gezogen werden.
- v. a. Gastrinome
- selten: VIPome, Glukagonome und Somatostatinome7
Anamnese
- Alter
- Hypoglykämie
- Normalerweise entsteht eine Hypoglykämie mehrere Stunden nach der Mahlzeit (75 %). In einer retrospektiven Studie wurde jedoch festgestellt, dass ca. 20 % der Teilnehmer*innen sowohl nüchterne als auch postprandiale Symptome angaben. Bei 6 % lagen nur postprandiale Symptome vor.3
- übliche Anfangssymptome
- Diplopie
- Visustrübungen
- Kopfschmerzen
- Palpitationen
- Schwäche
- typische neuroglykopene Symptome
- kognitive Einschränkungen
- Verhaltens- und Persönlichkeitsänderungen
- psychomotorische Unruhe
- Verwirrtheit, Desorientation, Amnesie, Bewusstseinsstörungen
- Krampfanfall
- Stupor5
- Die Hypoglykämie-Symptome treten in der Regel morgens am ausgeprägtesten auf.
- Faktoren, die die Symptome verschlimmern können, sind physische Aktivität, Alkohol, das Auslassen von Mahlzeiten, Gewichtsabnahme sowie eine Behandlung mit Sulfonylharnstoffen.
- Infolge der Hypoglykämie treten auch adrenerge und cholinerge Symptome auf.
- adrenerge Symptome
- Palpitationen
- Tremor
- Nervosität/Ängstlichkeit
- cholinerge Symptome
- Schwitzen
- Hunger
- Parästhesien5
- adrenerge Symptome
- Epileptische Anfälle (meist generalisierte tonisch-klonische Anfälle) treten bei ca. 12 % der Fälle auf.
- Viele Patient*innen nehmen an Gewicht zu.
- Lokale Symptome aufgrund der Tumormassen kommen sehr selten vor.
- Liegen zusätzlich Menstruationsstörungen bzw. eine erektile Dysfunktion, eine Anamnese mit Nierensteinen oder erhöhtes Serumkalzium vor, besteht der Verdacht einer MEN Typ 1.
Klinische Untersuchung
- Das klassische Befundbild bei Insulinomen ist eine Triade aus:
- episodischer Hypoglykämie
- ZNS-Dysfunktion aufgrund einer Hypoglykämie (Verwirrtheit, Angstgefühle, Stupor, Krämpfe, Koma etc.)
- Besserung der zentralnervösen Symptome nach Glukosezufuhr.5
Ergänzende Untersuchungen in der Hausarztpraxis
- Die Anamnese kann hinsichtlich der Differenzialdiagnosen viele Hinweise geben.
- Ggf. Nachweis eines erniedrigten Blutzuckerspiegels zum Zeitpunkt der Symptome
Diagnostik bei Spezialist*innen
- Unter stationären Bedingungen wird ein standardisiertes Regime für den Nachweis von Insulinomen befolgt (Fastentest).
- Einfachster und sicherster Test ist die Provokation einer Hypoglykämie durch den Fastentest stationär mit engmaschigen Blutzuckerkontrollen sowie Bestimmungen von Insulin und C-Peptid. Typisch für das Insulinom ist die fehlende physiologische Insulinsuppression bei Abfall des Blutzuckers im Hungerversuch.5
Standardisiertes Regime
- Durchführung stationär
- Während der Untersuchung werden Glukose, Insulin, C-Peptid und ggf. Proinsulin gemessen.
- Sechsstündige (erweiterte) Glukosebelastung
- Die Glukosebelastung erfolgt nach den üblichen Richtlinien, wird aber von 2 auf 6 Stunden erweitert.
- 3-Tage-Fastentest
- Glukose und Insulin werden nach einem festgelegten Schema und bei Hypoglykämie-Symptomen gemessen.
- Die Diagnose gilt als wahrscheinlich, wenn in der gleichen Probe Hypoglykämie sowie ein erhöhter Insulin- und C-Peptid-Spiegel nachgewiesen werden.
- Diagnosekriterien
- Blutglukosewert < 50 mg/dl (2,8 mmol/l) mit Symptomen einer Hypoglykämie
- Besserung der Symptome nach dem Essen
- erhöhtes Plasmainsulin ≥ 6 μU/ml (≥ 36 pmol/l)
- erhöhtes C-Peptid im Plasma (≥ 0,2 nmol/l)
- erhöhter Proinsulin Wert (≥ 5 pmol/l)
- Fehlen von Sulfonylharnstoff im Plasma9
- Bei einer signifikanten Hypoglykämie wird der Test beendet, wenn die Blutproben entnommen wurden.
- In den meisten Fällen ist ein Fasten über 2 Tage ausreichend, um die Diagnose zu erkennen.9
- Ein negativer 3-Tage-Fastentest weist eine hohe Spezifität auf.
- Bei multiplen Insulinomen oder Symptomen anderer endokriner Erkrankungen Untersuchung auf MEN Typ 1. Ausschluss von:
- Hyperprolaktinämie aufgrund eines Hypophysenadenoms
- Hyperparathyreoidismus aufgrund einer Nebenschilddrüsen-Hyperplasie
- Hypergastrinämie aufgrund eines Gastrinoms.
Lokalisationsdiagnostik
- Sollte nur erfolgen, nachdem die Diagnose biochemisch bestätigt wurde, da 80 % der Insulinome < 2 cm, 30 % < 1 cm sind und damit mittels CT oder Ultraschall schwer nachzuweisen sind.
- Der Zweck der bildgebenden Diagnostik bei einem Insulinom ist die Lokalisierung, nicht der Nachweis des Tumors.
- Bildgebende Verfahren
- 3-Phasen-CT: Sensitivität 60–80 %
- MRT: Sensitivität 85–90 %
- endoskopischer Ultraschall: Sensitivität 75–90 %5
- selektive pankreatische Arteriografie mit intraarterieller Injektion von Kalzium (stimuliert die Insulinsekretion in neoplastischen Zellen) sowie perkutane transhepatische Pankreasvenen-Katheterisierung mit Insulinmessung
- Früher oft angewendet, ist das Verfahren mittlerweile den anderen unterlegen.5
- nuklearmedizinische Verfahren: GLP1-Rezeptor-vermittelte Bildgebung mittels PET/CT
- Insulinome exprimieren den GLP1-Rezeptor auf ihrer Oberfläche.
- Sensitivität bis 95 % beschrieben10
- Somatostatinrezeptor PET/CT
- Maligne Isulinome exprimieren häufig nicht den GLP1-Rezeptor, aber den Somatostatinrezeptor Subtyp 2 (SST2).5
- Bei fehlendem Nachweis des Insulinoms durch bildgebende Verfahren bleibt die intraoperative Palpation des Pankreas, ggf. kombiniert mit intraoperativem Ultraschall.
- Kombination beider Verfahren: Sensitivität 85–95 %5
Indikationen zur Überweisung
- Überweisung zu Fachärzt*in für Endokrinologie zur Untersuchung und Behandlung bei Verdacht auf Insulinom
Therapie
Therapieziele
- Ziel der Behandlung ist eine vollständige Heilung.
- Bei malignen Insulinomen mit Metastasen soll eine Symptomlinderung erreicht werden.
- Die Vermeidung von Hypoglykämien ist das Hauptziel.4
- Eine adjuvante Therapie wird innerhalb von klinischen Studien empfohlen.1
Allgemeines zur Therapie
- Bei benignen Insulinomen gilt eine Tumorresektion als kurative Behandlung.3
- Bei metastasierten malignen Insulinomen sollte die Entfernung des Primärtumors und ein Debulking der Fernmetastasen zur Verbesserung der Hypoglykämie-Symptomatik erwogen werden.1
- Die Therapie sollte interdisziplinär in einem spezialisierten Zentrum erfolgen.1
Empfehlungen für Patient*innen
- Bis zum Operationstermin können kohlenhydratreiche Mahlzeiten in häufigen Intervallen (2–3 Stunden) die Hypoglykämie-Episoden dämpfen.
- Komplexe Kohlenhydrate sollten bevorzugt werden.5
Medikamentöse Therapie
- Angeraten ist eine symptomatische Behandlung mit Diazoxid oder dem Somatostatin-Analogon Octreotid, um hypoglykämische Episoden vor dem Operationstermin zu vermeiden oder um palliativ zu behandeln.1,4
- Bei der Gabe von Diazoxid sollte gleichzeitig Hydrochlorothiazid gegeben werden, um Ödeme und Hyperkaliämie zu vermeiden und die hyperglykämische Wirkung zu potenzieren.1
- Bei metastasierten Insulinomen kommen infrage:
- Chemotherapie
- Targeted-Therapie mit Everolimus oder Sunitinib.4-5
Operative Therapie
- Tumorresektion
- Eine sorgfältige präoperative Überwachung des Glukosespiegels ist wichtig.
- Üblicherweise wird präoperativ eine 10-prozentige Dextrose-Lösung verabreicht.
- beim wahrscheinlich benignen Insulinom Enukleation oder limitierte Pankreasresektion1
- bei potenziell malignem Insulinom formale Pankreasteilresektion mit Lymphadenektomie1
- Der Einsatz von Ultraschall während der Operation erleichtert die Lokalisierung, vor allem weil ein Teil der Insulinome die gleiche Konsistenz wie normales Pankreasparenchym aufweist.
- Bei besonderen Lokalisationen oder multiplen Tumoren kann es erforderlich sein, größere Teile des Pankreas zu entfernen oder eine vollständige Whipple-Operation durchzuführen.5
- Bei maligenen Insulinomen und vollständig resezierbarem Primärtumor oder nicht auffindbarem Primärtumor sollten resektable Metastasen entfernt werden.1
- Ein Tumordebulking ist bei einem metastasierten Krankheitsbild zur Symptomkontrolle indiziert.1
- Patient*innen mit MEN 1 leiden aufgrund des Hyperparathyreoidismus häufig an Hyperkalzämie. In diesen Fällen muss vor der Insulinomresektion eine Parathyreoidektomie durchgeführt werden.
Verlauf, Komplikationen und Prognose
Verlauf
- Der Zeitraum vom Symptombeginn bis zum Diagnosezeitpunkt variiert von wenigen Wochen bis zu mehreren Jahrzehnten.
- Ca. 5 % der Patient*innen, die eine kurative Behandlung auf ein benignes Insulinom erhalten haben, entwickeln später ein Rezidiv.
- Die Prognose ist bei einem Rezidiv nicht so günstig wie beim ersten Auftreten.
Komplikationen
- Unbehandelt können Insulinome zu schwerer Hypoglykämie und irreversiblen Hirnschäden führen.
- Durch kompensatorisches Essen kann Übergewicht/Adipositas entstehen.4
- Je nach Studie variieren postoperative Morbidität und Mortalität.
- Lokale Komplikationen dominieren, u. a. Fistelbildung, Abszesse und Pankreatitis.
- Wurde ein großer Teil des Pankreas entfernt, können die Patient*innen Diabetes mellitus entwickeln.
Prognose
- Die Einteilung der Tumoren nach TNM/UICC-Klassifikation bzw. nach der WHO-Klassifikation für NET des Pankreas nach dem Ki67-Index erlaubt eine Prognoseabschätzung.5
- Die Prognose ist sehr gut nach einer vollständigen Resektion des benignen Insulinoms.
- In einer Studie aus Finnland war die Lebenserwartung bei gutartigen Insulinomen nicht gegenüber der Normalbevölkerung gemindert, bei metastasierter Erkrankung betrug das mittlere Überleben 3,4 Jahre.11
Patienteninformationen
Patienteninformationen in Deximed
Illustrationen
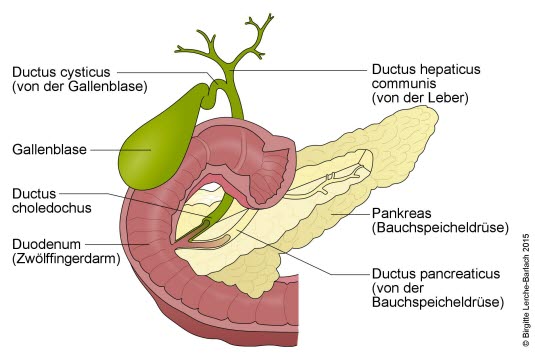
Gallenblase und Bauchspeicheldrüse
Quellen
Leitlinie
- Deutsche Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten (DGVS). Neuroendokrine Tumore. AWMF-Leitlinie Nr. 021-026. S2k, Stand 2018. www.awmf.org
Literatur
- Deutsche Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten (DGVS), Neuroendokrine Tumore. AWMF-Leitlinie Nr. 021 - 026, Stand 2018. www.awmf.org
- Ali ZA. Insulinoma. emedicine.medscape, 7.1.2022 emedicine.medscape.com
- Placzkowski KA, Vella A, Thompson GB, et al. Secular trends in the presentation and management of functioning insulinoma at the Mayo Clinic, 1987-2007. J Clin Endocrinol Metab 2009; 94: 1069-73. www.ncbi.nlm.nih.gov
- Hofland J, Kaltsas G, de Herder WW. Advances in the Diagnosis and Management of Well-Differentiated Neuroendocrine Neoplasms. Endocr Rev. 2020 Apr 1;41(2):371–403. www.ncbi.nlm.nih.gov
- de Herder WW , Zandee WT , Hofland J et al. Insulinoma. In: Endotext [Internet]. South Dartmouth (MA): MDText.com, Inc.; 2000– 2020 Oct 2. www.ncbi.nlm.nih.gov
- Vortmeyer AO, Huang S, Lubensky I, Zhuang Z. Non-islet origin of pancreatic islet cell tumors. J Clin Endocrinol Metab 2004; 89: 1934-8. PubMed
- Goretzki PE, Agca A, Lammers BJ, Schwarz K. In Becker H, Ghadimi BM (Hrsg.): Allgemein- und Viszeralchirurgie II, spezielle operative Techniken. Elsevier Urban und Fischer Verlag, 2015, S. 85-106.
- Insulin Autoimmune Syndrome (Hirata Disease): A Comprehensive Review Fifty Years After Its First Description. Cappellani D, Macchia E, Falorni A, Marchetti P. Diabetes Metab Syndr Obes. 2020 Apr 1;13:963-978. pubmed.ncbi.nlm.nih.gov
- Shin JJ, Gorden P, Libutti SK. Insulinoma: pathophysiology, localization and management. Future Oncol. 2010 Feb. 6 (2):229-37. www.ncbi.nlm.nih.gov
- Glucagon-like peptide-1 receptor imaging for the localisation of insulinomas: a prospective multicentre imaging study. The Lancet Diabetes & Endocrinology, Early Online Publication, 25 July 2013. www.thelancet.com
- Peltola E, Hannula P, Huhtala H, Metso S, Sand J, Laukkarinen J, Tiikkainen M, Sirén J, Soinio M, Nuutila P, Moilanen L, Laaksonen DE, Ebeling T, Arola J, Schalin-Jäntti C, Jaatinen P. Long-term morbidity and mortality in patients diagnosed with an insulinoma. Eur J Endocrinol. 2021 Sep 1;185(4):577-586. doi: 10.1530/EJE-21-0230. www.ncbi.nlm.nih.gov
Autor*innen
- Franziska Jorda, Dr. med., Fachärztin für Viszeralchirurgie, Ärztin in Weiterbildung Allgemeinmedizin, Kaufbeuren
- Birgit Wengenmayer, Dr. med., Fachärztin für Allgemeinmedizin, Freiburg
- Die ursprüngliche Version dieses Artikels basiert auf einem entsprechenden Artikel im norwegischen hausärztlichen Online-Handbuch Norsk Elektronisk Legehåndbok (NEL, https://legehandboka.no/).