Allgemeine Informationen
Definition
- Hämangiome sind gutartige Gefäßtumoren mit charakteristischem klinischem Verlauf, der gekennzeichnet ist von einer schnellen, frühen Proliferation gefolgt von einer langsameren spontanen Rückbildung (Involution).1
- Je nach Lokalisation und Größe kann es zu Beeinträchtigungen oder Residuen kommen, die eine Therapie erfordern.
- Bei Hämangiomen in unkomplizierter Lage und ohne Funktionseinschränkungen kann die spontane Rückbildung abgewartet werden.2
Häufigkeit
- Infantile Hämangiome sind die häufigsten gutartigen Tumoren im Kindesalter und treten bei 4‒5 % aller Säuglinge auf.3
- Häufiger bei Mädchen (3:1)
Ätiologie
- Die Pathogenese ist nicht vollständig geklärt.4
- Es besteht wohl ein Ungleichgewicht der Angiogenesefaktoren und eine Erhöhung der Spiegel des vaskulären endothelialen Wachstumsfaktors (VEGF), des basischen Fibroblasten‐Wachstumsfaktors (bFGF) und der Matrix‐Metalloproteinasen (MMP) 2 und 9, was zur Proliferation des Hämangioms führt.4
- Eine Hypoxie des Gewebes scheint ein weiterer Faktor zu sein.
- In der Regressionsphase nehmen die Konzentrationen der Proteine wieder ab.
- Es wird zwischen unkomplizierten und komplizierten infantilen Hämangiomen unterschieden.
Pathogenese
- Infantile Hämangiome bestehen noch nicht bei der Geburt. Die Diagnose wird in der Regel im Laufe der ersten 4‒6 Lebenswochen gestellt.5
- Hämangiome weisen einen charakteristischen klinischen Verlauf auf:
- Als Vorstufe können manchmal bereits Teleangiektasien oder anämische, rötliche oder blasslivide Makulae zu sehen sein.2
- In der proliferativen Phase wächst das Hämangiom rasch, am schnellsten im Alter von 2‒3 Monaten.6
- Nach der Proliferation ist das Hämangiom eine gewisse Zeit lang stabil (Übergangsphase).
- Involutionsphase (Schrumpfung) typischerweise in der zweiten Hälfte des ersten Lebensjahres. Sie kann 2‒10 Jahre andauern.
- Komplikationen2
- funktionelle Beeinträchtigungen
- Insbesondere im Gesicht kann es durch Ausbreitung des Hämangioms zu Störungen der Lidfunktion, des Zahnwachstums oder dauerhaften Deformitäten oder Gesichtsasymmetrien kommen.
- Im Extremfall ist eine Obstruktion der Atemwege möglich.
- Ulzerationen durch rasches Wachstum der Hämangiome können Schmerzen und Blutungen verursachen, und es besteht die Gefahr einer Superinfektion.
- häufig anogenital oder intertriginös
- Hämangiomgewebe setzt größere Mengen an Deiodinase frei, das Schilddrüsenhormone deaktiviert und so zu einer Hypothyreose führen kann.
- Mitbeteiligung innerer Organe und assoziierte Fehlbildungen können auftreten.
- funktionelle Beeinträchtigungen
Prädisponierende Faktoren
- Niedriges Geburtsgewicht7
- Hellhäutige Abstammung
- Höheres Alter der Mutter
- Anomalien der Plazenta5
- Frühgeburt oder geringes Geburtsgewicht
ICPC-2
- Hämangiom / Lymphangiom
ICD-10
- D18 Hämangiom und Lymphangiom
- D18.0 Hämangiom
Diagnostik
Diagnostische Kriterien
- Manchmal lässt sich ein infantiles Hämatom durch Anamnese und Klinik eindeutig bestimmen, dann ist keine weitere Diagnostik erforderlich.
- Ist die Veränderung bereits bei der Geburt vorhanden und ändert ihre Größe kaum, ist eher von einer vaskulären Malformation auszugehen.
- Bei Vorliegen mehrerer Hämangiome ist es sinnvoll, die Beteiligung innerer Organe durch weitere Diagnostik auszuschließen.
Differenzialdiagnosen
- Naevus flammeus
- Andere vaskuläre Tumore
- pyogenes Granulom
- kaposiformes Hämangioendotheliom
- Nichtvaskulären Raumforderungen
- Dermoidzyste
- nasales Gliom
- Myofibrom
- Sarkom
- Vaskuläre Fehlbildungen
- Venen, Arterien und Lymphgefäße können betroffen sein.
Anamnese
- Zeitpunkt des Auftretens der Veränderung
- Größenveränderung: Manchmal hilft die wochenweise Kontrolle der Größe bei der Differenzialdiagnose.8
- Begleitsymptome wie Wachstumsretardierung, reduzierte Aktivität und Schläfrigkeit können auf eine begleitende Hypothyreose hinweisen.
Klinische Untersuchung
- Infantile Hämangiome treten in der Regel im Laufe der ersten 4‒6 Lebenswochen auf.5
- Charakteristischer klinischer Verlauf
- Als Vorstufe können manchmal bereits Teleangiektasien oder anämische, rötliche oder blasslivide Makulae zu sehen sein.2
- In der proliferativen Phase wächst das Hämangiom rasch, am schnellsten im Alter von 2‒3 Monaten.6
- Nach der Proliferation ist das Hämangiom eine gewisse Zeit lang stabil (Übergangsphase).
- Involutionsphase (Schrumpfung) typischerweise in der zweiten Hälfte des ersten Lebensjahres. Diese Phase kann 2‒10 Jahre andauern.
- Die meisten infantilen Hämangiome sind lokalisiert, entweder erhaben oder im Hautniveau, sehr häufig an Kopf und Hals.
- Dann gibt es segmentale Hämangiome, die mit Fehlbildungen der Gefäße oder innerer Organe einhergehen können.
- Eine weitere Sonderform: multifokale infantile Hämangiome (5 oder mehr) mit oder ohne extrakutaner Beteiligung
- 80 % der infantilen Hämangiome treten fokal und solitär auf.
- Lokalisation
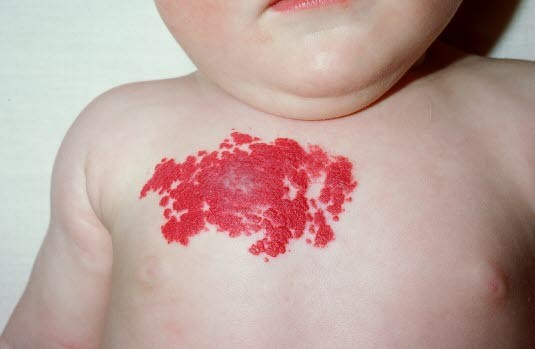 Hämangiom: Proliferationsphase
Hämangiom: Proliferationsphase- 60 % der kutanen Hämangiome befinden sich an Kopf oder Hals.
- 25 % am Rumpf
- 15 % an den Extremitäten
- Hämangiome können nicht nur an der Haut auftreten, sondern auch z. B. in Leber, Gastrointestinaltrakt, Larynx, Zentralnervensystem, Pankreas, Gallenblase, Thymus, Milz, Lymphknoten, Lunge, Harnblase und Nebennieren.
- Frühe Anzeichen (0‒6 Wochen)
- Festzustellen ist eine beginnende Erblassung der Haut. Danach bilden sich feine Teleangiektasien und danach ein rotes oder tiefrotes Mal oder eine Papel, die von einem schwachen Ring vaskulärer Erblassung umgeben ist.
- Spätere Anzeichen (0‒12 Monate)
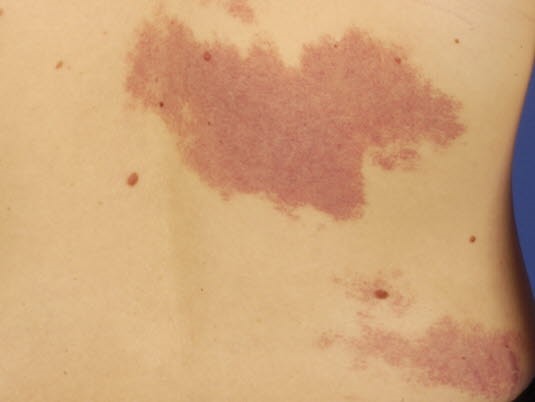 Hämangiom: Regressionsphase
Hämangiom: Regressionsphase- Wenn das Hämangiom wächst, zeigt es sich kuppelförmig, beulenartig, plaqueähnlich, tumorartig oder als Kombination daraus.
- Befindet sich das Hämangiom in der Rückbildungsphase (Involution), verblasst die Färbung, die Schwellung bildet sich zurück.
- 50‒60 % der Hämangiome hinterlassen dauerhafte Veränderungen an der Haut wie Teleangiektasien, oberflächliche erweiterte Venen, bläschenartige Narben oder Hypo/Hyperpigmentierungen.
Leitlinie: Weitere Diagnostik2
- Bei nicht sicherer Diagnose eines infantilen Hämangioms oder bei Verdacht auf Beteiligung innerer Organe kommen weitere Untersuchungen in Betracht:
Sonografie
- Ein Hämangiom zeigt in der Sonografie ein typisches Flussmuster, es lässt sich Ausdehnung und Stadium bestimmen.
- Beteiligung innerer Organe können entdeckt werden.
- Bei Verdacht auf eine kardiale Beteiligung ist eine Echokardiografie sinnvoll.
MRT
- Kann ebenfalls zur Differenzialdiagnostik hilfreich sein.
- Bei flächigen segmentalen Hämangiomen in lumbosakraler Lokalisation müssen spinale, urogenitale und anale Fehlbildungen ausgeschlossen werden.
Augenärztliche Untersuchung
- Bei Nähe des Hämangioms zum Auge, ein Hämangiom kann den Visus beeinflussen.
Laryngoskopie
- Bei Hämangiomen im Bereich der oberen Luftwege, um eine Obstruktion auszuschließen.
TSH-Bestimmung
- Bei sehr großen Hämangiomen oder bei klinischem Verdacht auf eine Hypothyreose.
Biopsie und Histologie
- Zur weiteren Abklärung bei unklaren Tumoren zum Malignitätsausschluss
Indikationen zur Überweisung
- Kleine unkomplizierte Hämangiome heilen von selbst aus.
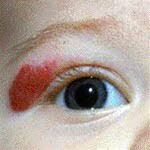 Hämangiom: periorbitale Läsion
Hämangiom: periorbitale Läsion - Bei ungünstigen Lokalisationen (Auge, Gesicht, Luftwegen), sehr großen Hämangiomen, Zweifel an der richtigen Diagnose oder zur Einleitung einer Therapie sollte eine Überweisung zur fachärztlichen Untersuchung/Weiterbehandlung erfolgen (je nach Fragestellung an Kinder-Ophthalmologie, HNO, Pädiatrie, Kinder-Kardiologie)
Therapie
Therapieziele
- Wachstumsstopp und rasche Rückbildung
- Prävention funktionell und ästhetisch beeinträchtigender Komplikationen
- Abheilung von Ulzerationen
Allgemeines zur Therapie
- In vielen Fällen ist keine Behandlung erforderlich.
- Bei komplizierten Hämangiomen sollte so früh wie möglich mit einer Behandlung begonnen werden.
- Therapie der Wahl ist Propranolol
Medikamentöse Therapie
Propanolol
- Vor dem Einsatz von Propranolol sollte ein EKG, bei Verdacht auf eine kardiale Erkrankung und/oder positiver Familienanamnese eine Echokardiografie durchgeführt werden.
- Die Therapie mit Propranolol wird einschleichend mit einer Dosis von 1 mg/kg KG pro Tag begonnen und im stationären Setting täglich, im ambulanten Setting wöchentlich auf die Zieldosis 2 (‒3) mg/kg KG pro Tag, verteilt auf 2, in begründeten Fällen 3 Einzeldosen gesteigert.
- Die Behandlung unter einem Lebensalter von 5 Wochen ist off label.
- Eine stationäre Einstellung mit Monitoring des Blutdrucks, der Herzfrequenz und des Blutzuckers wird empfohlen bei:
- Kindern unter 8 Wochen
- relevanten kardialen oder
- respiratorischen Begleiterkrankungen
- assoziierten Fehlbildungen
- schwierigen sozialen Verhältnissen.
- Eine Behandlung sollte mindestens 6 Monate betragen, die Dosierung muss ggf. an das wachsende Körpergewicht des Kindes angepasst werden.
- Nebenwirkungen
- Schlafstörungen
- kalte Extremitäten
- Diarrhö
- nächtliche Unruhe
- Bronchospasmus
- Bradykardie
- Hypoglykämie
- arterielle Hypotonie
Nadolol und Atenolol
- Andere selektiven Beta-Blockern sind auch wirksam, für das infantile Hämangiom nicht zugelassen (off label).
Kortikosteroide
- Systemische Kortikosteroide sind nur noch bei Therapieversagen unter Propranolol oder lebensbedrohlichen Obstruktionen zusätzlich indiziert.
- Dosierung: 2‒5 mg Prednisolon-Äquivalent/kg KG pro Tag2
Weitere Therapien
- Eine lokale Behandlung mit Betablockern stellt möglicherweise eine Alternative dar.9
- Auch dies ist eine Off-Label-Therapie und sollte nur bei sehr kleinen Hämangiomen zur Anwendung kommen.2
- Laser
- Chirurgische Exzision
- Kann notwendig sein bei ulzerierenden, blutenden oder lebensbedrohlichen Hämangiomen.
- ggf. spätere Beseitigung von Hämangiomresten aus ästhetischen oder funktionellen Gründen
- Der beste Zeitpunkt ist nach der Regression, also im 4.‒5. Lebensjahr.
Verlauf, Komplikationen und Prognose
Verlauf
- Die Erkrankung beginnt im Säuglingsalter und geht im Alter von 1–5 Jahren allmählich zurück.
- Die Dauer der Rückbildungsphase variiert und kann auf der Basis von Größe oder Aussehen der Läsionen nicht vorhergesagt werden.
- Bei 80‒90 % der Tumoren ist die Regression im Alter von 4 Jahren abgeschlossen.2
Komplikationen
- Ulzeration
- Kommt bei 5‒10 % der Hämangiome vor, vor allem bei gemischten oberflächlichen/tiefen und bei Hämangiomen an der Lippe, im Perineum und an intertriginösen Stellen.12
- Es kann zu Sekundärinfektionen kommen.
- Atemwegsobstruktion bei Hämangiomen, die auf die Atemwege drücken.
- Sehstörungen durch ein Hämangiom: Das betrifft vor allem diejenigen, die auf dem oberen, medialen Augenlid lokalisiert sind.13
- Große kutane oder viszerale Hämangiome (besonders in der Leber) sind selten. Sie können infolge des erhöhten Minutenvolumens zu einer Herzinsuffizienz führen.
Prognose
- Unkomplizierte Hämangiome heilen meist folgenlos aus, bei den komplizierten kommt es auf Größe, Anzahl der Hämangiome und Beteiligung innerer Organe an.
- Eine frühzeitige Propranolol-Therapie ist günstig.
- Nach einer Propranolol-Therapie kommt es in 15‒20 % aller Fälle zu einem Rebound-Effekt in meist begrenztem Ausmaß. Eine erneute Therapie ist selten notwendig.2
Patienteninformationen
Patienteninformationen in Deximed
Illustrationen

Hämangiom: Proliferationsphase

Hämangiom: Regressionsphase
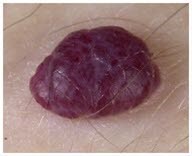
Hämangiom

Hämangiom: Proliferationsphase

Hämangion: periorbitale Läsion
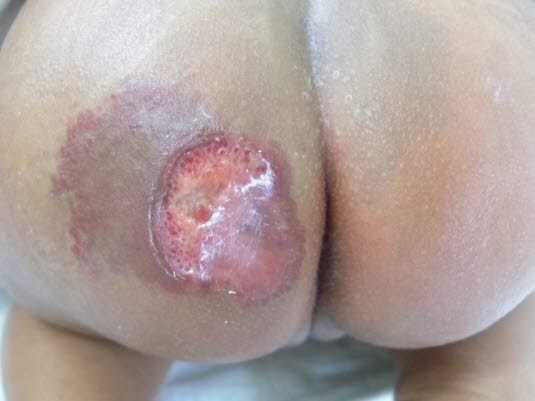
Hämangiom: Ulzerationen
Quellen
Leitlinien
- Deutsche Gesellschaft für Kinderchirurgie. Hämangiome, infantil im Säuglings- und Kleinkindesalter. AWMF-Leitlinie Nr. 006-100. S2k, Stand 2020. www.awmf.org
Literatur
- Antaya RJ. Infantile hemangioma. Medscape, last updated Nov 2020 emedicine.medscape.com
- Deutsche Gesellschaft für Kinderchirurgie. Hämangiome, infantil im Säuglings- und Kleinkindesalter. AWMF-Leitlinie Nr. 006-100, Stand 2020. www.awmf.org
- Krowchuk DP, Frieden IJ, Mancini AJ, et al. Clinical Practice Guideline for the Management of Infantile Hemangiomas. Pediatrics 2019; 143: e20183475. pmid:3058406. www.ncbi.nlm.nih.gov
- Rotter A, de Oliveira ZNP. Infantile hemangioma: pathogenesis and mechanisms of action of propranolol. J Dtsch Dermatol Ges. 2017 onlinelibrary.wiley.com
- Léauté-Labrèze C, Hoeger P, Mazereeuw-Hautier J, et al. A randomized, controlled trial of oral propranolol in infantile hemangioma. N Engl J Med 2015; 372: 735-46. doi:10.1056/NEJMoa1404710 DOI
- Tollefson MM, Frieden IJ. Early growth of infantile hemangiomas: what parents' photographs tell us. Pediatrics. 2012; 130: e314-20. doi:10.1542/peds.2011-3683 DOI
- Hemangioma Investigator Group, Haggstrom AN, Drolet BA, et al. Prospective study of infantile hemangiomas: demographic, prenatal, and perinatal characteristics. J Pediatr 2007; 150: 291-4. PMID: 17307549 PubMed
- Chang LC, Haggstrom AN, Drolet BA, et al. Growth characteristics of infantile hemangiomas: implications for management. Pediatrics 2008; 122: 360-7. pmid:18676554 PubMed
- Ni N, Langer P, Wagner R, Guo S. Topical timolol for periocular hemangioma: report of further study. Arch Ophtalmol 2011; 377-9. 10.1001/archophthalmol.2011.24. pubmed.ncbi.nlm.nih.gov
- Stier MF, Glick SA, Hirsch RJ. Laser treatment of pediatric vascular lesions: Port wine stains and hemangiomas. J Am Acad Dermatol 2008; 58: 261-85. PMID: 18068263 PubMed
- Brightman LA, Brauer JA, Terushkin V, et al. Ablative fractional resurfacing for involuted hemangioma residuum. Arch Dermatol 2012; 148: 1294-8. pmid: 22910902 PubMed
- Kim HJ, Colombo M, Frieden IJ. Ulcerated hemangiomas: clinical characteristics and response to therapy. J Am Acad Dermatol 2001; 44: 962-72 PubMed
- Ceisler, EJ, Santos, L, Blei, F. Periocular hemangiomas: what every physician should know. Pediatr Dermatol 2004; 21: 1. PubMed
- Poetke M, Frommeld T, Berlien HP. PHACE syndrome: new views on diagnostic criteria. Eur J Pediatr Surg 2002; 12: 366-74. PubMed
- Winter PR, Itinteang T, Leadbitter P, et al. PHACE syndrome--clinical features, aetiology and management. Acta Paediatr 2016 Feb; 105(2: 145-53. pmid:26469095 PubMed
- Munden A, Butschek R, Tom W, et al. Prospective study of infantile hemangiomas: Incidence, clinical characteristics, and association with placental anomalies. Br J Dermatol 2014 doi.org/10.1111/bjd.12804 pubmed.ncbi.nlm.nih.gov
- North, PE, Waner, M, Brodsky, MC. Are infantile hemangiomas of placental origin?. Ophthalmology 2002; 109: 633. PubMed
- Regnier S, Dupin N, Le Danff C, et al. Endothelial cells in infantile haemangiomas originate from the child and not from the mother (a fluorescence in situ hybridization-based study. Br J Dermatol 2007; 157: 158-60. pmid:17578438 PubMed
- Drolet BA, Frommelt PC, Chamlin SL, et al. Initiation and use of propranolol for infantile hemangioma: report of a consensus conference. Pediatrics 2013;131:128-140 pubmed.ncbi.nlm.nih.gov
- Chinnadurai S, Fonnesbeck C, Snyder KM, Pharmacologic Interventions for Infantile Hemangioma. A Meta-analysis. Pediatrics 2016 pubmed.ncbi.nlm.nih.gov
Autor*innen
- Monika Lenz, Fachärztin für Allgemeinmedizin, Neustadt am Rübenberge
- Die ursprüngliche Version dieses Artikels basiert auf einem entsprechenden Artikel im norwegischen hausärztlichen Online-Handbuch Norsk Elektronisk Legehåndbok (NEL, https://legehandboka.no/).