Zusammenfassung
- Definition:Schlaganfall: gefäßbedingte Erkrankungen des Gehirns mit dem gemeinsamen Merkmal einer plötzlich auftretenden Schädigung von Hirngewebe aufgrund eines Gefäßverschlusses oder einer Hirnblutung. Transitorisch ischämische Attacke (TIA): umschriebene neurologische Funktionsstörung mit vollständiger Reversibilität innerhalb von 24 h.
- Häufigkeit:In Deutschland ca. 270.000 Schlaganfälle pro Jahr.
- Symptome und Befunde:Erstbeurteilung durch standardisierten neurologischen Untersuchungsalgorithmus FAST: Fazialisparese (Face), verringerte Kraft im Arm (Arm), Sprach-/Wortfindungsstörungen oder undeutliche Aussprache (Speech). Wenn diese Symptome vorliegen, dann umgehende Einweisung (Time).
- Diagnostik:Initial in Stroke Unit Durchführung von CT oder MRT zum Ausschluss/Nachweis Blutung und Beurteilung des ischämischen Areals. Im Verlauf weitere Diagnostik zur Klärung der Ätiologie (EKG, Echokardiografie, Bildgebung der hirnversorgenden Arterien).
- Therapie:Bei ischämischem Insult systemische Thrombolyse (möglichst innerhalb von 4,5 h nach Symptombeginn) und mechanische Thrombektomie (möglichst innerhalb 6 h). Je nach Ergebnis der Bildgebung können diese Maßnahmen aber auch in den folgenden Stunden noch sinnvoll sein. Medikamentöse Sekundärprävention, Rehabilitation.
Allgemeine Informationen
Definition
- Schlaganfall: gefäßbedingte Erkrankungen des Gehirns mit dem gemeinsamen Merkmal einer plötzlich auftretenden Schädigung von Hirngewebe aufgrund eines Gefäßverschlusses oder einer Hirnblutung1
- Transitorisch ischämische Attacke (TIA): umschriebene neurologische Funktionsstörung mit vollständiger Reversibilität innerhalb von 24 h1
- Der Begriff basiert allein auf Befunden aus der klinischen Untersuchung.
Häufigkeit
- Schlaganfall ist weltweit:2
- die zweithäufigste Todesursache
- die Hauptursache von Behinderung und
- ein wesentlicher Kostenfaktor für Gesundheitssysteme.
- Inzidenz
- in Deutschland ca. 270.000 Schlaganfälle jährlich1
- ca. 200.000 Erstereignisse
- ca. 70.000 Rezidive
- 1-Jahres-Inzidenz ca. 336/100.000 Einw.3
- In den letzten 15 Jahren ist die Häufigkeit von Schlaganfällen etwa gleich gegeblieben.
- Die Sterblichkeit am Schlaganfall ist in den letzten 15 Jahren erheblich zurückgegangen – bei Frauen von 500, bei Männern von 600 auf 300/100.000 Einw.4
- in Deutschland ca. 270.000 Schlaganfälle jährlich1
- Alter
- ansteigende Inzidenz mit dem Alter, ab dem 65. Lebensjahr häufiger als koronare Ereignisse5
- Geschlecht
- Lebenszeitprävalenz des Schlaganfalls bei Männern geringfügig höher als bei Frauen2
- Sozioökonomischer Status
- Inzidenz am höchsten bei niedrigem Sozialstatus und am niedrigsten bei hohem Sozialstatus2
- bei Frauen deutlichere Ausprägung des sozialen Gradienten
- Inzidenz am höchsten bei niedrigem Sozialstatus und am niedrigsten bei hohem Sozialstatus2
- Kosten
Ätiologie und Pathogenese
Ätiologie des ischämischen Schlaganfalls (ca. 85 %)
- Arterielle Ischämie am häufigsten, anhand der TOAST-Kriterien kann eine Einteilung der Ätiologie erfolgen in:8-11
- Makroangiopathie (ca. 10 %)
- extrakranielle oder intrakraniellen Arterie mit Obstruktion ≥ 50 % (z. B. Karotisstenose)
- Mikroangiopathie (ca. 25 %)
- lakunäre Infarkte in der zerebralen Bildgebung
- Kardioembolie (ca. 25 %)
- Vorhofflimmern/-flattern, intrakardialer Thrombus, Herzklappenprothese, Vorhofmyxom
- andere Ursachen (ca. 10 %)
- z. B. Dissektion, Vaskulitis, Koagulopathien, Vasospasmen, Drogen
- ungeklärte Ätiologie („kryptogen“): ca. 30 %
- ESUS (Embolic Stroke of Determined Source, ca. 15 %) stellt eine Weiterentwicklung des Konzepts des kryptogenen Schlaganfalls dar.8-9
- Es beruht darauf, dass die Mehrzahl der kryptogenen Schlaganfälle wahrscheinlich embolisch aus einer versteckten Quelle getriggert sind, und erfordert eine standardisierte Diagnostik.8-9
- Makroangiopathie (ca. 10 %)
- Venöse Ischämie deutlich seltener durch Sinusvenenthrombose/ Hirnvenenthrombose5,12
Ätiologie des hämorrhagischen Schlaganfalls (ca. 15 %)
- Intrazerebrale Blutung
- Subarachnoidalblutung
Pathogenese
Schlaganfall
- Hauptursache des Schlaganfalls ist der Abfall des Blutflusses unter den Grenzwert, der für den Erhalt der funktionellen Integrität der Gehirnzellen erforderlich ist.13
- Die ungenügende Blutzufuhr triggert eine komplexe schädigende Kaskade biochemischer Mechanismen.13-15
- u. a. Entzündung, mangelnde Energiebereitstellung, Azidose, Exzitotoxizität, Toxizität durch freie Radikale und Zytokine, Komplementaktivierung, Verschlechterung der Blut-Hirn-Schranke, Leukozyteninfiltration
- Letztlich führen diese Mechanismen zum Zelltod.
TIA
- Das pathogenetische Verständnis der TIA (reversibles neurologisches Defizit mit vollständiger Rückbildung innerhalb 24 h) hat sich durch die moderne Bildgebung (MRT) verändert.16
- Streng genommen sollte der Begriff auf Patient*innen ohne Läsionsnachweis im MRT eingeschränkt werden.17
- Die transiente Symptomatik mit nachgewiesener Läsion ist mit erhöhtem Risiko für Schlaganfall mit bleibender Behinderung verbunden.17
- Das Problem bei flüchtigen neurologischen Ereignissen ohne pathologischen Befund in der zerebralen Bildgebung ist, dass es auch viele andere Ursachen geben kann, die nicht zwangsläufig zu einer lebenslangen Medikation führen müssen. So kann beispielsweise eine Migräne mit dem Bild eines Schlaganfalls einhergehen (siehe auch Differenzialdiagnosen). Kompliziert wird dies dadurch, dass eine Migräne und speziell auch eine Behandlung mit Triptanen das Risiko für Schlaganfälle erhöhen können.18
Disponierende Faktoren
- Es gibt nicht-modifizierbare und modifizierbare Risikofaktoren für einen ischämischen und hämorrhagischen Schlaganfall.
Nicht-modifizierbare Risikofaktoren19
- Alter
- zunehmendes Risiko mit dem Alter
- Geschlecht
- Bei jungen Frauen ist das Risiko etwas höher als bei Männern, bei Älteren ist das Risiko für Männer geringfügig höher als bei Frauen.
- Ethnizität
- erhöhtes Risiko bei afrikanischer Abstammung – und zugleich schlechtere protektive Wirksamkeit von Betablockern und ACE-Hemmern
- Genetik
- erhöhtes Risiko bei positiver Familienanamnese
Modifizierbare Risikofaktoren für ischämischen Schlaganfall
- In der Interstroke-Studie wurden 10 modifizierbare Risikofaktoren identifiziert:19-20
- arterielle Hypertonie
- Rauchen
- abdominale Adipositas: erhöhtes Taille-Hüfte-Verhältnis
- ungesunde Ernährung
- Inaktivität
- Diabetes mellitus
- erhöhter Alkoholkonsum
- psychosozialer Stress und Depression
- kardiale Ursachen
- Verhältnis Apolipoprotein B/Apolipoprotein A1, d. h. LDL/HDL.
- Östrogenhaltige Ovulationshemmer erhöhen das Schlaganfallsrisiko.12
Modifizierbare Risikofaktoren für hämorrhagischen Schlaganfall19-20
- Arterielle Hypertonie
- Rauchen
- Abdominale Adipositas: erhöhtes Taille-Hüfte-Verhältnis
- Erhöhter Alkoholkonsum
- Ungesunde Ernährung
ICPC-2
- K89 Transiente zerebrale Ischämie /TIA
- K90 Schlaganfall/zerebrovask. Insult
- K91 Zerebrovaskuläre Erkrankung
ICD-10
- I61 Intrazerebrale Blutung
- I61.0 Intrazerebrale Blutung in die Großhirnhemisphäre, subkortikal
- I61.1 Intrazerebrale Blutung in die Großhirnhemisphäre, kortikal
- I61.2 Intrazerebrale Blutung in die Großhirnhemisphäre, nicht näher bezeichnet
- I61.3 Intrazerebrale Blutung in den Hirnstamm
- I61.4 Intrazerebrale Blutung in das Kleinhirn
- I61.5 Intrazerebrale intraventrikuläre Blutung
- I61.6 Intrazerebrale Blutung an mehreren Lokalisationen
- I61.8 Sonstige intrazerebrale Blutung
- I61.9 Intrazerebrale Blutung, nicht näher bezeichnet
- I63 Hirninfarkt
- I63.0 Hirninfarkt durch Thrombose präzerebraler Arterien
- I63.1 Hirninfarkt durch Embolie präzerebraler Arterien
- I63.2 Hirninfarkt durch nicht näher bezeichneten Verschluss oder Stenose präzerebraler Arterien
- I63.3 Hirninfarkt durch Thrombose zerebraler Arterien
- I63.4 Hirninfarkt durch Embolie zerebraler Arterien
- I63.5 Hirninfarkt durch nicht näher bezeichneten Verschluss oder Stenose zerebraler Arterien
- I63.6 Hirninfarkt durch Thrombose der Hirnvenen, nichteitrig
- I63.8 Sonstiger Hirninfarkt
- I63.9 Hirninfarkt, nicht näher bezeichnet
- I64 Schlaganfall, nicht als Blutung oder Infarkt bezeichnet
- G45 Zerebrale transitorische Ischämie und verwandte Syndrome
- G45.9 Zerebrale transitorische Ischämie, nicht näher bezeichnet
Diagnostische Kriterien
- Akut aufgetretene neurologische Symptome
- Nachweis einer Ischämie/Blutung in der zerebralen Bildgebung
Differenzialdiagnosen (Stroke Mimics)
- Auch im Zentrum einer Maximalversorgung liegt die initiale Fehldiagnose bei ca. 10 %, im präklinischen Bereich ist von höheren Quoten auszugehen.21
- Wesentliche „Stroke Mimics“ sind:21
Zerebrale Ursachen (die 3 häufigsten)
- Epileptischer Anfall (vor allem Todd-Parese = passagere Lähmung nach einem epileptischen Anfall)
- Migräne mit Aura
- Funktionelle/dissoziative Störung
Zerebrale Ursachen (andere)
- Intrakranielle Raumforderung
- Entzündlich
- Synkopen
Isolierte Hirnnervenausfälle
- Periphere Fazialisparesen
- Vestibulopathien
Metabolische Ursachen
- Hypoglykämie, Hyperglykämie
- Elektrolytstörungen
Verschlechterung des Allgemeinzustands (insb. bei älteren Menschen)
- Exsikkose
- Infekt, Sepsis
Pseudolähmungen
- Orthopädisch bedingte Bewegungseinschränkungen (z. B. Schenkelhalsfraktur, Rotatorenmanschettenruptur)
Präklinische Diagnostik und Versorgung
- Schlaganfall/TIA sind grundsätzlich medizinische Notfälle, bei jedem Verdacht soll unverzüglich die Notruf-Telefonnummer 112 gewählt werden.1
- Jeder andere Versuch, medizinische Hilfe zu organisieren, führt zu potenziell bedrohlicher Verzögerung der Versorgung.1
Initiale Untersuchung
- Die initiale klinische Untersuchung soll nach dem ABCDE-Schema erfolgen:1
- Airway (Atemwege)
- Breathing (Beurteilung der Atmung)
- Circulation (Kreislauf)
- Disability (neurologischer Zustand)
- Exposure (Beurteilung in entkleidetem Zustand).11
- Ggf. sollen bereits nach ABC lebensrettende Maßnahmen durchgeführt werden.1 (siehe auch Basic Life Support, Advanced Life Support)
- Hiervon sind aber nur wenige Patient*innen mit Schlaganfall betroffen.1
- Ansonsten wird im nächsten Schritt der neurologische Status überprüft.1
- Hierfür soll ein standardisierter neurologischer Untersuchungsalgorithmus (z. B. FAST) verwendet werden, dieser weist mit hoher Sicherheit neurologische Defizite nach und ermöglicht eine gezielte Einweisung.1
Initiale Versorgung
- Wenn zeitnah möglich, sollte ein venöser Zugang zur vorsorglichen Absicherung gelegt werden. Vorteile sind:1
- bei Bedarf i. v. Applikation von Medikamenten
- Möglichkeit zur Blutzuckermessung
- Volumengabe bei Exsikkose
- Abnahme von Laborblut (je nach rettungsdienstlichem Versorgungskonzept).
- Eine Hypoglykämie ist ein typisches „Stroke Mimic“ und sollte daher ausgeschlossen werden.
- Zurückhaltendes Blutdruckmanagement bei initial häufig erhöhtem Blutdruck: Zu rasche Senkung kann eine Ischämie verstärken, ein zu hoher Blutdruck ist bei Blutung ungünstig (klinische Unterscheidung der Ätiologie aber nicht möglich).
- Der Nutzen einer routinemäßigen Sauerstoffgabe ist nicht belegt.1
- Antikoagulation (Heparin) oder Thrombozytenaggregationshemmer (ASS) sollten vor Bildgebung in der Klinik nicht verabreicht werden, da eine Blutung präklinisch nie ausgeschlossen werden kann.5
DEGAM-Empfehlungen zur vorstationären Diagnostik und Versorgung1
Initiale Untersuchung
ABCDE-Schema
- Die initiale Untersuchung von Notfallpatient*innen soll standardisiert nach dem ABCDE-Schema erfolgen. Ergibt sich aus ABC ein sofortiger Handlungsbedarf, soll entsprechend gehandelt werden.
FAST
- Face
- Lassen Sie die Person lächeln. Hängt ein Mundwinkel herab? Dies kann auf Gesichtslähmung/Halbseitenlähmung hinweisen.
- Arm
- Bitten Sie die Person, die Arme nach vorne zu strecken und dabei die Handflächen nach oben zu drehen.
- Bei einer Lähmung können nicht beide Arme gehoben werden, ein Arm sinkt ab oder dreht sich.
- Speech
- Lassen Sie die Person einen einfachen Satz nachsprechen.
- Ist sie dazu nicht in der Lage oder klingt die Stimme verwaschen, liegt vermutlich eine Sprachstörung vor.
- Time
- Falls mindestens einer der o. g. Tests positiv ist: Ohne weiteren Verzug 112 anrufen („Time is brain“)!
- Siehe Tabelle FAST-Test.
- Neurologisch Versierte können die NIHSS (National Institutes of Health Stroke Scale) zur umfassenderen Beurteilung der klinischen Schwere eines Schlaganfalles benutzen, diese wird aber überwiegend erst in der Klinik verwendet.11,22
- Für jedes Kriterium der NIHSS werden zwischen 0 und max. 4 Punkte vergeben (Gesamtpunktzahl 0–42 Punkte), je höher die Punktzahl, desto schwerer der Schlaganfall (NIHSS Rechner).
- Merke: Ischämische und hämorrhagische Schlaganfälle können anhand der klinischen Untersuchung nicht differenziert werden.23
- Bei Telefonkontakt mit der Praxis und V. a. Schlaganfall sollten medizinische Fachangestellte den FAST-Test anwenden und ggf. unverzüglich den Rettungsdienst aktivieren (Telefon-Nr. 112).
Initiale Versorgung
Venöser Zugang
- Sofern ein venöser Zugang in einem akzeptablen Zeitrahmen herstellbar ist, soll er als Absicherungsmaßnahme angelegt werden, da jeder Schlaganfall eine potenziell akut lebensbedrohliche Situation darstellt.
Blutzucker
- Die Blutzuckermessung soll erfolgen, um die Differentialdiagnose einer Hypoglykämie sicher auszuschließen.
- Bei niedrigen BZ-Werten (< 60 mg/dl) soll Glukose i. v. gegeben werden.
Sauerstoff
- Die Gabe von Sauerstoff sollte erst ab einer Sättigung < 95 % erfolgen.
Blutdruck
- Bei einem Wert < 120 mmHg systolisch und Hinweisen auf eine Exsikkose sollte kristalloide Infusionslösung verabreicht werden.
- Blutdruckwerte ≥ 220 mmHg können per vorsichtiger medikamentöser Titration (z. B. mit Nitrendipin-Trinkampullen) um 15 % gesenkt werden.
Sonstiges
- Die anamnestischen Daten, einschließlich der Beginn der Symptomatik und mögliche Lyse-Kontraindikationen sowie bereits erfolgte therapeutische Interventionen sollen dokumentiert werden. Ein Medikamentenplan soll zur Mitgabe vorbereitet werden.17
- Die Zeit des Wartens auf den Rettungsdienst sollte genutzt werden, um Patient*innen und Bezugspersonen grundlegende Informationen zu vermitteln (z. B. nicht unbegleitet aufstehen, Nahrungs-/Flüssigkeitskarenz) und ggf. beruhigend einzuwirken.
Indikationen zu Klinikeinweisung bzw. ambulanter Abklärung
Akuter Schlaganfall oder TIA innerhalb der letzten 48 h1,17,24
- Diese Patient*innen sollen umgehend auf einer Stroke Unit behandelt werden.
TIA > 48 h und < 14 Tage1,17
- Hochrisikopatient*innen sollen einer Stroke Unit zugewiesen werden:
- bekanntes Vorhofflimmern
- bekannte Stenosen hirnversorgender Arterien
- sonstige frühere kardiovaskuläre Erkrankungen
- Hoher ABCD2-Score (≥ 4): berücksichtigt für den Score werden Alter, Blutdruck, Art der Symptome, Symptomdauer und Vorliegen eines Diabetes mellitus.
Symptomatik > 14 Tage zurückliegend1,17
- In der Regel ist eine ambulante Abklärung ausreichend, diese sollte schnellstmöglich innerhalb eines Monats nach Symptombeginn komplettiert werden.
- Bei ambulanter Abklärung unterscheiden sich Diagnostik und Sekundärprävention nicht von Patient*innen nach vollendetem Schlaganfall.
Gründe gegen Krankenhauseinweisung1
- Hausärzt*innen können sich unter Abwägung von Nutzen und Schaden und Berücksichtigung des Wunsches von Patient*innen/Betreuer*innen für eine palliative Therapie und gegen eine stationäre Einweisung entscheiden.
- In diesem Fall Verzicht auf Rettungsdienst und Einleitung supportiver Maßnahmen
Diagnostik und Therapie in der Stroke Unit
Konzept der Stroke Unit
- Stroke Units (Schlaganfall-Spezialstationen) sind Sondereinrichtungen mit einem integrativen Behandlungskonzept für Schlaganfallpatient*innen im Akutstadium.17
- Dieses Konzept umfasst Früherkennung, präklinische Notfallversorgung, zügige Überweisung in Zentren mit derartigen Stationen, dortige Notfallaufnahme, neuroradiologische und sonstige apparative Sofortdiagnostik, Einbeziehung einer Intensivstation, schließlich Weiterverlegung auf Allgemeinstationen, in Rehabilitationseinrichtungen oder häusliche Pflege.17
- In ländlichen Regionen telemedizinische Anbindung der Notaufnahmen regionaler Krankenhäuser an überregionale Stroke Units (Tele-Stroke-Units)17
Diagnostik
Initiale Bildgebung17
- In der Stroke Unit erfolgt eine rasche Bildgebung durch CT oder MRT zur Unterscheidung zwischen Ischämie und Blutung.
- Computertomografie (CT)
- diagnostischer Standard: breit verfügbar, universell anwendbar
- Durch CT-Angiografie mit Kontrastmittel können mit hoher Sicherheit extra- und intrakranielle Gefäßpathologien erfasst werden.
- Informationen zur Gewebsperfusion und Differenzierung zwischen abgestorbenem Gewebe (Infarkt) und minderperfundiertem Gewebe (Penumbra)
- Magnetresonanztomografie (MRT)
- im Vergleich zur CT höhere Sensitivität zum sicheren Nachweis infarzierten Hirngewebes in der Schlaganfallfrühphase, Abschätzung des Infarktalters möglich
- Nachteile sind höherer logistische Aufwand, längere Untersuchungsdauer und geringere Verfügbarkeit.
Monitoring17
- Akute Schlaganfallpatient*innen (TIA und Hirninfarkt) sollten zumindest in den ersten 2–3 Tagen apparativ überwacht werden.
- Das apparative Monitoring sollte mindestens umfassen: Blutdruck, Herzfrequenz, EKG, Atmung, Sauerstoffsättigung und Körpertemperatur.
Sonstige Diagnostik17
- EKG-Monitoring
- Ein mehrtägiges EKG-Monitoring (Telemetrie, im weiteren Verlauf evtl. LZ-EKG) sollte erfolgen, wenn der Nachweis von Vorhofflimmern oder anderer Rhythmusstörungen therapeutische Konsequenzen hat.
- Darstellung der extra- und intrakraniellen hirnversorgenden Gefäße
- So früh wie möglich (innerhalb von 24–48 Stunden) sollte eine nichtinvasive Diagnostik der extra- und intrakraniellen Gefäße erfolgen.
- In Betracht kommen je nach Verfügbarkeit und Expertise:
- Duplexsonografie
- CT-Angiografie
- MR-Angiografie.
- Echokardiografie (TTE, TEE)
- Eine transthorakale Echokardiografie (TTE) sollte zur Bestimmung der Ätiologie durchgeführt werden, wenn diese durch die initiale Diagnostik nicht geklärt werden konnte (z. B. Vorhofflimmern oder hochgradige Karotisstenose).
- Ist die Ätiologie nach Routinediagnostik (zerebrale Bildgebung, Darstellung der extra- und intrakraniellen Gefäße, EKG, Langzeit-EKG und TTE) ungeklärt, sollte bei therapeutischer Konsequenz ergänzend eine transösophageale Echokardiografie (TEE) durchgeführt werden.
Akuttherapie des ischämischen Schlaganfalls
- Ziel der therapeutischen Intervention beim ischämischen Hirninfarkt ist die Wiederherstellung einer ausreichenden Perfusion mit der Rettung des Penumbra-Gewebes (Penumbra = Halbschatten: Differenzareal zwischen bereits nekrotischem und umgebendem noch vitalem Hirngewebe)5
- Die Ausdehnung der Penumbra kann näherungsweise mit CT- oder MRT-Verfahren abgeschätzt werden („Mismatch“ zwischen diffusions- und perfusionsgestörtem Areal).5
Rekanalisation – Thrombolyse
- Die systemische Thrombolysetherapie ist die Standardtherapie beim ischämischen Schlaganfall im Zeitfenster bis 4,5 h.17
- Gelingt der Therapiebeginn innerhalb von 3 Stunden, so erhöht sich die Wahrscheinlichkeit eines guten Ergebnisses weiter.5
- Mit zunehmendem Zeitfenster sinkt der Nutzen im Vergleich zum Blutungrisiko.5
- Blutungsrisiko unter Thrombolyse 3–7 % im Vergleich zu sonst 0,5–2 %
- Dennoch kann eine Thrombolyse auch verzögert sinnvoll sein, wenn die Bildgebung eine relevante Penumbra zeigt.11,17
- im Zeitfenster 4,5–9 h
- bei unbekanntem Symptombeginn („Wake-up“-Schlaganfall)
- Abhängigkeit der Thrombolyseindikation vom klinischen Schweregrad17
- Eine Thrombolyse soll bei behindernden Schlaganfallsymptomen durchgeführt werden.
- Bei milden, nicht behindernden Symptomen kann auf die Thrombolyse verzichtet werden.
Rekanalisation – endovaskuläre Therapie
- Die endovaskuläre Schlaganfalltherapie durch mechanische Thrombektomie ist lange bekannt, war zwischenzeitlich in den Hintergrund getreten, ist aufgrund günstiger Studienergebnisse aber mittlerweile fester Bestandteil der Behandlung.17,25-28
- Die Thrombektomie wird zusätzlich zur vorher begonnen systemischen Thrombolyse durchgeführt.
- Insbesondere Verschlüsse der großen Gefäße (distale Arteria carotis und Hauptstamm der A. cerebri media) durch große embolisch bedingte Thromben sprechen teilweise ungenügend auf die systemische Thrombolyse an.5
- Diese Thromben werden kathetergestützt (Stent-Retriever) durchdrungen und mit einem Stent-Gitter eingefangen.5
Leitlinie: Rekanalisation bei ischämischem Schlaganfall17
Systemische Thrombolyse, Standardtherapie
- Patient*innen mit ischämischem Schlaganfall, die innerhalb von 4,5 h nach Symptombeginn bzw. dem Zeitpunkt, an dem sie zuletzt gesund gesehen wurden, behandelt werden können und keine Kontraindikationen aufweisen, sollen mit einer systemischen Thrombolyse mit Alteplase behandelt werden.
- Die systemische Thrombolyse im 4,5-h-Zeitfenster erwachsener Patient*innen soll unabhängig vom Alter erfolgen.
Systemische Thrombolyse im erweiterten oder unklaren Zeitfenster
- Bei Patient*innen mit ischämischem Schlaganfall im unklaren Zeitfenster oder nach dem Erwachen, die mehr als 4,5 h zuvor zuletzt gesund gesehen wurden, sich aber innerhalb von 4,5 h nach Erkennen der Symptome in der Klinik vorstellen und bei denen ein DWI/FLAIRMismatch (Diffusion Weighted Imaging: DWI; Fluid-Attenuated Inversion-Recovery-Bildgebung: FLAIR, bei Mismatch liegt Ereignis maximal 4–5 Stunden zurück, Anm. der Redaktion) in der MRT vorliegt, soll eine i. v. Thrombolyse mit Alteplase erfolgen.
- Bei Patient*innen mit ischämischem Schlaganfall im 4,5- bis 9-h-Zeitfenster (bekannter Beginn oder ab der Mitte des Schlafs bei unbekannter Symptomdauer) und einem Mismatch zwischen im CT oder MRT dargestelltem Infarktkern und Penumbra sollte eine i. v. Thrombolyse mit Alteplase erfolgen.
Endovaskuläre Therapie
- Bei Patient*innen mit ischämischem Schlaganfall, klinisch relevantem neurologischem Defizit und Verschluss einer großen Arterie im vorderen Kreislauf soll, wenn innerhalb von 6 h möglich, eine mechanische Thrombektomie erfolgen, um das funktionelle Ergebnis zu verbessern.
- Jenseits des 6-h-Zeitfensters soll eine mechanische Thrombektomie relevanter Verschlüsse im vorderen Kreislauf erfolgen, wenn durch erweiterte Bildgebung (z. B. Darstellung eines kleinen Infarktkerns, Mismatch) im Kontext der klinischen Symptomatik zu vermuten ist, dass rettbares Risikogewebe vorliegt.
- Patient*innen, die für eine endovaskuläre Schlaganfalltherapie in Betracht kommen und die keine Kontraindikation für eine systemische Thrombolyse haben, sollen so früh wie möglich auch mit Alteplase behandelt werden, wobei keine der beiden Behandlungen die andere verzögern darf.
Akuttherapie des hämorrhagischen Schlaganfalls
Intrakranielle Blutung
- Grundsätzlich senkt eine Blutdrucksenkung auf Werte um 140 mmHg und noch tiefer die Ausdehnung der Blutung und die Häufigkeit von Nachblutungen.5
- Da präklinisch Ischämie vs. Blutung nicht differenziert werden kann, sind Werte um 160 mmHg tolerierbar.
- Je nach Verlauf werden im Rahmen der stationären Behandlung erforderlich:5
- Anlage einer externen Liquordrainage
- mikrochirurgische Hämatomausräumung
- neuroprotektive und hirndrucksenkende Intensivtherapie.
Subarachnoidalblutung (SAB)
- SAB sind in 85 % der Fälle durch Ruptur eines Aneurysmas ausgelöst, Ausschaltung erfolgt katheterinterventionell (Coiling) oder operativ (Clipping).5
- Weitere Maßnahmen im Rahmen der intensivmedizinischen Behandlung sind Therapien gegen Vasospasmen und/oder Hirndruck, Anlage einer Liquordrainage.5
Weitere Maßnahmen in der Akutphase
Physiotherapie
- Bei allen Schlaganfallpatient*innen sollte innerhalb von 48 h nach Schlaganfallbeginn mit der Mobilisierung („Out-of-Bed“-Aktivität) begonnen werden.17
- Dauer von 30–60 min pro Tag, durchgeführt an 5–7 Tagen pro Woche29
Ergotherapie
- Durch frühzeitige, gezielte Ergotherapie sollten z. B. Defizite u. a. der oberen Extremität inkl. Feinmotorikstörungen der Hand baldmöglichst verbessert werden.17
Logopädie
- Frühzeitige logopädische Evaluation zur Detektion und Behandlung einer Dysphagie wird empfohlen.17
- Zur Verbesserung einer Aphasie oder Dysarthie gibt es keine Evidenz.17
Sekundärprävention
Antithrombotische Therapie
Thrombozytenaggregationshemmer
- Mit der Thrombozytenfunktionshemmung wird die frühe Sekundärprävention bereits in der Akutphase eingeleitet.11
- Basis ist die Monotherapie mit ASS 100 mg/d oder Clopidogrel 75 mg/d.1
- Clopidogrel als Monotherapie ist in Deutschland nur in Ausnahmefällen verordnungsfähig und deutlich teurer, daher ist in der Regel ASS zu bevorzugen.1
- Bis zu 3 Wochen nach einem ischämischen Schlaganfall soll eine doppelte Plättchenhemmung (DAPT) mit ASS und Clopidogrel angeboten werden.30-31
- Die 3-wöchige DAPT ist als erweiterte Akutbehandlung zu verstehen, für eine generelle Empfehlung einer dualen Plättchenhemmung gibt es Hinweise darauf, dass der Schaden durch Blutungen den Benefit deutlich überschreitet.1
- Den Hausärzt*innen kommt eine wichtige Rolle zu bei der Beendigung der dualen und Überleitung zu einer Monotherapie.1
- Auch bei wiederholtem Schlaganfall unter Behandlung gibt es keine allgemeine Empfehlung zur Erweiterung oder Umstellung der antithrombotischen Therapie.1,29
- Eine Beurteilung der Wirksamkeit der Thrombozytenaggregationshemmer durch Thrombozytenfunktionstest wird nicht empfohlen.29
- Ein großzügiger begleitender Einsatz von PPI bei Patient*innen ohne gastrointestinale Probleme sollte vermieden werden.29
- Um mögliche unerwünschte Wirkungen durch einen Dauereinsatz von PPI zu vermeiden, kann stattdessen der H2-Antagonist Famotidin eingesetzt werden.
- Bei Komedikation mit NSAR sollte die reduzierte Wirksamkeit von ASS berücksichtigt werden: zeitlich versetzte Gabe der NSAR (i. d. R. mindestens 30 min) nach Einnahme des ASS empfohlen.29
- Zeitpunkt des Beginns der Thrombozytenaggregationshemmung
Antikoagulation
- Beim kardioembolischen Schlaganfall sollte statt der Thrombozytenaggregationshemmung eine orale Antikoagulation mit den Patient*innen besprochen werden.11
- Verhinderung von 2/3 der Rezidive
- Die DEGAM sieht keine ausreichende Evidenz, um NOAK gegenüber Vitamin-K-Antagonisten (VKA) zu bevorzugen, die DGN präferiert im Allgemeinen NOAK.1
- Zu Details der Differenzialtherapie mit VKA bzw. NOAK siehe Artikel Antikoagulation.
Leitlinie: Antithrombotische Sekundärprävention1,17,29-30
Thrombozytenaggregationshemmung, Monotherapie (Standard)
- Den Patient*innen soll ASS 100 mg/d (nur bei echter Unverträglichkeit Clopidogrel 75 mg/d) angeboten werden, Entscheidung über die Medikation nach individuellen klinischen Umständen und individueller Verträglichkeit.
Thrombozytenaggregationshemmung, duale Plättchenhemmung
- Patient*innen nach einem ischämischen Schlaganfall sollte eine duale Plättchenhemmung für max. 30 Tage angeboten werden.
- Die DEGAM empfiehlt ASS 100 mg/d + Clopidogrel 75 mg/d
- Eine Kombination von Ticagrelor mit Clopidogrel ist, anders, als die DGN empfiehlt, keine Alternative – Ticagrelor hat keinen Netto-Vorteil vor einer Gabe von ASS allein (Anm. des Reviewers).32-33
- Bei Patient*innen mit erhöhtem intra- oder extrakraniellen Blutungsrisiko sollte keine duale Therapie zur frühen Schlaganfall-Sekundärprävention erfolgen.
Orale Antikoagulation
- Patient*innen über 18 Jahre mit ischämischem Schlaganfall oder TIA und permanentem, persistierendem oder paroxysmalem Vorhofflimmern soll – sofern keine Kontraindikation besteht – eine dauerhafte OAK mittels Vitamin-K-Antagonisten (Phenprocoumon) oder mittels der neuen direkten Nicht-Vitamin-K-Antagonisten (NOAK) angeboten werden. Die Entscheidung, welche Substanzgruppe gewählt wird, fällt im gemeinsamen Gespräch zwischen Patient*in und Ärzt*in nach Würdigung von Komorbidität, Komedikation und Patientenpräferenz.
- Höheres Lebensalter ist bei Patient*innen nach ischämischem Schlaganfall oder TIA mit Vorhofflimmern keine Kontraindikation für eine orale Antikoagulation. Auch Gebrechlichkeit und Sturzgefahr sind nicht per se Kontraindikationen.
- Eine orale Antikoagulation bei Patient*innen mit Vorhofflimmern und kognitiven Einschränkungen oder einer Demenz ist gerechtfertigt, solange die regelmäßige Medikamenteneinnahme und Kontrolle gewährleistet ist.
VKA vs. NOAK
- Speziell für hochbetagte, multimorbide, niereninsuffiziente und mit Multimedikation behandelte Patient*innen könnte eine VKA-Therapie von Vorteil sein (in den NOAK-Zulassungsstudien nicht abgebildet).
- Bei einer Antikoagulation mit VKA soll eine Ziel-INR von 2,5 ± 0,5 angestrebt werden.
- Die Dosierung der NOAK sollte sich strikt an den Empfehlungen der Hersteller orientieren, um häufig zu beobachtende Unterdosierungen zu vermeiden.
- Kontrollen der Nierenfunktion sollen mindestens 1 x jährlich erfolgen, bei instabilen Situationen häufiger.
- Real-World-Untersuchungen haben in Deutschland keinen Vorteil von NOAK gegenüber VKA gezeigt, eher sogar eine Überlegenheit der VKA hinsichtlich der Verhinderung embolischer Ereignisse. Allenfalls Hirnblutungen traten unter NOAK etwas seltener auf.
- NOAK sollten nicht eingesetzt werden bei:
- Patient*innen mit einer gut funktionierenden Antikoagulation mit VKA (TTR > 70 %)
- einer unsicheren Adhärenz – die deutlich kürzere HWZ der DOAK verzeiht Fehler weniger als beim lang wirkenden Phenprocoumon.
- hohem Risiko für gastrointestinale Blutungen
- schweren Nierenfunktionsstörungen (eGFR < 30 ml/min)
- nach Herzklappenersatz und/oder relevanter Mitralstenose.
- DOAK können eine Indikation sein bei:
- spezifischen Interaktionen von VKA mit Arznei- und Nahrungsmitteln
- spezifischen Kontraindikationen von VKA (z. B. schwere Lebertoxizität)
- stark schwankenden INR-Werten unter VKA trotz guter Therapie-Adhärenz
- hohem Risiko intrazerebraler Blutungen
- frisch diagnostiziertem Vorhofflimmern, das akut einer Rhythmisierung oder Ablation zugeführt werden soll.
Weitere medikamentöse Therapie
Lipide
- Patient*innen sollen nach einem Schlaganfall eine Sekundärprävention mit einem Statin angeboten werden.1,29 Sie sollen dabei über eine geringe Größenordnung des Schutzeffektes durch Statine informiert werden – in der größten diesbezüglichen Studie34 betrug die absolute Risikoreduktion in 4,9 Jahren 1,9 %.
- Die Art der Durchführung einer Statintherapie ist seit längerem Gegenstand kontroverser Diskussion.
- Die DEGAM empfiehlt die Gabe einer Fixdosis eines Statins.1
- Die DGN empfiehlt eine zielwertorientierte Statintherapie, das LDL soll < 70 mg/dl gesenkt werden.29
- Zur Erreichung des Zielwerts empfiehlt die DGN ggf. die zusätzliche Gabe von Ezetimib.29Allerdings gibt es keine Studienbelege für eine Schutzwirkung von Ezetimib hinsichtlich der Verhinderung neuer Schlaganfälle.
Arterielle Hypertonie
- Patient*innen mit arterieller Hypertonie sollen nach Schlaganfall langfristig antihypertensiv behandelt werden.1,29
- Der Blutdruck soll < 140/90 mmHg gesenkt werden.1,29
- Eine weitere Blutdrucksenkung bringt in der Regel keinen Vorteil.
- Die Behandlung soll möglichst mit dem Thiazid-Diuretikum Chlortalidon35 und/oder ACE-Hemmer (bei Unverträglichkeit AT-Rezeptorblocker) erfolgen.
- insbesondere bei älteren/multimorbiden Patient*innen Auswahl der Antihypertensiva unter Berücksichtigung von Begleiterkrankungen und Medikamenteninteraktionen
- Zeitpunkt des Behandlungsbeginns
- Die antihypertensive Behandlung kann in den ersten Tagen nach Symptombeginn begonnen werden.29
Diabetes mellitus
- Patient*innen mit Diabetes mellitus und nach stattgehabtem Schlaganfall sollen entsprechend den Empfehlungen der NVL Diabetes und der DEGAM-S3-Leitlinie „Hausärztliche Risikoberatung zur kardiovaskulären Prävention“36 beraten werden.1
Hormontherapie
- Nach einem Schlaganfall sollte eine laufende Hormontherapie beendet werden.1
- Frauen in der Postmenopause, die eine Hormonersatztherapie zur Linderung von Wechseljahresbeschwerden beginnen oder fortführen wollen, sollten zum Nutzen-Risiko-Verhältnis beraten werden unter Beachtung ihrer Wünsche und Präferenzen.1
Diagnostik und Behandlung eines OSAS
- Bei V. a. OSAS nach Schlaganfall/TIA sollte eine Überweisung zu Spezialist*innen zur weiteren Diagnostik/ggf. Therapieeinleitung angeboten werden.1
- Bei OSAS sollte auf abendlichen Alkoholgenuss und die Einnahme von Hypnotika/Sedativa verzichtet und ggf. eine Gewichtsreduktion angestrebt werden.1
- CPAP und Unterkieferprotrusionsschienen sind Therapie der 1. Wahl.1
Interventionelle/operative Maßnahmen
Extra- und intrakranielle Stenosen
- Zu Diagnostik und Therapie extrakranieller Stenosen siehe Artikel Karotisstenose.
- Patient*innen mit intrakraniellen Stenosen werden im Allgemeinen mit Thrombozytenaggregationshemmern behandelt, bei rezidivierenden Symptomen/Hirninfarkten kann im Einzelfall Stentimplantation erwogen werden.37
Persistierendes Foramen ovale (PFO)
- Patient*innen unter 60 Jahren mit einem PFO und ohne alternative Ätiologie trotz umfassender Suche soll ein interventioneller Verschluss angeboten werden, wenn
ein mindestens mäßiger Shunt und/oder ein Vorhofseptumaneurysma besteht.1
Lebensstilmodifikation
- Auch wenn für die Sekundärprävention im Gegensatz zur Primärprävention wenig Evidenz vorliegt, ist anzunehmen, dass Lebensstilmodifikationen in der Sekundärprävention ähnlich wichtig sind wie in der Primärprävention37
- Entsprechend können daher die DEGAM-Empfehlungen zur Primärprävention angewendet werden:1,36
Ernährung und Genussmittel
- Die Ernährung sollte abwechslungsreich und an den Empfehlungen zur mediterranen oder nordischen Kost ausgerichtet sein.
- Bei Bedarf sollte durch Hausärzt*innen die Intensivierung der Ernährungsberatung durch Teilnahme an strukturierter Schulung empfohlen werden.
- Salz
- Die Salzaufnahme sollte reduziert werden, insbesondere bei arterieller Hypertonie.
- Alkohol
- Der Alkoholkonsum sollte beschränkt werden.
- Rauchen
- Das Rauchen sollte eingestellt werden.
Nahrungsergänzungsmittel
- Eine Supplementierung mit Vitamin- bzw. Antioxidanzien-Präparaten sollte nicht generell empfohlen werden.
Körperliche Aktivität
- Die Patient*innen sollten zu regelmäßiger körperlicher Aktivität ermutigt werden, orientiert an Fähigkeiten und Vorlieben des Einzelnen
- Patient*innen, die nur eingeschränkt in der Lage sind, körperlich aktiv zu sein, sollten so intensiv üben, wie es individuell sicher möglich ist, und die sitzend verbrachte Zeit minimieren.
Übergewicht/Adipositas
- Hausärzt*innen sollen durch unterstützende Gespräche bei der Gewichtsreduktion helfen.
- Die Beratung soll individualisiert, praxisnah und zielorientiert erfolgen und explizit psychosoziale Faktoren einbeziehen.
Rehabilitation im Rahmen der hausärztlichen Versorgung
- Zu den allgemeinen Prinzipien der stationären und poststationären Reha siehe auch Schlaganfall, Rehabilitation.
- Nach der Akutbehandlung (Phase A) erfolgen Frührehabilitation (Phase B) und weiterführende neurologische Rehabilitation (Phase C) stationär, die Anschlussheilbehandlung kann stationär oder ambulant erfolgen.1
- Innerhalb von 3 Monaten nach einer Rehabilitationsmaßnahme kann zudem eine Intensivierte Rehabilitationsnachsorge (IRENA, Kostenträger Rentenversicherung) durchgeführt werden, diese wird durch Rehabilitationsärzt*innen empfohlen und veranlasst.
- Hausärzt*innen versorgen die Patient*innen in allen Phasen nach dem Schlaganfall, da nicht jede Patient*in stationär aufgenommen wird und auch nur ein Teil eine Rehabilitationsmaßnahme erhält.
Zielsetzung und Planung
- Der Erfolg einer Reha-Maßnahme hängt auch davon ab, in welchem Maß Patient*innen das Rehabilitationsziel mitbestimmen. Therapieziele sollten daher unter Berücksichtigung der Komponenten Teilhabe, Aktivitäten und Körperfunktionen mit den Patient*innen gemeinsam erarbeitet werden.1
- Patient*innen sollten unterstützt werden, ihre persönlichen Therapieziele zu definieren.
- Die Ziele sollten evaluierbar und zeitlich bestimmt sein und schriftlich festgelegt werden.
- Patient*innen, soziales Umfeld und das Rehabilitationsteam sollten fortlaufende Kenntnis der festgelegten Rehabilitationsziele haben.
- Die Ziele sollten regelmäßig überprüft und bei Bedarf angepasst werden.
- Die Entscheidung über Auswahl und Verordnung von Therapien sollte auf der Grundlage standardisierter Assessmentverfahren getroffen werden.1
- Bei ambulanter Versorgung führen Heilmittelerbringer im Rahmen ihrer jeweiligen Therapie standardisierte Assessments durch, deren Ergebnisse den Hausärzt*innen als Befundbericht zur Verfügung gestellt werden.
- Vom hausärztlichen Team kann der gebräuchliche und unkomplizierte Barthel-Index durchgeführt werden, der komplexe Tätigkeiten allerdings nur unzureichend erfasst.
Versorgungsbereiche
- In der ambulanten Versorgung übernimmt in den meisten Fällen die Hausarztpraxis die Koordination der Therapie, in die Planung und Durchführung sollten verschiedene Berufsgruppen einbezogen werden.1
Heilmittelversorgung
- Zu den Heilmitteln zählen Ergotherapie, die physikalische Therapie (Krankengymnastik bzw. Physiotherapie) und die Stimm-, Sprech- und Sprachtherapie (Logopädie).
- U. a. folgende Indikationsschlüssel stehen zur Verfügung:
- physikalische Therapie ZN2 (ZNS-Erkrankungen) mit den Heilmitteln KG-ZNS (spezielle Krankengymnastik zur Behandlung von Erkrankungen des ZNS unter Einsatz neurophysiologischer Techniken nach Bobath, Vojta oder PNF oder KG)
- Ergotherapie EN2 (ZNS-Schädigungen) mit den Heilmitteln MFB (motorisch-funktionelle Behandlung), NOB (Hirnleistungstraining/neuropsychologisch orientierte Behandlung), PFB (psychisch-funktionelle Behandlung) und SPB (sensomotorisch-perzeptive Behandlung)
- Logopädie SP5 (Störungen der Sprache nach Abschluss der Sprachentwicklung), SP6 (Störungen der Sprechmotorik) und SC1 (Störungen des Schluckakts).
Hilfsmittelversorgung
- Durch Hilfsmittel sollen Teilhabe und Aktivität im Alltag auf einem möglichst hohen Niveau wiederhergestellt werden.
- Eine Listung im Hilfsmittelverzeichnis des GKV-Spitzenverbandes ist entgegen verbreiterter Auffassung für die Verordnungsfähigkeit eines Hilfsmittels nicht entscheidend, da es sich nicht um eine Positivliste handelt.
Pflegerische Versorgung
- Es gibt verschiedene Leistungen der Kranken- und Pflegversicherung zur Vermeidung von Versorgungslücken für Schlaganfallpatient*innen mit Unterstützungsbedarf und für pflegende Angehörige.
- Möglichst vor Rückkehr ins häusliche Umfeld Klärung des Bedarfs an Hilfestellung durch spezielle Ausstattung, räumliche Veränderung und/oder Hilfsmittel
Neuropsychologie
- Die Feststellung der Indikation erfolgt in einem zweistufigen Verfahren:
- fachärztliche Feststellung einer erworbenen Hirnschädigung (im Rahmen der fachärztlichen Erstkonsultation, Entlassbrief nicht ausreichend)
- Feststellung von neuropsychologischen Gesundheitsstörungen durch Psychotherapeut*innen/Ärzt*innen mit neuropsychologischer Zusatzqualifikation.
Empfehlungen zur Therapie nach Schlaganfall
- Die DEGAM hat umfangreiche Empfehlungen zur Therapie verschiedener residueller Störungen veröffentlicht, die im Detail der DEGAM-Leitlinie entnommen werden können.1
- Im Folgenden eine Auswahl der Empfehlungen:
DEGAM-Empfehlungen zur Therapie nach Schlaganfall1
Bewegungsapparat
- Schlaganfallpatient*innen mit Paresen sollten angeboten werden:
- Maßnahmen zur Verbesserung von Muskelkraft, Bein- und Armaktivität
- zusätzlich elektrische Muskelstimulationsverfahren.
- Bei Geh- und Gangstörungen soll Gehtraining angeboten werden.
- Hand- und Handgelenksorthesen sollen bei Armparese nicht routinemäßig eingesetzt werden (keine Wirkung auf Schmerz, Funktion, Bewegungsausmaß).
- Bei orofazialer Beeinträchtigung sollten Maßnahmen zur Verbesserung der motorischen Funktion der mimischen Muskulatur angeboten werden.
- Bei Spastik sollten Physiotherapie und Krafttraining angeboten werden, ergänzend können angeboten werden: elektrische Stimulation, lokale intramuskuläre Injektion von Botulinumtoxin (fokale Spastik), intrathekales Baclofen (multifokale Spastik), orale antispastische Medikamente wie Baclofen, Tizanidin, Dantrolen oder Diazepam (generalisierte Spastik).
- Bei Störungen der posturalen Kontrolle/des Gleichgewichts sollen Maßnahmen zur Verbesserung von Gleichgewicht, Ausdauer und Muskelkraft angeboten werden.
- Bei hohem Sturzrisiko sollte eine Beurteilung der Sturzgefahren im häuslichen Umfeld erfolgen, Beratung zur Beseitigung von Gefahrenquellen.
Schwindel
- Physiotherapie (sog. Schwindelkompensationstraining) und Physiotherapie am Gerät (v. a. Laufbandtraining) sind die wichtigsten Behandlungsempfehlungen.
Sprech- und Sprachstörungen, Dysphagie
- Bei Aphasie soll hochfrequente Sprachtherapie angeboten werden.
- Bei Dysarthrie sollte eine sprachtherapeutische Therapie angeboten werden.
- Bei Dysphagie soll eine Schluckrehabilitation angeboten werden.
Wahrnehmungsstörungen
- Spezifisches übendes Training zur Verbesserung der Raumkognition unter Einbezug von Alltagsanforderungen kann empfohlen werden.
- Bei Gesichtsfelddefiziten kann Kompensationstraining angeboten werden.
- Eine vernachlässigten Raumhälfte (Neglect) sollte exploriert und Funktionstraining angeboten werden.
- Maßnahmen zur Verbesserung der Sensibilität sollten angeboten werden (z. B. sensorische Stimulation, sensomotorisches Training, u. a.).
Schmerzen
- Physiotherapeutische Maßnahmen zur Schmerzreduktion sollen angeboten werden.
- Bei chronischen Schmerzen sollte interdisziplinäre Behandlung (ärztlich, physio-ergo-, psychotherapeutisch, pflegerisch) angeboten werden.
- Bei leichter bis mäßiger Schwäche eines Armes oder einer Hand kann die Spiegeltherapie ergänzend zur Verbesserung der Armfunktion eingesetzt werden.
- Schlaganfall-Patient*innen mit neuropathischem Schmerz sollte initial Amitriptylin, Duloxetin, Gabapentin oder Pregabalin angeboten werden.
- Bei ungenügender Schmerzreduktion sollte auf ein anderes Schmerzmedikament der Basisempfehlung zurückgegriffen werden.
- Die Patient*innen sollten zu Bewegung, Haltungsänderungen und optimierten Bewegungs- und Lagerungspositionen angeleitet werden.
- Optionen bei Schulterschmerzen nach Schlaganfall oder bei regionalen Schmerzsyndromen
- Behandlung mit Schienen oder Orthesen, Tape-Behandlung, Lagerungsbehandlung, elektrische Stimulation, Injektion von Botulinumtoxin oder Lokalanästhetikum, orales NSAR oder Kortikoid
- Schmerzhypersensitivität (Central Post-Strope Pain = CPSP)
- Ein Therapieversuch kann mit Amitriptylin und Lamotrigin erfolgen.
- Pregabalin, Gabapentin, Carbamazepin oder Phenytoin können als Therapeutika der 2. Wahl berücksichtigt werden.
Kognitive Funktionen
- Bei Aufmerksamkeitsstörungen sollte übendes Funktionstraining auf Basis einer neuropsychologischen Diagnostik angeboten werden, evtl. ergänzt durch andere Maßnahmen wie z. B. kognitiv-verhaltenstherapeutische Methoden, Bewegungstraining, Freizeitaktivitäten.
- Bei Gedächtnisstörungen soll übendes Funktionstraining auf Basis einer neuropsychologischen Diagnostik angeboten werden, bei schweren Gedächtnisstörungen multisensorische Stimulation oder körperliches Training.
- Zur Verbesserung der Problemlösefähigkeit und des Arbeitsgedächtnisses soll übendes Training angeboten werden.
- Kognitive übende Verfahren sollten mit Methoden des Verhaltensmanagements kombiniert werden.
Angst/Depression/affektive Störungen
- Nach Schlaganfall sollte regelmäßig ein Assessment bezüglich Angst und Depression angeboten werden.
- Schlaganfallpatient*innen mit emotionalen Beschwerden (Angst, Depression) können von einer Behandlung mit Antidepressiva profitieren, diese sollen aber nicht routinemäßig angeboten werden.
- Bei Depression oder Angststörung kann eine Psychotherapie angeboten werden.
Harn- und Stuhlinkontinenz
- Alle Patient*innen sollten hinsichtlich Harn- und Stuhlinkontinenz exploriert werden, diagnostische und therapeutisch sollten angeboten werden:
- strukturiertes Inkontinenzassessment (z. B. ICIQ), Ultraschalluntersuchung der Harnwege mit Restharnbestimmung, Urinteststreifen
- Zur Reduktion der Inkontinenzepisoden sollte körperliches Training und ggf. eine Gewichtsreduktion empfohlen werden.
- Optionen bei Dranginkontinenz: Blasen- und Beckenbodentraining, evtl. anticholinergie Therapie (nach Ausschluss Restharn)
- Optionen bei Belastungsinkontinenz: Beckenbodentraining, Duloxetin, Pessartherapie
- Die medikamentöse Therapie einer Stuhlinkontinenz kann mit Loperamid (und bei Unverträglichkeit mit Codeinphosphat) durchgeführt werden.
Sexualität
- Liegen Störungen der sexuellen Funktionsfähigkeit vor, sollten Hausärzt*innen eine Beratung und eine Abklärung möglicher Ursachen anbieten.
Eingeschränkte Selbstversorgung
- Im häuslichen Umfeld lebenden Patient*innen mit Einschränkungen der persönlichen und instrumentellen Aktivitäten des täglichen Lebens soll ergotherapeutisches Alltagstraining angeboten werden.
Soziale Teilhabe
- Patient*innen und Angehörige sollen informiert werden über: finanzielle Hilfen und sozialstaatliche Leistungen (inkl. Unterstützung bei Anträgen), psychosoziale und sozialrechtliche Beratungsangebote, Selbsthilfegruppen.
Verlauf, Komplikationen und Prognose
Komplikationen
- Zu Komplikationen und ihrer Behandlung siehe Artikel Rehabilitation nach einem Schlaganfall.
Verlauf und Prognose
- Das Risiko, an einem Schlaganfall zu versterben, hat sich in Deutschland nahezu halbiert, die Überlebensraten betragen:38
- 93 % nach 30 Tagen
- 75–93 % nach 1 Jahr
- 55 % nach 5 Jahren.
- Bei hämorrhagischen Schlaganfällen ist die Prognose schlechter als bei ischämischen.38
- Bei den ischämischen Schlaganfällen haben die kardioembolisch bedingten die schlechteste Prognose.39
- 35 % der Betroffenen sind in den ersten Monaten auf pflegerische Versorgung angewiesen.38
- 40–50 % der Patient*innen weisen chronische mittelschwere (z. B. gehfähig, aber Hilfe im Alltag nötig) bis schwere Behinderungen auf.38,40
- Prädiktoren für ein gutes Behandlungsergebnis sind:38,40
- Aufnahme in Stroke Unit
- kurze Zeit zwischen Symptom- und Behandlungsbeginn
- junges Alter
- kleine Infarktgröße
- guter Zustand früh nach dem Schlaganfall (Sprachfähigkeiten, Kraft in den Armen, Gehfähigkeit)
- Therapieadhärenz
- Selbständigkeit vor dem Schlaganfall
- Berufstätigkeit
- Hilfe durch Familienangehörige.
- Nicht zu unterschätzende Bedeutung hat die Motivation: Je aktiver Patient*innen mitwirken und sich anstrengen, umso größer sind die Fortschritte.40
Verlaufskontrolle
- In der deutschen Regelversorgung gibt es bislang keine einheitlich geregelte flächendeckende Schlaganfallnachsorge.41
- Bestandteile der Nachsorge sind:
- Beurteilung des neurologischen, neuropsychologischen und psychischen Verlaufs
- Kontrolle der Risikofaktoren
- Anpassung der nichtmedikamentösen (Lebensstil) und medikamentösen Therapie, Beurteilung der Therapieadhärenz
- Erfassung des Bedarfs an Heil- und Hilfsmitteln, Rehabilitation, Pflege und ggf. entsprechende Unterstützung.
Fahreignung
- Empfehlenswert ist die Überprüfung der Fahreignung schon in der betreuenden Rehabilitationseinrichtung im Rahmen einer eingehenden neuropsychologischen Evaluation mit Dokumentation darüber im Entlassungsbrief.1
- Bei Zweifelsfällen im weiteren Verlauf ist eine Fahrverhaltensprobe durch Neuropsycholog*in sinnvoll (Beurteilung der emotionalen Kontrollfähigkeit, Einsichtsfähigkeit und krankheitsbedingter Persönlichkeitsveränderungen).1
- Einschränkungen oder Verluste von Extremitätenfunktionen infolge einer Störung des zentralen oder peripheren Nervensystems erfordern eine neurologische/verkehrsmedizinische Begutachtung.1
- Siehe auch Artikel Beurteilung der Fahreignung.
Patienteninformationen
Patienteninformationen in Deximed
Patienteninformationen der DEGAM
Weitere Informationen
- Siehe Artikel Beurteilung der Fahreignung.
Video
-
Hemichorea nach Schlaganfall im Bereich der Stammganglien (mit freundlicher Genehmigung von Herrn Dr. Dagge)
Illustrationen
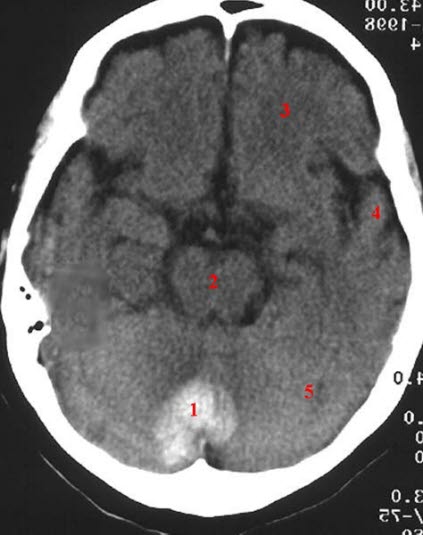
Hämatom im Zerebellum, CT
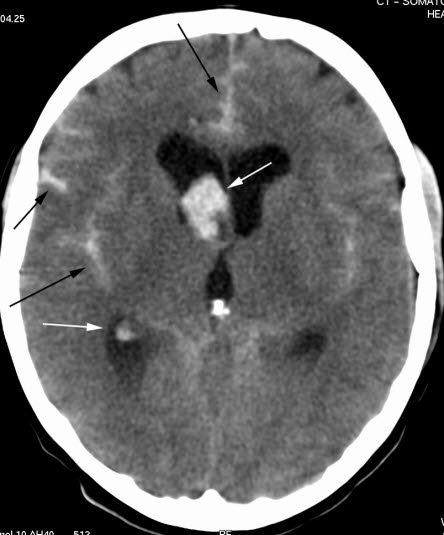
Subarachnoidalblutung (CT)
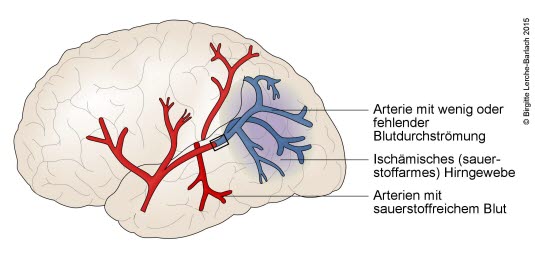
Schlaganfall
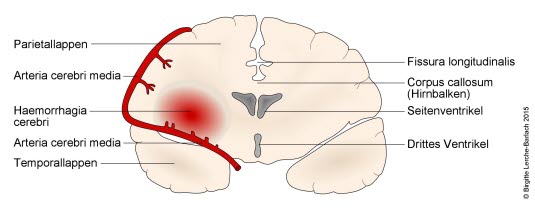
Hirnblutung
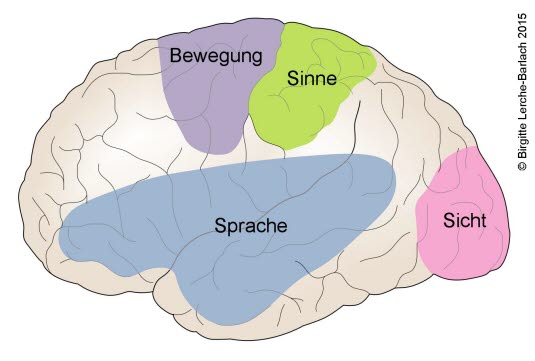
Anatomie des Gehirns, funktionell
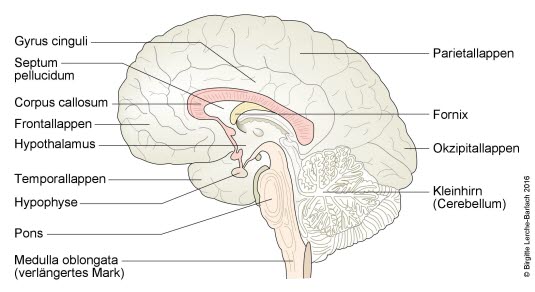
Anatomie des Gehirns, medialer Längsschnitt
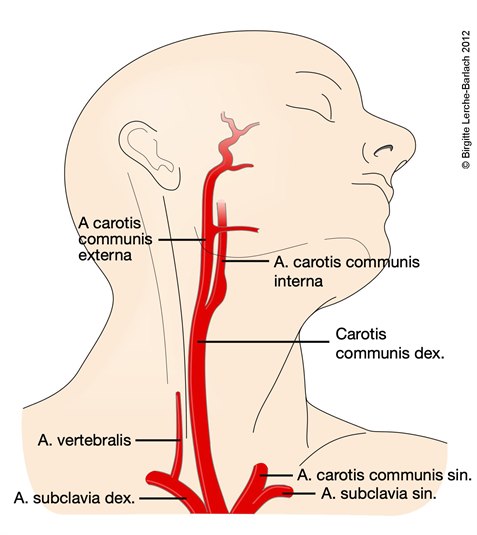
Arterie carotis und vertebralis
Quellen
Leitlinien
- Deutsche Gesellschaft für Allgemeinmedizin und Familienmedizin. Schlaganfall. AWMF-Leitlinie Nr. 053-011. S3, Stand 2020. www.awmf.org
- Deutsche Gesellschaft für Allgemeinmedizin und Familienmedizin. Hausärztliche Risikoberatung zur kardiovaskulären Prävention. AWMF-Leitlinie 053-024. S3, Stand 2016. www.degam.de
- Deutsche Gesellschaft für Allgemeinmedizin und Familienmedizin: Neue Thrombozyten-Aggregationshemmer, Einsatz in der Hausarztpraxis. AWMF-Leitlinie Nr. 053-041. S2e, Stand 2019. www.awmf.org
- Deutsche Gesellschaft für Neurologie, Deutsche Schlaganfall-Gesellschaft. Akuttherapie des ischämischen Hirninfarktes. AWMF-Leitlinie Nr. 030-046. S2e, Stand 2021. www.awmf.org
- Deutsche Gesellschaft für Neurologie, Deutsche Schlaganfall-Gesellschaft. Sekundärprophylaxe ischämischer Schlaganfall und transitorische ischämische Attacke – Teil 1: Plättchenhemmer, Vorhofflimmern, Hypercholesterinämie und Hypertonie. AWMF-Leitlinie Nr. 030-133. S2k, Stand 2022. www.awmf.org
- Deutsche Gesellschaft für Neurologie, Deutsche Schlaganfall-Gesellschaft. Sekundärprophylaxe ischämischer Schlaganfall und transitorische ischämische Attacke – Teil 2: Lebensstil, arterielle Stenosen, andere Antithrombotika-Indikationen, Hormone, Diabetes mellitus, Schlafapnoe. AWMF-Leitlinie Nr. 030-143. S2k, Stand 2022. www.awmf.org
Literatur
- Deutsche Gesellschaft für Allgemeinmedizin und Familienmedizin. Schlaganfall. AWMF-Leitlinie Nr. 053-011, Stand 2020. www.awmf.org
- Busch M, Schienkiewitz A, Nowossadeck E, et al. Prävalenz des Schlaganfalls bei Erwachsenen im Alter von 40 bis 79 Jahren in Deutschland. Bundesgesundheitsbl 2013; 56: 656-660. doi:10.1007/s00103-012-1659-0 DOI
- Stahmeyer J, Stubenrauch S, Geyer S, et al. Häufigkeit und Zeitpunkt von Rezidiven nach inzidentem Schlaganfall. Dtsch Arztebl Int 2019; 116: 711-717. www.aerzteblatt.de
- Robert Koch-Institut (Hrsg). Gesundheit in Deutschland 2015. Gesundheitsberichterstattung des Bundes. Gemeinsam getragen von RKI und Destatis. www.rki.de
- Groß N, Erbguth F. Könnte es ein Schlaganfall sein? CME 2017; 14: 9-23. doi:10.1007/s11298-017-5978-1 DOI
- Kolominsky-Rabas PL, Heuschmann PU, Marschall D et al. Lifetime cost of ischemic stroke in Germany: results and national projections from a population-based stroke registry: the Erlangen Stroke Project. Stroke 2006; 37: 1179-83. www.ncbi.nlm.nih.gov
- Luengo-Fernandez R, Violato M, Candio P, et al. Economic burden of stroke across Europe: A population-based cost analysis. Eur Stroke J 2020; 5: 17-25. doi:10.1177/2396987319883160 DOI
- Diener HC, Grond M. Embolic Stroke of Undetermined Source. Cardiovasc 2018; 18: 38-40. doi:10.1007/s15027-018-1405-0 DOI
- Böttger P, Grond M, Lemm H, et al. 10 Kernaussagen zum Embolic Stroke of Undetermined Source und kryptogenen Schlaganfall. Med Klin Intensivmed Notfmed 2018; 113: 664–671. www.springermedizin.de
- Adams H Jr, Bendixen B, Kappelle L, et al. Classification of subtype of acute ischemic stroke. Definitions for use in a multicenter clinical trial. TOAST. Trial of Org 10172 in Acute Stroke Treatment. Stroke 1993;24:35-41. pubmed.ncbi.nlm.nih.gov
- Küpper C, Heinrich J, Müler K, et al. Der akute Schlaganfall. MMW - Fortschritte der Medizin 2019; 51: 22-28. doi:10.1007/s15006-019-0008-8 DOI
- Berlit P. Schlaganfall: Differenzialdiagnostische Übersicht. eMedpedia. Zugriff 17.07.22. www.springermedizin.de
- Hossmann K. Pathophysiological basis of translational stroke research. Folia Neuropathol 2009; 47: 213-227. www.termedia.pl
- Heiss W. The Pathophysiology of Ischemic Stroke Studied by Radionuclide Imaging. J Neurol Neuromedicine 2016; 1: 22-28. www.jneurology.com
- Kuriakose D, Xiao Z. Pathophysiology and Treatment of Stroke: Present Status and Future Perspectives. Int J Mol Sci 2020; 21: 7609. doi:10.3390/ijms21207609 DOI
- Easton J, Albers G, Caplan L, et al. Discussion: Reconsideration of TIA terminology and definitions. Neurology. 2004; 62: 29-34. pubmed.ncbi.nlm.nih.gov
- Deutsche Gesellschaft für Neurologie, Deutsche Schlaganfall-Gesellschaft. Akuttherapie des ischämischen Hirninfarktes. AWMF-Leitlinie Nr. 030-046. Stand 2021. www.awmf.org
- Gudmundsson L, Scher A, Aspelund T et al. Migraine with aura and risk of cardiovascular and all cause mortality in men and women: prospective cohort study. BMJ 2010;341:c3966. www.bmj.com
- Boehme A, Esenwa C, Elkind M. Stroke Risk Factors, Genetics, and Prevention. Circ Res 2017; 120: 472-495. doi:10.1161/CIRCRESAHA.116.308398 DOI
- O'Donnell MJ, Xavier D, Liu L, et al. Risk factors for ischaemic and intracerebral haemorrhagic stroke in 22 countries (the INTERSTROKE study): a case control study. Lancet 2010; 376: 112-23. pubmed.ncbi.nlm.nih.gov
- Lakatos L, Christ M, Müller M, et al. „Stroke mimics“ – Differenzialdiagnose des Schlaganfalls in der Notfallmedizin. Notfall Rettungsmed 2021; 24: 990–996. doi:10.1007/s10049-021-00877-x DOI
- Schuler L, Bolognese M, Lakatos L. Strukturierte Erkennung von Patienten mit Schlaganfall in der Notfallsituation. Notfall Rettungsmed 2021; 24: 984-989. doi:10.1007/s10049-021-00916-7 DOI
- Kraft P, Nasri S, Dreikorn M. Diagnostik und Akuttherapie des ischämischen Schlaganfalls. DNP - Die Neurologie und Psychiatrie 2019; 20: 28-32. doi:10.1007/s15202-019-2118-7 DOI
- Stroke Unit Trialists' Collaboration. Organised inpatient (stroke unit) care for stroke. Cochrane Database Syst Rev. 2013 Sep 11;9:CD000197. pubmed.ncbi.nlm.nih.gov
- Berkhemer OA, Fransen PSS, van den Berg LA, et al. A randomized trial of intraarterial treatment for acute ischemic stroke. N Engl J Med 2014. doi:10.1056/NEJMoa1411587 DOI
- Goyal M, Demchuk AM, Menon BK, et al for the ESCAPE Trial Investigators. Randomized assessment of rapid endovascular treatment of ischemic stroke. N Engl J Med 2015. doi:10.1056/NEJMoa1414905 DOI
- Campbell BCV, MitchellPJ, Kleinig TJ, et al for the EXTEND-IA Investigators. Endovascular therapy for ischemic stroke with perfusion-imaging selection. N Engl J Med 2015. doi:10.1056/NEJMoa1414792 DOI
- Jovin TG, Chamorro A, Cobo E, et al. Thrombectomy within 8 Hours after Symptom Onset in Ischemic Stroke. N Engl J Med 2015. doi:DOI: 10.1056/NEJMoa1503780 DOI
- Deutsche Gesellschaft für Neurologie, Deutsche Schlaganfall-Gesellschaft. Sekundärprophylaxe ischämischer Schlaganfall und transitorische ischämische Attacke – Teil 1: Plättchenhemmer, Vorhofflimmern, Hypercholesterinämie und Hypertonie. AWMF-Leitlinie Nr. 030-133. Stand 2022. dgn.org
- Deutsche Gesellschaft für Allgemeinmedizin und Familienmedizin: Neue Thrombozyten-Aggregationshemmer. Einsatz in der Hausarztpraxis. DEGAM-Leitlinie. AWMF-Leitlinie Nr. 053-041. S2e. Stand 2019 www.awmf.org
- Ge F, Lin H, Liu Y et al. Dual antiplatelet therapy after stroke or transient ischaemic attack – how long to treat? The duration of aspirin plus clopidogrel in stroke or transient ischaemic attack: a systematic review and meta-analysis Eur J Neurol. 2016;23:1051-7. pubmed.ncbi.nlm.nih.gov
- Johnston C, Amarenco P, Albers G et al for the SOCRATES Steering Committee and Investigators. Ticagrelor versus Aspirin in acute stroke or transient ischemic attack. N Engl J Med 2016;375:35-43. www.nejm.org
- Johnston C, Amarenco P, Denison H, et al. for the THALES Investigators. Ticagrelor and aspirin or aspirin alone in acute ischemic stroke or TIA. N Engl J Med 2020;383:207-17. www.nejm.org
- Amarenco P, Bogousslawsky J, Callahan A, et al. The Stroke Prevention by Aggressive Reduction in Cholesterol Levels (SPARCL) Investigators. N Engl J Med 2006;549:59. www.nejm.org
- Furberg C, Wright J, Davis B et al for the ALLHAT officers. Major outcomes in high-risk hypertensive patients randomized to angiotensin-converting enzyme inhibitor or calcium channel blocker vs diuretic. JAMA 2002;288:2981-97. pubmed.ncbi.nlm.nih.gov
- Deutsche Gesellschaft für Allgemeinmedizin (DEGAM). Leitlinie: Hausärztliche Risikoberatung zur kardiovaskulären Prävention. S3, Stand 2017 www.awmf.org
- Deutsche Gesellschaft für Neurologie, Deutsche Schlaganfall-Gesellschaft. Sekundärprophylaxe ischämischer Schlaganfall und transitorische ischämische Attacke – Teil 2: Lebensstil, arterielle Stenosen, andere Antithrombotika-Indikationen, Hormone, Diabetes mellitus, Schlafapnoe. AWMF-Leitlinie Nr. 030-143. Stand 2022. dgn.org
- Siegmar N, von Büdigen H. Lebenserwartung und Prognose nach einem Schlaganfall. Schlaganfall Begleitung, Zugriff 01.08.22. schlaganfallbegleitung.de
- Jauch E. Ischemic stroke. Medscape, updated Jul 14, 2022. Zugriff 01.08.22 emedicine.medscape.com
- Prognose und Verlauf bei Schlaganfall. Neurologen und Psychiater im Netz. Zugriff 01.08.22. www.neurologen-und-psychiater-im-netz.org
- Kunz J, von Büdigen H. Schlaganfall-Nachsorge. Zugriff 01.08.22. schlaganfallbegleitung.de
Autor*innen
- Michael Handke, Prof. Dr. med., Facharzt für Innere Medizin, Kardiologie und Intensivmedizin, Freiburg i. Br.
- Günther Egidi, Dr. med., Arzt für Allgemeinmedizin, Bremen (Review)
- Die ursprüngliche Version dieses Artikels basiert auf einem entsprechenden Artikel im norwegischen hausärztlichen Online-Handbuch Norsk Elektronisk Legehåndbok (NEL, https://legehandboka.no/).
Link lists
Relevante Artikel
Leitlinien
- DEGAM-Leitlinie Schlaganfall
- AWMF-Leitlinie Akuttherapie des ischämischen Horninfarktes
- DEGAM-Leitlinie Hausärztliche Risikoberatung zur kardiovaskulären Prävention
- DEGAM-Leitlinie Neue Thrombozyten-Aggregationshemmer, Einsatz in der Hausarztpraxis
- AWMF-Leitlinie Sekundärprophylaxe ischämischer Schlaganfall und transitorische ischämische Attacke – Teil 1: Plättchenhemmer, Vorhofflimmern, Hypercholesterinämie und Hypertonie
- AWMF-Leitlinie Sekundärprophylaxe ischämischer Schlaganfall und transitorische ischämische Attacke – Teil 2: Lebensstil, arterielle Stenosen, andere Antithrombotika-Indikationen, Hormone, Diabetes mellitus, Schlafapnoe