Zusammenfassung
- Definition:Anisakiasis ist eine zoonotische Spulwurminfektion, verursacht durch die Darmparasiten Anisakis simplex, Anisakis physeteris, Anisakis pegreffii oder die Pseudoterranova-Spezies.
- Häufigkeit:Weltweites Vorkommen, vor allem aber in Regionen, in denen häufig roher Fisch verzehrt wird.
- Symptome:Symtome können akut oder chronisch auftreten. Akut: Bauchschmerzen, Übelkeit, Erbrechen, Diarrhö sowie allergische Reaktionen. Chronisch: anhaltende abdominelle Beschwerden und Gewichtsverlust.
- Befunde:Keine spezifischen klinischen Befunde. Evtl. Auftreten von mildem Fieber und/oder Nachweis einer Leukozytose.
- Diagnostik:Die Diagnostik stützt sich auf die Anamnese und kann ggf. über eine Gastroskopie gesichert werden.
- Therapie:Derzeit ist keine spezifische antiparasitäre Medikation verfügbar. Ggf. können die Larven/Würmer endoskopisch entfernt werden.
Allgemeine Informationen
Definition
- Anisakiasis ist eine parasitäre Erkrankung, verursacht durch eine Infektion mit Larven von Würmern des Anisakis-Komplexes (Anisakis simplex, Anisakis physeteris, Anisakis pegreffii) oder der Pseudoterranova-Spezies.
- Die Erkrankung wird auch Heringswurmkrankheit, die Parasiten werden auch „Sushi-Würmer“ genannt.
- Infektionen des Menschen können durch den Verzehr von larvenhaltigen Meeresfischen (z. B. Hering oder Makrele), die ungenügend erhitzt,
nur schwach mariniert oder ungenügend geräuchert sind, zustande kommen.1 - Klinisch manifestiert sich die Erkrankung vor allem im Gastrointestinaltrakt und durch allergische Reaktionen.
Häufigkeit
- Seefische sind weltweit häufig von Anisakis befallen (Heringe bis zu 70 %).1
- Infektionen des Menschen treten besonders in Ländern auf, in denen
Fisch häufig roh genossen wird (z. B. in Japan, Holland).1 - Erkrankungsfälle werden in Deutschland nur selten beobachtet, mit
der Zunahme des Verzehrs von Sushi könnten sie häufiger werden.1 - Fallberichte aus Europa nehmen zu, vor allem aus Italien und Spanien.2-5
- Die weltweite Prävalenz wird wahrscheinlich aufgrund der eingeschränkten diagnostischen Möglichkeiten und der unspezifischen klinischen Manifestation unterschätzt.
- Die geschätzte Inzidenz liegt in der europäischen Union liegt bei 0.32/100,000.3
Ätiologie und Pathogenese
- Die Erreger von Anisakiasis sind Fadenwürmer der Gattung Anisakis, vor allem Anisakis simplex oder der Pseudoterranova-Spezies.
- Anisakis simplex gehört mit mehreren humanpathogenen Spezies zu den Nematoden und ist ein Darmparasit bei fischfressenden Meeressäugern (Delphinen, Robben u. a.). Kleinkrebse sind erste Zwischenwirte, Fische zweite und dritte Zwischenwirte.1
- Infizierte Meeressäuger (z. B. Wale, Delphine, Robben, Seelöwen) scheiden die Eier mit dem Kot aus, und diese werden im Wasser zu infektiösen Larven.
- Diese Larven werden von Krustentieren aufgenommen, die wiederum von Fischen gefressen werden.
- Der Mensch nimmt die Larven durch den Verzehr von unzureichend erhitztem Fisch auf.
- Lachs, Hering, Kabeljau, Makrele und Tintenfisch übertragen die Anisakis-Spezies; Heilbutt, Kabeljau und der rote Schnapper übertragen die Pseudoterranova-Spezies.
- Die Larven nisten sich in der Mukosa des Magen-Darm-Traktes ein, beginnen mit der Reifung, sterben aber nach einiger Zeit ab, da der Mensch nicht der natürliche Wirt ist.
- Der absterbende Organismus induziert eine Entzündungsreaktion im Ösophagus, Magen oder Darm.
- In manchen Fällen penetriert die Larve die Darmwand und bildet einen Abszess in der Peritonealhöhle.
- Eine Übertragung von Mensch-zu-Mensch findet nicht statt.6
Prädisponierende Faktoren
- Verzehr von rohem Fisch, der nicht tiefgefroren war, oder von unzureichend erhitztem Fisch.
ICPC-2
- D73 Gastroenteritis vermutlich infektiös
ICD-10
- B81.0 Anisakiasis
Diagnostik
Diagnostische Kriterien
- Klinische Symptome nach Verzehr von rohem Fisch
- Endoskopischer Nachweis
- Anisakis-spezifische Antikörper sind ein hilfreiches Instrument bei der Diagnose, aber nicht flächendeckend verfügbar.7
Differenzialdiagnosen
- Akute Lebensmittelvergiftung
- Virale Gastroenteritis
- Andere parasitäre oder bakterielle Darminfektionen
- Gastraler Ulkus
- Colitis ulcerosa
- Morbus Crohn
- Divertikulitis
- Appendizitis
- Darmischämie
- Gastrointestinaler Tumor
- Intussuszeption
Anamnese
- Verzehr von rohem oder ungenügend erhitztem Fisch
- Evtl. Auftreten von mildem Fieber
- In bis zu 40 % der Fälle kommt es zu einer allergischen Reaktion.4,8
- Unmittelbar nach dem Verzehr kann es zu Juckreiz und einem Kribbelgefühl im Oropharynx kommen.
- Weitere allergische Symptome wie Urtikaria, Angioödem oder selten eine anaphylaktische Reaktion können auftreten.
- Gastrointestinale Symptome
- Häufig ist die gastrale Form der Anisakiasis, bei der es in der Regel nach 1–8 Stunden zu Bauchschmerzen, Übelkeit und Erbrechen kommt.7,9-10
- Bei der selteneren intestinalen Form kommt es 5–7 Tage nach dem Verzehr zu starken Bauchschmerzen mit ggf. blutiger Diarrhö. Das klinische Bild kann einer Appendizitis, Ileitis oder Divertikulitis ähneln.7
Klinische Untersuchung
- Keine spezifischen Befunde
- Evtl. mildes Fieber
- Evtl. allergische Symptome (Urtikaria)
- Bei der intestinalen Form ggf. Peritonismus
Ergänzende Untersuchungen in der Hausarztpraxis
- Evtl. Nachweis einer Leukozytose/Eosinophilie
Diagnostik bei Spezialist*innen
- Eine spezifische Serodiagnostik ist nur in Speziallaboratorien verfügbar.
- Beratung in Fragen der Diagnostik z. B. durch das Bernhard-Nocht-Institut für Tropenmedizin
- Durch eine Gastroskopie kann der Parasit ggf. nachgewiesen werden und die Diagnose histopathologisch gesichert werden.
- Bei Dünndarmbefall kann mittels Computertomografie möglicherweise eine ödematöse Darmwand, Aszites und Phlegmone des mesenterischen Fettgewebes nachgewiesen werden.11
Indikationen zur Überweisung
- Bei Verdacht auf eine Infektion werden die Patient*innen zur weiteren Diagnostik und Therapie an eine gastroenterologische Praxis überwiesen, in der eine Gastroskopie durchgeführt werden kann.
- Bei Verdacht auf Anisakiasis und anhaltenden Beschwerden zur Sanierung von Infektionsherden im Bauchraum
Therapie
Therapieziele
- Entfernung der Larven/der Parasiten – die Erkrankung wird dadurch geheilt.
- Da die endoskopische Entfernung des Parasiten nach Passage in den Darmtrakt schwierig ist, sollte bei Verdacht auf Anisakiasis frühzeitig eine Überweisung zur Gastroskopie stattfinden.
Allgemeines zur Therapie
- Derzei gibt es keine nachgewiesen wirksame medikamentöse Therapie.
- Die Entfernung des Parasiten (durch Regurgitation, Endoskopie oder Operation) ist kurativ.
- Wenn sich der Parasit im distalen Magen-Darm-Trakt befindet und endoskopisch nicht entfernt werden kann, ist eine symptomatische Therapie meist ausreichend, da der Parasit nur wenige Tage im Darmtrakt überlebt.
- Eine Operation kann notwendig werden, wenn der Parasit in die Darmwand oder in den Bauchraum penetriert ist.
Medikamentöse Therapie
- Derzeit gibt es keine nachgewiesen wirksame medikamentöse Therapie.
- Es wird von erfolgreichen Behandlungen mit Albendazol berichtet, eine ausreichend gute Datenlage fehlt jedoch.12-14
Weitere Therapien
- Gastroskopie
- Die Larven können durch eine Gastroskopie nachgewiesen und mit einer Zange entfernt werden.
- Operative Therapie
- Eine operative Therapie kann bei Auftreten von Granulomen oder Abszessen im Abdomen, bei Peritonitis oder Darmobstruktion notwendig werden.
Prävention
- Krebse oder Meeresfische sollten nur nach ausreichendem vorherigem Erhitzen oder sicherem Konservieren (Marinieren, Räuchern) verzehrt werden.
- Die Larven sterben bei Temperaturen von über 60 °C oder unter –20 °C sowie auch in Salzlake ab.1
- Roher Fisch (z. B. für Sushi) sollte vor dem Verzehr laut FDA wie folgt gelagert worden sein:6
- bei –20 °C oder unterhalb für 7 Tage – oder –
- bei –35 °C oder darunter, bis gefroren, dann bei –35 °C oder darunter für 15 Stunden – oder –
- bei –35 °C oder darunter, bis gefroren, dann bei –20 °C oder darunter für 24 h.
- Beim Kochen oder Braten von Fisch auf ausreichende Temperaturen achten: Kerntemperatur im Fisch mindesten 63 °C.6
Meldepflicht
- Keine krankheits- oder erregerspezifische Meldepflicht nach dem IfSG1
Verlauf, Komplikationen und Prognose
Verlauf
- Allergische Symptome treten üblicherweise unmittelbar nach dem Verzehr von larvenhaltigem Fisch auf.
- Gastrale Symptome entwickeln sich nach einer Inkubationszeit von 1–8 Stunden.
- Nach endoskopischer Entfernung des Parasiten klingen die Beschwerden in der Regel ab.
- Intestinale Anisakiasis tritt nach 5-7 Tagen auf.
- Verdauungsbeschwerden können auch nach dem Absterben der Larven
fortbestehen. - Eine Infektion mit Anisakis simplex wird als mögliche Ursache für rezidivierende akute spontane Urtikaria in Gebieten der Welt diskutiert, in denen häufig ungekochter Fisch gegessen wird.15
Komplikationen
- Chronische Darmentzündung
- Chronische Bauchschmerzen
- Abszess
- Eosinophile Granulome
- Peritonitis
- Ileus
- Darmdurchbruch
Prognose
- Gastrale Anasakiasis: Symptome sistieren meist prompt nach Entfernung des Parasiten.
- Intestinale Anasakiasis: Abheilung meist unter symptomatischer Therapie durch Absterben des Parasiten im Darmtrakt. Jedoch besteht, durch die Induktion eines Entzündungsprozesses, die Gefahr von Komplikationen (s. o.).
- Verdauungsbeschwerden können nach Absterben des Parasiten fortbestehen.
Patienteninformationen
Worüber sollten Sie die Patient*innen informieren?
- Vorbeugung einer Infektion mit Anisakis: Fisch vor dem Verzehr kochen oder braten. Verzehr von rohem Fisch vermeiden, der nicht tiefgefroren war. Auch Räuchern oder das Einlegen in Salzlake tötet die Parasiten ab.
Patienteninformationen in Deximed
Illustrationen
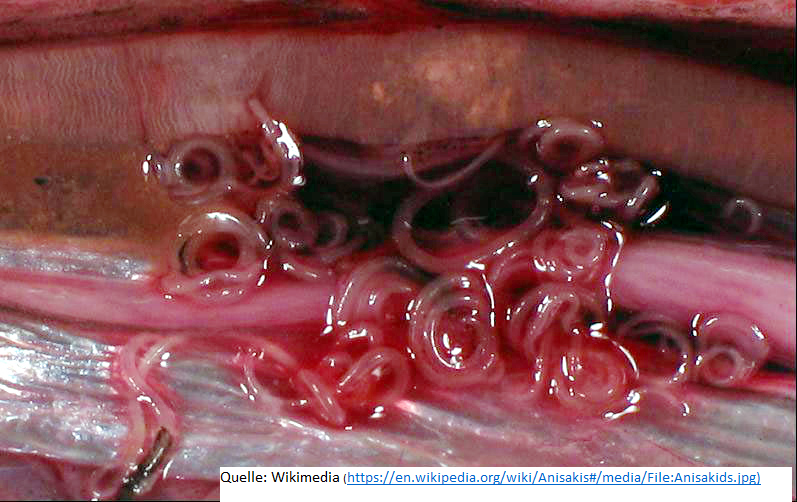
Anisakis-Larven im Körper eines Herings (Quelle: Wikipedia)
Quellen
Literatur
- Robert Koch-Institut. Steckbriefe seltener und importierter Infektionskrankheiten, Seite 115. Stand 2011. Zugriff 10.11.2022 edoc.rki.de
- Carmo J, et al. Anisakiasis: a growing cause of abdominal pain! BMJ Case Rep 2017. casereports.bmj.com
- Uña-Gorospe M, et al. Occupational disease due to Anisakis simplex in fish handlers. Int Marit Health . 2018;69(4):264-269. pubmed.ncbi.nlm.nih.gov
- Cavallero S, et al. Anisakiasis in Italy: Analysis of hospital discharge records in the years 2005-2015. PLoS One . 2018 Dec 11;13(12):e0208772. pubmed.ncbi.nlm.nih.gov
- Guardone L, et al. Human anisakiasis in Italy: a retrospective epidemiological study over two decades. Parasite . 2018;25:41. www.ncbi.nlm.nih.gov
- CDC. Centers for Disease Control and Prevention. Parasites - Anisakiasis. Zugriff 10.11.2022. www.cdc.gov
- Shimamura Y, et al. Common Symptoms from an Uncommon Infection: Gastrointestinal Anisakiasis. Can J Gastroenterol Hepatol. 2016; 2016: 5176502. www.ncbi.nlm.nih.gov
- Daschner A, et al. Gastric anisakiasis: an underestimated cause of acute urticaria and angio-oedema?, Br J Dermatol. 1998;139(5):822. pubmed.ncbi.nlm.nih.gov
- Bucci C, et al. Anisakis, just think about it in an emergency! Int J Infect Dis. 2013 Nov;17(11):e1071-2. www.ijidonline.com
- Repiso Ortega A, et al. Gastrointestinal anisakiasis. Study of a series of 25 patients. Gastroenterol Hepatol. 2003 Jun-Jul;26(6):341-6. pubmed.ncbi.nlm.nih.gov
- Takabayashi T, et al. Anisakiasis presenting to the ED: clinical manifestations, time course, hematologic tests, computed tomographic findings, and treatment., Am J Emerg Med 2014; 32: 1485-9. pmid:25440233 pubmed.ncbi.nlm.nih.gov
- Pacios E, et al. Albendazole for the treatment of anisakiasis ileus., Clin Infect Dis 2005; 41: 1825. pmid:16288416 pubmed.ncbi.nlm.nih.gov
- Moore DA, et al. Treatment of anisakiasis with albendazole., Lancet. 2002;360(9326):54. pubmed.ncbi.nlm.nih.gov
- Carlin AF, et al. Case Report: A Common Source Outbreak of Anisakidosis in the United States and Postexposure Prophylaxis of Family Collaterals., Am J Trop Med Hyg . 2018 Nov;99(5):1219-1221 www.ncbi.nlm.nih.gov
- Deutsche Dermatologische Gesellschaft. Urtikaria, Klassifikation, Diagnostik und Therapie. AWMF-Leitlinie Nr. 013-028. Stand 2022. register.awmf.org
Autor*innen
- Christina Weingartner, Dr. med., Ärztin in Weiterbildung Allgemeinmedizin, München
- Die ursprüngliche Version dieses Artikels basiert auf einem entsprechenden Artikel im norwegischen hausärztlichen Online-Handbuch Norsk Elektronisk Legehåndbok (NEL, https://legehandboka.no/).