Zusammenfassung
- Definition:Histologischer Nachweis einer Entzündung der Magenmukosa.
- Häufigkeit:Keine wirklich zuverlässigen Daten zu Inzidenz und Prävalenz. Lebenszeitprävalenz auf Basis ärztlicher Diagnosen ca. 20 %.
- Symptome:Dyspeptische Beschwerden, häufig asymptomatisch.
- Befunde:Im Allgemeinen kein typischer klinischer Befund, evtl. epigastrischer Druckschmerz, evtl. neurologische Symptome/Blässe bei Vitamin-B12-Mangel bzw. perniziöser Anämie.
- Diagnostik:Endoskopie und Biopsien mit histologischem Nachweis einer Gastritis, ggf. Nachweis einer Helicobacter-pylori-Infektion.
- Therapie:Abhängig von der Ursache: Absetzen von Noxen, symptomatische Therapie mit PPI, H.-pylori-Eradikation, Vitamin-B12-Substitution bei perniziöser Anämie.
Allgemeine Informationen
Definition
- Gastritis ist definiert als histologisch nachgewiesene Entzündung der Magenmukosa.1
Zur Terminologie
- Häufig undifferenzierte Verwendung des Begriffs „Gastritis“ für sowohl klinische Beschwerden (Dyspepsie) als auch endoskopische (makroskopische Läsionen) und histologische Befunde, die nur bedingt miteinander zusammenhängen.2
- Die Diagnose Gastritis kann nur bei histologischem Entzündungsnachweis gestellt werden.1
Klassifikation
- Es existieren verschiedene Klassifikationssysteme mit uneinheitlicher Anwendung.3
Klassifikation nach dem zeitlichen Verlauf
- Akute vs. chronische Gastritis
- Der Zeitraum zur Unterscheidung zwischen akuter und chronischer Gastritis ist nicht genau definiert.4
- Die Begriffe werden häufig als Synonym für selbstlimitierende und nicht-selbstlimitierende Verläufe verwendet.
ABCD-Klassifikation2
Typ-A-Gastritis (Autoimmungastritis)
- Relativ selten, ca. 3–6 % der Gastritiden
- Ausgelöst durch Autoantikörper gegen die Parietal- und Hauptzellen des Magens
- Beschränkt auf den Magencorpus
Typ-B-Gastritis (bakterielle Gastritis, v. a. durch H. pylori)
- Ca. 20–50 % der Gastritiden (in entwickelten Ländern, weltweit Anteil ca. 80–90 %)
- Ganz überwiegend durch Helicobacter-pylori-Infektion verursacht
Typ-C-Gastritis (chemische Gastritis)
- Ca. 30–50 % der Gastritiden, deutliche Zunahme des Anteils in den letzten Jahren
- Vor allem Antrum betroffen
- Typische Ursachen sind Medikamente (NSAR, ASS), Galle- und Duodenalreflux, Genussmittel (Alkohol, Kaffee, Nikotin).
Typ-D-Gastritis (Diverses)
- Seltene Ursachen, u. a.:
- Systemerkrankungen, Autoimmunerkrankungen
- seltene virale, bakterielle oder parasitäre Infektionen
- Gastritiden unbekannter Ursache: granulomatöse, eosinophile und kollagene Gastritritis5-7
Sydney-Klassifikation
- Dimensionen der Sydney-Klassifikation3,8
- Ätiologie (Ursachen bzw. Risikofaktoren)
- Topografie (Ausdehnung und räumliche Anordnung)
- Antrum-, Korpus- oder Pangastritis
- Morphologie (Erscheinungsbild und Eigenschaften)
- Grad der Entzündung, Aktivität, Chronizität
- Atrophie
- Metaplasie
- Vorhandensein und Dichte einer H.-pylori-Besiedelung
- endoskopisch zu erkennende Eigenschaften (z. B. Rötung, Blutung, Erosion)
Häufigkeit
- Keine wirklich zuverlässigen epidemiologischen Daten zu Inzidenz und Prävalenz der Gastritis9
- Prävalenz
- Aus einer Erhebung mit anamnestischen Angaben aus dem Jahr 2009 des RKI ergibt sich eine Lebenszeitprävalenz einer ärztlich diagnostizierten Gastritis von 20,5 % (Frauen 23,3 %, Männer 17,5 %).3
- häufig aber auch asymptomatischer Verlauf
- Alter
- ansteigende Häufigkeit von Gastritiden mit dem Lebensalter3
- Geschlecht
- Frauen sind häufiger betroffen als Männer.3
- Ursache
- In Deutschland ist der überwiegende Teil der Gastritiden H.-pylori-assoziiert oder chemisch induziert.3
Ätiologie
Umweltbedingt
- Übertragbar
- bakteriell: H. pylori (ganz überwiegend), Enterokokkus, Treponema pallidum
- viral: CMV, EBV, Enterovirus
- mykotisch: Candidiasis, Mucormykosis, Actinomyces, Histoplasmosis
- parasitisch: Cryptosporidium, Strongyloides stercoralis, Anisakiasis
- Nicht übertragbar
- chemisch
- endogen: Gallensaft
- exogen: NSAR, ASS, Alkohol, Doxycylin
- physikalisch
- Bestrahlung
- chemisch
Wirtsbezogen
- Immunvermittelt
- autoimmun
- allergisch
- lymphozytisch
- eosinophil
- kollagen
- Graft-versus-Host-Erkrankung
- angeborene Immundefekte
- Assoziiert mit systemischen Erkrankungen
- M. Crohn
- Vaskulitis
- Sarkoidose
- Ischämie
Pathogenese
- Es gibt eine Vielfalt von Prozessen, die durch eine akute oder chronische Entzündungsreaktion und Schädigung der schützenden Magenschleimhaut gekennzeichnet sind.9
- Eine H.-pylori-Infektion führt zu einer starken Entzündungsreaktion mit Verminderung des Mucins und gesteigerter Mukosapermeabilität mit zytotoxischer Wirkung auf die Epithelzellen.
- NSAR und Alkohol vermindern die Durchblutung der Schleimhaut mit Verlust der mukosalen Schutzbarriere.
- Bei autoimmuner Gastritis stimulieren Antiparietalzell-AK ein chronisches mononukleäres und lymphozyäres Infiltrat mit Verlust der Parietal- und Hauptzellen im Korpus.
- Bei atrophischer Gastritis wird die Säurebarriere gegen eine bakterielle Überwucherung geschwächt, in seltenen Fällen können Mukosaschäden (z. B. Ulkus, Magenkarzinom, Fremdkörperingestion) zu einer invasiven bakteriellen Infektion führen.10
Atrophische Gastritis als Vorstufe von Neoplasien
- Gastritiden können histopathologisch in zwei Hauptformen eingeteilt werden:
- nicht-atrophische
- atrophische Formen.
- Diese Einteilung bezieht ihre Bedeutung vor allem aus dem unterschiedlichen Risiko für die Entstehung einer Neoplasie.4,10
- Über 90 % der Malignome des Magens entstehen auf dem Boden einer Atrophie.4
- Die atrophische Gastritis ist definiert als Verlust der Magendrüsen mit oder ohne Metaplasie.10
- Hauptursachen für eine atrophische Gastritis sind:4,10
- H.-pylori-Infektion (verantwortlich für ca. 90 % der Malignome)
- autoimmune Gastritis (siehe hierzu auch Artikel Perniziöse Anämie)
- Vermutlich begünstigt ein „Atrophie-assoziiertes Mikrobiom“ die Malignomentstehung.1
- Geschätztes Risiko durch eine atrophische Gastritis:10
- 0,1–0,3 % pro Jahr für die Entstehung eines Magenkarzinoms
- 0,4–0,7 % pro Jahr für die Entstehung eines neuroendokrinen Tumors (NET).
Disponierende Faktoren
- Disponierende Faktoren für eine Autoimmungastritis9
- nordeuropäische/skandinavische Abstammung
- sonstige Autoimmunerkrankungen
ICPC-2
- D07 Dyspepsie / Verdauungsstörung
- D87 Magenfunktionsstörung
ICD-10
- K29.0 Akute hämorrhagische Gastritis
- K29.1 Sonstige akute Gastritis
- K29.2 Alkoholgastritis
- K29.3 Chronische Oberflächengastritis
- K29.4 Chronische atrophische Gastritis
- K29.5 Chronische Gastritis, nicht näher bezeichnet
- K29.6 Sonstige Gastritis
- K29.9 Gastroduodenitis, nicht näher bezeichnet
Diagnostik
Diagnostische Kriterien
- Diagnosestellung durch histologischen Nachweis einer Entzündung in der Magenmukosa9
Differenzialdiagnosen
- Wichtige Differenzialdiagnosen:9
Anamnese
- Symptome der Gastritis sind unspezifisch und können auch auf andere Erkrankungen hinweisen.11
- Symptome der akuten Gastritis:
- Schmerzen und Druckempfindlichkeit im Oberbauch
- Appetitlosigkeit
- Völlegefühl
- Blähungen
- Übelkeit und Erbrechen
- Aufstoßen.
- Bei der chronischen Gastritis häufig keine oder nur geringe Symptome3
- bei autoimmuner Genese evtl. neben gastrointestinalen auch neurologische (z. B. Parästhesien, Gangstörungen, kognitive Einschränkungen) und hämatologische Symptome (perniziöse Anämie) eines chronischen Vitamin-B12-Mangels9
- Genussmittel
- Medikamente
- NSAR
- Kortikosteroide
- ASS
- SSRI
- Vorerkrankungen
- Ulkuskrankheit, H.-pylori-Infektion
- Autoimmunerkrankungen
- St. n. Operationen im Bereich Magen-Darm, Gallenwegen
- Alarmsymptome12
- Erstmanifestation einer Dyspepsie im Alter > 40 Jahre
- an Intensität zunehmende Symptome
- Störung des Nachtschlafs durch die Symptome
- rezidivierendes Erbrechen, Hämatemesis
- Dysphagie
- Gewichtsverlust
- Fieber
- Teerstuhl, Blut im Stuhl
Klinische Untersuchung
- Es gibt keinen typischen klinischen Befund für eine Gastritis.3
- Epigastrischer Druckschmerz
- Blässe (perniziöse Anämie/Vitamin-B12-Mangel)
- Neurologische Defizite (Vitamin-B12-Mangel/perniziöse Anämie)13
Ergänzende Untersuchungen in der Hausarztpraxis
Labor
- Blutbild (Anämie?), Differenzialblutbild
- bei Verdacht auf perniziöse Anämie, Vitamin-B12-Mangel
- Antikörper gegen Intrinsic Factor
- Vitamin B12
- zur Interpretation der Ergebnisse sowie evtl. Bestimmung weiterer Laborparameter siehe Artikel Perniziöse Anämie, Vitamin-B12-Mangel
- Nichtinvasive Tests auf H.-pylori-Infektion: im Rahmen der hausärztlichen Diagnostik können nichtinvasive Tests auf H. pylori eingesetzt werden.
- Antigen-Stuhltest
- Harnstoff-Atemtest
- zu Details siehe Artikel Helicobacter-pylori-Infektion.
Sonografie Abdomen
- Ausschluss anderer Ursachen epigastrischer Beschwerden
Diagnostik bei Spezialist*innen
Ösophago-Gastro-Duodenoskopie (ÖGD)
- Die ÖGD ermöglicht den histologischen Nachweis einer Gastritis, den Nachweis einer H.-pylori-Infektion sowie die Erfassung von Ulzera und Tumoren.
- Inspektion der Schleimhaut von Ösophagus, Magen, Duodenum
- Biopsien: jeweils 2 Biopsien aus Antrum und Corpus, Biopsie für den Urease-Schnelltest, Duodenalbiopsien12
- Nachweis einer nicht-atrophischen bzw. atrophischen Gastritis
- Das Malignomrisiko einer atrophischen Gastritis kann durch Score-Systeme weiter individualisiert werden.4
- Zu Details des invasiven Nachweises von H. pylori siehe Artikel Helicobacter-pylori-Infektion.
- Eine ÖGD sollte durchgeführt werden bei:
Indikationen zur Überweisung
- Bei klinischem Verdacht zur histologischen Diagnosestellung
- Bei Alarmsymptomen
Therapie
Therapieziele
- Ziele der Behandlung sind:9
- Verminderung der Magenschleimhautentzündung
- Symptombesserung
- Eliminierung der Ursache
Therapie verschiedener Gastritisformen
Typ-A-Gastritis (autoimmune Gastritis)
- Im Vordergrund steht der Ausgleich eines Vitamin-B12-Mangels
- Zu Details siehe die Artikel Vitamin-B12-Mangel und Perniziöse Anämie.
Typ-B-Gastritis (überwiegend H.-pylori-assoziiert)
- Eradikation von H. pylori durch medikamentöse Tripel- oder Quadrupel-Therapie17-18
- Zu Details der Behandlung inkl. Therapieprotokollen siehe Artikel Helicobacter-pylori-Infektion.
Typ-C-Gastritis (v. a. durch Genussmittel, Medikamente)
- Allgemeinmaßnahmen
- wenn möglich, Absetzen/Reduktion von auslösenden Medikamenten, v. a. NSAR, ASS
- Verzicht auf magenschleimhautreizende Genussmittel11
- Alkohol
- Koffein
- Nikotin
- schonende Kost11
- z. B. Tee, Haferschleim und Zwieback
- statt wenige große Mahlzeiten Verteilung der Nahrungsaufnahme auf 5–6 kleinere, gut gekaute Mahlzeiten
- Medikamentöse Therapie
- Sofern Allgemeinmaßnahmen nicht ausreichen, können ergänzend Protonenpumpeninhibitoren (PPI) verabreicht werden.
- Standarddosierungen verschiedener PPI19
- Omeprazol 20 mg
- Pantoprazol 40 mg
Typ-D-Gastritis (Diverses)
- Behandlung der jeweiligen Grunderkrankung/-störung wie:
- Systemerkrankungen (z. B. Sarkoidose, Vaskulitiden)
- seltene virale, bakterielle (phlegmonöse Gastritis) oder parasitäre Infektionen
- biliärer Reflux
- Stressgastritis (intensivmedizinische Patient*innen).
Verlauf, Komplikationen und Prognose
Komplikationen
- Erhöhtes Malignomrisiko bei Patient*innen mit atrophischer Gastritis1,10
- Ulkuskrankheit
- Komplikationen eines Vitamin-B12-Mangels
Verlauf und Prognose
- Verlauf und Prognose werden durch die Grunderkrankungen bestimmt
- Siehe hierzu auch die Artikel:
Verlaufskontrolle
- Das optimale endoskopische Überwachungsintervall für Patient*innen mit atrophischer Gastritis ist nicht genau definiert, individuelle Entscheidung gemeinsam mit den Patient*innen.10
- Bei Patient*innen mit fortgeschrittener atrophischer Gastritis sollte eine endoskopische Kontrolle alle 3 Jahre erwogen werden.10
- Bei H.-pylori-Infektion sollte nach Eradikation immer eine Erfolgskontrolle durchgeführt werden.18
Patienteninformationen
Patienteninformationen in Deximed
Illustrationen
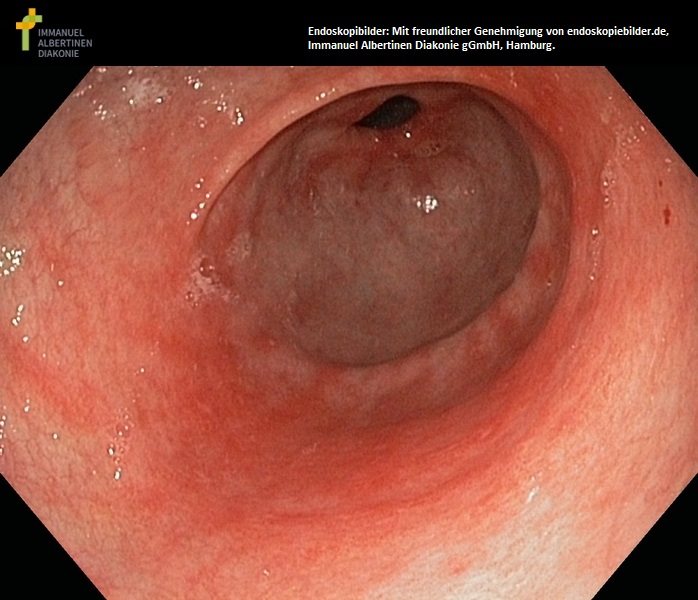
Antrum mit Schleimhautatrophie, atrophische Gastritis (mit freundlicher Genehmigung von endoskopiebilder.de, Immanuel Albertinen Diakonie gGmbH, Hamburg)
Quellen
Leitlinien
- Deutsche Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten. Helicobacter pylori und gastroduodenale Ulkuskrankheit. AWMF-Leitlinie Nr. 021-001. S2k, Stand 2022. www.awmf.org.
Literatur
- Rugge M, Savarino E, Sbaraglia M, et al. Gastritis: The clinico-pathological spectrum. Digestive and Liver Disease 2021; 53: 1-10. pubmed.ncbi.nlm.nih.gov
- Stiefelhagen P. Gastritis: Verschiedene Ursachen, Symptome und Risiken. MMW-Fortschritte der Medizin 2020; 162: 20-22. doi:10.1007/s15006-020-0243-z DOI
- Gastritis, Magen- und Zwölffingerdarmgeschwüre. Gesundheitsberichterstattung des Bundes, Robert Koch-Institut in Zuammenarbeit mit dem Statistischen Bundesamt. Heft 55. September 2013. www.rki.de
- Rugge M, Sugano K, Sacchi D, et al. Gastritis: An Update in 2020. Curr Treat Options Gastro 2020; 18: 488–503. doi:10.1007/s11938-020-00298-8 DOI
- Vieth M, Stolte M. Gastritis aus histologischer Sicht. Internist 2006; 47: 578-587. doi:10.1007/s00108-006-1618-7 DOI
- von Armin U. Neue Nomenklatur für eosinophile gastrointestinale Erkrankungen. GastroNews 2022; 09: 51-53. doi:10.1007/s15036-022-3110-1 DOI
- Försch S, Neurath M. Deutsche Gesellschaft für Innere Medizin (DGIM). Granulomatöse Gastritis. eMedpedia, publiziert am 05.01.15. Zugriff 31.10.22. www.springermedizin.de
- Dixon MF, Genta RM, Yardley JH et al. Classification and grading of gastritis. The updated Sydney System. International Workshop on the Histopathology of Gastritis, Houston 1994. Am J Surg Pathol. 1996;20(10): 1161–1181. www.ncbi.nlm.nih.gov
- BMJ Best Practice. Gastritis. Last reviewed Sep 25, 2022. Zugriff 25.10.2022. bestpractice.bmj.com
- Shah S, Piazuelo M, Kuipers E, et al. AGA Clinical Practice Update on the Diagnosis and Management of Atrophic Gastritis: Expert Review. Gastroenterology 2021; 161: 1325–1332. doi:10.1053/j.gastro.2021.06.078 DOI
- Was ist Gastritis? Internisten im Netz. Letzte Aktualisierung 18.08.17. Zugriff 24.10.22. www.internisten-im-netz.de
- Gottschalk L, Andresen V, Layer P. Reizdarmsyndrom und funktionelle Dyspepsie. Internist 2022; 63: 51-61. doi:10.1007/s00108-021-01218-3 DOI
- Marcus A. Chronic Gastritis. Medscape, updated Jun 07, 2019. Zugriff 30.10.21. emedicine.medscape.com
- Gerste R. Funktionelle Dyspepsie: Bei Infektion mit Helicobacter löst oder bessert Erreger-Eradikation die Symptome. Dtsch Arztebl 2022; 119: A-825. www.aerzteblatt.de
- Madisch A, Andresen V, Enck P, Labenz J, Frierling T, Schemann, M:. Diagnose und Therapie der funktionellen Dyspepsie. Dtsch Arztebl Int 2018; 115: 222-32. doi:DOI: 10.3238/arztebl.2018.0222. www.aerzteblatt.de
- Rabeneck L, Wristers K, Souchek J et al. Impact of upper endoscopy on satisfaction in patients with previously uninvestigated dyspepsia. Gastrointest Endosc 2003; 57: 295-9. pubmed.ncbi.nlm.nih.gov
- Deutsche Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten. Helicobacter pylori und gastroduodenale Ulkuskrankheit. AWMF-Leitlinie Nr. 021-001. S2k, Stand 2022. www.awmf.org
- Fischbach W, Malfertheiner P: Helicobacter pylori infection—when to eradicate, how to diagnose and treat. Dtsch Arztebl Int 2018; 115: 429–36. www.aerzteblatt.de
- Deutsche Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten. Gastroösophageale Refluxkrankheit. AWMF-Leitlinie Nr. 021-013, Stand 2014 (in Überarbeitung). www.awmf.org
Autor
- Michael Handke, Prof. Dr. med., Facharzt für Innere Medizin, Kardiologie und Intensivmedizin, Freiburg i. Br.