Ventrikuläre Rhythmusstörungen und plötzlicher Herztod
Häufigkeit
- Der plötzliche Herztod zählt zu den häufigsten Todesursachen, weltweit verantwortlich für bis zu 50 % aller kardiovaskulär bedingten Todesfälle.1
- 2/3 der Fälle von plötzlichem Herztod beruhen auf Kammerflimmern.1
- In Deutschland ca. 100.000 Fälle/Jahr mit Herzkreislaufstillstand2
- ca. 65–80 % durch ventrikuläre Herzrhythmusstörungen2
- Jährliche Inzidenz des plötzlichen Herztods in Deutschland ca. 80/100.0003
- 34 % der Fälle im Alter < 65 Jahre3
- Das Risiko des plötzlichen Herztods ist bei Männern größer als bei Frauen.
- ca. 75 % der Fälle bei Männern4-5
Ätiologie und Pathogenese
- Zunehmendes Risiko für plötzlichen Herztod mit dem Alter6
- Ursachen bei jüngeren Personen v. a.:
- Ionenkanalerkrankungen
- Kardiomyopathien
- Myokarditis
- Koronaranomalien.
- Ursachen bei älteren Menschen v. a.:
- KHK: akutes Koronarsyndrom, chronisches Koronarsyndrom
- Herzinsuffizienz unterschiedlicher Ätiologie
- Klappenerkrankungen.
- Ursachen bei jüngeren Personen v. a.:
- Häufigste pathophysiologische Kaskade für plötzlichen Herztod7
- ventrikuläre Tachykardien mit Degeneration zu Kammerflimmern und schließlich Asystolie
- Bei 70–80 % der Betroffenen liegt eine koronare Herzkrankheit vor.6,8
- Erstes Ereignis häufig letal, in nur 10–15 % der Fälle eines plötzlichen Herztods sind bereits zuvor Arrhythmien aufgetreten.9
- Die Identifikation der Ursache eines plötzlichen Herztodes ist wichtig für die Beurteilung des Risikos für Angehörige.1
Diagnostik bei V. a. ventrikuläre Arrhythmien bzw. dokumentierten ventrikulären Arrhythmien
- Der Abschnitt basiert auf dieser Referenz.6
- Nichtinvasiv
- 12-Kanal-EKG
- LZ-EKG
- Event-Rekorder oder implantierbarer Loop-Rekorder
- bei sporadischen Symptomen
- Stresstest
- V. a. KHK
- V. a. belastungsabhängige ventrikuläre Tachykardie
- Bildgebung
- transthorakale Echokardiografie bei allen Patient*innen
- Kardio-MRT: In den aktuellen Leitlinien wird der Anwendungsbereich des MRT deutlich ausgeweitet.1
- Genetische Diagnostik: auch die genetische Diagnostik wird in den aktuellen Leitlinien deutlich aufgewertet, auch als Baustein der Risikostratifikation hinsichtlich ICD-Indikation.1
- Provokationstests: z. B. Ajmalin-Test bei Verdacht auf Brugada-Syndrom u. a.
- toxikologisches Screening: v. a. bei jungen Patient*innen nach überlebtem plötzlichem Herztod
- Invasiv
- Koronarangiografie bei V. a. relevante KHK
- elektrophysiologische Untersuchung bei ausgewählten Patient*innen
Prädisponierende Faktoren
- Koronare Herzerkrankung
- Reduzierte systolische LV-Funktion10-12
- Genetische Prädisposition
Indikationen zur ICD-Implantation
- ICD ermöglicht die Terminierung von ventrikulärer Tachykardie und Kammerflimmern und somit Verhinderung des plötzlichen Herztods.13-16
- Durch Schrittmacherfunktion des ICD werden auch bradykarde Rhythmusstörungen behandelt.17
- Sekundärprophylaktische Indikation bei St. n. Kammerflimmern oder hämodynamisch nicht tolerierter ventrikulärer Tachykardie
- Primärprophylaktische Implantation eines ICD führt zu geringerer Mortalität bei Risikopatient*innen.
- Wichtiges Kriterium für ein erhöhtes Risiko ist eine eingeschränkte linksventrikuläre Funktion (EF ≤ 35 %).
- Wenn ein ICD indiziert ist, sollte evaluiert werden, ob die Patient*innen von einer gleichzeitigen CRT (kardiale Resynchronisationstherapie) profitieren könnten (ICD-CRT-System).6
Leitlinie: Indikationen zur ICD-Therapie6
Sekundärprävention
- ICD-Implantation ist empfohlen bei Patient*innen mit dokumentiertem Kammerflimmern oder hämodynamisch nicht tolerierter ventrikulärer Tachykardie bei Abwesenheit reversibler Ursachen (I/A).
Primärprävention
- KHK mit reduzierter LV-Funktion
- ICD-Implantation ist empfohlen bei Patient*innen mit KHK, symptomatischer Herzinsuffizienz (NYHA II–III) und LVEF ≤ 35 % trotz ≥ 3 Monate optimaler medikamentöser Therapie (I/A).
- Dilatative Kardiomyopathie, hypokinetische Kardiomyopathie
- ICD-Implantation sollte erwogen werden bei Patient*innen mit Kardiomyopathie, symptomatischer Herzinsuffizienz (NYHA II–III) und LVEF ≤ 35 % trotz ≥ 3 Monate optimaler medikamentöser Therapie (IIa/A).
- Arrhythmogene rechtsventrikuläre Kardiomyopathie (ARVC)
- ICD-Implantation sollte erwogen werden bei Patient*innen mit hämodynamisch tolerierter anhaltender ventrikulärer monomorpher Tachykardie (IIa/C).
- Hypertrophe Kardiomyopathie
- ICD-Implantation sollte erwogen werden bei Patient*innen ≥ 16 Jahre und mit einem geschätzten 5-Jahres-Risiko für plötzlichen Herztod ≥ 6 % (IIa/B).
ICD-Therapie
Allgemeines zur Therapie
- Erstimplantation eines ICD im Jahr 198022
- Im Jahr 2020 wurden in Deutschland insgesamt über 39.000 ICD-Interventionen vorgenommen23
- Implantationen: 31.331
- Aggregatwechsel: 10.100
- Revisionen/Systemwechsel/Explantationen: 7.761
-
Behandlungsprinzip
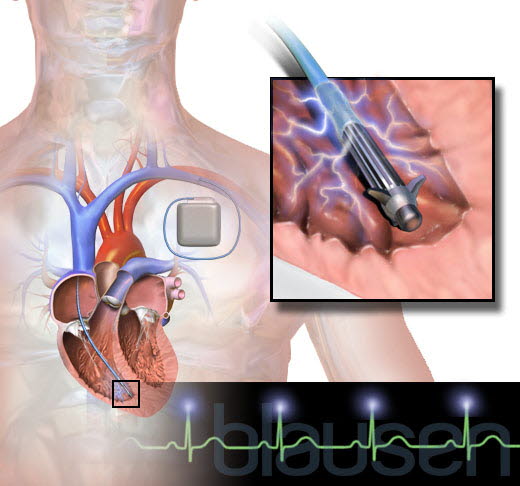 ICD: implantierbarer Kardioverter-Defibrillator
ICD: implantierbarer Kardioverter-Defibrillator- gleichzeitige Depolarisation des Myokards durch einen elektrischen Impuls und dadurch Terminierung der ventrikulären Tachykardie bzw. des Kammerflimmerns
- Komponenten
- Ein ICD besteht wie ein Herzschrittmacher aus dem Aggregat und mindestens einer Sonde (rechtsventrikuläre Sonde mit Schockelektrode(n) und Stimulations/Detektionselektrode).
- Zweikammersysteme haben zusätzlich eine Sonde im rechten Vorhof (insoweit missverständliche, aber übliche Bezeichnung).
- Dreikammersysteme zusätzlich mit 3. Sonde in der Koronarvene für kardiale Resynchronisationstherapie (ICD-CRT)
- ICD-Aggregate etwas größer als reine Stimulationsschrittmacher
- Trend zu immer kleineren Aggregaten mit gutem kosmetischem Ergebnis
- Implantation
- Durchführung unter lokaler Anästhesie und Sedierung
- Platzierung des Aggregats üblicherweise unterhalb der linken Klavikula
- bei linksseitiger Implantation günstigere Ausrichtung des Stromflusses für effektive Defibrillation
- Sondenführung über V. subclavia oder V. cephalica
- bis vor kurzem routinemäßige Testung der Wirksamkeit des ICD durch Induktion von Kammerflimmern am Ende der Implantation
- Neuere Daten zeigen gleich gute Wirksamkeit auch ohne intraoperativen Test.24
Therapieformen und Nachsorge
- Antitachykarde Stimulation
- nach Detektion einer ventrikulären Tachykardie zunächst Versuch der Unterbrechung mit antitachykarder Stimulation
- schnelle Abgabe von Impulsen zur Erzeugung refraktären Myokards und dadurch Unterbrechung des Erregungskreises
- zwei Stimulationsformen
- Burst-Stimulation: konstantes Intervall zwischen den Stimulationen
- Ramp-Stimulation: abnehmendes Intervall zwischen den Stimulationen
- durch erfolgreiche antitachykarde Stimulation Vermeidung einer sonst notwendigen, die Patient*innen belastenden Schockabgabe
- Defibrillation
- Defibrillation notwendig bei Detektion von Kammerflimmern bzw. nicht erfolgreicher antitachykarder Stimulation einer ventrikulären Tachykardie
- zunächst Aufladen des Kondensators
- Dauer ca. 7–10 s
- Abgabe eines biphasischen Schocks von 30–40 J
- Nachsorge
- ICD werden nach der initialen Einstellung im weiteren Verlauf üblicherweise alle 6 Monate kontrolliert.
Komplikationen
Perioperative Komplikationen
- Pneumothorax
- Hämatothorax
- Taschenhämatom
- Tascheninfektion
- Thrombosen
- Sondendislokation
- Perikarditis
- Myokardperforation
Komplikationen im weiteren Verlauf
- Komplikationen und Fehlfunktionen im weiteren Verlauf nach einer ICD-Implantation sind relativ häufig.25-26
- Inadäquate Schocks (Abgabe von Schocks ohne Vorliegen einer ventrikulären Tachykardie)
- Ursachen27
- Fehlinterpretation von supraventrikulären Tachykardien durch die Detektionsalgorithmen
- Sondendefekte
- T-Wellen Oversensing
- elektromagnetische Interferenz
- 12-Jahres-Inzidenz 20 %28
- Ursachen27
- Infektion
- 12-Jahres-Inzidenz 6 %28
- Sondenversagen
- 12-Jahres-Inzidenz 17 %28
- Psychosomatische Beeinträchtigungen, Angststörungen2,29
- Multiple adäquate Schocks („elektrischer Sturm“)
- adäquate Therapie durch den ICD mit Wiederbeginn der Rhythmusstörung in kurzer Zeit
- Notfall, sofortige Krankenhauseinweisung
- evtl. antiarrhythmische Therapie mit Amiodaron
- Sedation, ggf. Narkose mit Intubation und Beatmung
Nichtkardiale Operationen
- Störsignale durch Elektrokauter können inadäquate ICD-Therapie auslösen.
- Perioperativ Deaktivierung der ICD-Therapiefunktion31
- Rhythmusmonitoring und Defibrillationsbereitschaft, solange ICD-Therapie deaktiviert31
MRT-Untersuchungen
- MRT galt lange bei ICD-Patient*innen als absolut kontraindiziert.
- Viele der heute am Markt befindlichen Systeme gelten als „bedingt MR-sicher“32
- Durchführung aber nur nach sorgfältiger Abwägung von Nutzen und Risiko33
- Umprogrammierung vor der Untersuchung in speziellen MR-Modus, die Schockfunktion des ICD ist während der Untersuchung deaktiviert.32
Fahrerlaubnis
- Eine intensive Aufklärung über die Fahrtauglichkeit ist von großer Bedeutung.
- Die folgenden Angaben beziehen sich auf die entsprechenden Leitlinien der Deutschen Gesellschaft für Kardiologie.36
Privatfahrer*innen mit ICD
- Sekundärprävention
- Fahreignung 3 Monate nach Implantation
- Primärprävention
- Fahreignung 1–2 Wochen nach Implantation
- Nach adäquatem Schock
- Fahreignung nach 3 Monaten
- Nach inadäquatem Schock
- Fahreignung nach Beseitigung der zugrunde liegenden Ursache
- Nach Aggregatwechsel
- Fahreignung nach 1 Woche
Berufsfahrer*innen mit ICD
- In der Regel nach ICD-Implantation nicht fahrgeeignet
- Siehe auch Artikel Beurteilung der Fahreignung.
Vorgehen am Lebensende
- Ziel sollte Vermeidung von sinnlosen oder unerwünschten Schocktherapien sein.37
- Ggf. ICD-Deaktivierung37
- durch qualifiziertes Personal
- nach adäquater Diskussion mit den Patient*innen
- in Absprache mit den betreuenden Kardiolog*innen/Elektrophysiolog*innen
Patienteninformationen
Patienteninformationen in Deximed
Illustrationen

ICD: implantierbarer Kardioverter-Defibrillator
Quellen
Leitlinien
- European Society of Cardiology. Guidelines for the management of patients with ventricular arrhythmias and the prevention of sudden cardiac death. Stand 2022. www.escardio.org
- European Society of Cardiology. Guidelines on cardiac pacing and cardiac resynchronization therapy. Stand 2021. www.escardio.org
- Deutsche Gesellschaft für Kardiologie. Pocket-Leitlinie Fahreignung bei kardiovaskulären Erkrankungen. Stand 2018. www.leitlinien.dgk.org
- Deutsche Gesellschaft für Kardiologie und Deutsche Röntgengesellschaft. Konsensuspapier: MR-Untersuchungen bei Patienten mit Herzschrittmachern und implantierbaren Kardioverter-Defibrillatoren. Stand 2017. www.leitlinien.dgk.org
Literatur
- Eckardt L, Könemann H, Bosch R, et al. Kommentar zu den Leitlinien 2022 der ESC zu ventrikulären Arrhythmien und Prävention des plötzlichen Herztodes. Kardiologie 2023. doi:10.1007/s12181-022-00589-7 DOI
- Trappe HJ, Gummert J. Current pacemaker and defibrillator therapy. Dtsch Arztebl Int 2011; 108: 372-380. doi:10.3238/arztebl.2011.0372 DOI
- Martens E, Sinner M, Siebermair J, et al. Incidence of sudden cardiac death in Germany: results from an emergency medical service registry in Lower Saxony. Europace 2014; 16: 1752-1758. doi:10.1093/europace/euu153 DOI
- Seidl K, Senges J. Worldwide utilization of implantable cardioverter/defibrillators now and in the future. Card Electrophysiol Rev 2003; 7: 5-13. PubMed
- Zipes DP, Wellens HJ. Sudden cardiac death. Circulation 1998; 98: 2334-51. pubmed.ncbi.nlm.nih.gov
- European Society of Cardiology: Guidelines for the management of patients with ventricular arrhythmias and the prevention of sudden cardiac death, Stand 2022. www.escardio.org
- Huikuri HV, Castellanos A, Myerburg RJ. Sudden death due to cardiac arrhythmias. N Engl J Med 2001; 345: 1473-82. New England Journal of Medicine
- Fox C, Evans J, Larson M, et al. Temporal trends in coronary heart disease mortality and sudden cardiac death from 1950 to 1999: the Framingham Heart Study. Circulation 2004; 110: 522-527. doi:10.1161/01.CIR.0000136993.34344.41 DOI
- Myerburg RJ, Kessler KM, Castellanos A. Sudden cardiac death. Structure, function, and time-dependence of risk. Circulation 1992; 85(1 suppl): I2-I10. pubmed.ncbi.nlm.nih.gov
- Hohnloser SH, Kuck KH, Dorian P, et al. DINAMIT Investigators. Prophylactic use of an implantable cardioverter-defibrillator after acute myocardial infarction. N Engl J Med 2004; 351: 2481-8. pubmed.ncbi.nlm.nih.gov
- Bardy GH, Lee KL, Mark DB, et al. Sudden Cardiac Death in Heart Failure Trial (SCD-HeFT) Investigators. Amiodarone or an implantable cardioverter-defibrillator for congestive heart failure. N Engl J Med 2005; 352: 225-37. New England Journal of Medicine
- Ezekowitz JA, Rowe BH, Dryden DM, et al. Systematic review: implantable cardioverter defibrillators for adults with left ventricular systolic dysfunction. Ann Intern Med 2007; 147: 251-62. PubMed
- The Antiarrhythmics versus Implantable Defibrillators (AVID) Investigators. A comparison of antiarrhythmic-drug therapy with implantable defibrillators in patients resuscitated from near-fatal ventricular arrhythmias. N Engl J Med 1997;337: 1576 – 1583. doi:10.1056/NEJM199711273372202 DOI
- Connolly SJ, Gent M, Roberts RS, et al. Canadian implantable defibrillator study (CIDS): a randomized trial of the implantable cardioverter defibrillator against amiodarone. Circulation 2000;101:1297–1302. doi:10.1161/01.CIR.101.11.1297 DOI
- Kuck KH, Cappato R, Siebels J, et al. Randomized comparison of antiarrhythmic drug therapy with implantable defibrillators in patients resuscitated from cardiac arrest: the Cardiac Arrest Study Hamburg (CASH). Circulation 2000;102: 748-754. www.ahajournals.org
- Connolly SJ, Hallstrom AP, Cappato R, et al. Meta-analysis of the implantable cardioverter defibrillator secondary prevention trials. AVID, CASH and CIDS studies. Antiarrhythmics vs Implantable Defibrillator study. Cardiac Arrest Study Hamburg. Canadian Implantable Defibrillator Study. Eur Heart J 2000;21:2071–2078. doi:10.1053/euhj.2000.2476 DOI
- European Society of Cardiology. Guidelines on cardiac pacing and cardiac resynchronization therapy, Stand 2021. www.escardio.org
- Moss AJ, Zareba W, Hall WJ, et al. The Multicenter Automatic Defibrillator Implantation Trial II Investigators: prophylactic implantation of a defibrillator in patients with myocardial infarction and reduced ejection fraction. N Engl J Med 2002; 346: 877–83.doi:10.1056/NEJMoa013474 DOI
- Bardy GH, Lee KL, Mark DB. Amiodarone or an implantable cardioverter-defibrillator for congestive heart failure. N Engl J Med 2005; 352: 225–37. doi:10.1056/NEJMoa043399 DOI
- Kadish A, Dyer A, Daubert JP, et al. Defibrillators in Non-Ischemic Cardiomyopathy Treatment Evaluation Investigators. Prophylactic defibrillator implantation in patients with nonischemic dilated cardiomyopathy. N Engl J Med 2004;350:2151–2158. doi:10.1056/NEJMoa033088 DOI
- Desai AS, Fang JC, Maisel WH, et al. Implantable defibrillators for the prevention of mortality in patients with nonischemic cardiomyopathy: a meta-analysis of randomized controlled trials. JAMA 2004;292:2874 – 2879. doi:10.1001/jama.292.23.2874 DOI
- Mirowski M, Reid PR, Mower MM, et al. Termination of malignant ventricular arrhythmias with an implanted automatic defibrillator in human beings. N Engl J Med 1980; 303:322. PubMed
- Markewitz A, Nowak B, Fröhlig G, et al. Jahresbericht 2020 des Deutschen Herzschrittmacher- und Defibrillator-Registers – Teil 2: Implantierbare Kardioverter-Defibrillatoren (ICD). Herzschr Elektrophys 2022; 33: 414-431. doi:10.1007/s00399-022-00894-4 DOI
- Bänsch D, Bonnemeier H, Brandt J, et al. Intra-operative defibrillation testing and clinical shock efficacy in patients with implantable cardioverter-defibrillators: the NORDIC ICD randomized clinical trial. Eur Heart J 2015; 36: 2500-2507. doi:10.1093/eurheartj/ehv292 DOI
- Alter P, Waldhans S, Plachta E, Moosdorf R, Grimm W. Complications of implantable cardioverter defibrillator therapy in 440 consecutive patients. Pacing Clin Electrophysiol 2005; 28: 926-32. PubMed
- Kloppe A, Schiedat F, Mügge A, et al. Sachgerechtes Vorgehen bei Herzschrittmacher- und ICD-Fehlfunktion. Herzschr Elektrophys 2020; 31: 64-72. doi:10.1007/s00399-020-00669-9 DOI
- Gehi AK, Mehta D, Gomes JA. Evaluation and management of patients after implantable cardioverter-defibrillator shock. JAMA 2006; 296: 2839-47. pubmed.ncbi.nlm.nih.gov
- van der Heijden A, Borleffs C, Buiten M, et al. The clinical course of patients with implantable cardioverter-defibrillators: Extended experience on clinical outcome, device replacements, and device-related complications.. Heart Rhythm 2015; 12: 1169-1176. doi:10.1016/j.hrthm.2015.02.035 DOI
- Ladwig KH, Baumert J, Marten-Mittag B, Kolb C, Zrenner B, Schmitt C. Posttraumatic stress symptoms and predicted mortality in patients with implantable cardioverter-defibrillators: results from the prospective living with an implanted cardioverter-defibrillator study. Arch Gen Psychiatry 2008; 65: 1324-30. PubMed
- Ginzburg D, Tavenaux M, Sperzel J, et al. Psychische Störungen nach ICD-Mehrfachschocks und deren psychotherapeutische Behandlung. Kardiologe 2011; 5: 114-121. doi:10.1007/s12181-011-0331-5 DOI
- Nowak B, Israel C, Willems S, et al. Empfehlungen zum Einsatz von Elektrokautern bei Patienten mit Herzschrittmachern und implantierten Defibrillatoren. Kardiologe 2010; 4: 383-388. leitlinien.dgk.org
- Beitzke D. Sichere MRT-Untersuchung bei Patienten mit Herzschrittmacher und ICD. Radiologe 2019. doi:10.1007/s00117-019-0567-9 DOI
- Bovenschulte H, Schlüter-Brust K, Liebig T. MRI in patients with pacemakers—overview and procedural management. Dtsch Arztebl Int 2012; 109: 270-75. doi:10.3238/arztebl.2012.0270 DOI
- Sommer T, Bauer W, Fischbach K, et al. MR-Untersuchungen bei Patienten mit Herzschrittmachern und implantierbaren Kardioverter-Defibrillatoren. Kardiologe 2017; 11: 97. doi:10.1007/s12181-017-0124-6 DOI
- Hartel F, et al. Leitlinien zum Fahrverbot bei ICD-Patienten: Anspruch und Realität. Clin Res Cardiol 103, Suppl 1, April 2014. P1775 der 80. Jahrestagung der Deutschen Gesellschaft für Kardiologie (DGK). dgk.org
- Deutsche Gesellschaft für Kardiologie. Pocket-Leitlinie Fahreignung bei kardiovaskulären Erkrankungen. Stand 2018. leitlinien.dgk.org
- Carlsson J, Paul N, Dann M, et al. The deactivation of implantable cardioverter-defibrillators:medical, ethical, practical, and legal considerations. Dtsch Arztebl Int 2012; 109: 535-541. doi:10.3238/arztebl.2012.0535 DOI
Autor*innen
- Michael Handke, Prof. Dr. med., Facharzt für Innere Medizin, Kardiologie und Intensivmedizin, Freiburg i. Br.
- Die ursprüngliche Version dieses Artikels basiert auf einem entsprechenden Artikel im norwegischen hausärztlichen Online-Handbuch Norsk Elektronisk Legehåndbok (NEL, https://legehandboka.no/).