Zusammenfassung
- Definition:Fehlbildungen des Herzens oder der großen Gefäße, die auf einer anomalen Entwicklung in der Embryonalperiode beruhen.
- Häufigkeit:Rund 1 % aller Neugeborenen kommt mit einem angeborenen Herzfehler zur Welt. Bei 0,12 % liegt ein schwerer, häufig zyanotischer Herzfehler vor.
- Symptome:Bei schweren Herzfehlern bald postnatal Symptome der Herzinsuffizienz mit Tachypnoe, Schwitzen, Trinkschwäche, evtl. Zyanose. Je nach Art und Ausprägung des Herzfehlers Symptome evtl. auch erst im weiteren Verlauf der kindlichen Entwicklung oder im Erwachsenenalter.
- Befunde:Abhängig vom spezifischen Vitium, möglich sind unterschiedliche Herzgeräusche, Hypoxämie, Tachykardie, hebender Herzspitzenstoß, Hepatosplenomegalie, abgeschwächte Femoralispulse.
- Diagnostik:Pulsoxymetrie im Rahmen des postnatalen Primärscreenings, definitive Diagnose erfolgt durch Echokardiografie.
- Therapie:Operative oder katheterinterventionelle Korrektur.
Allgemeine Informationen
Definition
- Als angeborene Herzfehler wird eine Reihe von Fehlbildungen des Herzens oder der großen Gefäße bezeichnet, die auf einer anomalen Entwicklung in der Embryonalperiode beruhen.
- Strukturell sind die angeborenen Herzfehler bereits bei der Geburt vorhanden, klinisch können sie je nach Art und Ausprägung des Herzfehlers rasch postnatal oder auch erst im weiteren Verlauf manifest werden.
Klassifikation in zyanotische und nicht-zyanotische Herzfehler
- Eine klinisch und diagnostisch bedeutsame Klassifikation der angeborenen Fehlbildungen kann in zyanotische und nicht-zyanotische Herzfehler vorgenommen werden.
Zyanotische Herzfehler
- Fallot–Tetralogie (TOF)
- Transposition der großen Arterien (TGA)
- Univentrikuläres Herz
- Trikuspidalatresie
- Pulmonalatresie
Nicht-zyanotische Herzfehler (mit Li-Re-Shunt)
- Ventrikelseptumdefekt (VSD)
- Vorhofseptumdefekt (ASD)
- Persistierender Ductus arteriosus (PDA)
- Truncus arteriosus
Nicht-zyanotische Herzfehler (ohne Shunt)
- Aortenklappenstenose
- Aortenisthmusstenose
- Pulmonalklappenstenose
Herzfehler ohne oder mit Zyanose, Entwicklung einer Zyanose im Verlauf
- Einige angeborene Herzfehler können je nach individueller Ausprägung primär ohne oder mit Zyanose auftreten, z. B. atrioventrikulärer Septumdefekt (AVSD).1
- Im weiteren Verlauf kann auch bei primär azyanotischen Herzfehlern mit Links-Rechts-Shunt eine Zyanose entstehen, wenn es im Rahmen einer pulmonalen Druckerhöhung zur Shuntumkehr kommt (Eisenmenger-Reaktion).
Häufigkeit
- Rund 1 % aller Neugeborenen kommt mit einem angeborenen Herzfehler zur Welt.2
- ca. 6.000 Kinder/Jahr in Deutschland3
- Bei 80 % aller Herzfehler handelt es sich um isolierte Fehlbildungen.
- Ca. 0,12 % der Neugeborenen mit schweren Vitien (ca. 900 Kinder/Jahr in Deutschland)4
- nicht dauerhaft mit dem Leben vereinbare Herzfehler, klinisch meist mit Zyanose
- Mehr als 90 % der Patient*innen erreichen mittlerweile das Erwachsenenalter.5
- Insgesamt durch die zunehmende Lebenserwartung steigende Anzahl – ca. 300.000 Kinder, Jugendliche und Erwachsene in Deutschland leben aktuell mit einem angeborenen Herzfehler.3
Häufigkeit der verschiedenen angeborenen Herzfehler3
- Ventrikelseptumdefekt (VSD): 31 %
- Vorhofseptumdefekt (ASD): 7 %
- Persistierender Ductus arteriosus (PDA): 7 %
- Pulmonalklappenstenose: 7 %
- Aortenisthmusstenose (Coarctatio): 5–8 %
- Aortenklappenstenose: 3–6 %
- Fallot-Tetralogie (TOF): 5,5 %
- Atrioventrikulärer Septumdefekt (AVSD): 4,8 %
- Transposition der großen Arterien (TGA): 4,5 %
- Hypoplastisches Linksherzsyndrom (HLHS): 3,8 %
- Pulmonalatresie mit Ventrikelseptumdefekt: 2,5–3,4 %
- Pulmonalatresie ohne Ventrikelseptumdefekt: 2,4 %
- Trikuspidalatresie: 1–2 %
- Double Inlet Ventricle: 1,5 %
- Double Outlet Ventricle: 1,2 %
- Angeborene korrigierte Transposition der großen Gefäße: 1 %
- Truncus arteriosus communis: 0,5–1,0 %
- Hypertroph-obstruktive Kardiomyopathie: 0,4 %
- Supravalvuläre Aortenstenose (Williams-Beuren-Syndrom): 0,4 %
Ätiologie und Pathogenese
- Bei der Mehrzahl der Herzfehler wird eine multifaktorielle Ätiologie angenommen.
- Interaktion zwischen genetischer Disposition und Umweltfaktoren
- Bei den meisten Herzfehlern sind vermutlich Gendefekte beteiligt, jedoch nur wenige der auslösenden Mutationen bekannt.6
- bekannte genetische Ursachen bei weniger als 20 % der Herzfehler7
- Das Risiko für Geschwister von Betroffenen ist im Vergleich zum allgemeinen Risiko von 1 % etwa 3-fach erhöht (2,7 %), insgesamt aber immer noch niedrig.8
- Bei einigen chromosomalen Syndromen treten Herzfehler stark gehäuft auf:
- Trisomie 21 mit Herzfehler bei ca. 50 %, davon ca. die Hälfte AVSD9
- Turner-Syndrom mit Aortenisthmusstenose bei ca. 30 % der Betroffenen10
- Bei den meisten syndromalen Herzfehlern liegen De-novo-Mutationen vor, d. h. die Eltern sind nicht Anlageträger der krankhaften Veränderung.6,8
- Nicht-syndromale Herzfehler sind wahrscheinlich häufiger erblich bedingt als bisher gedacht.6,8
Prädisponierende Faktoren
- Metabolische Störungen
- Diabetes mellitus in der Schwangerschaft11
- Phenylketonurie12
- Nutritive Faktoren
- Medikamente
- Isotretinoin, Antiepileptika, Lithium, Folsäure-Antagonisten, Indometacin u. a.16
- Infektionen17
- Röteln u. a.
- Ionisierende Strahlung18
- Mütterliche Gerinnungsstörungen19
ICPC-2
- K73 Angebor. Anomalie Herz/Gefäßsystem
ICD-10
- Q20 Angeborene Fehlbildungen der Herzhöhlen und verbindender Strukturen
- Q20.0 Truncus arteriosus communis
- Q20.1 Rechter Doppelausstromventrikel [Double outlet right ventricle]
- Q20.2 Linker Doppelausstromventrikel [Double outlet left ventricle]
- Q20.3 Diskordante ventrikuloarterielle Verbindung
- Q20.4 Doppeleinstromventrikel [Double inlet ventricle]
- Q20.5 Diskordante atrioventrikuläre Verbindung
- Q20.6 Vorhofisomerismus
- Q20.8 Sonstige angeborene Fehlbildungen der Herzhöhlen und verbindender Strukturen
- Q20.9 Angeborene Fehlbildung der Herzhöhlen und verbindender Strukturen, nicht näher bezeichnet
- Q21 Angeborene Fehlbildungen der Herzsepten
- Q21.0 Ventrikelseptumdefekt
- Q21.1 Vorhofseptumdefekt
- Q21.2 Defekt des Vorhof- und Kammerseptums
- Q21.3 Fallot-Tetralogie
- Q21.4 Aortopulmonaler Septumdefekt
- Q21.8 Sonstige angeborene Fehlbildungen der Herzsepten
- Q21.9 Angeborene Fehlbildung des Herzseptums, nicht näher bezeichnet
- Q22 Angeborene Fehlbildungen der Pulmonal- und der Trikuspidalklappe
- Q22.0 Pulmonalklappenatresie
- Q22.1 Angeborene Pulmonalklappenstenose
- Q22.2 Angeborene Pulmonalklappeninsuffizienz
- Q22.3 Sonstige angeborene Fehlbildungen der Pulmonalklappe
- Q22.4 Angeborene Trikuspidalklappenstenose
- Q22.5 Ebstein-Anomalie
- Q22.6 Hypoplastisches Rechtsherzsyndrom
- Q22.8 Sonstige angeborene Fehlbildungen der Trikuspidalklappe
- Q22.9 Angeborene Fehlbildung der Trikuspidalklappe, nicht näher bezeichnet
- Q23 Angeborene Fehlbildungen der Aorten- und der Mitralklappe
- Q23.0 Angeborene Aortenklappenstenose
- Q23.1 Angeborene Aortenklappeninsuffizienz
- Q23.2 Angeborene Mitralklappenstenose
- Q23.3 Angeborene Mitralklappeninsuffizienz
- Q23.4 Hypoplastisches Linksherzsyndrom
- Q23.8 Sonstige angeborene Fehlbildungen der Aorten- und Mitralklappe
- Q23.9 Angeborene Fehlbildung der Aorten- und Mitralklappe, nicht näher bezeichnet
- Q24 Sonstige angeborene Fehlbildungen des Herzens
- Q24.0 Dextrokardie
- Q24.1 Lävokardie
- Q24.2 Cor triatriatum
- Q24.3 Infundibuläre Pulmonalstenose
- Q24.4 Angeborene subvalvuläre Aortenstenose
- Q24.5 Fehlbildung der Koronargefäße
- Q24.6 Angeborener Herzblock
- Q24.8 Sonstige näher bezeichnete angeborene Fehlbildungen des Herzens
- Q24.9 Angeborene Fehlbildung des Herzens, nicht näher bezeichnet
- Q25 Angeborene Fehlbildungen der großen Arterien
- Q25.0 Offener Ductus arteriosus
- Q25.1 Koarktation der Aorta
- Q25.2 Atresie der Aorta
- Q25.3 Stenose der Aorta (angeboren)
- Q25.4 Sonstige angeborene Fehlbildungen der Aorta
- Q25.5 Atresie der A. pulmonalis
- Q25.6 Stenose der A. pulmonalis (angeboren)
- Q25.7 Sonstige angeborene Fehlbildungen der A. pulmonalis
- Q25.8 Sonstige angeborene Fehlbildungen der großen Arterien
- Q25.9 Angeborene Fehlbildung der großen Arterien, nicht näher bezeichnet
Diagnostik
Diagnostische Kriterien
- Kreislauf
- Manche Herzfehler führen postnatal – insbesondere nach Verschluss des Ductus arteriosus – zu einer raschen hämodynamischen Verschlechterung mit Schock-Symptomatik.
- Zyanose
- Herzgeräusch (siehe auch Artikel Herzgeräusche bei Kindern)
- Herzgeräusche bei Neugeborenen sind in einem hohen Prozentsatz durch angeborene Herzfehler bedingt und rasch abklärungbedürftig.22
- Echokardiografie
- Die definitive Diagnose wird in den allermeisten Fällen mit der Echokardiografie gestellt: Darstellung des Defektes und Erfassung der funktionellen Auswirkungen.
Differenzialdiagnosen
- Andere Ursachen für Schock
- Nichtkardial bedingte Zyanose4
- Atemnotsyndrom
- Mekoniumaspiration
- gastroösophagealer Reflux
- Krampfanfälle
- u. a.
- Physiologische Herzgeräusche (siehe auch Artikel Herzgeräusche bei Kindern)
Anamnese
- Evtl. Familienanamnese angeborener Herzfehler
- Evtl. Familienanamnese monogenetischer Erbkrankheiten
- Exposition gegenüber teratogenen Faktoren in der Schwangerschaft? (Diabetes mellitus, Alkohol, Medikamente, Infektionen, ionisierende Strahlung)
Klinische Untersuchung
- In Abhängigkeit von Art und Ausprägung des Herzfehlers
- Evtl. Zeichen der Herzinsuffizienz
- Tachypnoe, Tachykardie, verstärktes Schwitzen, Hepatosplenomegalie
- Evtl. Zyanose
- Evtl. hyperdynamer Herzspitzenstoß bei Volumenbelastung
- Evtl. abgeschwächte Femoralispulse
- Evtl. Herzgeräusch (siehe auch Artikel Herzgeräusche bei Kindern)
Ergänzende Untersuchungen in der Hausarztpraxis
Diagnostik bei Spezialist*innen
Echokardiografie
- Die Echokardiografie ist das wichtigste Verfahren zur Diagnosestellung.
- Darstellung von Struktur und Größe des Defektes/der Defekte
- Größe der Herzhöhlen
- Funktion der Ventrikel
- Morphologie und Funktion der Herzklappen
- Darstellung und Quantifizierung von Shunts
- Abgang und strukturelle Veränderungen der großen Gefäße
- Abschätzung des pulmonal-arteriellen Drucks
Pulsoxymetrie
- Im Rahmen der Primärdiagnostik bei V. a. Herzfehler
EKG
- Häufig unspezifische Veränderungen22
- Im Einzelfall (z. B. überdrehter Linkstyp bei AVSD) Hinweis auf spezifischen Herzfehler22
Röntgen-Thorax
- Im Rahmen der Primärdiagnostik im Allgemeinen nicht notwendig
- Bei Erwachsenen zum Nachweis/Ausschluss von Differenzialdiagnosen bei Dyspnoe23
MRT/CT
- Ergänzend vor allem bei unzureichenden echokardiografischen Schallbedingungen
- Die kardiale MRT kann sowohl bei Kindern als auch bei Erwachsenen mit angeborenen Herzfehlern angewendet werden.24
- Bei Erwachsenen stehen mit zunehmendem Alter Komorbiditäten wie sekundäre Kardiomyopathien im Fokus.
Herzkatheteruntersuchung
- Ist heutzutage für die Primärdiagnostik im Allgemeinen entbehrlich.
- Planung und Durchführung von Eingriffen
Indikationen zur Überweisung
- Eine Überweisung zur Kinderkardiologie sollte erfolgen bei22,25-27
- Neugeborenen mit Herzgeräusch
- auskultatorischem Verdacht auf ein pathologisches Geräusch
- holosystolische Geräusche
- spätsystolische Geräusche
- Lautstärke ≥ 3/6
- kontinuierliche Geräusche
- Geräuschen mit palpablem Schwirren
- Geräuschen mit gleichzeitig kardialen Symptomen (Brustschmerz, Palpitationen, Synkope)
- abgeschwächten Pulsen der unteren Extremität
- einem pathologischen EKG
- klinischen Hinweisen auf Erkrankungen, die gehäuft mit Herzfehlern assoziiert sind
- plötzlichem Herztod in der Familie
- Gedeihstörung, verminderter Leistungsfähigkeit im Vergleich zu Gleichaltrigen
- starker Beunruhigung der Eltern trotz Aufklärung.
- Das Alter des Kindes ist ein wichtiger Aspekt bei der Entscheidung.
- bei Neugeborenen mit Herzgeräusch Herzfehler in 1/3 der Fälle, sofortige Abklärung sinnvoll22
- im 1. Lebensjahr bei verdächtigem Geräusch, insbesondere in Kombination mit inzwischen sich entwickelnder Klinik (Zyanose, Gedeihstörung, Herzinsuffizienz), Abklärung notwendig25
- Bis zum Ende des 1. Lebensjahr werden strukturelle Herzerkrankungen ganz überwiegend erfasst.25
- Im 2. und 3. Lebensjahr sind Herzgeräusche selten ein Zuweisungsgrund (v. a. verursacht durch Aortenisthmusstenosen und Vorhofseptumdefekte).25
- Im Schulkindalter werden sich manifestierende angeborene Herzfehler selten entdeckt, im Vordergrund stehen Herzgeräusche durch erworbene Myokarditiden und Kardiomyopathien (z. B. hypertrophe Kardiomyopathie, dilatative Kardiomyopathie).25
- Eine Unterscheidung zwischen pathologischen und nicht pathologischen Herzgeräuschen ist häufig bereits in der Hausarztpraxis möglich.25
- Asymptomatische Patient*innen mit nach gründlicher klinischer Untersuchung geringer Wahrscheinlichkeit für eine strukturelle Herzerkrankung können durch Hausärzt*innen nachkontrolliert werden.25
Therapie
Therapieziele
- Bei hämodynamisch kritischen Vitien postnatal Überleben des Kindes
- Bei Herzfehlern mit eingeschränkter Prognose möglichst Korrektur des Herzfehlers und Normalisierung der Prognose sowie Erreichen einer möglichst guten Lebensqualität
Therapieoptionen
Medikamentöse Therapie
- Evtl. postnatal Gabe von Prostglandin E zum Offenhalten des Ductus arteriosus bei ductusabhängigen Herzfehlern
- Palliative Behandlung einer Herzinsuffizienz, einer pulmonalen Hypertonie
Chirurgische und interventionelle Therapie
- Z. T. ist eine definitive Korrektur eines Herzfehlers durch einen einmaligen operativen Eingriff möglich, z. T. müssen im Lauf der Entwicklung des Kindes auch abgestufte operative Verfahren angewandt werden.
- Bei einigen Herzfehlern sind heutzutage katheterinterventionelle Verfahren eine Option bzw. Hybrideingriffe mit einer Kombination aus Operation und Katheterintervention.
- Näheres siehe die entsprechenden Artikel zu den einzelnen Herzfehlern:
- Ventrikelseptumdefekt (VSD)
- Vorhofseptumdefekt (ASD)
- Persistierender Ductus arteriosus (PDA)
- Aortenisthmusstenose
- Aortenklappenstenose
- Fallot-Tetralogie (TOF)
- Transposition der großen Arterien (TGA)
- Hypoplastisches Linksherzsyndrom (HLHS)
- Pulmonalatresie
- Univentrikuläres Herz
- Truncus arteriosus communis
Erwachsene mit angeborenen Herzfehlern (EMAH)
Prävalenz und Bedeutung für die hausärztliche Praxis
- Durch Verbesserungen in Therapie und Nachsorge gibt es eine ansteigende Zahl von Patient*innen mit angeborenen Herzfehlern im Erwachsenenalter (EMAH).28
- in Deutschland mehr als 300.000 Patient*innen29
- Gruppe von Patient*innen mit teilweise neuen, unerwarteten Problemen
- Hausärzt*innen und Internist*innen kommt eine zentrale Rolle bei der EMAH-Versorgung zu29
- Weichenstellung für richtige, zeitgerechte Diagnostik und Behandlung
- Erinnerung der Patient*innen an die notwendige Nachsorge
- Überweisung an geeignete Anlaufstellen
- Den EMAH-Spezialist*innen/Zentren kommt die Aufgabe zu,29
- die Zusammenarbeit mit ihren Zuweiser*innen zu intensivieren.
- das notwendige Wissen zur Führung von EMAH zu vermitteln.
- Eine Adressliste aller pädiatrischen und internistischen Kardiolog*innen mit der Zusatzqualifikation EMAH enthält die Broschüre Erwachsene mit angeborenem Herzfehler der Kinderherzstiftung für Patient*innen und Ärzt*innen nichtkardiologischer Fachrichtungen wie Hausärzt*innen und Internist*innen.
- Während bei der Mehrzahl der Patient*innen der Herzfehler und seine Behandlung im Kindes- und Jugendalter bereits bekannt sind, werden manche Vitien erst im Erwachsenenalter klinisch manifest und erstmalig diagnostiziert, z. B.:
- Vorhofseptumdefekt: klinisch manifest durch Zeichen der pulmonalen Hypertonie, (Rechtsherz-)Insuffizienz
- Aortenisthmusstenose: klinisch manifest durch sekundäre arterielle Hypertonie/hypertensive Endorganschäden
- Der Übergang von der allgemeinärztlichen Versorgung zur spezialisierten EMAH-Betreuung erfolgt teilweise noch zu spät.29
Häufige medizinische Probleme bei EMAH-Patient*innen
- Herzrhythmusstörungen
- Ein signifikanter Anteil entwickelt Rhythmusstörungen im Rahmen des Herzfehlers selbst oder als Folge interventioneller/operativer Eingriffe.30
- Arrhythmien, insbesondere Vorhofarrhythmien nehmen bei EMAH-Patient*innen mit steigendem Alter kontinuierlich zu.31
- Grundsätzlich kann das gesamte Spektrum von Rhythmusstörungen vorhanden sein.32
- Entwicklung einer Herzinsuffizienz
- Endokarditis
- Bei Verdacht (Fieber, Nachtschweiß, Embolie) ist eine frühzeitige Diagnostik (Blutkultur, Echokardiografie) wichtig.
- Endokarditisprophylaxe empfohlen bei Hochrisikopatient*innen:28
- zyanotische Vitien
- Residualdefekte in der Nähe von Fremdmaterial (Patch, Conduit)
- Klappenprothese
- 6 Monate nach OP/Intervention mit Verwendung von Fremdmaterial
- Z. n. Endokarditis
Hausärztliche Verlaufskontrollen
- Die Untersuchungen sollten Folgendes umfassen:
- Anamnese hinsichtlich Veränderungen von Symptomatik und körperlicher Belastbarkeit
- Klinische Untersuchung auf:
- Zeichen der Herzinsuffizienz
- Veränderungen des Blutdrucks
- Veränderungen des Auskultationsbefundes (siehe auch Artikel Herzgeräusche bei Erwachsenen)
- EKG (siehe auch Checkliste EKG)
- Bei V. a. Arrhythmien evtl. ergänzend Langzeit-EKG
- Belastungstests eher durch Spiroergometrie bei EMAH-Spezialist*innen
Körperliche Aktivität und Sport
- Individuelle Empfehlungen zu körperlicher Aktivität und Sport für EMAH-Patient*innen
- Betreuende Ärzt*innen waren in der Vergangenheit eher zu zurückhaltend hinsichtlich der Empfehlungen zur körperlichen Aktivität.5
- Entgegen bisheriger Sicherheitsbedenken ist der plötzliche Herztod während sportlicher Aktivität extrem selten.33
- Grundsätzlich ist die körperliche Aktivität günstig für:5
- körperliche Belastbarkeit
- psychosoziales Wohlergehen
- soziale Integration
- Vermeidung künftiger kardialer Morbidität
- Dynamische Belastungen sind günstiger als statische.5
- Kein Wettkampfsport bei schweren Veränderungen (z. B. pulmonale Hypertonie, Eisenmenger-Syndrom)
Schwangerschaft und Herzfehler
- Im Vergleich zu früher erreichen mehr Frauen auch mit relevanten angeborenen Herzfehlern das gebärfähige Alter.
Risikostratifizierung
- Grundsätzlich kann eine Schwangerschaft auch bei Frauen mit angeborenem Herzfehler erwogen werden, für die Entscheidung muss eine Beurteilung des zu erwartenden mütterlichen und kindlichen Risikos vorgenommen werden.
- Vom spezifischen Vitium unabhängige Risikofaktoren für mütterliche Komplikationen (Herzinsuffizienz, symptomatische Rhythmusstörung, Schlaganfall/transiente ischämische Attacke, Tod)34
- Herzinsuffizienz > NYHA II vor Beginn der Schwangerschaft oder Zyanose
- Ejektionsfraktion (EF) des Systemventrikels < 40 %
- Obstruktion: Aortenstenose < 1,5 cm2 bzw. max. Gradient > 30 mmHg (vor der Schwangerschaft); Mitralstenose < 2 cm2
- anamnestisch bereits kardiovaskuläre Komplikationen (Herzrhythmusstörungen, Lungenödem, Schlaganfall/TIA)
- Dysfunktion des subpulmonalen rechten Ventrikels/schwere Pulmonalklappeninsuffizienz
- Vom spezifischen Vitium unabhängige Risikofaktoren für kindliche Komplikationen (intrauterine Wachstumsretardierung, Frühgeburtlichkeit, intrakranielle Blutung, Fehlgeburt, neonatales Versterben, Totgeburt)34
- Herzinsuffizienz > NYHA II vor Beginn der Schwangerschaft oder Zyanose
- Ejektionsfraktion (EF) des Systemventrikels < 40 %
- Obstruktion: Aortenstenose < 1,5 cm2 bzw. max. Gradient > 30 mmHg (vor der Schwangerschaft); Mitralstenose < 2 cm2
- Alter der Mutter < 20 oder > 35 Jahre
- Mutter ist Raucherin.
- Behandlung der Mutter mit Antikoagulanzien
- Risiko in Abhängigkeit vom spezifischen Herzfehler34
- niedriges Risiko (kardiale Komplikationen oder Tod > 1 ‰ und < 1 %)
- Links-Rechts-Shunt ohne pulmonale Hypertonie
- korrigierte Fallot-Tetralogie (ohne schwere Pulmonalinsuffizienz oder rechtsventrikuläre Dysfunktion)
- korrigierte Aortenisthmusstenose ohne Aneurysma oder Restenosierung
- Zustand nach biologischem Klappenersatz mit guter Klappenfunktion und normaler Herzfunktion
- leichte bis mittelschwere Pulmonalstenose
- mittleres Risiko (kardiale Komplikationen oder Tod 1–5 %)
- leicht- bis mittelgradige Aorten- oder Mitralstenose
- zyanotischer Herzfehler ohne pulmonale Hypertonie
- univentrikuläres Herz mit guter Ventrikelfunktion
- mechanische Herzklappe
- schwere Pulmonalstenose
- rechter Systemventrikel mit nicht schwerer Dysfunktion
- hohes Risiko (kardiale Komplikationen oder Tod > 5 %)
- schwere Aorten- oder Mitralstenose
- pulmonale Hypertonie/Eisenmenger-Syndrom
- univentrikuläres Herz mit schlechter Ventrikelfunktion
- rechter Systemventrikel mit schwerer Dysfunktion
- niedriges Risiko (kardiale Komplikationen oder Tod > 1 ‰ und < 1 %)
Kontrazeption
- Bei der Wahl der richtigen Verhütungsmethode benötigen Frauen mit angeborenem Herzfehler eine individuelle Beratung.35
- Allerdings erhalten über 40 % der Frauen mit angeborenem Herzfehler keine angemessenen Informationen über schwangerschaftsbedingte Risiken und Verhütungsmethoden.36
- 20 % der betroffenen Frauen benutzen Verhütungsmethoden, die in ihrer spezifischen Situation kontraindiziert sind.36
- Ungeeignete Verhütungsmethoden verwenden vor allem Frauen mit schweren Herzfehlern, zyanotischen Herzfehlern und Eisenmenger-Syndrom.35
- Von den Frauen mit hohem schwangerschaftsassoziiertem Risiko verwenden 28 % keine Verhütungsmittel trotz sexueller Beziehung.36
- Regeln für Schwangerschaftsverhütung und ggf. Schwangerschaftabbruch34,37
- Barrieremethoden sollten nur absolut zuverlässigen Frauen mit niedrigem kardialem Risiko empfohlen werden.
- Östrogenhaltige Kontrazeptiva („Kombinationspille“) sind bei Herzfehlern mit erhöhtem Thrombembolierisiko nicht empfohlen (zyanotische Herzfehler, pulmonale Hypertonie, schlechte Ventrikelfunktion, atriale Arrhythmien, Fontan-Zirkulation, Herzklappenprothesen).
- Gestagen-Monopräparate: Die alleinige Desogestrel-Gabe ist nicht mit einem erhöhten Thromboembolierisiko assoziiert.
- Bei herkömmlichen „Minipillen“ (niedrig dosierte Gestagen-Monopräparate) ist nur in ca. 45–50 % der Fälle eine Hemmung der Ovulation gegeben.
- Gestagen-Implantate (Oberarm) sind besonders für Patientinnen mit Compliance-Problemen geeignet.
- Ein progesteronbeschichtetes Intrauterinpessar ist ein wirksames und sicheres Verhütungsmittel, wie bei Implantaten keine Complianceprobleme.
- Depot-Gestagenpräparate („3-Monatesspritze“) sind nicht als Kontrazeptivum der ersten Wahl anzusehen.
- Kupferspiralen sind eine Option, wenn hormonaler Kontrazeption vermieden werden soll, allerdings häufig mit verstärkter Menstruationsblutung verbunden.
- Tubensterilisation sollte bei sehr hohem Schwangerschaftsrisiko erwogen werden (pulmonale Hypertonie, Eisenmenger-Syndrom).
- medizinische Indikation für Schwangerschaftsabbruch bei mittlerem bis hohem Risiko
- Saug-Kürettage in Regionalanästhesie ist die Methode der Wahl.
Fetale Echokardiografie
- Wegen des erhöhten kindlichen Risikos einer Herzerkrankung wird eine differenzierte fetale Echokardiografie in der 19. bis 22. SSW empfohlen.34
Nichtkardiale Eingriffe
- Die perioperative Mortalität und Morbidität ist bei EMAH-Patient*innen erhöht.38
- Entscheidend für das perioperative Outcome sind:38
- Identifizierung von Hochrisikopatient*innen
- das Verständnis des individuellen pathophysiologischen Befundes
- der intraoperative Erhalt des Herzzeitvolumens
- Das wichtigste Untersuchungsverfahren zur Beurteilung ist die Echokardiografie.38
Verlauf, Komplikationen und Prognose
- Verlauf und Prognose sowie häufige Komplikationen sind abhängig von der Art des Herzfehlers und der individuellen Ausprägung.
- Näheres siehe die entsprechenden Artikel zu den einzelnen Herzfehlern:
- Ventrikelseptumdefekt (VSD)
- Vorhofseptumdefekt (ASD)
- Persistierender Ductus arteriosus (PDA)
- Aortenisthmusstenose
- Aortenklappenstenose
- Fallot-Tetralogie (TOF)
- Transposition der großen Arterien (TGA)
- Hypoplastisches Linksherzsyndrom (HLHS)
- Pulmonalatresie
- Univentrikuläres Herz
- Truncus arteriosus communis
- Entscheidende Verbesserung des Überlebens durch Fortschritte der letzten 50 Jahre in Kinderkardiologie und Kinderherzchirurgie34
- Mindestens 85 % der betroffenen Neugeborenen erreichen das Erwachsenenalter.34
- Die unterschiedlichen Langzeitverläufe sind oft gekennzeichnet durch:39
- Rest- und Folgezuständen des Herzfehlers
- nichtkardiale Komorbiditäten
- Auch EMAH-Patient*innen sollte verstärkt der Nutzen präventivmedizinischer Maßnahmen nahegebracht werden: adäquater Lebensstil mit ausreichend Sport/Bewegung und gesunder Ernährung.39
Patienteninformationen
Patienteninformationen in Deximed
Patientenverbände
- Bundesverband Herzkranke Kinder e. V.: Leben mit Herzfehler
- Kinderherzen – Fördergemeinschaft Deutsche Kinderherzzentren e. V.
- Interessengemeinschaft Das herzkranke Kind e. V.
- Herzklopfen – Elterninitiative Herzkranke Kinder Südbaden e. V.
- Kinderherzstiftung: Haben Sie Fragen zum Herzfehler Ihres Kindes?
Weitere Informationen
- Eine Adressliste aller pädiatrischen und internistischen Kardiologen mit der Zusatzqualifikation EMAH enthält die Broschüre Erwachsene mit angeborenem Herzfehler der Kinderherzstiftung für Patient*innen und Ärzt*innen nichtkardiologischer Fachrichtungen wie Hausärzt*innen und Internist*innen.
- Siehe auch Artikel Beurteilung der Fahreignung.
Illustrationen


Das Herz
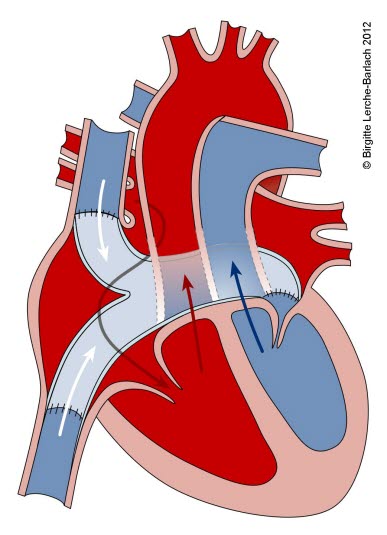
Transposition der großen Gefäße
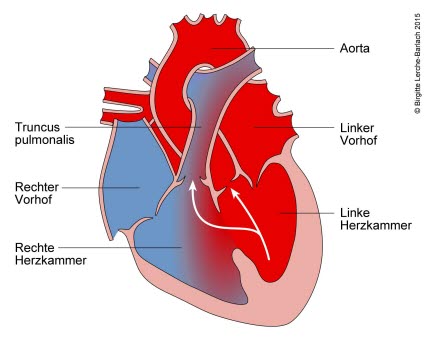
Ventrikelseptumdefekt, VSD
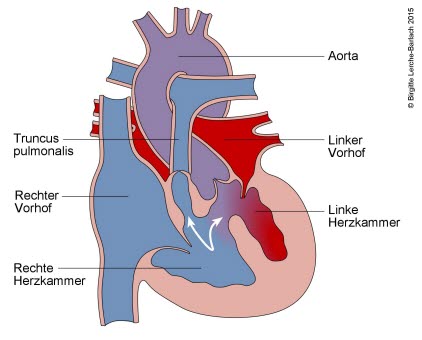
Fallot-Tetralogie
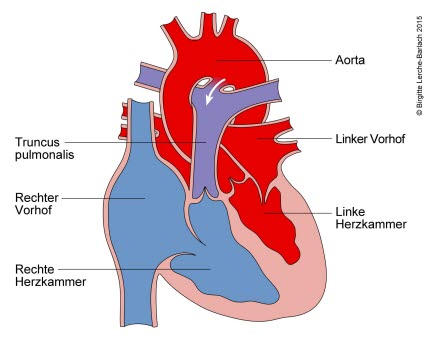
Persistierender Ductus arteriosus
Quellen
Leitlinien
- Deutsche Gesellschaft für Pädiatrische Kardiologie. S2k-Leitlinie Abklärung einer Zyanose im Kindes- und Jugendalter. AWMF-Nr. 023-002, Stand 2017. register.awmf.org
- Deutsche Gesellschaft für Pädiatrische Kardiologie. S2k-Leitlinie Abklärung eines Herzgeräusches im Kindes- und Jugendalter. AWMF-Nr. 023-001, Stand 2017. register.awmf.org
- European Society of Cardiology. Management of adult congenital heart disease. Stand 2020. www.escardio.org
Literatur
- Deutsche Gesellschaft für pädiatrische Kardiologie und angeborene Herzfehler. Atrioventrikuläre Septumdefekte (AVSD). Stand 2019. register.awmf.org
- Saenz RB, Beebe DK, Triplett LC. Caring for infants with congential heart disease and their families. Am Fam Phys 1999. pubmed.ncbi.nlm.nih.gov
- Angeborene Herzfehler - Klinische Relevanz, Überlebensrate und Häufigkeit. Kompetenznetz angeborene Herzfehler. Zugriff 31.03.23. www.kompetenznetz-ahf.de
- Deutsche Gesellschaft für Pädiatrische Kardiologie. S2k-Leitlinie Abklärung einer Zyanose im Kindes- und Jugendalter. AWMF-Nr. 023-002, Stand 2017. register.awmf.org
- European Society of Cardiology. Management of adult congenital heart disease. Stand 2020. www.escardio.org
- Drei neue Gendefekte für seltene Herzfehler gefunden. Aerzteblatt.de 02.08.2016. Zugriff 13.12.18. www.aerzteblatt.de
- Gelb B, Chung W. Complex Genetics and the Etiology of Human Congenital Heart Disease. Cold Spring Harb Perspect Med 2014; 4: a013953. www.ncbi.nlm.nih.gov
- Sifrim A, Hitz M, Wilsdon A, et al. Distinct genetic architectures for syndromic and nonsyndromic congenital heart defects identified by exome sequencing. Nat Genet 2016; 48: 1060–1065. doi:10.1038/ng.3627 DOI
- Ulmer H. Atrioventrikulärer Septumdefekt (AVSD). Deutsche Herzstiftung e.V. - Herzblatt 2/2012 (Zugriff 13.12.18). herzstiftung.de
- Haas N, Rickers C, Kozlik- Feldmann R, et al. für die Deutsche Gesellschaft für Pädiatrische Kardiologie. Aortenisthmusstenose im Kindes- und Jugendalter. AWMF-Nr. 023-010. Stand 2018. www.awmf.org
- Narchi H, Kulaylat N. Heart disease in infants of diabetic mothers. Images Paediatr Cardiol 2000; 2: 17–23. pmid:22368579 PubMed
- Levy H, Guldberg P, Güttler F, et al. Congenital heart disease in maternal phenylketonuria: report from the Maternal PKU Collaborative Study. Pediatr Res 2001;49:436-442. doi:11328945 www.ncbi.nlm.nih.gov
- Yang J, Qiu H, Qu P, et al. Prenatal Alcohol Exposure and Congenital Heart Defects: A Meta-Analysis. PLoS One 2015; 10: e0130681. doi:10.1371/journal.pone.0130681 DOI
- Koletzko B, Pietrzik K. Gesundheitliche Bedeutung der Folsäurezufuhr. Dtsch Arztebl 2004; 101: A-1670. www.aerzteblatt.de
- Ionescu-Ittu R, Marelli AJ, Mackie AS, Pilote L. Prevalence of severe congenital heart disease after folic acid fortification of grain products: time trend analysis in Quebec, Canada. BMJ 2009; 338: b1673. BMJ (DOI)
- Lynch T, Abel D. Teratogens and Congenital Heart Disease. J Diagn Med Sonogr 2015;31:310-305. doi:10.1177/8756479315598524 DOI
- Sologashvili T, Prêtre R, Ponti A, et al. Was Allgemeinärzte über Herzoperationen bei Kindern wissen müssen - Angeborene Fehlbildungen des Herzens. Schweiz Med Forum 2017;17:570-578. medicalforum.ch
- Wiesel A, Stolz G, Queisser-Wahrendorf A. Evidence for a teratogenic risk in the offspring of health personnel exposed to ionizing radiation?! Birth Defects Res A Clin Mol Teratol 2016; 106: 475-479. doi:10.1002/bdra.23532 www.ncbi.nlm.nih.gov
- Dolk H, McCullough N, Callaghan S, et al. Risk factors for congenital heart disease: The Baby Hearts Study, a population-based case- control study. PLoS ONE 2020; 15: e0227908. doi:10.1371/journal.pone.0227908 DOI
- Abdul-Khaliq H, Berger F. Angeborene Herzfehler: Die Diagnose wird häufig zu spät gestellt. Dtsch Arztebl 2011; 108: A1683. www.aerzteblatt.de
- De-Wahl Granelli A, Wennergren M, Sandberg K, et al. Impact of puls oximetry screening on the detection of duct dependent congenital heart disease: a Swedish prospective screening study in 39821 newborns. BMJ 2009; 338: a3037. BMJ (DOI)
- Deutsche Gesellschaft für Pädiatrische Kardiologie. S2k-Leitlinie Abklärung eines Herzgeräusches im Kindes- und Jugendalter. AWMF-Nr. 023-001, Stand 2017. register.awmf.org
- Ho VB. Radiologic Evaluation of suspected congenital heart disease in adults. Am Fam Physician 2009; 80: 597-602. American Family Physician
- Vollbrecht T, Luetkens J. Kardiale MRT bei angeborenen Herzfehlern - vom Fetus zum Erwachsenen. Radiologe 2022; 62: 933–940. doi:10.1007/s00117-022-01062-y DOI
- Weber R. Herzgeräusche bei Kindern - Welche müssen genauer abgeklärt werden? Allgemeinarzt - online. Zugriff 14.12.18 www.allgemeinarzt-online.de
- Punnoose A, Burke A, Golub R. Innocent (Harmless) Heart Murmurs in Children. JAMA 2012; 308: 305. doi:10.1001/jama.2012.6223 DOI
- Giuffre RM, Walker I, Vaillancourt S, et al. Opening Pandoras's box: parental anxiety and the assessment of childhood murmurs. Can J Cardiol 2002; 18: 406-14. www.ncbi.nlm.nih.gov
- Diller GP, Breithardt G, Baumgartner H. Congenital heart defects in adulthood. Dtsch Arztebl Int 2011; 108: 452-459. doi:10.3238/arztebl.2011.0452 DOI
- Kaemmerer H, Freilinger S, Neidenbach R, et al. Versorgung von Erwachsenen mit angeborenen Herzfehlern in Deutschland – tragende Rolle von Internisten und Hausärzten. Internist 2022; 63: 95-102. doi:10.1007/s00108-021-01211-w DOI
- Hernandez A, Paul T, Abrams D, et al. Arrhythmias in congenital heart disease: a position paper of the European Heart Rhythm Association (EHRA), Association for European Paediatric and Congenital Cardiology (AEPC), and the European Society of Cardiology (ESC) Working Group on Grown-up Congenital Heart Disease, endorsed by HRS, PACES, APHRS, and SOLAECE. Europace 2018; 20: 1719-1720. doi:10.1093/europace/eux380 DOI
- Schneider H, Müller M, Krause U, et al. Herzrhythmusstörungen und Langzeitprognose erwachsener Patienten mit angeborenem Herzfehler. Z Herz- Thorax- Gefäßchir 2021; 35: 126-132. doi:10.1007/s00398-021-00434-1 DOI
- Ruperti-Repilado F, Thomet C, Schwerzmann M. ESC-Leitlinie 2020 zur Behandlung von Erwachsenen mit angeborenem Herzfehler (ACHD). Herz 2021; 46: 14-27. doi:10.1007/s00059-020-05003-0 DOI
- Siaplaouras J, Albrecht C, Helm P, et al. Sportliche Aktivität mit angeborenem Herzfehler. Monatsschr Kinderheilkd 2019; 167: 51-57. doi:10.1007/s00112-017-0381-2 DOI
- Uebing A, Gatzoulis M, von Kaisenberg C, et al. Mutterschaft mit angeborenem Herzfehler. Dtsch Arztebl 2008; 105: 347-354. doi:10.3238/arztebl.2008.0347 DOI
- Register Angeborene Herzfehler: Fehlende Information - Verhütungsmethode häufig falsch gewählt. Zugriff 15.12.18 www.herzregister.de
- Vigl M, Kaemmerer M, Seiffert-Klaus V, et al. Contraception in women with congenital heart disease. Am J Cardiol 2010; 106: 1317-1321. doi:10.1016/j.amjcard.2010.06.060 DOI
- Schemm S, Schemm A, Schwenkhagen A, et al. Kontrazeption bei Frauen mit angeborenen Herzfehlern. Gynäkologe 2019; 52: 463-472. doi:10.1007/s00129-019-4432-8 DOI
- Massoth C, Zarbock A, Wenk M. Nichtkardiale Eingriffe bei Erwachsenen mit angeborenen Herzfehlern. Anaesthesist 2019; 68: 245-258. doi:10.1007/s00101-019-0575-1 DOI
- Neidenbach R, Nagdyman N, Oberhoffer R, et al. Angeborene Herzfehler im Langzeitverlauf. Pädiatrie 2017; 29: 28-33. doi:10.1007/s15014-017-0942-9 DOI
Autor*innen
- Michael Handke, Prof. Dr. med., Facharzt für Innere Medizin, Kardiologie und Intensivmedizin, Freiburg
- Die ursprüngliche Version dieses Artikels basiert auf einem entsprechenden Artikel im norwegischen hausärztlichen Online-Handbuch Norsk Elektronisk Legehåndbok (NEL, https://legehandboka.no/).