Zusammenfassung
- Definition:Gehört zur Gruppe der Fadenwürmer (Nematoden), die beim Menschen durch Kontakt mit den Eiern und Larven des Parasiten Infektionen hervorrufen und die hauptsächlich in den feuchtwarmen Böden tropischer und subtropischer Länder vorkommen.
- Häufigkeit:Mehr als 1 Mrd. Menschen sind von mindestens einer Helmintheninfektion betroffen.
- Symptome:Oft asymptomatisch, schwere Verläufe sind möglich.
- Befunde:Oft kein spezifischer klinischer Befund, doch am ehesten typisch ist ein Rektumprolaps.
- Diagnostik:Nachweis von Eiern im Stuhl.
- Therapie:Die Behandlung erfolgt mit Anthelminthika (Mebendazol).
Allgemeine Informationen
Definition
- Infektion mit Trichuris trichiura, nach seiner charakteristischen Form auch Peitschenwurm (Whipworm) genannt
Helminthen
- Die über das Erdreich übertragenen Helminthen stellen eine Gruppe parasitischer Würmer dar, die beim Menschen durch Kontakt mit den Eiern und Larven des Parasiten Infektionen hervorrufen, und die hauptsächlich in den feuchtwarmen Böden tropischer und subtropischer Länder vorkommen.1-2
- Die adulten Würmer können über Jahre hinweg im menschlichen Verdauungstrakt leben.
- Die drei dominierenden Helmintheninfektionen sind Ascariasis, Trichuriasis und Ankylostomiasis. Diese treten oft zusammen auf, und insbesondere Kinder sind häufig mit allen drei Helminthen chronisch infiziert.3
Häufigkeit
- Prävalenz
Peitschenwurm
- Geografische Verbreitung
- Trichuriasis ist eine weltweit häufig vorkommende intestinale Helmintheninfektion.
- Für Deutschland liegen keine epidemiologischen Daten vor. Bei Einreisenden aus Endemiegebieten mit entsprechenden Symptomen, sollte an die Möglichkeit einer Infektion gedacht werden.
- Prävalenz
- Überwiegend in subtropischen und tropischen Regionen, wobei große regionale Unterschiede festzustellen sind.5
- In Endemiegebieten sind mitunter mehr als 90 % der Individuen von der Infektion betroffen.
- Betroffene Altersgruppen
- Vor allem Kinder zwischen 5 und 15 Jahren sind betroffen. Dies ist wahrscheinlich auf die hohe Exposition in dieser Altersklasse und eine später einsetzende partielle Immunität zurückzuführen.5
Ätiologie und Pathogenese
Infektionszyklus

Trichuris, zweigeschlechtlich
- Infizierte Individuen scheiden Eier aus, die 2–4 Wochen im Erdboden zu einer infektiösen Form heranreifen.
- Diese Eier werden dann z. B. über verschmutztes Wasser oder Nahrungsmittel oral aufgenommen und gelangen so in den Dickdarm, wo sie zu Larven heranreifen.5
- Die Würmer paaren sich und das Weibchen produziert bis zu 200.000 Eier pro Tag, die über den Stuhl ausgeschieden werden.
- Die adulten Würmer sind 3–5 cm lang und haben eine Lebenserwartung von 1–8 Jahren.5
- Frühestens nach 3 Monaten können die Eier im Stuhl einer infizierten Person nachgewiesen werden.3
- Eine direkte Übertragung von Mensch zu Mensch ist nicht möglich.
Prädisponierende Faktoren
- Klima: feuchte tropische und subtropische Regionen
- Schlechte sanitäre Bedingungen6
ICPC-2
- D96 Würmer / andere Parasiten
ICD-10
- B79 Trichuriasis
Diagnostik
Diagnostische Kriterien
- Diagnosesicherung erfolgt durch den mikroskopischen Nachweis der Wurmeier im Stuhl.
Differenzialdiagnosen
Anamnese
- Symptomausprägung ist abhängig von der Erregerlast.
- Bei nur wenigen Würmern sind die Infektionen oft asymptomatisch.
- Bei höherer Wurmlast5
- Diarrhö, teilweise blutig
- abdominelle Schmerzen
- Gewichtsverlust
- Schwächegefühl
- Appetitlosigkeit
- seltener: Urtikaria
- Bei massivem Befall kann es zu einem Trichuris Dysentery Syndrome (TDS) kommen.5,7
- chronische schleimig-blutige Diarrhö
- ausgeprägte Eisenmangelanämie mit entsprechenden Symptomen
- körperliche und kognitive Entwicklungsverzögerung
Klinische Untersuchung
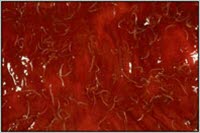
Trichuris im Darm
- Der Peitschenwurm ist dünn und 3–5 cm lang.
- Der am ehesten typische Befund ist ein Rektumprolaps.3
- Dieser tritt hauptsächlich bei stark infizierten Personen auf, ggf. können ebenfalls adulte Würmer festgestellt werden.
- Trommelschlegelfinger
- Anämiezeichen
Ergänzende Untersuchungen in der Hausarztpraxis

Trichuriasis, Eier
- Stuhlprobe zum mikroskopischen Nachweis der charakteristischen Eier5
- Die Eier bei der Trichuriasis haben eine charakteristische zylindrische Form. Sie sind 20 x 50 µm groß, glatt und dickschalig und haben hyaline Verdickungen an beiden Enden.
- Evtl. okkultes Blut im Stuhl
- Evtl. Eisenmangelanämie
- Evtl. Eosinophilie
Therapie
Therapieziel
- Den Parasiten eliminieren (bzw. die Parasitenbelastung in Endemiegebieten reduzieren).
Allgemeines zur Therapie
- Individuell
- Anthelminthika8
- Mebendazol
- Albendazol (in Deutschland erst ab 6 Jahren zugelassen)
- ggf. Behandlung von Mangelerscheinungen
- Anthelminthika8
- Global
- Verbesserung der sanitären Bedingungen und Trinkwasserversorgung in Endemiegebieten
- Gesundheitsaufklärung
- Chemoprophylaxe
Medikamentöse Therapie
- Mebendazol 2 x 100 mg oder 1 x 500 mg über 3 Tage9
- Ist wirksam, aber in der Schwangerschaft während des ersten Trimenons kontraindiziert und sollte nur mit Vorsicht während des 2. und 3. Schwangerschaftstrimenons angewandt werden.
- Anwendung bei Kindern unter 2 Jahren nicht empfohlen
- evtl. Wiederholung der Behandlung nach 2 Wochen
- Albendazol 1 x 400 mg für 3 Tage
- Laut embryotox.de sollten im 1. Trimenon einer Schwangerschaft andere Medikamente bevorzugt werden.
- Weniger wirksam: Ivermectin 200 µg/kg KG für 3 Tage
- Soll laut Fachinformation im 1. Trimenon einer Schwangerschaft nur angewendet, wenn es „eindeutig erforderlich“ ist.
- in Deutschland „off label“
Prävention
- Verbesserung der sanitären Bedingungen in Endemiegebieten6
- Die Entwicklung von Impfstoffen sieht sich vor große Probleme gestellt; mit einer Verfügbarkeit ist daher in absehbarer Zeit nicht zu rechnen.10
- Die WHO empfiehlt für Endemiegebiete die regelmäßige medikamentöse Prophylaxe mit Mebendazol (500 mg) oder Albendazol (400 mg) für vulnerable Gruppen wie Schulkinder und Schwangere. 2020 wurden so über 436 Mio. Kinder in Endemiegebieten behandelt.2
Verlauf, Komplikationen und Prognose
Verlauf
- Bei schwerer Infektion mit Entwicklungsverzögerungen und Malassimilation besteht das Risiko weiterer Infektionen.
Prognose
- Trichuris trichiura ist resistenter gegenüber Antihelminthika als andere Parasiten, deshalb kann eine vollständige Eradikation nicht immer erreicht werden. Aber auch eine Reduktion der Wurmzahl kann zu einer deutlichen Besserung der Symptome führen.3
- Es besteht das Risiko einer Reinfektion, deswegen werden regelmäßige Behandlungen in Endemiegebieten empfohlen.11
Patienteninformationen
Patienteninformationen in Deximed
Illustrationen

Trichuris, zweigeschlechtlich
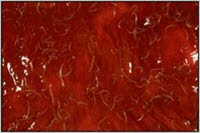
Trichuris im Darm

Trichuriasis, Eier
Quellen
Literatur
- Bethony J, Brooker S, Albonico M, et al. Soil-transmitted helminth infections: ascariasis, trichuriasis, and hookworm. Lancet 2006; 367: 1521-32. PubMed
- WHO. Soil-transmitted helmith infections. 2022, online abgerufen am 19.11.2022. www.who.int
- Viswanath A, Yarrarapu SNS, Williams M. Trichuris Trichiura. [Updated 2022 Aug 22]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2022 www.ncbi.nlm.nih.gov
- Statistisches Bundesamt. Diagnose der Krankenhauspatienten in Deutschland, online abgefragt am 19.11.2022. www-genesis.destatis.de
- Else KJ, Keiser J, Holland CV, et al. Whipworm and roundworm infections. Nat Rev Dis Primers 6, 44 (2020). www.nature.com
- Strunz EC, Addiss DG, Stocks ME, et al. Water, sanitation, hygiene, and soil-transmitted helminth infection: a systematic review and meta-analysis. PLoS Med. 2014 Mar 25;11(3):e1001620. www.ncbi.nlm.nih.gov
- Mohamed, Z, Zueter, A Zairi, et al. Trichuris dysentery syndrome: Do we learn enough from case studies? Tropical Biomedicine 32(3):1-6, 2015. www.researchgate.net
- Mejia R. Anthelminthic therapies. UpToDate, last updated Aug 25, 2021. www.uptodate.com
- Kurth F, Suttorp N. Trichuriasis. In: Suttorp N, Möckel M, Siegmund B, Dietel M, Hrsg. Harrisons Innere Medizin. 20. Auflage. Berlin: ABW Wissenschaftsverlag; 2020 eref.thieme.de
- Zawawi A, Else KJ. Soil-Transmitted Helminth Vaccines: Are We Getting Closer? Front Immunol. 2020 Sep 30;11:576748 www.ncbi.nlm.nih.gov
- Landeryou T, Maddren R, Rayment Gomez S, et al. Longitudinal monitoring of prevalence and intensity of soil-transmitted helminth infections as part of community-wide mass drug administration within the Geshiyaro project in the Bolosso Sore district, Wolaita, Ethiopia. PLoS Negl Trop Dis. 2022 Sep 19;16(9). pubmed.ncbi.nlm.nih.gov
Autor*innen
- Bonnie Stahn, Dr. med, Fachärztin für Allgemeinmedizin, Hamburg
- Die ursprüngliche Version dieses Artikels basiert auf einem entsprechenden Artikel im norwegischen hausärztlichen Online-Handbuch Norsk Elektronisk Legehåndbok (NEL, https://legehandboka.no/).