Zusammenfassung
- Definition:Eine Aortendissektion bezeichnet eine Verletzung der inneren Gefäßwand der Aorta mit Einblutung zwischen die Gefäßwandschichten. Abhängig von der Lokalisation unterscheidet man Dissektionen Typ A nach Stanford mit Beteiligung der Aorta ascendens und/oder des Aortenbogens und Typ B nach Stanford, die sich auf die Aorta descendens beschränken.
- Häufigkeit:Die Inzidenz von Aortendissektionen liegt bei etwa 6/100.000 Fälle pro Jahr, wobei Typ-A-Dissektionen häufiger auftreten.
- Symptome:Typisch sind plötzliche, stärkste Brustschmerzen, seltener auch Rücken- oder Bauchschmerzen. Durch Minderperfusion der Aortenäste kann es zu Organschädigung und vielseitigen weiteren Symptomen kommen.
- Befunde:Bei schweren Verläufen Kreislaufinstabilität bis zum Schock. Im Übrigen oft arterieller Hypertonus, Blutdruck- oder Pulsdifferenz beider Arme, Pulsdefizit, neu aufgetretenes Diastolikum bei Aortenklappeninsuffizienz.
- Diagnostik:Zeitnahe Diagnostik zum Ausschluss anderer Differenzialdiagnosen und Nachweis der Aortendissektion mittels bildgebender Untersuchung (CT-Angiographie, Echokardiografie, seltener MRT)
- Therapie:Behandlung in einem spezialisierten Zentrum. Bei Typ-A-Dissektionen unverzügliche chirurgische Therapie mit Implantation einer Aortenprothese. Bei Typ-B-Dissektion konservative Therapie oder endovaskuläre Therapie, seltener chirurgische Therapie.
Allgemeine Informationen
Definition
- Eine akute Aortendissektion (AAD) bezeichnet eine Verletzung der aortalen Gefäßwand mit intramuraler Einblutung und Auftrennung der Gefäßwandschichten.1-4
- wichtigste Entität des akuten Aortensyndroms (AAS)
- seltenes, jedoch akutes und lebensbedrohliches Krankheitsbild
- Einteilung nach Lokalisation entsprechend der Stanford-Klassifikation1-2
- Stanford-Typ A: mit Beteiligung der Aortenwurzel und Aorta ascendens
- Stanford-Typ B: beginnt im absteigenden Ast der Aorta ohne Beteiligung der Aorta ascendens
- Klinisch manifestiert sich eine Aortendissektion mit plötzlichem, starkem, restrosternalem Brustschmerz bzw. Rückenschmerzen
- abhängig von der Lokalisation ggf. Ausstrahlung zwischen die Schulterblätter bzw. in Abdomen und Rücken
- Komplikationen der Aortendissektion
- Aortenruptur
- Ischämien in versorgten Organen und Extremitäten, z. B. ischämischer Schlaganfall
- hämorrhagischer bzw. kardiogener Schock
- Herzbeteiligung mit Aortenklappeninsuffizienz und Perikarderguss
- Die bildgebende Untersuchung der Wahl zum Nachweis einer Aortendissektion ist in der Regel die CT-Angiografie.2
- Die Therapie sollte an einem Zentrum mit Herz- bzw. Gefäßchirurgie erfolgen.
- Möglichkeit der chirurgischen, endovaskulären oder konservativen Therapie abhängig vom Befund und des individuellen Risikos2
- Unbehandelt ist die Letalität sehr hoch.
Akutes Aortensyndrom (AAS)3-4
- Akutes Krankheitsbild der Aorta, charakterisiert durch Notfallsituationen mit ähnlichen klinischen Charakteristika
- Umfasst folgende Entitäten:
- akute Aortendissektion (AAD)
- intramurales Aortenhämatom (IMH)
- penetrierendes Aortenulkus (PAU)
- traumatische Aortenverletzungen (TAV)
Häufigkeit
- Populationsbezogene Erhebung der Region Oxford2,5
- Inzidenz von 6/100.000 pro Jahr
- Stanford-Typ-A-Dissektionen mit 71,2 %
- Stanford-Typ-B-Dissektionen mit 28,8 %
- Inzidenz von 6/100.000 pro Jahr
- Inzidenz abhängig von vorbekannter arterieller Hypertonie1,6
- 21/100.000 pro Jahr bei Menschen mit arterieller Hypertonie
- 5/100.000 pro Jahr bei Menschen ohne arterielle Hypertonie
- Erkrankungsgipfel > 50. Lebensjahr2
- Männer sind häufiger betroffen als Frauen.2
Ätiologie und Pathogenese
Ätiologie
- Chronische Schädigung oder Schwächung der Gefäßwand der Aorta
- z. B. durch arterielle Hypertonie
- Durch zunehmende Dilatation vermehrter Wandstress
- Letztlich akute Wandeinblutung bzw. Dissektion
Pathogenese
- Bei einer akuten Aortendissektion kommt es zum Einriss der innersten Gefäßwandschicht, der Intima, z. T. auch der Media.
- In diese Aufspaltung der Gefäßwand tritt das strömende Blut ein (Entry).
- Aufspaltung in der Regel in Richtung des Blutstroms
- Durch fortschreitende Aufspaltung entstehen zwei Lumina, das wahre und falsche Gefäßlumen, die durch die Dissektionsmembran voneinander getrennt sind.
- Bei einem ggf. vorhandenen distalen, erneuten Intimaeinriss kann es zum Wiedereintritt des Blutes aus dem falschen in das richtige Lumen kommen (Re-Entry).
Klassifikation
- Stanford-Klassifikation2,4
- Typ-A-Aortendissektionen
- Alle Dissektionen, die auch die Aorta ascendens betreffen.
- Typ-B-Aortendissektion
- Beginn distal der linken A. subclavia ohne Beteiligung der Aorta ascendens
- Typ-A-Aortendissektionen
- DeBakey-Klassifikation2,4
- Typ DeBakey I
- Beteiligung der Aorta ascendens und descendens
- Typ DeBakey II
- Dissektion nur der Aorta ascendens
- Typ DeBakey III
- Dissektion nur der Aorta descendens
- Typ IIIa: Beschränkt sich auf die deszendierende thorakale Aorta.
- Typ IIIb: Ausdehnung bis unterhalb des Zwerchfells
- Typ DeBakey I
- Einteilung nach klinischem Verlauf1,3-4
- akute Aortendissektion: ≤ 14 Tage
- subakute Aortendissektion: 15–90 Tage
- chronische Aortendissektion: > 90 Tage
- Klassifikation der akuten Aortensyndrome (AAS)1,3-4
- Klasse 1: klassische Aortendissektion (AD)
- Klasse 2: intramurales Aortenhämatom (IMH)
- Klasse 3: umschriebene/diskrete Aortendissektion mit Vorwölbung
- Klasse 4: penetrierendes Aortenulkus (PAU) nach Plaqueruptur
- Klasse 5: iatrogene oder traumatische Aortenverletzungen (TAV)
Prädisponierende Faktoren
- Der gesamte Abschnitt basiert auf diesen Referenzen.1,7
- Arterielle Hypertonie1-4,7
- wichtigster Risikofaktor
- bei etwa 70 % der Betroffenen1-2
- Atherosklerose
- Aortenaneurysma
- Diabetes mellitus1,7
- Rauchen2
- Erbliche Bindegewebserkrankungen1
- Marfan-Syndrom (MFS)
- Ehlers-Danlos-Syndrom (EDS)
- familiäre Form der thorakalen Aortenaneurysmen und Aortendissektionen
- Erbliche Vaskulopathien
- Entzündliche Gefäßerkrankungen1
- Riesenzellarteriitis
- Takayasu-Arteriitis
- systemischer Lupus erythematodes
- rheumatische Aortitis
- Morbus Behçet
- Syphilis
- mykotische Aortitis
- Morbus Ormond (retroperitoneale Fibrose)
- Iatrogene Dissektion
- z. B. Katheterinterventionen bzw. Aortenklappen-/Aortenoperation
- Substanzmissbrauch (z. B. Kokain)
- Einnahme von Fluorchinolonen8-9
- Aktuelle Daten relativieren diesen Zusammenhang allerdings.10
ICPC-2
- K99 Herz-/Gefäßerkrankung, andere
ICD-10
- I71.-: Aortenaneurysma und -dissektion
I71.0-: Dissektion der Aorta - I71 Aortenaneurysma und -dissektion
- I71.0 Dissektion der Aorta [jeder Abschnitt]
- I71.1 Aneurysma der Aorta thoracica, rupturiert
- I71.3 Aneurysma der Aorta abdominalis, rupturiert
- I71.5 Aortenaneurysma, thorakoabdominal, rupturiert
- I71.8 Aortenaneurysma nicht näher bezeichneter Lokalisation, rupturiert
- Q25 Angeborene Fehlbildungen der großen Arterien
- Q25.4 Sonstige angeborene Fehlbildungen der Aorta
Diagnostik
Diagnostische Kriterien
Leitlinie: Diagnostik bei V. a. Aortendissektion2-4
- Klinischer Verdacht auf ein akutes Aortensyndrom
- Labordiagnostik (s. u.)
- Bildgebende Diagnostik
- Vorrangige Untersuchungen sind CT, MRT und TEE.
- CT-Angiografie bzw. MR-Angiografie
- zur optimalen Einschätzung der Dissektionsausdehnung
- überlegen für Diagnose von IMH, PAU undTAV
- transösophageale Echokardiografie (TEE)
- bessere Darstellung des Blutflusses und der Lokalisation von Einrissen
- geeignet für instabile Patient*innen und für die Überwachung von Veränderungen (intraoperativ/intensivmedizinisch)
Risikoscore zur Erhöhung der Vortestwahrscheinlichkeit4,11
- Risiko-Score von 0–3 Punkte (je 1 Punkt pro positive Kategorie)
- Hochrisiko-Anamnese
- Marfan-Syndrom (oder andere Bindegewebserkrankungen)
- Familienanamnese für Aortenerkrankungen
- bekannte Aortenklappenerkrankung
- bekanntes thorakales Aortenaneurysma
- vorangegangene Manipulation im Bereich der Aorta (einschl. herzchirurgischer Eingriff)
- Hochrisiko-Schmerzmerkmale
- Hochrisiko-Untersuchungsmerkmale
- Evidenz eines Perfusionsdefizits
- Pulsdefizit
- Unterschiede im systolischen Blutdruck
- fokale neurologische Defizite (im Zusammenhang mit entsprechendem Schmerz)
- diastolisches Herzgeräusch über Erb (neu und im Zusammenhang mit entsprechendem Schmerz)
- Hypotension oder Schock
- Evidenz eines Perfusionsdefizits
Differenzialdiagnosen
- Akutes Koronarsyndrom (ACS)
- Aortenaneurysma
- Mesenterialischämie
- Lungenembolie
- Pyelonephritis
- Nierensteine
- Rückenmarksverletzung
- Andere Ursachen von akuten Brustschmerzen
- Andere Ursachen eines akuten Abdomens
Anamnese
- Akuter Beginn der Beschwerden
- Klinische Beschwerden1,3-4,7,12-13
- akute Brustschmerzen oder Rückenschmerzen
- abruptes Einsetzen des Schmerzes
- Lokalisation besonders retrosternal und zwischen den Schulterblättern
- Wandern des Schmerzes
- stärkster jemals erlebter Schmerz („Vernichtungsschmerz")
- Bauchschmerzen
- Synkope
- Schock
- akute Brustschmerzen oder Rückenschmerzen
- Akute Komplikationen3-4,13
- Aortenklappeninsuffizienz
- Herzbeuteltamponade
- Myokardinfarkt
- akute Herzinsuffizienz
- Pleuraerguss
- neurologische Defizite (Koma, Schlaganfall)
- Rückenmarksverletzung
- Mesenterialischämie mit akuten Bauchschmerzen
- akutes Nierenversagen
- Ischämie der unteren Extremitäten
- Klinische Merkmale einer Bindegewebserkrankung (z. B. Hochwuchs bei Marfan Syndrom)
- Familienanamnese mit Aortenerkrankungen2
Klinische Untersuchung
- Allgemeine körperliche Untersuchung inkl. Vitalparameter
- oft erhöhter Blutdruck (ca. 50 %)12
- Zeichen eines Schocks
- Blutdruckdifferenz (ca. 15 %)1,12,14
- Seitendifferenz in Puls oder Blutdruck zwischen den Armen
- Pulsdefizit (ca. 19 %)2
- Differenz zwischen Herzfrequenz und tastbarer Pulsfrequenz
- Diastolisches Herzgeräusch1,12
- Ausdruck einer Aortenklappeninsuffizienz bei Typ-A-Dissektion
- Zeichen eines Perikardergusses oder einer Perikardtamponade (ca. 13 %)1
- gestaute Halsvenen, paradoxer Puls und arterielle Hypotonie
- Klinische Zeichen einer Bindegewebserkrankung
- z. B. Marfan-Syndrom (MFS) oder Ehlers-Danlos-Syndrom (EDS)
Diagnostik bei Spezialist*innen
Labordiagnostik
- Erforderliche Laborparameter3-4
- Blutbild
- C-reaktives Protein (CRP), Procalcitonin
- Entzündung, SIRS, Sepsis
- Creatinkinase (CK)
- Reperfusionsschaden, Rhabdomyolyse
- Troponin I oder T
- Myokardischämie, Myokardinfarkt
- D-Dimere
- erhöht bei Aortendissektion, Lungenembolie, Thrombose
- hohe Spezifität, somit zum Ausschluss einer Aortendissektion geeignet3-4
- Kreatinin, GOT, GPT, Laktat, Glukose
- Blutgase
- metabolische Störung, Oxygenierung
EKG
- Ausschluss anderer Erkrankungen mit Primärsymptom Brustschmerz (z. B. Herzinfarkt)
- Ggf. Nachweis ischämietypischer EKG-Veränderungen auch bei Aortendissektion
- Bei Typ-A-Dissektionen und Beteiligung der Koronargefäße kann es zum Herzinfarkt kommen.
- Unauffälliges EKG bei 38 % der Typ-B-Dissektionen2
Bildgebende Diagnostik
- Ziel der akuten bildgebenden Diagnostik4
- differenzialdiagnostische Abklärung
- Nachweis einer Dissektionslamelle, die 2 Lumina
innerhalb der Aorta trennt, als Beweis einer Aortendissektion.
- Transthorakale Echokardiografie (TTE)
- als initiales bildgebendes Verfahren in allen Verdachtsfällen empfohlen2-4
- CT, MRT und TEE sind gleichermaßen zuverlässig in Bestätigung oder Ausschluss einer akuten Aortendissektion (AAD).4,15
- CT-Angiografie
- transösophageale Echokardiografie (TEE) MR-Angiografie
- Wiederholung der Bildgebung bei:4
- negativem Befund und fortbestehendem klinischem Verdacht
- bei unkomplizierter Typ-B Aortendissektion und konservativer Behandlung
- Röntgen des Thorax
Indikationen zur Klinikeinweisung
- Sofortige Krankenhauseinweisung bei Verdacht auf die Erkrankung
- Transport in notärztlicher Begleitung in ein Herz- und Gefäßzentrum mit notwendiger Expertise1-2
- Das Krankenhaus sollte vorab informiert werden.
Therapie
Therapieziele
- Vitalfunktionen stabilisieren.
- Suffiziente Schmerztherapie
- Komplikationen vermeiden.
- Grundlegende Therapiekonzepte erstellen:
- operative oder endovaskuläre Versorgung der Dissektion
- konservative Therapie.
Allgemeines zur Therapie
- Behandlung in einem Herz- und Gefäßzentrum mit Expertise in operativen und endovaskulären Therapieverfahren1-2
- In der Regel intensivmedizinische Überwachung und Behandlung
- engmaschige Überwachung der Vitalfunktionen
- immer begleitend medikamentöse Therapie (Analgesie, Blutdrucksenkung)
- Therapiekonzept abhängig vom Typ und Lokalisation der akuten Aortendissektion
- Typ-A-Aortendissektion4,16
- Notfallindikation zur chirurgischen Therapie
- unkomplizierte Typ-B-Aortendissektion2,4
- konservative Therapie empfohlen
- ggf. endovaskuläre Therapie (TEVAR)
- komplizierte Typ-B-Aortendissektion2-4
- endovaskuläre Therapie (TEVAR) empfohlen
- ggf. chirurgischer Eingriff
- Berücksichtigung individueller klinischer und anatomischer Aspekte2
- Typ-A-Aortendissektion4,16
Leitlinie: Empfehlungen für die Behandlung der Aortendissektion2-4
- Bei allen Patient*innen mit Aortendissektion wird eine medikamentöse Therapie einschließlich Schmerzstillung und Blutdruckeinstellung empfohlen (I/C).
- Bei Patient*innen mit Typ-A-Aortendissektion wird ein dringlicher chirurgischer Eingriff empfohlen (I/B).
- Bei Patient*innen mit akuter Typ-A-Aortendissektion und einer Malperfusion von Organen sollte ein Hybrid-Eingriff (d. h. Ersatz der Aorta ascendens und/oder des Aortenbogens zusammen mit einer perkutanen zusätzlichen aortalen oder arteriellen Seitenastprozedur) erwogen werden (IIa/B).
- Bei unkomplizierter Typ-B-Aortendissektion wird empfohlen, immer eine medikamentöse Therapie durchzuführen (I/C).
- Bei unkomplizierter Typ-B-Aortendissektion sollte zusätzlich eine thorakale endovaskuläre Aortenreparatur (TEVAR) erwogen werden (IIa/B).
- Bei komplizierter Typ-B-Aortendissektion wird eine thorakale endovaskuläre Aortenreparatur (TEVAR) empfohlen (I/C).
- Bei komplizierter Typ-B Aortendissektion kann ein chirurgischer Eingriff erwogen werden (IIb/C).
Medikamentöse Therapie
Blutdrucksenkung
- Ziel der Blutdrucksenkung2,4
- Senkung des systolischen Blutdrucks auf < 120 mmHg bzw. auf das niedrigste Niveau, um die vitalen Funktionen aufrechtzuerhalten.
- Eingesetzte intravenöse Antihypertensiva2,7
- Betablocker (z. B, Esmolol, Metoprolol)
- Vasodilatatoren (z. B. Labetolol, Nitroprussid)
- Im weiteren Verlauf Umstellung auf eine orale antihypertensive Medikation2
- Senkung auf 130/80 mmHg und tiefer (wenn toleriert)
- In den meisten Fällen ist eine Kombinationstherapie mit mehreren Antihypertensiva notwendig.1
Analgesie
- Suffiziente Analgesie, z. B. mit Opioidanalgetika (Morphin)1
Operative Therapie
Aortendissektion Typ A
- Indikation zur unverzüglichen chirurgischen Therapie3-4
- Offen chirurgischer Ersatz der Aorta mit Aortenprothese aus Kunststoff1
- Ein häufig eingesetztes Material für Gefäßprothesen ist das Polymer Dacron.
- auch klappentragendes Conduit verfügbar (Gefäßprothese mit Herzklappe)
- Bei langen Dissektionen bis in die distale Aorta Einsatz einer Gefäßprothese mit frei flottierendem distalen Ende in der Aorta descendens, das in einem Zweiteingriff an eine weitere Prothese angeschlossen wird (Elephant-Trunk-Technik).1
- Aufrechterhaltung des Kreislaufs durch Herz-Lungen-Maschine
- Ggf. weitere herz- und gefäßchirurgische Maßnahmen (z. B. Aortenklappenreparatur)
- Bei Malperfusion mit Organschädigung kommen ggf. Hybrid-Eingriffe zum Einsatz.4
- offen chirurgischer Ersatz der Aorta ascendens und/oder des Aortenbogens
- parallel perkutane aortale oder arterielle Seitenastprozedur
Aortendissektion Typ B
- Mögliche Indikation bei komplizierter akuter Aortendissektion Typ B2-3
- Es fehlen randomisierte Studien, die ein endovaskuläres oder offenes Vorgehen bei akuter komplizierter Typ-B-Dissektion vergleichen.2
Endovaskuläre Therapie
Thorakale endovaskuläre Aortenreparatur (TEVAR)
- Indikationen
- komplizierte Typ-B-Aortendissektion2-4
- ggf. bei unkomplizierter Typ-B-Aortendissektion und Risikokonstellationen, z. B.:
- großer Aortendurchmesser
- unkontrollierbare Schmerzen
- therapierefraktäre arterielle Hypertonie
- Risikofaktoren für eine chronische Expansion.
- Verfahren
- Zugang über die A. femoralis communis
- intraluminale Platzierung eines Stentgrafts1
- zum Abdecken der Eintrittsstelle der Dissektion (Entry)
- Verhindert Kompression des wahren Lumens durch das unter Druck stehende falsche Lumen.
- Führt zur Thrombosierung des falschen Lumens.
- Gefahr der Verlegung von Arterienästen der Aorta
Weitere spezielle Verfahren2
- Implantation von Dissektionsstents (PETTICOAT-Technik)
- Endovaskuläre Fenestration
- Elephant-Trunk-Techniken
- Verfahren zur Revaskularisation einzelner Aortenäste
Prävention
- Behandlung von Grunderkrankungen und Risikofaktoren
- Blutdruckeinstellung bei arterieller Hypertonie
- Blutzuckereinstellung bei Diabetes mellitus
- Nikotinkarenz
- Regelmäßige Kontrollen bei Aortenaneurysma
Verlauf, Komplikationen und Prognose
Verlauf
- Die Erkrankung beginnt mit plötzlich auftretenden Schmerzen im Bauch-/Rückenbereich.
- Es kommt häufig zu einer schnellen Progression, die dazu führt, dass die Patient*innen einen Schock erleiden und versterben.
Komplikationen
- Komplikationen der Aorta1
- Ruptur der Aorta (Ruptur des falschen Lumens)
- rasche Expansion der Aorta
- Aortenklappeninsuffizienz
- Perikardtamponade
- Bei Typ-A-Dissektion kann es zu einem hämorrhagischen Perikarderguss mit Herzbeuteltamponade kommen.
- Hämorrhagischer Pleuraerguss
- Akute Herzinsuffizienz
- Arterielle Hypotonie, Kreislaufinstabilität, Schock
- Malperfusion der aortalen Äste mit Organversagen1-4
- Myokardinfarkt
- ischämischer Schlaganfall
- Mesenterialischämie
- renale Ischämie mit akutem Nierenversagen
- spinale Ischämie mit Querschnittsyndrom
- eine der schwerwiegendsten Komplikationen2
- Ischämie der Extremitäten
- zerebrale Minderperfusion mit neurologischen Defiziten bis zum Koma
- Therapierefraktäre Hypertonie2
- fortbestehende Hypertension trotz Gabe von 3 verschiedenen Antihypertensiva
- Zeichen der Instabilität oder der renalen Malperfusion
Prognose
- Stanford Typ-A-Dissektion
- Unkomplizierte Stanford Typ-B-Dissektion mit konservativer Therapie2,17
- 30-Tage-Letalität von 2,4 %
- Überlebensrate nach 1 Jahr von 86,2–100 %
- Überlebensrate nach 5 Jahren von 59–97,2 %
- Komplizierte Stanford Typ-B-Dissektion mit endovaskulärer Therapie2,17
- 30-Tage-Letalität von 7,3 %
- Überlebensraten nach 1 Jahr von 62–100 %
- Überlebensraten nach 5 Jahren von 61–87 %
Verlaufskontrolle
- Regelmäßige klinische Verlaufskontrollen, z. B. 1 und 6 Monate nach Ereignis und anschließend in jährlichen Intervallen1,3
- Nach Rekonstruktion von Herzklappen jährliche Echokardiografie1
- Nach Reimplantation der Koronararterien ergometrische Verlaufskontrollen und bei klinischer Symptomatik ggf. Koronarangiografie
- Risikofaktoren für Progredienz der Dissektion, Aneurysmabildung
oder Ruptur1- Durchmesser der Aorta
- unzureichend behandelter arterieller Hypertonus
- perfundiertes falsches Lumen
- fortgeschrittenes biologisches Alter
Patienteninformationen
Patienteninformationen in Deximed
Illustrationen
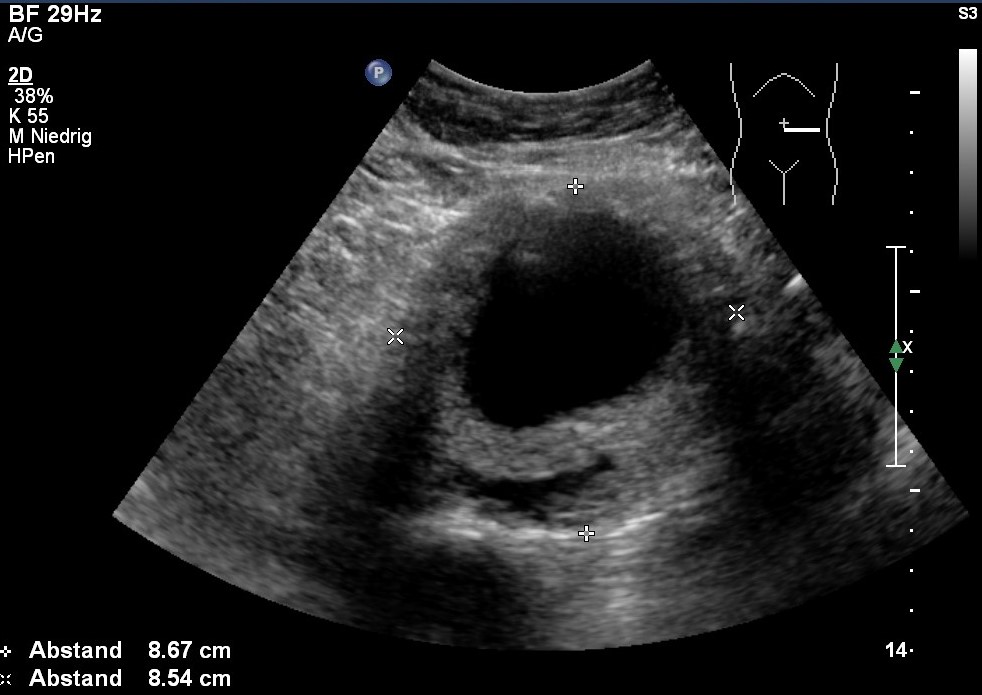
Bauchaortenaneurysma mit Dissektion in der Sonografie (mit freundlicher Genehmigung von sonographiebilder.de ©Albertinen-Diakoniewerk e. V., Hamburg).
Quellen
Leitlinien
- Deutsche Gesellschaft für Gefäßchirurgie und Gefäßmedizin (DGG). Typ B Aortendissektion. AWMF-Leitlinie Nr. 004–034. S2k, Stand 2018. www.awmf.org
- Deutsche Gesellschaft für Kardiologie (DGK). Pocket-Leitlinie: Aortenerkrankungen. Stand 2014. www.dgk.de
- European Society of Cardiology (ESC). Aortic Diseases Guidelines. Stand 2015. www.escardio.org
Literatur
- Weigang, E; Nienaber, CA.; Rehders, TC.; Ince, H; Vahl, C-F; Beyersdorf, F. Management von Patienten mit Aortendissektion. Dtsch Arztebl 2008; 105(38): 639-45. doi:10.3238/arztebl.2008.0639 DOI
- Deutsche Gesellschaft für Gefäßchirurgie und Gefäßmedizin (DGG). Typ B Aortendissektion. AWMF-Leitlinie Nr. 004–034, Stand 2018. www.awmf.org
- European Society of Cardiology (ESC). Aortic Diseases Guidelines. Stand 2015. www.escardio.org
- Deutsche Gesellschaft für Kardiologie (DGK). Pocket-Leitlinie: Aortenerkrankungen. Stand 2014. leitlinien.dgk.org
- Howard DP, Banerjee A, Fairhead JF, et al. Population-based study of incidence and outcome of acute aortic dissection and premorbid risk factor control: 10-year results from the Oxford Vascular Study. Circulation. 2013;127(20):2031-2037. doi:10.1161/CIRCULATIONAHA.112.000483 pubmed.ncbi.nlm.nih.gov
- Olsson C, Thelin S, Stahle E, et al. Thoracic aortic aneurysm and dissection: increasing prevalnece and improved outcomes reported in a nationwide population-based study of more than 14000 cases from 1987 to 2002 . Circulation 2006; 114: 2611-8. pubmed.ncbi.nlm.nih.gov
- Pape LA, Awais M, Woznicki EM. Presentation, Diagnosis, and Outcomes of Acute Aortic Dissection: 17-Year Trends From the International Registry of Acute Aortic Dissection. J Am Coll Cardiol 2015 Jul 28; 66(4): 350-8. pmid:26205591 PubMed
- Singh S, Nautiyal A. Aortic Dissection and Aortic Aneurysms Associated with Fluoroquinolones: a Systematic Review and Meta-Analysis of Observational Studies. Am J Med 2017. pmid:28739200 PubMed
- Pasternak B, Inghammar M, Svanström H. Fluoroquinolone use and risk of aortic aneurysm and dissection: Nationwide cohort study. BMJ 2018 Mar 8; 360: k678. pmid: 29519881 PubMed
- Gopalakrishnan C, Bykov K, Fischer MA, Connolly JG, Gagne JJ, Fralick M. Association of Fluoroquinolones With the Risk of Aortic Aneurysm or Aortic Dissection. JAMA Intern Med. 2020. PMID: 32897307. pubmed.ncbi.nlm.nih.gov
- Rogers AM, Hermann LK, Booher AM, et al. Sensitivity of the aortic dissection detection risk score, a novel guideline-based tool for identification of acute aortic dissection at initial presentation: results from the international registry of acute aortic dissection. Circulation. 2011;123(20):2213-2218. doi:10.1161/CIRCULATIONAHA.110.988568 pubmed.ncbi.nlm.nih.gov
- Klompas M. Does this patient have an acute thoracic aortic dissection?. JAMA 2002; 287: 2262-72. PubMed
- Thrumurthy SG, Karthikesalingam A, Patterson BO, et al. The diagnosis and management of aortic dissection. Clinical review. BMJ 2012; 344: d8290. BMJ (DOI)
- Hagan PC, Nienaber CA, Isselbacher EM, et al. The International Registry of Acute Aortic Dissection (IRAD) : new insights into an old disease. JAMA 2000; 283: 897-903. PubMed
- Shiga T, Wajima Z, Apfel CC, Inoue T, Ohe Y. Diagnostic Accuracy of Transesophageal Echocardiography, Helical Computed Tomography, and Magnetic Resonance Imaging for Suspected Thoracic Aortic Dissection: Systematic Review and Meta-analysis. Arch Intern Med 2006; 166: 1350-6. PubMed
- Safi HJ, Estrera AL. Aortic dissection. Br J Surg 2004; 91: 523-5. PubMed
- Moulakakis KG, Mylonas SN, Dalainas I, Kakisis J, Kotsis T, Liapis CD. Management of complicated and uncomplicated acute type B dissection. A systematic review and meta-analysis. Ann Cardiothorac Surg. 2014;3(3):234-246. doi:10.3978/j.issn.2225-319X.2014.05.08 pubmed.ncbi.nlm.nih.gov
Autor*innen
- Jonas Klaus, Arzt, Freiburg im Breisgau
- Die ursprüngliche Version dieses Artikels basiert auf einem entsprechenden Artikel im norwegischen hausärztlichen Online-Handbuch Norsk Elektronisk Legehåndbok (NEL, https://legehandboka.no/).