Allgemeine Informationen
Definition
- Es liegen unterschiedliche Definitionen vor:
- Mädchen im Alter von 14 Jahren, bei denen noch keine Menstruation aufgetreten ist und die sekundären Geschlechtsmerkmale fehlen: Brustwachstum, Schamhaare und Wachstumsschub.1-2
- Mädchen im Alter von 16 Jahren, bei denen noch keine Menstruation aufgetreten ist, während die sekundären Geschlechtsmerkmale ausgebildet sind.3
- Mädchen, die das 15. Lebensjahr vollendet haben, bei denen noch keine Menstruation aufgetreten ist.4
Pubertät
- Während der Pubertät finden körperliche Veränderungen statt, die in Tanner-Stadien angegeben werden können.5
- Der normale Menstruationszyklus ist ein komplexes Zusammenwirken von Hypothalamus-Hypophysen-Ovar-Achse und Uterus/Vagina.
- Jede Störung dieses Zusammenwirkens kann eine Amenorrhö auslösen.
Tanner-Stadien5
- Beginnender Wachstumsschub (8–10 Jahre)
- Brustwarze hebt sich.
- keine Behaarung im Schambereich
- Tanner-Stadien für weibliche Brust (1) und Schamhaar (1)
- Thelarche (9–11 Jahre)
- Brust entwickelt sich.
- keine Behaarung im Schambereich
- Tanner-Stadien für weibliche Brust (2) und Schamhaar (1)
- Adrenarche (9–11 Jahre)
- Brust entwickelt sich.
- Behaarung im Schambereich entwickelt sich.
- Tanner-Stadien für weibliche Brust (2) und Schamhaar (2)
- Maximaler Wachstumsschub (11–13 Jahre)
- deutliche Brustentwicklung
- deutliche, aber noch mäßige Behaarung im Schambereich
- Tanner-Stadien für weibliche Brust (3) und Schamhaar (3)
- Menarche (12–14 Jahre)
- Brust deutlich sichtbar
- Behaarung im Schambereich deutlich sichtbar
- Physiologischer Fluor albus tritt rund 6–9 Monate vor der Menarche auf.6
- Tanner-Stadien für weibliche Brust (4) und Schamhaar (4)
- Erwachsene Merkmale (13–15 Jahre)
- Brust und Behaarung im Schambereich deutlich entwickelt
- Tanner-Stadien für weibliche Brust (5) und Schamhaar (5)
Häufigkeit
- Für die Häufigkeit der primären Amenorrhö liegen keine gesicherten Zahlen vor.
- Die Häufigkeit der Amenorrhö als Symptom (primäre und sekundäre Amenorrhö) liegt bei 3–5 % der Frauen im fertilen Alter.3
- Ursächlich für die primäre Amenorrhö sind in 65 % der Fälle genetische Störungen, die zur
- Gonadendysgenesie
- Androgeninsensitivität (partielle oder komplette Androgenresistenz) oder
- zur Fehlbildung der Müller-Gänge mit anatomischen Anomalien führt.3
- Weitere Ursachen3
- Anomalien des Genitaltraktes
- endokrinologische Ursachen mit Ovarialinsuffizienz durch Störungen der Hypothalamus-Hypophysen-Ovar-Achse
Diagnostische Überlegungen
- Gründliche Anamnese und eine körperliche Untersuchung sind obligat.7-9
- Primäre Amenorrhö mit Pupertätsentwicklungsstörung?6
- in 50 % der Fälle Störungen der Hypophyse und des
Hypothalamus (hypogonadotroper Hypogonadismus) durch:- chronische Erkrankungen des Kinder- und Jugendalters (z. B. Essstörungen, zystische Fibrose, chronisch-entzündliche Darmerkrankungen, juvenile chronische Arthritis, Hypothyreose)
- Schädel-Hirn-Trauma und chirurgische Eingriffe bei ZNS-Tumoren.
- aber auch durch Ovarialinsuffizienz (hypergonadotroper Hypogonadismus) bedingt
- in 50 % der Fälle Störungen der Hypophyse und des
- Primäre Amenorrhö mit zeitgerechter Pupertätsentwicklung?6
- a. e. durch genitale Missbildungen
- Primäre Amenorrhö mit Virilisierung oder Androgenisierung?6
- a. e durch PCO-Syndrom, nicht klassisches adrenogenitales Syndrom, androgenproduzierende Nebennierenrinden- oder Ovarialtumoren
Einstufungsdiagnostik10
- Hypergonadotroper Hypogonadismus (FSH erhöht, Estradiol erniedrigt)
- Turner-Syndrom (45 X0)
- Sweyer-Syndrom (vollständige 46,XY Gonadendysgenesie)
- partielle Deletion des X-Chromosoms
- Gonadendysgenesie
- Enzymdefekte, z. B. 17-OH-Hydroxylase-Mangel
- Gonadotropinresistenz (z. B. Autoantikörper gegen Ovargewebe)
- Schädigung von Ovarialgewebe durch Chemo- oder Strahlentherapie im Kindesalter
- Galaktosämie
- Hypogonadotroper Hypogonadismus (FSH erniedrigt)
- Pubertas tarda: verspätetes Einsetzen der Pubertät
- Kallmann-Syndrom
- Tumoren i. B. des Hypothalamus und Hypophyse, z. B. Kraniopharyngeom
- Schädel-Hirn-Trauma
- Anorexia nervosa u. a. Mangel- bzw. Fehlernährung
- Leistungssport
- psychischer Stress
- Disorders of Sex Development (DSD)
- komplette Androgenresistenz
- ovotestikuläre 46,XX-DSD
- Genitale Fehlbildungen
- Uterus: Agenesie oder Anomalie z. B. Mayer-von-Rokitansky-Küster-Syndrom
- Hymenalatresie
- Endokrinopathien
- Hyperprolaktinämie (Prolaktinom, Mikroprolaktinom, Medikamente)
- Hypothyreose
- M. Cushing
- adrenogenitales Syndrom
- androgenproduzierende Nebennierenrinden- oder Ovarialtumoren
- polyzystisches Ovar-Syndrom (PCO)
Abwendbar gefährliche Verläufe
- Zunächst immer prüfen, ob die Patientin schwanger ist, wenn die sekundären Geschlechtsmerkmale entwickelt sind.
- Essstörungen, Leistungssport oder Stress müssen als mögliche Ursachen in Erwägung gezogen werden.
- Die konstitutionelle Entwicklungsverzögerung ist eine Ausschlussdiagnose.6
ICPC-2
- Fehlende/spärliche Menstruation
ICD-10
- N91.0 Primäre Amenorrhö
- N91.2 Amenorrhö, nicht näher bezeichnet
Differenzialdiagnosen
Verspätetes Einsetzen der Pubertät
- Keine auffälligen Symptome oder klinischen Befunde
- Häufig positive Familienanamnese6
- Fehlendes Brustwachstum und offene Wachstumsfugen
- FSH niedrig, Prolaktin normal
Psychischer Stress
- Kann zu verspäteter Menarche führen.
- Es kommt zu einer ungenügenden pulsatilen Stimulation des Hypophysenvorderlappens durch GnRH, wodurch eine hypothalamischen Amenorrhö entsteht.3
- Kann durch jegliche Form von physischem oder psychischem Stress entstehen (z. B. Essstörungen, Leistungssport, schwere Allgemeinerkrankungen)
- Eine genetische Disposition liegt vor.
Körperliches Training
- Bei mehr als 15 Stunden/Woche besteht Gefahr der Amenorrhö.
Anorexia nervosa
- Siehe Artikel Anorexia nervosa (Magersucht).
- Niedriges Körpergewicht
- Verweigerung von kalorienreicher Nahrung, gestörte Körperwahrnehmung, Minderwertigkeitsgefühl, Hyperaktivität in Form von u. a. sehr hoher Trainingsintensität
- Stimmungsschwankungen, Zwangsstörungen, Angstzustände
- Amenorrhö meist bei einem Gewicht unter 50 kg
- Androgenisierung: Niedriger Östrogenspiegel führt zu einem relativen Androgenüberschuss, Rückbildung von Fett und Muskeln.
- FSH normal oder etwas zu niedrig, PRL normal, Östrogenspiegel ist niedrig.
Hypothyreose
- Siehe Artikel Hypothyreose.
- Charakteristisch sind Antriebslosigkeit, Kälteintoleranz, Muskelschmerzen, erhöhter Schlafbedarf, Gewichtszunahme (gewöhnlich mäßig), Verstopfung, Schwindel, Parästhesie, Haarausfall und undeutliche Stimme.
- Klinische Befunde können trockene und kalte Haut, trockenes Haar und Spliss, spröde und dünne Nägel, periorbitale Ödeme, Bradykardie, langsame Sehnenreflexe und psychomotorische Trägheit sein.
- Laboruntersuchungen zeigen erhöhte TSH- und niedrige FT4-Werte.
Prolaktinom
- Siehe Artikel Hypophysenerkrankungen und Hypophysentumoren.
- Ein Anstieg von Prolaktin (PRL) führt zu Störungen in der GnRH-Ausschüttung, was wiederum zu niedrigen FSH- und LH-Werten führt. Durch niedrige Gonadotropine verringert sich die Ovarialfunktion und damit auch die Produktion von Östradiol.
- Bei vielen Frauen ist Amenorrhö das einzige Symptom, aber es treten auch Galaktorrhö (30 %), verringerte Libido, Scheidentrockenheit und Osteoporose (im späten Stadium) auf.
- Bei Makroadenomen (>1 cm) können Störungen der anderen Hypophysenachsen, Beeinträchtigung benachbarter Strukturen (z. B. N. opticus) und damit neurologischen Symptome, wie Kopfschmerzen/Visusstörungen auftreten.11
- Eine Schwangerschaft sollte ausgeschlossen werden. Bei einer Schwangerschaft vergrößert sich die Hypophyse um 100 %, und es können Symptome eines vorher asymptomatischen Tumors auftreten.
- Hormonuntersuchungen zeigen hohes PRL (> 4- bis 6-Fache der Norm)3, normales/niedriges FSH, LH und Östradiol.
- DD (milde) Hyperprolaktinämie: Hypothyreose, Medikamente (z. B. Neuroleptika), Stimulation der Brustwarzen
- Medikamentöse Therapie mit Dopaminagonisten, vorzugsweise wird Cabergolin, alternativ Bromocriptin oder Quinagolid eingesetzt. Spricht der Tumor nicht auf die medikamentöse Behandlung an, ist ein chirurgischer Eingriff indiziert.11
Gonadendysgenesie
- Angeborene Fehlentwicklung oder fehlenden Anlage der Gonaden
- Bei komplettem Funktionsausfall kommt es zu Stranggonaden
und ein weiblicher Phänotyp mit Scheide und Uterus entwickelt sich. Allerdings bleibt die Brustentwicklung aus. - Dies geschieht auch bei männlichem Karyogramm, da Testosteron zur Ausbildung der männlichen Geschlechtsorgane fehlt und kein testikuläres Anti-Müller-Hormon die Uterusentwicklung verhindert.3
- FSH ist hoch, PRL ist normal und der Östrogenspiegel ist niedrig.
- Turner-Syndrom?
Uterusagenesie oder -anomalie
- Eine Müller-Gang-Anomalie mit fehlender Vagina und fehlendem Uterus bei der Geburt oder ein rudimentär ausgebildeter Uterus sind die Ursache von 15 % der Fälle einer primären Amenorrhö.12
- Synonym: Mayer-Rokitansky-Küster-Hauser-Syndrom (MRKH-Syndrom)
- Vermutlich liegt die Ursache in der embryonalen Aktivierung des Anti-Müller-Hormons, das eine Fehlbildung des weiblichen Genitaltrakts verursacht.8,13
- Die Patientin kann unter zyklischen Bauchschmerzen leiden, wenn Endometriumgewebe in einem rudimentären Uterus vorhanden ist, und es kann zu Mittelschmerz und Brustempfindlichkeit kommen.
- Die sekundären Geschlechtsmerkmale sind normal entwickelt.
- Nierenfehlbildungen (40 %), skeletale Fehlbildungen (10–12 %) oder Störungen des Gehörs können mit dem MRKH-Syndrom assoziiert sein.6
- Die Erkrankung kann bei einer gynäkologischen Untersuchung oder über Ultraschall/MRT entdeckt werden.
- FSH und PRL sind normal.
- Um eine komplette Androgenresistenz (Karyotyp: 46,XY) auszuschließen, muss eine Karyotypbestimmung durchgeführt werden.9
Hymenalatresie oder vertikales Vaginalseptum
- Hymenalatresie: vollständiger Verschluss der Vaginalöffnung6
- Ein vertikales Vaginalseptum kann auf verschiedenen Höhen in der Vagina liegen und kann im Rahmen eines Syndroms entdeckt werden.6
- McKusick-Kaufmann-Syndrom (Herzfehler, Vaginalsepten, Polydaktylie)
- Bardet-Biedel-Syndrom (Vaginalseptum, hypoplastischer Uterus, Retinitispigmentosa, Polydaktylie, mentale Retardierung, Nieren- und Herzfehlbildungen)
- Beide Befunde führen zu monatlichen Bauchschmerzen, aber das Menstruationsblut kann nicht abfließen.14
- Es kommt zu Hämatokolpos (Blut in der Vagina), Hämatometra (Blut im Uterus) und später Hämatosalpinx (Blut in den Eileitern) und Hämoperitoneum (Blut in der Bauchhöhle).
- Die sekundären Geschlechtsmerkmale sind normal entwickelt.
- Die chirurgische Resektion des Septums bzw. Exzision des Hymens sind Therapie der Wahl.6
Turner-Syndrom
- Siehe Artikel Turner-Syndrom.
- Diese Gonadendysgenesie tritt bei 1 von 2.500 neugeborenen Mädchen auf.15
- Das Syndrom kennzeichnet sich durch das Fehlen eines X-Chromosoms, der Karyotyp ist 45,X0; unvollständige Formen (Mosaik-Typus) können auftreten.
- Typische klinische Erscheinungsformen sind Kleinwuchs, kurzer Hals, hoher Gaumen, weiter Mamillenabstand, Cubitus valgus (unvollständig streckbarer Ellenbogen) und kurze Mittelhand- und Mittelfußknochen.
- Die Pubertät setzt spät ein, und sekundäre Geschlechtsmerkmale fehlen.
- Die Intelligenz ist normal.
- Die FSH- und LH-Werte sind hoch, der Östrogenspiegel ist niedrig.
- Durch die Karyotypbestimmung wird die Diagnose bestätigt.
Komplette Androgenresistenz
- Die Erkrankung tritt selten auf. Der Karyotyp ist 46,XY.
- Der Zustand wird auch Morris-Syndrom genannt.
- Es besteht eine komplette Androgenresistenz, da ein Androgenrezeptordefekt vorliegt.16
- Die Brüste sind entwickelt, aber der Warzenhof ist blass.
- Der Schambereich und die Achselhöhlen sind nicht behaart.
- Die Vagina ist aufgrund einer Aplasie im oberen Bereich verkürzt. Der Uterus fehlt.
- Die Hoden liegen intraabdominell oder in der Leiste.3
Kallmann-Syndrom
- Ist kennzeichnet durch Anosmie, Hypogonadismus und Östrogenausfall.17
- Es besteht ein hypogonadotroper Hypogonadismus aufgrund eines Gonadotropin-Releasing-Hormons (GnRH)-Mangels durch Genmutation.
PCO-Syndrom
- Der Abschnitt basiert auf dieser Referenz.3
- Siehe Artikel Polyzystisches Ovarsyndrom (PCOS).
- Häufigste gynäkologisch-endokrinologische Störung (Prävalenz ca. 5–10 %, bei Frauen mit Oligo-/Amenorrhö 40 %)
- Patientinnen weisen einen Hirsutismus, Akne, biochemische Zeichen der Hyperandrogenämie (Testosteron erhöht, LH/FSH-Quotient > 2), eine Oligo-/Amenorrhö und sonografisch polyzystische Ovarien auf.
- In ca. 50 % der Fälle besteht zudem eine Adipositas sowie eine Insulinresistenz mit Hyperinsulinämie.
- Die Therapie beinhaltet meist antiandrogene Ovulationshemmer, bei Insulinstoffwechselstörungen und/oder Adipositas ist eine Behandlung mit Metformin zu erwägen (Off Lable Use).
Nichtklassisches adrenogenitales Syndrom (AGS)
- Der Abschnitt basiert auf dieser Referenz.3
- Gekennzeichnet durch primäre oder (meist) sekundäre Amenorrhö verbunden mit Hirsutismus und Akne
- Ursächlich sind milde Enzymdefekte der adrenalen Steroidbiosynthese.
- Testosteron ist erhöht.
- Beim klassische AGS kommt es zur Ausbildung intersexueller Genitale, diese Variante macht sich bereits bei der Geburt durch eine Nebennierenrindeninsuffizienz bemerkbar.
Anamnese
Besonders zu beachten
Menarche und Menstruationsverlauf
- Liegt primäre oder sekundäre Amenorrhö vor?
- Geschlechtsverkehr?
Sport und Ernährung
- Übermäßiges Training und Anorexia nervosa ausschließen.
- Psychische Symptome, Depressionen oder Angstzustände?
Geschlechtsreife
- Wann haben sich die Brüste entwickelt?
- Scham- und Achselbehaarung?
Bauchschmerzen?
- Leidet die Patientin unter Bauchschmerzen?
- Wenn ja, treten diese monatlich oder in unregelmäßigen Abständen auf?
Vererbung?
- Wann trat die Menarche bei den weiblichen Familienmitgliedern 1. Grades ein?
- Gendefekte in der Familie?
Frühere Zytostatika- oder Strahlentherapie
- ZNS
- Kann zu hypothalamischer Amenorrhö führen.
- Becken
- Kann zu prämaturer Ovarialinsuffizienz führen.
Andere Ursachen
- Fehlender Geruchssinn: Verdacht auf Kallmann-Syndrom
- Zyklische Bauchschmerzen und Spannungen in der Brust: Verdacht auf Obstruktion
Klinische Untersuchungen
In der Hausarztpraxis
- Keine unnötigen klinischen Untersuchungen bei jungen Mädchen bei der ersten Konsultation
- Größe und Gewicht, BMI, Beurteilung der Größe über Wachstumskurven
- Brustentwicklung und Schambehaarung beurteilen: Liegt eine konstitutionelle Entwicklungsverzögerung vor?
- Evtl. einen Schwangerschaftstest durchführen.
- Auffällige Befunde
- kurzer Hals, Minderwuchs, weiter Mamillenabstand: Verdacht auf Turner-Syndrom
- Gynäkologische Untersuchung
- Bei regelmäßigen, monatlichen Bauchschmerzen sollte gynäkologisch untersucht werden.
- Hymenalatresie oder vaginale Aplasie sind seltene Erkrankungen und werden in einer gynäkologischen Untersuchung festgestellt.
- Entwickelte Brust, aber keine Scham- und Achselbehaarung
- Es könnte sich um eine Androgenresistenz handeln, d. h. die Patientin hat einen weiblichen Phänotyp, aber einen männlichen Karyotyp mit fehlendem Hodendeszensus.
- Sind Hoden ausgebildet, sollen diese aufgrund des hohen Risikos einer malignen Transformation nach der Pubertät entfernt werden.14
Diagnostik bei Spezialist*innen
Gynäkologische Untersuchung
- Bei regelmäßigen, monatlichen Bauchschmerzen sollte gynäkologisch untersucht werden.
- Hymenalatresie oder vaginale Aplasie sind seltene Erkrankungen und werden in einer gynäkologischen Untersuchung festgestellt.
Labor
- Östradiol, FSH, LH, TSH, FT4, PRL, Testosteron
- Hohe FSH-Werte sind Anzeichen einer fehlenden negativen Rückkopplung aufgrund einer Ovarialinsuffizienz.
- Niedrige FSH-Werte sind Anzeichen einer Hypophysen- oder Hypothalamusinsuffizienz.
- Speziallabor: z. B. GnRH-Test zur Differenzierung von hypothalamischen und hypophysären Störungen bei hypogonadotropen Hypogonadismus3
Bildgebung
- Ultraschall
- Sind die sekundären Geschlechtsmerkmale normal ausgebildet, soll eine Ultraschalluntersuchung des Uterus durchgeführt werden.
- Ggf. MRT
- kleines Becken, Hypophyse
- Ggf. Röntgenaufnahmen der Knochen zur Knochenalterbestimmung
- Ggf. Urografie
- Operative Diagnostik
- Ggf. diagnostische Laparoskopie
Genetische Diagnostik
- Karyotypbestimmung (obligat bei hypergonadotroper primärer Amenorrhö)3
Diagnostik bei Fehlen von sekundären Geschlechtsmerkmalen
- Die Diagnose stützt sich auf Laboruntersuchungen und die Karyotypbestimmung.
- Hypogonadotroper Hypogonadismus (FSH und LH niedrig)
- Die häufigste Ursache ist eine konstitutionelle Entwicklungsverzögerung.12-13
- Eine positive Familienanamnese stützt die Diagnose.
- Eine konstitutionelle Ursache unterscheidet sich nicht von Ursachen im Zusammenhang mit einer Hypophysen- oder Hypothalamusinsuffizienz.18
- Kallmann-Syndrom: gekennzeichnet durch Anosmie, Hypogonadismus und Östrogenausfall17
- Die häufigste Ursache ist eine konstitutionelle Entwicklungsverzögerung.12-13
- Hypergonadotroper Hypogonadismus (FSH und LH erhöht)
- Wird durch eine Gonadendysgenesie hervorgerufen.
- Das Turner-Syndrom (Karyotyp 45,X0) ist die häufigste Form der Gonadendysgenesie bei Frauen.
- Typische physische Befunde sind kurzer Hals, weiter Mamillenabstand und Kleinwuchs.
- Der Mosaik-Typus tritt bei ca. 25 % der Patientinnen mit Turner-Syndrom auf.19
- Andere seltene Ursachen für eine reine Gonadendysgenesie treten bei einem Karyotyp von 46,XY oder XX auf.8
Maßnahmen und Empfehlungen
Indikationen zur Überweisung
- Mädchen im Alter von 16 Jahren, die noch keine Menstruation haben, sollen an eine gynäkologische Praxis überwiesen werden.
- Eine Überweisung ist auch bei Verdacht auf Hymenalatresie oder vaginale Aplasie notwendig.
Empfehlungen
- Die Therapie einer primären Amenorrhö erfolgt in der gynäkologischen Praxis.
- Wenn möglich kausale Therapie durchführen.
- Ansonsten Therapie mittels hormoneller Therapie mit Östrogen und Gestagen wie bei der hormonellen Kontrazeption, nachdem andersweitig therapiebare Störungen und organische Ursachen ausgeschlossen wurden.10
- Im Falle der Hymenalatresie oder bei vaginalen Septen erfolgt die chirurgische Sanierung.
Komplikationen
- Der Abschnitt basiert auf dieser Referenz.3
- Infertilität
- Ausbleibende Pubertät
- Bei Amenorrhö mit Estrogenmangel: Osteopenie/Osteoporose, klimakterische Symptome und Risikofaktor für kardiovaskuläre Erkrankungen.
- Bei Amenorrhö mit erhaltener Östrogensekretion und jahrelangem Bestehen: Risiko der Endometriumhyperplasie
Patienteninformationen
Patienteninformationen in Deximed
Illustrationen
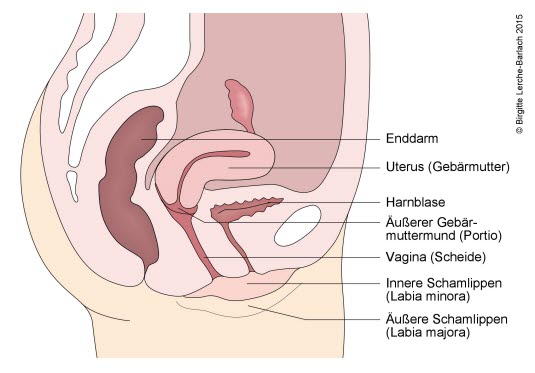
Seitenansicht der inneren Genitalien
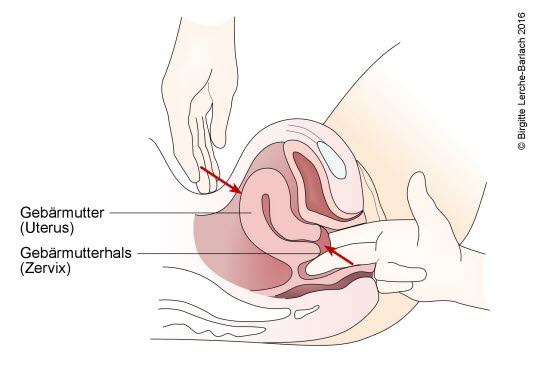
Palpation des Uterus
Quellen
Literatur
- Master-Hunter T, Heiman DL. Amennorrhea: Evaluation and treatment. Am Fam Physician 2006; 73: 1374-82. PubMed
- Klein DA, Poth MA. Amenorrhea: an approach to diagnosis and management. Am Fam Physician 2013; 87: 781-8 American Family Physician
- Frank-Herrmann P, Strowitzki T. Amenorrhö: Woran denken?. Journal für klinische Endokrinologie und Stoffwechsel 2013; 6: 12-18. www.kup.at
- Desirée Dunstheimer, Kirsten Salzgeber. Primäre Amenorrhö. Korasion, Fachzeitschrift für Kinder- und Jugendgynäkologie – Mitteilungsblatt der Arbeitsgemeinschaft Kinder- und Jugendgynäkologie e. V. 2017. www.kindergynaekologie.de
- Marshall WA, Tanner JM. Variations in patterns of pubertal changes in girls. Arch Dis Child 1969; 44: 291-303. PubMed
- Dingeldein I, Hürlimann R. Die primäre Amenorrhö Das Symptom mit und ohne Störungen der Pubertätsentwicklung. Gynäkologie- Schweizer Zeitschrift für Gynäkologie und Geburtshilfe in der Praxis 2009. www.rosenfluh.ch
- Kiningham RB, Apgar BS, Schwenk TL. Evaluation of amenorrhea. Am Fam Physician 1996; 53: 1185-94. American Family Physician
- Pletcher JR, Slap GB. Menstrual disorders. Pediatr Clin North Am 1999; 46: 505-18. PubMed
- Reindollar RH, Byrd JR, McDonough PG. Delayed sexual development: a study of 252 patients. Am J Obstet Gynecol 1981; 140: 371-80. PubMed
- Uhl B. Gynäkologie und Geburtshilfe Compact. Stuttgart: Thieme, 2006.
- Rieben C, Christ E. Prolaktin – was gibt’s Neues? Hyperprolaktinämie – Ätiologie, Diagnostik, Therapie. GynäkologieSchweizer Zeitschrift für Gynäkologie und Geburtshilfe in der Praxis, 2019. www.rosenfluh.ch
- Folch M, Pigem I, Konje JC. Müllerian agenesis: etiology, diagnosis, and management. Obstet Gynecol Surv 2000; 55: 644-9. PubMed
- Seldmeyer IL, Palmert MR. Delayed puberty: analysis of a large case series from an academic center. J Clin Endo Metab 2002; 87: 1613-20. PubMed
- The Practice Committee of the American Society for Reproductive Medicine. Current evaluation of amenorrhea. Fertil Steril 2004; 82(suppl 1): 33-9. pubmed.ncbi.nlm.nih.gov
- Bedei I. Ullrich-Turner-Syndrom – pränatale Diagnostik, Korasion, Fachzeitschrift für Kinder- und Jugendgynäkologie, 03/2018. www.kindergynaekologie.de
- Hiort, Olaf; Holterhus, Paul-Martin; Sinnecker, Gernot H. G.; Kruse, Klaus. Androgenresistenzsyndrome - Klinische und molekulare Grundlagen. Deutsches ärzteblatt 1999; 11: 686-692. www.aerzteblatt.de
- Traggiai C, Stanhope R. Delayed puberty. Best Pract Res Clin Endocrinol Metab 2002; 16: 139-51. PubMed
- Albanese A, Stanhope R. Investigation of delayed puberty. Clin Endocrinol (Oxf) 1995; 43: 105-10. PubMed
- Simpson J, Rajkovic A. Ovarian differentiation and gonadal failure. Am J Med Genet 1999; 89: 186-200. PubMed
Autor*innen
- Kristine Scheibel, Dr. med., Fachärztin für Allgemeinmedizin, Norderney
- Marlies Karsch-Völk, Dr. med., Fachärztin für Allgemeinmedizin, München
- Erika Baum, Prof. Dr. med., Professorin für Allgemeinmedizin, Biebertal (Review)
- Die ursprüngliche Version dieses Artikels basiert auf einem entsprechenden Artikel im norwegischen hausärztlichen Online-Handbuch Norsk Elektronisk Legehåndbok (NEL, https://legehandboka.no/).