Zusammenfassung
- Definition:Seltene Sonderform des diabetischen Fußes mit schmerzloser, nichtinfektiöser Zerstörung von Knochen und Gelenken als Folge der Neuropathie.
- Häufigkeit:6.000 bis 8.500 Neuerkrankungen in Deutschland jährlich.
- Symptome:Meist schmerzlose Schwellung, Rötung und Überwärmung des Fußes im akuten Stadium.
- Befunde:In der Regel schwere Neuropathie. Im Akutstadium geschwollener, überwärmter Fuß. Im chronischen Stadium Fußdeformität, klassisches Endstadium Tintenlöscherfuß.
- Diagnostik:Bei Patient*innen mit diabetischer Neuropathie und akut geschwollenem Fuß sollte bis zum Beweis des Gegenteils von einem Charcot-Fuß ausgegangen werden. Röntgen des Fußes in 3 Ebenen unter Belastung. Bei unauffälligem Röntgen MRT.
- Therapie:Schnellstmögliche Immobilisierung und Entlastung, um weitere Knochenläsionen zu verhindern. Bei Komplikationen wie chronischen Druckulzera durch Exostosen und/oder Fußdeformitäten ggf. chirurgische Korrektur.
Allgemeine Informationen
Definition
- Seltene Sonderform des diabetischen Fußes mit schmerzloser, nichtinfektiöser Zerstörung von Knochen und Gelenken als Folge der Neuropathie. 1
- Charcot-Fuß bezeichnet sowohl akuten Krankheitszustand mit Weichteilödem, Rötung und Überwärmung des Fußes als auch den durch pathologische Frakturen chronisch deformierten Fuß.
- Synonym: diabetische Neuroosteoarthropathie (DNOAP)2
- Benannt nach Erstbeschreiber Jean-Martin Charcot (Neurologe, 1825‒1893)
Klassifikation
- Klassifikation der Verlaufsstadien der (DNOAP) nach Levin2
- Stadium 1 – akutes Stadium: Fuß gerötet, geschwollen, überwärmt, Röntgen ggf. noch normal
- Stadium 2 – Knochen und Gelenkveränderungen, Frakturen
- Stadium 3 – Fußdeformität: ggf. Plattfuß, später Wiegefuß
- Stadium 4 – zusätzliche plantare Fußläsion
Häufigkeit
- 6.000 bis 8.500 Neuerkrankungen in Deutschland jährlich3
- In bis zu 30 % der Fälle bilaterales Auftreten4
Ätiologie und Pathogenese
- Diabetische Neuropathie wichtigste Voraussetzung für Entstehung eines Charcot-Fußes, Genese jedoch multifaktoriell5
- Kombination aus:
- lokaler Osteopenie6 (Folge der autonomen Neuropathie mit lokaler Hyperperfusion des Knochens und Osteoklastenaktivierung)
- lokaler Entzündungsreaktion7
- muskulärer Imbalance (Folge der motorischen Neuropathie) und
- unbemerkten Mikrotraumen (fehlende Schmerzempfindung durch sensible Neuropathie); dies führt zu fortschreitenden periartikulären Stressfrakturen.1
- Durch fehlende Schmerzempfindung wird das instabile, frakturierte Fußskelett weiter belastet, das Fußgewölbe bricht ein und heilt nur unter erheblicher Fehlstellung aus.
- Klassischer „Tintenlöscherfuß“
Disponierende Faktoren
- Diabetes mit Neuropathie
- Andere Ursachen für Polyneuropathie, z. B. Alkoholabusus
ICPC-2
- T89 Diabetes 1 ohne Komplikationen
- T90 Diabetes 2 ohne Komplikationen
ICD-10
- M14.6 Neuropathische Arthropathie
Diagnostik
Diagnostische Kriterien
- Bei Patient*innen mit diabetischer Neuropathie und akut geschwollenem Fuß sollte bis zum Beweis des Gegenteils von einem Charcot-Fuß ausgegangen werden.
- Bei klinischem Verdacht Röntgen des Fußes in 3 Ebenen unter Belastung3
- falls unauffällig oder bei V. a. Abszess: MRT2
Differenzialdiagnosen
- Weichteilinfektion, Phlegmone
- Hämatom
- Tiefe Venenthrombose
- beim Charcot-Fuß teils begleitendes Lymphödem bis auf Kniehöhe5
- Osteomyelitis
- Arthritis
- Fraktur anderer Ursache
Anamnese
- Patient*in mit (diabetischer) Neuropathie
Akuter Charcot-Fuß
- Typischerweise (sub)akute Schwellung des Fußes und Überwärmung
- Folge eines Ermüdungsbruchs des Fußskeletts5
- Schmerzen können bestehen, aufgrund der Neuropathie jedoch selten.
- Uncharakteristische Symptome wie Unruhe, Kribbeln und Instabilitätsgefühl möglich
- Größeres Trauma nicht eruierbar
- Symptome können in Verbindung mit Aktivitäten auftreten, die den Fuß zusätzlich belasten, z. B. bei ungewöhnlich langen Spaziergängen.
- Häufig Auftreten nach längerer Immobilisierung und damit Schwächung des Fußskeletts, z. B. nach chirurgischem Eingriff am Fuß8-9
Chronischer Charcot-Fuß
- Progrediente (Mikro-)Frakturierungen des Fußskelettes, letztlich Zusammenbrechen der Fußarchitektur mit Deformierungen, Fehlbelastungen und schließlich Druckgeschwüren an der Haut
- typischerweise Plattfuß und schließlich charakteristischer Tintenlöscherfuß
- Druckgeschwüre und Infektionen an Haut und Knochen (Osteomyelitis) können als Spätfolge eine Amputation notwendig werden lassen.5
- Siehe Artikel Diabetische Fußgeschwüre.
Klinische Untersuchung
- In akutem Stadium auffällige Diskrepanz zwischen hochrotem, überwärmtem, entzündlich imponierendem Fuß und relativer Beschwerdefreiheit
- Alle Patient*innen weisen Neuropathie auf.
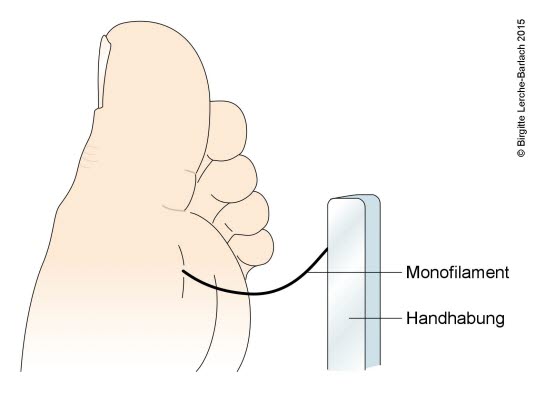 Monofilament
Monofilament - Diagnosestellung mithilfe eines Monofilaments nach Semmes-Weinstein (10 g), evtl. ergänzt durch eine Untersuchung des Vibrationssinns: Der Draht sollte senkrecht gegen die Haut gehalten und für ca. 2 Sekunden gegen die Hautfläche gedrückt werden. Drücken Sie so fest, dass sich das Filament biegt. Patient*in sollte nicht sehen können, wann und wo das Filament platziert wird. Vermeiden Sie den Bereich mit harter Haut.
 Charcot-Fuß (Quelle: Wikimedia commons)
Charcot-Fuß (Quelle: Wikimedia commons) - Fußdeformitäten und Hautdefekte
- charakterisiert durch Einbrechen des Fußgewölbes, im schlimmsten Fall unter Entwicklung einer plantaren Konvexität (Schaukelfuß- bzw. Tintenlöscher-Fehlstellung)
- In Kombination mit Neuropathie führt Kallusbildung am Knochen zu Druckgeschwüren.10-11
- Siehe auch TrainAMed Fußuntersuchung bei Diabetes mellitus (Universität Freiburg).
Ergänzende Untersuchungen in der Hausarztpraxis
- Hohe HbA1c-Werte als Hinweis auf lange Zeit nicht gut eingestellten Diabetes und vorliegende Neuropathie
Diagnostik bei Spezialist*innen
- Röntgen
- Röntgenaufnahmen des Fußes in 3 Ebenen mit Belastung3
- in den ersten Wochen oft Normalbefunde
- Röntgen ermöglicht nicht Ausschluss eines akuten Charcot-Fußes.
- MRT
- indiziert bei klinischem Verdacht und unauffälligem Röntgenbefund2,12
- Zeigt typisches Knochenödem, wie bei Stressfraktur.
- Knochenszintigraphie
- ggf. zur Differenzialdiagnostik bei V. a. Osteomyelitis
Indikationen zur Überweisung
- Sofortige Überweisung zur radiologischen Diagnostik bei Verdacht auf die Erkrankung13
- Bei bestätigter Diagnose sollte der Charcot-Fuß aufgrund der komplexen Diagnostik und Behandlung an spezialisierte Ambulanz überwiesen werden.
Checkliste zur Überweisung
Diabetischer Fuß
- Zweck der Überweisung
- Diagnostik? Konservative Behandlung? Hilfsmittelversorgung? Chirurgie?
- Anamnese
- Beginn des Diabetes. Beginn der Fußbeschwerden. Entwicklung der Beschwerden
- Schmerzen? Schwellungen? Gehprobleme? Anhaltende Beschwerden? Akute Verschlechterung?
- Andere relevante Krankheiten?
- Regelmäßige Medikamente?
- Konsequenzen. Funktionsverlust. Arbeitsunfähigkeit
- Klinische Untersuchung
- Schwellungen? Lokale Überwärmung? Neuropathie? Fußdeformität? Fußgeschwüre?
- Ergänzende Untersuchungen
- Röntgen? MRT?
Therapie
Therapieziele
- Wichtigste Maßnahme Immobilisierung und Entlastung, um weitere Skelett- und Gelenktraumatisierungen zu vermeiden.2,5
- Dabei kommt frühzeitiger Diagnose zentrale Rolle zu.
- bei rechtzeitger Diagnose und Entlastung Restitutio ad integrum möglich
Allgemeines zur Therapie
- Klinischer Verdacht sollte schnellstmöglich zu einer Entlastung durch Gips oder Therapiestiefel führen (z. B. Aircast).
- Auch wenn Ergebnis der Röntgenuntersuchung negativ, Entlastung des Fußes, bis per MRT ein Charcot-Fuß sicher ausgeschlossen ist.
Konservative Behandlung
Entlastung
- Reposition möglicher Frakturen oder Subluxationen3
- Bettruhe, Rollstuhl, Gehstützen, Gips für mindestens 12 Wochen14
- Behandlungsdauer teilweise 4–8 Monate notwendig, gelegentlich bis zu 2 Jahren15
- Anfertigung eines speziellen Unterschenkelgipses in Sandwichbauweise (Total Contact Cast) oder speziell gefertigter Aircast-Schiene1
- bei Gips regelmäßige Kontrolle (alle 1–2 Wochen, bei Beschwerden sofort) auf optimalen Sitz und Druckläsionen
- Mit Ergometerfahrrad kann Bewegung ohne Gewichtsbelastung erfolgen.
- Knochendichtereduktion durch Immobilisierung so teilweise vermeidbar16
- Schrittweise Wiederbelastung sollte erst erfolgen, wenn sich die klinischen Zeichen normalisiert haben und knöcherne Stabilisierung nachzuweisen ist.2
- Während der Behandlung eines Fußes Überbelastung des primär nicht betroffenen Fußes vermeiden.
Nach beendeter primärer Immobilisierung
- Schrittweiser Übergang zu spezialangepasstem orthopädischem Schuhwerk1
- Übergangsbehandlung mit dynamischer Unterschenkelorthese
- anschließend Maßschuh
Medikamentöse Therapie
- Es gibt keine gesichert wirksame medikamentöse Therapie.
- Heilversuche blieben überwiegend erfolglos mit:5,7
- Bisphosphonaten (Wirkung fraglich, cave: off label!1)
- Calcitonin
- Kortikosteroiden
- TNF-Agonisten.
Operative Therapie
- Indikationen zur operativen Therapie3
- (Sub-)akute Luxationen oder Luxationsfrakturen: offene Reposition
und interne Osteosynthese und Gipsverband oder Fixateur externe - drohende oder manifeste Ulzerationen infolge Knochendruck von
innen: Exostosenabtragung oder Korrekturarthrodese - fortbestehende Instabilität: Arthrodese
- schwere Deformität im oberen Sprunggelenk mit Instabilität: Arthrodese
- (Sub-)akute Luxationen oder Luxationsfrakturen: offene Reposition
Disease-Management-Programm (DMP)
Allgemeine Informationen
- In Deutschland wurden DMP bzw. strukturierte Behandlungsprogramme im Jahr 2002 bundesweit implementiert mit dem Ziel, eine Verbesserung der Qualität der medizinischen Versorgung und des Behandlungsablaufes für Patient*innen mit chronischen Erkrankungen zu erreichen.17
- Sie umfassen regelmäßige Arzttermine mit Beratungsgesprächen und Untersuchungen sowie die Vermittlung von Hintergrundinformationen z. B. durch Schulungen.18
- Derzeit gibt es in Deutschland DMP für Menschen mit den folgenden chronischen Erkrankungen:19
- Wer mehrere dieser Erkrankungen hat, kann für jede Erkrankung ein DMP in Anspruch nehmen.18
- Cave: Patientinnen mit Schwangerschaftsdiabetes werden nicht in das DMP aufgenommen.20
Ablauf
- Nach Gesprächen, Untersuchungen und Diagnose erstellen die Ärzt*innen auf Grundlage von DMP-Vorgaben einen individuellen Therapieplan.18
- Dieser umfasst u. a. die medikamentöse Behandlung und andere therapeutische Maßnahmen, Schulungstermine und regelmäßige Kontrolluntersuchungen, z. T. auch in anderen Praxen oder Kliniken.
Untersuchungen beim DMP Diabetes mellitus Typ 2
- Die notwendigen Untersuchungen orientieren sich an Richtlinien des Gemeinsamen Bundesausschusses.20
- Berechnung der geschätzten glomerulären Filtrationsrate
- mind. 1 x/Jahr
- Augenärztliche Untersuchung einschließlich Netzhautuntersuchung
- ein- oder zweijährlich (risikoabhängig)
- Inspektion der Füße einschließlich klinischer Prüfung auf Neuropathie und Prüfung des Pulsstatus
- mind. 1 x/Jahr
- Untersuchung der Füße bei erhöhtem Risiko, einschließlich Überprüfung des Schuhwerks
- sensible Neuropathie: mind. halbjährlich
- sensible Neuropathie und Zeichen einer peripheren arteriellen Verschlusskrankheit und/oder Risiken wie Fußdeformitäten (ggf. infolge Osteoarthropathie), Hyperkeratose mit Einblutung, Z. n. Ulkus, Z. n. Amputation: mind. alle 3 Monate
- Blutdruckmessung
- vierteljährlich, halbjährlich
- HbA1c-Messung
- vierteljährlich, halbjährlich
- Bei insulinpflichtigen Patient*innen Untersuchung der Spritzstellen auf Lipohypertrophie und der korrekten Injektionstechnik, bei starken Blutzuckerschwankungen auch häufiger
- vierteljährlich, mindestens halbjährlich
- Überprüfung auf psychische Begleiterkrankung (z. B. Depression)
- keine genaue Vorgabe, möglichst bei jedem Besuch
- Strukturierte Arzneimittelerfassung und Kontrolle auf mögliche Nebenwirkungen und Interaktionen
- bei Einnahme von fünf oder mehr Arzneimitteln mind. 1 x/Jahr
- Individuelle Beratung
- Ernährungsberatung
- Raucherberatung
- Beratung zu körperlicher Aktivität
- Stoffwechselselbstkontrolle
- Siehe auch Artikel Typ-2-Diabetes.
Verlauf, Komplikationen und Prognose
Verlauf
- Restitutio ad integram bei frühzeitiger Diagnose und adäquater Entlastung möglich
- Gleichzeitig vorliegende Durchblutungsstörungen verzögern die Heilung.
- Bei etwa 1/3 der Patient*innen treten Rezidive auf, vor allem bei zu früher Belastung.2
Komplikationen
- Fußdeformitäten
- Chronische Geschwüre durch Fehlbelastung bei Fußdeformitäten und Exostosen
- Amputation
Prognose
- 90 % der aktiven Charcot-Füße können konservativ und ambulant behandelt werden.3
- Durch konservative und/oder chirurgische Therapie kann die Extremität in > 90 % der Fälle erhalten werden.3
- Potenziell modifizierbare Risikofaktoren wie Hypertonie, Dyslipidämie, Rauchen und ein erhöhter BMI sollten therapiert werden, eine gute diabetische Stoffwechseleinstellung ist anzustreben.
Verlaufskontrolle
- Patient*innen sind im Verlauf als Hoch-Risikopatient*innen für erneute Fußkomplikationen einzustufen und benötigen engmaschige Kontrolluntersuchungen der Füße, gemäß DMP mind. alle 3 Monate.
- Schulung der Betroffenen, um ein Rezidiv selbst zu erkennen.
Patienteninformationen
Patienteninformationen in Deximed
Video
- TrainAMed Fußuntersuchung bei Diabetes mellitus (Universität Freiburg)
Illustrationen

Monofilament: Der Draht sollte senkrecht gegen die Haut gehalten und für ca. 2 Sekunden gegen die Hautfläche gedrückt werden. Drücken Sie so fest, dass sich das Filament biegt. Patient*in sollte nicht sehen können, wann und wo das Filament platziert wird. Vermeiden Sie den Bereich mit harter Haut.
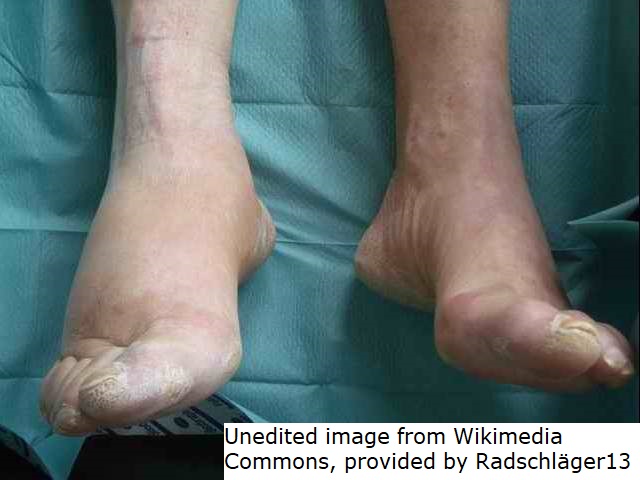
Charcot-Fuß, Stadium 1

Charcot-Fuß links

Charcot-Fuß (Quelle: Wikimedia commons, Charcots fot. Wikimedia commons: donated by Dr. Muzammil Irshad; https://commons.wikimedia.org/wiki/File:Diabetic_Charcot_Foot_Deformity.jpg).
Quellen
Leitlinien
- Deutsche Gesellschaft für Allgemeinmedizin und Familienmedizin e. V. DEGAM-Anwenderversion als Addendum zur Nationalen VersorgungsLeitlinie (NVL) Typ-2-Diabetes. AWMF-Register-Nr. nvl-001. Stand 2021. www.degam.de
- NVL-Programm von BÄK, KBV, AWMF. Nationale VersorgungsLeitlinie Typ-2-Diabetes - Teilpublikation, 2. Auflage. Stand 2021. www.leitlinien.de
Literatur
- Zimny S. Diabetische neuropathische Osteoarthropathie: Eine Sonderform des diabetischen Fußes Dtsch Arztebl 2015; 112(43): [7]; DOI: 10.3238/PersDia.2015.10.23.02 www.aerzteblatt.de
- NVL-Programm von BÄK, KBV, AWMF. Nationale VersorgungsLeitlinie Typ-2-Diabetes: Präventions- und Behandlungsstrategien für Fußkomplikationen. AWMF-Leitlinie Nr. nvl - 001c. Stand 2010 (abgelaufen). www.leitlinien.de
- Scherer M. Die ambulante Behandlung des Charcot-Fußes in der chirurgischen Praxis. Chirurgenmagazin 2018; 16(1): 1-4. www.surochir.de
- Rogers LC, Frykberg RG, Armstrong DG, et al. The Charcot Foot in Diabetes. J Am Podiatr Med Assoc 2011; 101(5): 437-46. meridian.allenpress.com
- Poll LW, Chantelau E. Charcot-Fuss: Auf die frühe Diagnose kommt es an. Dtsch Arztebl 2010; 107(7): A-272 / B-238 / C-234 www.aerzteblatt.de
- Petrova NL, Foster AV, Edmonds ME. Calcaneal bone mineral density in patients with Charcot neuropathic osteoarthropathy: differences between Type 1 and Type 2 diabetes. Diabet Med 2005; 22: 756-61. PubMed
- Jeffcoate WJ, Game F, Cavanagh PR. The role of proinflammatory cytokines in the cause of neuropathic osteoarthropathy (acute Charcot foot) in diabetes. Lancet 2005; 366: 2058-61. PubMed
- Jones KB, Maiers Yelden KA, Marsh JL et al. Ankle fractures in patients with diabetes mellitus. J Bone Joint Surg Br 2005; 87: 489-95. PubMed
- Holstein P, Lohmann M, Bitsch M et al. Achilles tendon lengthening, the panacea for plantar forefoot ulceration? Diabetes Metab Res Rev 2004; 20: 37-40. PubMed
- Fabrin J, Larsen K, Holstein PE. Long-term follow-up in diabetic Charcot feet with spontaneous onset. Diabetes Care 2000; 23: 796-800. PubMed
- Larsen K, Fabrin J, Holstein PE. Incidence and management of ulcers in diabetic Charcot feet. J Wound Care 2001; 10: 323-8. PubMed
- Chantelau E, Richter A, Schmidt Grigoriadis P et al. The diabetic charcot foot: MRI discloses bone stress injury as trigger mechanism of neuroarthropathy. Exp Clin Endocrinol Diabetes 2006; 114: 118-23. PubMed
- Baglioni P, Malik M, Okosieme OE. Acute Charcot foot. BMJ 2012; 344: e1397. BMJ (DOI)
- Pinzur MS, Lio T, Posner M. Treatment of Eichenholtz stage I Charcot foot arthropathy with a weightbearing total contact cast. Foot Ankle Int 2006; 27: 324-9. PubMed
- Stiegler H. Langzeitdiabetiker mit überwärmtem und geschwollenen Fuß. MMW-Fortschr Med 2010; 152(25-27): 47-49. link.springer.com
- Hastings MK, Sinacore DR, Fielder FA et al. Bone mineral density during total contact cast immobilization for a patient with neuropathic (Charcot) arthropathy. Phys Ther 2005; 85: 249-56. PubMed
- Fuchs S, Henschke C, Blümel M, et al. Disease-Management-Programme für Diabetes mellitus Typ 2 in Deutschland. Dtsch Arztebl Int 2014; 111: 453-63. www.aerzteblatt.de
- Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen (IQWiG). Was sind Disease-Management-Programme (DMP)?. Stand 2016. Letzter Zugriff 12.04.21. www.gesundheitsinformation.de
- Kassenärztliche Bundesvereinigung. Praxisnachrichten. DMP für Osteoporose-Patienten auf den Weg gebracht. Februar 2020. Letzter Zugriff 17.04.2021. www.kbv.de
- Gemeinsamer Bundesausschuss. Richtlinie des Gemeinsamen Bundesausschusses zur Zusammenführung der Anforderungen an strukturierte Behandlungsprogramme nach § 137f Absatz 2 SGB V. Stand 2021. Letzter Zugriff 12.04.2021. www.g-ba.de
- NVL-Programm von BÄK, KBV, AWMF. Nationale VersorgungsLeitlinie Typ-2-Diabetes - Teilpublikation, 2. Auflage. Stand 2021. www.leitlinien.de
- Deutsche Gesellschaft für Allgemeinmedizin und Familienmedizin e.V. DEGAM-Anwenderversion als Addendum zur Nationalen VersorgungsLeitlinie (NVL) Typ-2-Diabetes. AWMF-Register-Nr. nvl-001. Stand 2021. www.degam.de
Autor*innen
- Lino Witte, Dr. med., Arzt in Weiterbildung, Innere Medizin, Frankfurt
- Die ursprüngliche Version dieses Artikels basiert auf einem entsprechenden Artikel im norwegischen hausärztlichen Online-Handbuch Norsk Elektronisk Legehåndbok (NEL, https://legehandboka.no/).