Allgemeine Informationen
Definition
- Schleimhautschäden im Bereich von Magen (Ulcus ventriculi) oder Zwölffingerdarm (Ulcus duodeni), die
- bis in die Submukosa reichen.
- einen Diameter von >
Häufigkeit
- Prävalenz
- Lebenszeitprävalenz ca. 5–10 %3
- Inzidenz
- Alter und Lokalisierung
- Häufigkeit der Ulkuskrankheit (und einer H.-pylori-Infektion) nimmt mit dem Alter zu.6
- Geschlecht
- Verhältnis Frauen zu Männern ca. 1:16
Ätiologie und Pathogenese
- Die sog. peptischen Ulzera resultieren aus einem Missverhältnis zwischen:7
- schädigenden Faktoren
- Salzsäure
- Pepsin
- H.-pylori-Infektion
- nichtsteroidale Antirheumatika (NSAR)/ASS
- biliärer Reflux
- Schutzmechanismen
- Schleim
- Prostaglandine
- Bikarbonat
- gute Durchblutung der Schleimhaut.
- schädigenden Faktoren
- Wichtigste ätiologische Faktoren sind:
- H.-pylori-Infektion
- Einnahme von NSAR und/oder ASS9-10
- Seltenere Ursachen sind:101,
1011-1112Zollinger-Ellison-Syndromentzündliche Erkrankungen- eosinophile Gastroenteritis
- Morbus Crohn
- Morbus Behçet
- Sarkoidose
- Vaskulitiden
- idiopathisch
- Infektionen
- Ischämien oder Nekrosen
- kürzlich durchgeführte Interventionen wie transarterielle Chemoembolisation (
vermehrteTACE), perkutaneSäureproduktionStrahlentherapiedurchoderGastrinomRadioembolisation (SIRT), Coiling (am Magen oder Duodenum) St. n. MagenresektionCrack-Kokain-Abusus, Amphetamin-Abusus
- kürzlich durchgeführte Interventionen wie transarterielle Chemoembolisation (
Malignomemedikamenteninduziert oder -assoziiert- SSRI
- Biphosphonate, Kalium
- Sirolimus, Mycophenolat
- Chemotherapie (z. B. 5-FU oder MTX)
- Spironolakton
- neuroendokrine Tumoren bzw. mediatorinduziert
- Gastrinome (inkl. MEN-1)
- systemische Mastozytose
- Basophilie bei myeloproliferativen Erkrankungen
- Obstruktion
- Duodenalstenose, z. B. bei Pankreas anulare
- postoperativ
- Magenresektion
- Magen-Bypass
- schwere Erkrankungen („Stressulzera“)
- z.
M.ARDS, Schock,CrohnSepsis), Polytrauma, Verbrennungen idiopathischeLeber-/Nierenversagen- andauernde
Ulzeramechanische Beatmung
- z.
- Tumorinfiltration
- z. B. bei Pankreaskarzinom
Prädisponierende Faktoren
- Prädisponierende Faktoren sind:106-7
- zunehmendes Alter (> 60 Jahre)
- Medikamente: NSAR, ASS
- Rauchen
- St. n. Ulkuskrankheit
- positive Familienanamnese auf Ulkuskrankheit
- niedriger sozioökonomischer Status
Stresspsychosoziale Belastung,bei schwerer Grunderkrankung/intensivmedizinischer Behandlung- Depression
- schwere Grunderkrankung, Operationen, intensivmedizinische Behandlung
ICD 10
- K25 Ulcus ventriculi
- K25.0 Ulcus ventriculi: Akut, mit Blutung
- K25.1 Ulcus ventriculi: Akut, mit Perforation
- K25.2 Ulcus ventriculi: Akut, mit Blutung und Perforation
- K25.3 Ulcus ventriculi: Akut, ohne Blutung oder Perforation
- K25.4 Ulcus ventriculi: Chronisch oder nicht näher bezeichnet, mit Blutung
- K25.5 Ulcus ventriculi: Chronisch oder nicht näher bezeichnet, mit Perforation
- K25.6 Ulcus ventriculi: Chronisch oder nicht näher bezeichnet, mit Blutung und Perforation
- K25.7 Ulcus ventriculi: Chronisch, ohne Blutung oder Perforation
- K25.9 Ulcus ventriculi: Weder als akut noch als chronisch bezeichnet, ohne Blutung oder Perforation
- K26 Ulcus duodeni
- K26.0 Ulcus duodeni: Akut, mit Blutung
- K26.1 Ulcus duodeni: Akut, mit Perforation
- K26.2 Ulcus duodeni: Akut, mit Blutung und Perforation
- K26.3 Ulcus duodeni: Akut, ohne Blutung oder Perforation
- K26.4 Ulcus duodeni: Chronisch oder nicht näher bezeichnet, mit Blutung
- K26.5 Ulcus duodeni: Chronisch oder nicht näher bezeichnet, mit Perforation
- K26.6 Ulcus duodeni: Chronisch oder nicht näher bezeichnet, mit Blutung und Perforation
- K26.7 Ulcus duodeni: Chronisch, ohne Blutung oder Perforation
- K26.9 Ulcus duodeni: Weder als akut noch als chronisch bezeichnet, ohne Blutung oder Perforation
- K27 Ulcus pepticum, Lokalisation nicht näher bezeichnet
- K27.0 Ulcus pepticum, Lokalisation nicht näher bezeichnet: Akut, mit Blutung
- K27.1 Ulcus pepticum, Lokalisation nicht näher bezeichnet: Akut, mit Perforation
- K27.2 Ulcus pepticum, Lokalisation nicht näher bezeichnet: Akut, mit Blutung und Perforation
- K27.3 Ulcus pepticum, Lokalisation nicht näher bezeichnet: Akut, ohne Blutung oder Perforation
- K27.4 Ulcus pepticum, Lokalisation nicht näher bezeichnet: Chronisch oder nicht näher bezeichnet, mit Blutung
- K27.5 Ulcus pepticum, Lokalisation nicht näher bezeichnet: Chronisch oder nicht näher bezeichnet, mit Perforation
- K27.6 Ulcus pepticum, Lokalisation nicht näher bezeichnet: Chronisch oder nicht näher bezeichnet, mit Blutung und Perforation
- K27.7 Ulcus pepticum, Lokalisation nicht näher bezeichnet: Chronisch, ohne Blutung oder Perforation
- K27.9 Ulcus pepticum, Lokalisation nicht näher bezeichnet: Weder als akut noch als chronisch bezeichnet, ohne Blutung oder Perforation
Diagnostik
Diagnostische Kriterien
- Die Diagnosestellung einer Ulkuskrankheit erfolgt durch Endoskopie.
Differenzialdiagnosen
- Funktionelle Dyspepsie
- Gastroösophageale Refluxerkrankung
- Gastritis
- Magenkarzinom
- Gallensteinleiden
Pankreas-ErkrankungPankreaserkrankung- Perikarditis
- CCS, ACS
Anamnese
- Geringe Sensitivität und Spezifität der Symptomatik4
- Mögliche Symptome
:4- epigastrischer Schmerz
- Völlegefühl
- Blähung
- Übelkeit
.
- Abhängigkeit der Beschwerden von Mahlzeiten
- Nüchternschmerz, Besserung nach Mahlzeit (Duodenalulkus)1
- Beschwerden kurz nach einer Mahlzeit (Magenulkus)1
- Nächtliche Beschwerden6
- 50–80
- 30–40
- 50–80
- Bei starker Blutung Teerstuhl
- Gewichtsverlust (Malignom)
- Risikofaktoren
- Medikation: NSAR, ASS
- Rauchen
- Familienanamnese auf Ulkuskrankheit
- Systemerkrankungen
Klinische Untersuchung
- Häufig keine Befunde zu erheben.
- Druckschmerz bei epigastrischer Palpation
- Blässe bei blutungsbedingter Anämie
- Abwehrspannung bei Perforation
Ergänzende Untersuchungen in der Hausarztpraxis
Allgemeines Labor
- Blutbild (Anämie?)
- Ggf. Eisenstatus
- Evtl. Stuhltest auf okkultes Blut
Nichtinvasive Tests auf H. pylori
- Zu Details der Diagnostik siehe Artikel Helicobacter
- Im Rahmen der hausärztlichen Diagnostik können nichtinvasive Tests auf H. pylori eingesetzt werden, die invasiven Verfahren setzen eine Gastroskopie voraus.
- Eingeschränkte Kostenerstattung: Zwar sind die nichtinvasiven Tests sowohl für die Erstdiagnostik auf H. pylori als auch zur Beurteilung des Eradikationserfolges einsetzbar, allerdings werden Harnstoff-Atemtest und Stuhl-Antigennachweis nur zur Kontrolle des Eradikationserfolges erstattet oder zum Ausschluss einer Reinfektion bei gesicherter Erkrankung.
1213- Info laut KBV: Die Gebührenordnungsposition 32706 ist grundsätzlich nur berechnungsfähig zur Erfolgskontrolle nach Eradikationstherapie einer Helicobacter-pylori-Infektion (frühestens 4 Wochen nach Ende der Therapie) oder zum Ausschluss einer Reinfektion bei einer gastroduodenoskopisch gesicherten Ulcus-duodeni-Erkrankung oder bei Kindern mit begründetem Verdacht auf eine Ulkus-Erkrankung.
- Eingeschränkte Kostenerstattung: Zwar sind die nichtinvasiven Tests sowohl für die Erstdiagnostik auf H. pylori als auch zur Beurteilung des Eradikationserfolges einsetzbar, allerdings werden Harnstoff-Atemtest und Stuhl-Antigennachweis nur zur Kontrolle des Eradikationserfolges erstattet oder zum Ausschluss einer Reinfektion bei gesicherter Erkrankung.
- Für eine zuverlässige H.-pylori-Diagnostik (dies gilt für nichtinvasive und invasive Tests) sollten folgende Zeiträume eingehalten werden:
1310- 2 Wochen nach Ende einer Behandlung mit Protonenpumpen-Inhibitoren (PPI)
- 4 Wochen nach Eradikation oder sonstiger antibiotischer Therapie.
- Siehe auch Tabelle Sensitivität und Spezifität der verschiedenen Nachweismethoden von H. pylori.
Harnstoff-Atemtest
- Orale Aufnahme von mit Kohlenstoffisotopen (
13C13C oder14C14C) markiertem Harnstoff - Rasche Aufspaltung durch die Urease von H. pylori in Ammoniak und isotopenmarkiertes CO2, das über die Ausatemluft gemessen wird.14
- Sensitivität 85–95
1310
Stuhl-Antigentest
- Nachweis von Helicobacter-Antigen im Stuhl unter Verwendung monoklonaler Antikörper16-17
- Sensitivität 85–95
1310
Serologie
GeringereUnterscheidenSensitivitätnicht zwischen einer aktuellen undSpezifitäteinerimfrüheren,VergleichinzwischenzuaberAtem-eradiziertenund StuhltestInfektion.13,1810- Im klinischen Alltag wenig sinnvoll, Anwendung vor allem in epidemiologischen Studien
1213
Diagnostik bei Spezialist*innen
GastroskopieÖsophago-Gastro-Duodenoskopie (ÖGD)
- Goldstandard der Diagnostik7
Invasive Tests auf H. pylori
- Die Gastroskopie ermöglicht die Durchführung invasiver Tests auf H. pylori.
- Bei
jedempeptischem Ulcus ventriculi oder duodeni soll auf H. pyloriuntersuchtgetestet werden.1210 - Alle invasiven Verfahren basieren auf der Untersuchung von Gewebebiopsien.1
- Weitere Informationen siehe auch Artikel Helicobacter pylori.
Urease-Schnelltest
- Schneller, unkomplizierter und kostengünstigster Bedside-Test1
- Sensitivität 90–95
1310
PCR
- Molekulargenetische Diagnostik mittels Polymerase-Chain-Reaction (PCR)1
- Sensitivität 90–95
1310
Histologie
- Neben Nachweis von H. pylori kann durch eine histologische Untersuchung von Gewebe eine chronische Gastritis nachgewiesen und die Benignität eines Ulkus geklärt werden.
- Sensitivität 80–98
1310
Kultur
- In der Praxis nur im Zusammenhang mit Resistenzbestimmung von Bedeutung
1918 - Sensitivität 70–90 %, Spezifität 100 %
1310
Laboruntersuchungen
- Gastrin bei V.
CT/MRT
- Bei V.
Checkliste zur Überweisung
Ulkuskrankheit
Zweck der ÜberweisungEndoskopie? Therapie?
AnamneseSymptomatik?Frühere Ulzera? St. n. Eradikation?Einnahme von NSAR?Vorerkrankungen?
Klinische UntersuchungErgänzende UntersuchungenLabor:Hb, evtl.Ferritin,Blut im Stuhl?
Therapie
Therapieziele
- Ausheilung des Ulkus
- Eradikation einer H.-pylori-Infektion: signifikanter
EinRückgangpeptischesvonUlcusInzidenzventriculiundoderMortalitätduodenigastroduodenaleristUlkuserkrankungeneinedurchobligateEradikation,Indikationaußerdem Beitrag zurEradikation.Prävention des Magenkarzinoms1310Die Indikation besteht auch bei einem abgeheilten oder anamnestischen Ulkus.13
- Symptomlinderung
Allgemeines zur Therapie
- Die Behandlung beruht auf:
- Allgemeinmaßnahmen
- medikamentöser Therapie
- im Einzelfall interventionelle/operative Therapie von Komplikationen.
Allgemeinmaßnahmen
- Eine Behandlung mit NSAR sollte – wenn möglich – vermieden oder reduziert werden.
- Rauchstopp
- Keine spezielle Schonkost, entscheidend ist die individuelle Verträglichkeit von Speisen.
2019 - Berücksichtigung psychosomatischer Aspekte, ggf. Intervention1
- Stress, psychosoziale Belastung
- Angsterkrankungen, Depression.
H.-pylori-positive Ulkuskrankheit
- Zu Details der Eradikationstherapie siehe auch Artikel Helicobacter pylori.
PrinzipienAllgemeines derzur Eradikation
- Der Nachweis von H. pylori bei Ulcus ventriculi oder duodeni ist eine absolute Therapieindikation.
2120 - Bis vor Kurzem war die clarithromycinbasierte
TripeltherapieTripel-Therapie weltweit Standard, durch Resistenzen verminderte Wirksamkeit.2120- in Deutschland ca. 11
2221
- in Deutschland ca. 11
Vor Eradikation zunächst Prüfung, ob dieRisikofaktoren für eine primäre Clarithromycinresistenzvorhanden sind.2120- Herkunft aus Süd- oder Osteuropa
- frühere Behandlung mit Makrolidantibiotika
- Da die Einnahme von Makroliden häufig nicht sicher eruierbar ist, kann die häufige Einnahme von Antibiotika pragmatisch als indirektes Indiz hierfür gewertet werden.
1213
- Da die Einnahme von Makroliden häufig nicht sicher eruierbar ist, kann die häufige Einnahme von Antibiotika pragmatisch als indirektes Indiz hierfür gewertet werden.
BestehtDiekeinprätherapeutischeerhöhtesResistenzlageResistenzrisikoist von großer Relevanz,kanndiemitWahlderdesklassischenTherapieschemasclarithromycinbasiertensollteStandard-TripeltherapiediebegonnenWahrscheinlichkeitwerdeneiner möglichen Antibiotikaresistenz berücksichtigen.2110DieAllerdingsfrüherunzureichendeüblicheDatenTherapiedauerzurvonlokalen7 TagenResistenzlage für Deutschland, daher wird dieStandardClarithromycin-TripeltherapiebasierteerscheintTriple-Therapieaufgrund verminderter Wirksamkeitneuerdings nicht mehrvertretbar,zurdieErstlinientherapieTherapiedauer sollte heutzutage 14 Tage betragen (oder 10-tägige Bismut-Quadrupeltherapie)empfohlen.12,2310
EradikationsschemataTherapeutischer beiAlgorithmus
Erstlinientherapie
- Da
niedrigeminRisikoDeutschland die Resistenzraten fürClarithromycinresistenzClarithromycin auf > 10 % angestiegen sind, wird die bismuthaltige Quadrupel-Therapie bevorzugt als Erstlinientherapie für mindestens 10 Tage eingesetzt.10
Resistenzprüfung
ErstlinientherapieNach erfolgloser primärer Vierfach-Therapie sollte eine Resistenztestung erfolgen.10
Zweitlinientherapie
- Die Zweitlinientherapie soll unter Berücksichtigung der Resistenztestung über 14 Tage erfolgen mit:10
- Standard-
Tripeltherapie: PPI + Clarithromycin + Amoxicillin (oder Metronidazol)Tripel-Therapie oder BismutFluorochinolon-Quadrupeltherapie
- Standard-
ZweitlinientherapieBismuthaltigen Tripel-Quadrupeltherapie oderFluorchinolon-Tripeltherapie
Drittlinientherapie- Therapie
nach Resistenztestung.
- Therapie
Eradikationsschemata bei erhöhtem Risiko für Clarithromycinresistenz
Drittlinientherapie
ErstlinientherapieNach Versagen einer Zweitlinientherapie sollen weitere Therapieversuche nur durch Spezialist*innen erfolgen.10Bismut-QuadrupeltherapieabnehmendeoderkonkomittierendeantibiotischeQuadrupeltherapieTherapieoptionen nach fehlgeschlagener resistenzadaptierter Zweitlinientherapie
Zweitlinientherapie
Begleitmaßnahmen
Fluorchinolon-Tripeltherapie
TherapiesorgfältigenachAufklärung- Motivation
Resistenztestungzur Therapietreue - Einnahme der Medikamente vor den Mahlzeiten
- Milderung von Antibiotika-Nebenwirkungen durch Probiotika22
- Rauchstopp.
Therapieprotokolle12-1310,1913,20-21-22
- Bei allen Protokollen können folgende PPI 2 x tgl. verabreicht werden: Omeprazol 20
Bismut-Quadrupel-Therapie – 10 Tage
- PPI 1–0–1
- Bismut-Kalium-Salz 140 mg 3–3–3–3
- Tetracyclin 125 mg 3–3–3–3
- Metronidazol 125 mg 3–3–3–3
Standard-TripeltherapieTripel-Therapie (französisch) – 14 Tage
- PPI 1–0–1
- Clarithromycin 500
- Amoxicillin 1.000
Standard-TripeltherapieTripel-Therapie (italienisch) – 14 Tage
- PPI 1–0–1
- Clarithromycin 250–500
- Metronidazol 400–500
mg 1–0–1
Bismut-Quadrupeltherapie – 10 Tage
PPI 1–0–1Bismut-Kalium-Salz 140 mg 3–3–3–3Tetracyclin 125 mg 3–3–3–3Metronidazol 125 mg 3–3–3–3
Konkomittierende Quadrupeltherapie – 7 Tage
PPI 1–0–1Clarithromycin 500 mg 1–0–1Amoxicillin 1.000 mg 1–0–1Metronidazol 400–500mg 1–0–1
Fluorchinolon-TripeltherapieTripel-Therapie – 10 Tage
- PPI 1–0–1
- Levofloxacin 500 mg oder Moxifloxacin 400
- Zu Nebenwirkungen und Anwendungsbeschränkungen von Fluorchinolonen siehe auch Rote-Hand-Brief.
2423
- Zu Nebenwirkungen und Anwendungsbeschränkungen von Fluorchinolonen siehe auch Rote-Hand-Brief.
- Amoxicillin 1.000
H.-pylori-negative Ulkuskrankheit
- Eine NSAR-Therapie ist die häufigste Ursache für eine H.-pylori-negative Ulkuskrankheit und sollte möglichst beendet werden.4
- Medikamentöse Behandlung mit PPI für 4–8 Wochen4,7
- Nach Langzeiteinnahme von PPI ist ein Sä
ure-Reboundurerebound mit Refluxbeschwerden nach dem Absetzen möglich, daher ist eine allmähliche Reduktion sinnvoll.24-25-26
Präventiver Magenschutz
NSAR
WirdBeieineeinigenNSAR-Therapiemedikamentösenbegonnen,Therapiensollteodergleichzeitigklinischen Konstellationen ist einPPIpräventiververabreichtMagenschutzwerden, wenn mindestens 1 Risikofaktor vorliegt:13,25- indiziert.
Ulkus inBei derVorgeschichteAlterIndikationsstellung>ist65zuJahreschwere AllgemeinerkrankungKomedikation: Glukokortikoideberücksichtige,gerinnungsaktiveobSubstanzen, SSRIHelicobacter-pylori-InfektionRisikofaktoren (Eradikationandereindiziertals H. pylori)
NSAR undfür ASS
EinedasgleichzeitigeAuftretenBehandlunggastroduodenalermitUlzeraASSbzw.undRisikofaktorenNSARfürsollteUlkusblutungen/-komplikationenvon einer PPI-Medikation begleitet werdenvorliegen.1310
DualeRisikofaktoren Plättchenhemmungfür gastroduodenale Ulzera
BeiAltergleichzeitiger> 60BehandlungJahre- Ulkusanamnese
- Medikamente: NSAR, ASS
- Andere Risikofaktoren: schwere Begleiterkrankungen, schwere psychosoziale Belastungen, Rauchen
Risikofaktoren für Ulkusblutungen/-komplikationen
- Alter > 60 Jahre
- Ulkusanamnese
- Medikamente: NSAR, ASS, SSRI, P2Y12-Inhibtoren, Antikoagulanzien (Vit-K-Antagonisten, NOAK, Heparine), systemische Kortikosteroide
- Andere Risikofaktoren: schwere Begleiterkrankungen
PPI-Prophylaxe der H.-pylori-negativen Ulkuskrankheit10
- Wenn eine Therapie mit NSAR begonnen wird, soll gleichzeitig eine prophylaktische Therapie mit einem PPI durchgeführt werden, sofern ein weiterer Risikofaktor für das Auftreten eines gastroduodenalen Ulkus und/oder einer Ulkuskomplikationvorliegt. Wenn nur der Risikofaktor Alter (> 60 Jahre) und sonst kein Risikofaktor vorliegt, ist eine Prophylaxe nicht erforderlich.
- Wenn unter einer Dauertherapie mit NSAR ein gastroduodenales Ulkus und/oder eine obere gastrointestinale Ulkusblutung auftritt, sollte das NSAR bis zur Abheilung der Läsionen abgesetzt werden, und anschließend sollte im Falle einer erneuten Gabe eine dauerhafte PPI-Prophylaxe erfolgen.
- Nach Auftreten einer Ulkuskomplikation soll eine Dauerprophylaxe mit einem PPI immer dann erfolgen, wenn die NSAR-Medikation fortgesetzt wird. Dies gilt auch, wenn eine begleitende H.-pylori-Infektion erfolgreich behandelt wurde.
- Wenn eine Monotherapie mit ASS, einem P2Y12-Inhibitor, DOAK oder VKA durchgeführt wird, sollte eine PPI-Prophylaxe erfolgen, sofern mindestens ein weiterer Risikofaktor für das Auftreten eines gastroduodenalen Ulkus und/oder einer Ulkuskomplikation vorliegt. Wenn nur der Risikofaktor Alter (> 60 Jahre) und sonst kein Risikofaktor vorliegt, ist eine Prophylaxe nicht erforderlich.
- Nach Auftreten einer Ulkuskomplikation unter Thrombozytenaggregationshemmung und/oder Antikoagulation soll bei H.-pylori-negativen Patient*innen sowie auch nach erfolgreicher Eradikationstherapie bei zuvor H.-pylori-positiven Patient*innen eine Dauerprophylaxe mit einem PPI erfolgen, wenn die Thrombozytenaggregationshemmung und/oder Antikoagulation fortgesetzt wird.
- Tritt unter einer Monotherapie mit einem P2Y12-Inhibitor eine gastroduodenale Ulkusblutung auf, kann in Ergänzung zu einer dauerhaften PPI-Prophylaxe eine Umstellung auf ASS erwogen werden, wenn dies aus kardiovaskulärer Sicht vertretbar ist.
- Wenn unter einer Monotherapie mit ASS, einem P2Y12-Inhibitor, DOAK oder VKA eine obere gastroduodenale Ulkusblutung eintritt, sollte bei Therapiefortführung eine dauerhafte PPI-Prophylaxe erfolgen. Im Falle einer gastroduodenalen Ulkusblutung unter einer Dauertherapie mit ASS sollte keine Umstellung auf eine Monotherapie mit einem P2Y12-Inhibitor erfolgen.
- Im Falle einer gleichzeitigen Therapie mit zwei gerinnungsaktiven Substanzen soll eine Prophylaxe mit einem PPI erfolgen.
- Wenn unter einer Therapie mit systemischen Kortikosteroiden ein gastroduodenales Ulkus und/oder eine Ulkuskomplikation (z. B. Blutung) auftreten, sollte neben dem Ausschluss einer Infektion mit H. pylori nach Möglichkeit ein Wechsel auf ein anderes Medikament zusätzlich zu einer PPI-Therapie erfolgen. Ist dies nicht möglich, sollte die niedrigst mögliche Steroiddosis gegeben werden und
Clopidogreleine PPI-Propylaxe erfolgen. - Wenn eine Therapie mit SSRI durchgeführt wird, sollte eine
begleitendePPI-Prophylaxe erfolgen, sofern in der Vorgeschichte ein Ulkus und/oder einer Ulkuskomplikation aufgetreten ist oder eine Komedikation mit einem NSAR, einem Coxib oder einem P2Y12 vorliegt. Wenn eine Komedikation mit einem Antikoagulans (DOAK oder VKA) vorliegt, kann eine PPI-MedikationProphylaxe erfolgen.13
Interventionelle und operative Therapie
Interventionelle Therapie
- Eine interventionelle Therapie erfolgt überwiegend im Rahmen einer Blutung, seltener zur Behandlung von Magenausgangs- oder Duodenalstenosen.
- Ca. die Hälfte der OGI-Blutungen wird durch peptische Ulzera verursacht.1
- In der Mehrzahl der Fälle kann eine Blutung endoskopisch gestillt werden.
2726
Operation
- Indikationen zur Operation sind:
2726- interventionell nicht stillbare Blutung
- Perforation
- Malignom
- Magenausgangsstenose.
Verlauf, Komplikationen und Prognose
Komplikationen
- Blutung
- Die Ulkuskrankheit ist die häufigste Ursache für eine OGI-Blutung.
2827
- Die Ulkuskrankheit ist die häufigste Ursache für eine OGI-Blutung.
- Perforation
- Magenausgangsstenose
- H. Pylori erhöht das Risiko für Magenkarzinom und MALT-Lymphom.
- Siehe auch den Artikel Komplikationen bei Magengeschwüren.
Verlauf und Prognose
- Bei kausaler Behandlung sehr gute Prognose6
- Ohne Behandlung einer zugrunde liegenden H.-pylori-Infektion kommt es in 60–90 %
%der Fälle zu Rezidiven.6
Verlaufskontrolle
BeiNachderEradikationstherapieUlkuskrankheitsolltesollimmer eineKontrolle des TherapieerfolgsErfolgskontrolle durchgeführt werden (unabhängig von der Indikation zur Eradikation).1310Ein Magenulkus soll auf jeden Fall endoskopisch kontrolliert werden, ein Duodenalulkus im Fall von Komplikationen.13,29Beim unkomplizierten Duodenalulkus kann eine Kontrolle des Eradikationserfolgs mittels Harnstoff-Atemtest oder Stuhl-Antigentest erfolgen.13KontrolleDurchführung frühestens 4 Wochen nach- Nichtinvasiv kann die Erfolgskontrolle durchgeführt werden durch:
- 13C-Harnstoff-Atemtest – oder -
- Antigen-Stuhltest.
- Bei Vorliegen eines Magenulkus soll nach 4–8 Wochen eine endoskopisch-bioptische Kontrolle durchgeführt werden (bei unvollständiger Abheilung erneut Biopsien zum Malignitätsausschluss).10
- Eine endoskopische Verlaufskontrolle duodenaler Ulzera ist nicht empfohlen, kann aber im Einzelfall beim komplizierten Ulcus duodeni erwogen werden.10
Patienteninformationen
Patienteninformationen in Deximed
Illustrationen
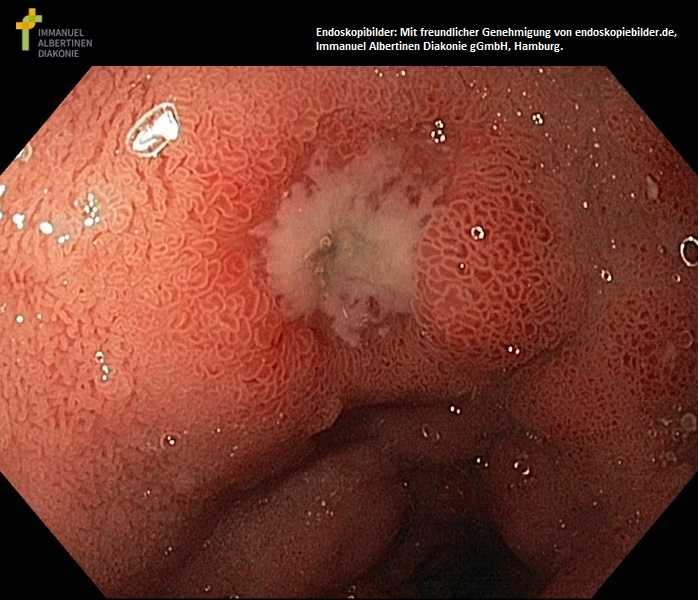
Ulus duodeni mit ödematöser Schleimhaut (mit freundlicher Genehmigung von endoskopiebilder.de, Immanuel Albertinen Diakonie gGmbH, Hamburg)
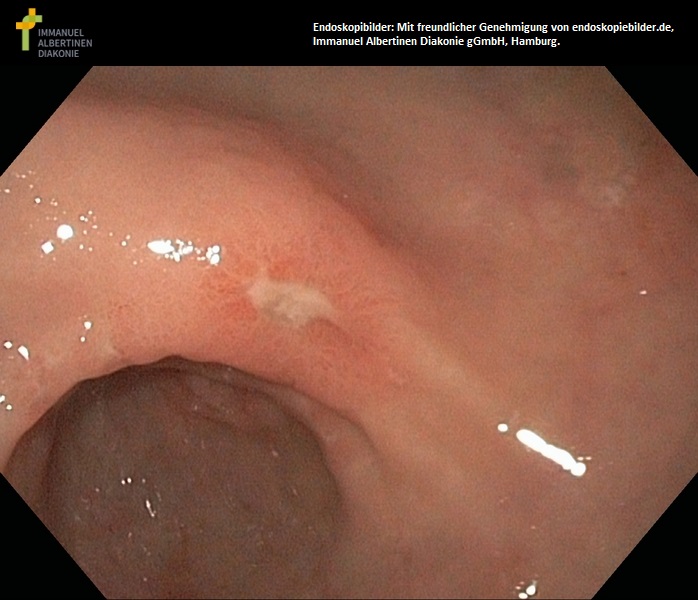
Antrum-Ulkus (mit freundlicher Genehmigung von endoskopiebilder.de, Immanuel Albertinen Diakonie gGmbH, Hamburg)
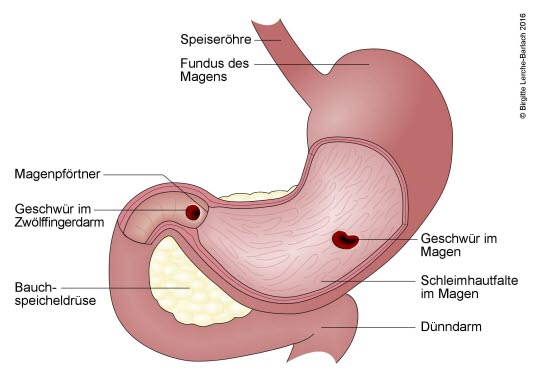
Magen- und Duodenalulkus
Quellen
Leitlinien
- Deutsche Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten. Helicobacter pylori und gastroduodenale Ulkuskrankheit. AWMF-Leitlinie Nr. 021-001. S2k, Stand 2022. www.awmf.org
Literatur
- Robert
-Koch-Institut (RKI). Gastritis, Magen- und Zwölffingerdarmgeschwüre. Gesundheitsberichterstattung des Bundes Heft 55, 2013. www.rki.de - Malfertheiner P. Peptic ulcer disease. Lancet 2009; 374: 1449-1461. doi:10.1016/S0140-6736(09)60938-7 DOI
- Lanas A, Chan FKL. Peptic ulcer disease. Lancet 2017; 390: 613–624. www.ncbi.nlm.nih.gov
- Dovjak P. Ulcus duodeni, Ulcus ventriculi und Helicobacter pylori. Z Gerontol Geriat
2172017; 50: 159-169. doi:10.1007/s00391-017-1190-x DOI - Sung J, Kuipers E, El-Serag H. Systematic review: the global incidence and prevalence of peptic ulcer disease. Aliment Pharmacol Ther 2009; 29: 938-46. doi:10.1111/j.1365-2036.2009.03960.x DOI
- Anand B. Peptic Ulcer Disease. Medscape, updated Apr 26, 2021. Zugriff 28.12.21. emedicine.medscape.com
- Peptic ulcer disease. BMJ Best Practice, last updated Dec 11, 2020, Zugriff 28.12.21. bestpractice.bmj.com
- Fashner J, Gitu A. Diagnosis and Treatment of Peptic Ulcer Disease and H. pylori Infection. Am Fam Physician 2015; 91: 236-242. www.aafp.org
- Mössner J. Nebenwirkungen von nichtsteroidalen Antiphlogistika (NSAR) im Gastrointestinaltrakt. eMedpedia. Zugriff 03.01.22 www.springermedizin.de
- Deutsche Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten. Helicobacter pylori und gastroduodenale Ulkuskrankheit. AWMF-Leitlinie Nr. 021-001. S2k, Stand 2022. register.awmf.org
- Malfertheiner P, Schulz C (DGIM). Helicobacter-pylori-assoziierte Erkrankungen. eMedpedia, Zugriff 29.12.21 www.springermedizin.de
- Charpignon C, Lesgourgues B, Pariente A et al. Peptic ulcer disease: one in five is related to neither Helicobacter pylori nor aspirin/NSAID intake. Aliment Pharmacol Ther 2013; 38: 946–54. www.ncbi.nlm.nih.gov
- Fischbach W. Aktuelle Diagnostik und Therapie der Helicobacter-pylori-Infektion. GastroNews 2019; 06: 28-34. doi:10.1007/s15036-019-0484-9 DOI
Deutsche Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten. Helicobacter pylori und gastroduodenale Ulkuskrankheit. AWMF-Leitlinie Nr. 021-001, Stand 2016 (abgelaufen).www.awmf.org- Keller J, Franke A, Storr M, et al. Klinisch relevante Atemtests in der gastroenterologischen Diagnostik – Empfehlungen der Deutschen Gesellschaft für Neurogastroenterologie und Motilität sowie der Deutschen Gesellschaft für Verdauungs- und Stoffwechselerkrankungen. Z Gastroenterol 2005; 43: 1071-1090. doi:10.1055/s-2005-858479 DOI
- Best L, Takwoingi Y, Siddique S, et al. Non‐invasive diagnostic tests for Helicobacter pylori infection. Cochrane Database of Systematic Reviews 2018; 3: CD012080. doi:10.1002%2F14651858.CD012080.pub2 Cochrane (DOI)
- Gisbert JP, Pajares JM. Diagnosis of Helicobacter pylori infection by stool antigen determination: A systematic review. Am J Gastroenterol 2001; 96: 2829-38. PubMed
- Calvet X, Ramirez-Lázaro MJ, Montserrat A, et al. Comparative accuracy of 3 monoclonal stool tests for diagnosis of Helicobacter pylori infection among patients with dyspepsia. Clin Infect Dis 2010; 50: 323-8. PubMed
Garza-Gonzalez E, Bosques-Padilla F, Tijerina-Menchaca R, et al. Comparison of endoscopy-based and serum-based methods for the diagnosis of Helicobacter pylori. Can J Gastroenterol 2003; 17: 101-6.PubMed- Fischbach W. Helicobacter Pylori-Infektion: Wann testen und wie therapieren? Dtsch Arztebl 2016 2016; 113: 4-6. doi:10.3238/PersInfek.2016.05.27.01 DOI
- Internisten im
NetztNetz: Magen-/Darmgeschwür. Zugriff 03.01.22. www.internisten-im-netz.de - Wagner S. Neue Empfehlungen in der H.-pylori-Leitlinie. MMW - Fortschritte der Medizin 2018; 19: 61-62. doi:10.1007/s15006-018-1090-z DOI
- Fischbach W, Malfertheiner P. Helicobacter pylori infection—when to eradicate, how to diagnose and treat. Dtsch Arztebl Int 2018; 115: 429-436. doi:10.3238/arztebl.2018.0429 DOI
YuanMcFarland L, Huang Y,FordWangAC, Khan KJL, et al.OptimumSystematicdurationreviewofandregimensmeta-analysis: Multi-strain probiotics as adjunct therapy for Helicobacter pylori eradication and prevention of adverse events.CochraneUnitedDatabaseEuropeanSystGastroenterolRev.J20132016;Dec4:11;12:CD008337546-561.Cochrane (DOI)www.ncbi.nlm.nih.gov- Bundesinstitut für Arzneimitel und Medizinprodukte.Rote-Hand-Brief zu Fluorchinolon-Antibiotika: Schwerwiegende und anhaltende, die Lebensqualität beeinträchtigende und möglicherweise irreversible Nebenwirkungen. Zugriff 02.01.22. www.bfarm.de
- Gross M, Aksoy J, op den Winkel P. Wann ist der Einsatz von PPI sinnvoll? MMW - Fortschrite der Medizin 2020; 162: 58-63. www.springermedizin.de
- Kim J, Blackett J, Jodorkovsky D. Strategies for Effective Discontinuation of Proton Pump Inhibitors. Curr Gastroenterol Rep 2018; 20: 27. doi:10.1007/s11894-018-0632-y DOI
- Behrman SW. Management of complicated peptic ulcer disease. Arch Surg 2005; 140: 201-8. PubMed
- Götz M. Gastrointestinale Blutungen. Gastroenterologe 2018; 13: 379-390. doi:10.1007/s11377-018-0285-2 DOI
Lübbers H, Mahlke R, Lankisch P, et al. Kontrollendoskopie in der Gastroenterologie: Sinnvoll oder Ballast? Dtsch Arztebl Int 2010; 107: 30-36. doi:10.3238/aerztebl.2010.0030DOI
Autor*innen
- Michael Handke, Prof. Dr. med., Facharzt für Innere Medizin, Kardiologie und Intensivmedizin, Freiburg i. Br.
- Guido Schmiemann, Dr. med., Facharzt für Allgemeinmedizin, Bremen (Review)
- Die ursprüngliche Version dieses Artikels basiert auf einem entsprechenden Artikel im norwegischen hausärztlichen Online-Handbuch Norsk Elektronisk Legehåndbok (NEL, https://legehandboka.no/).