Zusammenfassung
- Definition:Anämie, die durch Eisenmangel verursacht wird.
- Häufigkeit:Etwa 20 % der europäischen Frauen im reproduktionsfähigen Alter. Gesamtprävalenz 5–10 %.
- Symptome:Müdigkeit, Schwindel, verminderte Leistungsfähigkeit, Konzentrationsschwäche, Palpitationen, Dyspnoe, Thoraxschmerzen bei Anstrengung.
- Befunde:Blässe, Antriebslosigkeit, Tachykardie, Dyspnoe.
- Diagnostik:Hb, Ferritin, MCV, CRP, evtl. andere Eisenparameter.
- Therapie:Ursachenabklärung, Ernährungsberatung, ggf. Eisensubstitution.
Allgemeine Informationen
- Sofern nicht anders gekennzeichnet, basiert der gesamte Artikel auf diesen Referenzen.1-4
Definition
- Eisenmangel
- erniedrigtes Speichereisen (Ferritin)
- Eisenmangelanämie
- Eisenmangel + niedriger Hb-Wert
- Definition Anämie
- Hb < 12 g/dl (< 7,5 mmol/l) für Frauen (Norm 12–16 g/dl [7,5–9,9 mmol/l])
- Hb < 14 g/dl (< 8,7 mmol/l) für Männer (Norm 14–18 g/dl [8,7–11,2])
Häufigkeit
- Prävalenz in Europa
- ca. 5–10 %
- Frauen im gebärfähigen Alter ca. 20 %
- Kinder ca. 10–15 % (meist ernährungsbedingt)
Physiologie
- Eisenbilanz wird überwiegend durch die intestinale Resorption bestimmt.
- reguliert durch das hepatische Hormon Hepcidin
- Eisen geht nur durch Blutverlust, Hämolyse und durch Abschilferung von Epithelzellen verloren.
- Männer und nicht menstruierende Frauen verlieren ca. 1 mg Eisen pro Tag. Menstruierende Frauen verlieren 0,6–2,5 % mehr Eisen pro Tag.
- ca. 10–40 mg Eisen pro Menstruationszyklus, abhängig von der Stärke der Menstruationsblutung
- Bei einer Schwangerschaft werden netto ca. 600 mg zusätzliches Eisen benötigt.
- Eine Bluttransfusion mit 500 ml Blut enthält 250 mg Eisen.
Eisenresorption
- Nur 5–10 % des Nahrungseisens werden resorbiert.
- überwiegend im Duodenum
- Bei Eisenüberladung wird die Resorption verringert.
- Die Resorption kann sich bei einem Eisendefizit um das Drei- bis Fünffache erhöhen.
- Eisen in der Nahrung ist in 2 Formen verfügbar:
- Hämeisen, das in Fleisch und Fisch enthalten ist (Hämoglobin, Myoglobin, Zytochrome).
- Nicht-Hämeisen, das in Pflanzen und Milchprodukten enthalten ist.
- Hämeisen wird nahezu unabhängig von anderen Bestandteilen der Nahrung resorbiert, während Nicht-Hämeisen erst in die zweiwertige Eisenform reduziert werden muss.
- Die Bioverfügbarkeit von Nicht-Hämeisen ist auf die Magensäure angewiesen und je nach Nahrung, die entweder die Aufnahme stimuliert (z. B. Vitamin C, Fleisch) oder hemmt (z. B. Kalzium, Vollkorngetreide, Tee, Kaffee, Wein), sehr unterschiedlich.
Ätiologie und Pathogenese
- Eisenmangel entsteht, wenn der Eisenbedarf des Körpers die Eisenresorption aus der Nahrung übersteigt.
- Ein Kind im Wachstum hat nahezu den gleichen Eisenbedarf wie ein erwachsener Mann. Es isst jedoch weniger und hat daher ein deutlich größeres Risiko für Eisenmangel als ein Erwachsener.
- Häufige Ursachen für Eisenmangel
- Fehl- und Mangelernährung
- gestörte Resorption
- physiologischer Verlust bei Frauen (Menstruation)
- okkulter Blutverlust
Disponierende Faktoren
- Fehlernährung und Malabsorption oft in Kombination
- Personengruppen mit häufigem Eisenmangel
- Säuglinge, Milchanämie
- Kinder im Alter von 1–5 Jahren
- weibliche Jugendliche
- Schwangere
- Frauen, die zur Kontrazeption ein IUP verwenden (nicht Hormonspirale).
- Personen, die häufig Blut spenden.
- Personen, die NSAR und/oder Antikoagulanzien einnehmen.
- nach Magenresektion
- Von Zöliakie oder entzündlicher Darmerkrankung (ulzeröse Kolitis oder Morbus Crohn) Betroffene
- Infektion mit Helicobacter pylori
- Die Eradikation von H. pylori kann nachweislich den Eisenmangel korrigieren.
- Die Einnahme eines Protonenpumpenhemmers ist mit einem erhöhten Eisenmangelrisiko assoziiert.5
ICPC-2
- B80 Eisenmangelanämie
ICD-10
- Nach ICD-10-GM Version 20226
- D50.- Eisenmangelanämie
- D50.0 Eisenmangelanämie nach Blutverlust
- D50.1 Sideropenische Dysphagie
- D50.8 Sonstige Eisenmangelanämien
- D50.9 Eisenmangelanämie, nicht näher bezeichnet.
- E61.- Mangel an sonstigen Spurenelementen
- E61.1 Eisenmangel
- D50.- Eisenmangelanämie
Diagnostik
Diagnostische Kriterien
- Anämie, niedriges MCV
- Ferritin unter dem Grenzwert
- < 30 µg/l (< 63 pmol/l)1
- <12 µg/l (25 pmol/l): Eisenspeicher völlig entleert
- Normalwerte Erwachsene
- männlich: 30,0–400,0 µg/l (63–844 pmol/l)
- weiblich: 15,0–150,0 µg/l (32–317 pmol/l)
- < 30 µg/l (< 63 pmol/l)1
- Löslicher Transferrin-Rezeptor (sTfR) erhöht
- Eisenmangelanämie ist keine Abschlussdiagnose, sondern erfordert eine Ursachensuche.2
Differenzialdiagnosen
- Resorptionsstörungen (z. B. bei Zöliakie oder chronisch entzündlichen Darmerkrankungen)
- Anämie bei Infektion
- Anämie bei chronischer Erkrankung
- z. B. bei chronisch entzündlichen Erkrankungen wie rheumatoide Arthritis
- Chronischer Blutverlust, z. B. bei Menorrhagie
- Seltene genetische Ursachen, z. B. eisenrefraktäre Eisenmangelanämie (Iron-Refractory Iron Deficiency Anemia, IRIDA)
- Vitamin-B12-Mangel
- Folatmangel
- Myelodysplastisches Syndrom
- Thalassämie
Anamnese
Typische Symptome
- Müdigkeit, Schwindel, verminderte körperlich Leistungsfähigkeit, Palpitationen, Dyspnoe, Thoraxschmerzen bei Anstrengung
- In seltenen Fällen Schluckbeschwerden, Plummer-Vinson-Syndrom (mit Mundwinkelrhagaden, Zungenbrennen)
Akuter oder chronischer Blutverlust
- Akuter Blutverlust? Teerstuhl, Blutbeimengungen im Stuhl, Blut im Urin oder andere bekannte Blutungen?
- Starke Menstruationsblutungen? IUP (Spirale)? Blutspenden?
Ernährung
- Die Ernährungsanamnese ist besonders wichtig bei Kindern, Jugendlichen und alleinlebenden älteren Personen. Eine vollwertige Ernährung enthält ca. 5 mg Eisen pro 1.000 kcal zugeführter Energie.
- besonderes Augenmerk bei vegetarischer oder veganer Ernährung
- Größe und Gewicht sind Grundlage für die Bewertung des Ernährungsstatus.
- Deutsche Gesellschaft für Ernährung (DGE): Tabelle Eisenbedarf nach Altersgruppe und Geschlecht
- Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen (IQWiG): Tabellen zum Eisengehalt verschiedener Nahrungsmittel
Klinische Untersuchung
Allgemeines
- Anämiesymptome wie Blässe, Müdigkeit, Tachykardie, Tachypnoe
- Nur bei schwerem Eisenmangel: glatte Zunge, spröde Nägel, Cheilitis (Lippenentzündung)
Magen-Darm
- Palpation und ggf. Sonografie des Abdomens
- evtl. Tumoren
- Ulkuskrankheit oder Gastritis können zu Blutverlust führen.
- Rektal-digitale Untersuchung
Teleangiektasien
- Evtl. Hinweis auf Morbus Osler oder Alkoholkonsumstörung
- blutende Ösophagusvarizen bei chronischer Lebererkrankung, z. B. infolge einer Alkoholkonsumstörung
Ergänzende Untersuchungen
Leitlinie: Empfohlene Labordiagnostik2-3
- Algorithmus zur Abklärung eines Eisenmangels
- Serumferritin
- sensitivster Parameter des Eisenstoffwechsels
- Reflektiert die intrazelluläre Ferritinkonzentration und somit die Füllung der Eisenspeicher.
- Kann bei chronischen Leberkrankheiten oder systemischen Entzündungsreaktionen erhöht sein.
- Blutbild
- Hb, MCH und MCV vermindert
- Die Retikulozytenzahl kann normal oder niedrig sein, bei länger anhaltenden Blutungen aber auch kompensatorisch erhöht.
- erneute Blutbildkontrolle 1 Woche nach der Substitutionsbehandlung
- Bei typischer Dynamik mit Retikulozytose („Retikulozytenkrise“) und Hb–Anstieg ist die Diagnose einer alimentären Eisenmangelanämie belegt. Eine solche reaktive Retikulozytose tritt allerdings nur bei schwerer Anämie auf.
- Löslicher Transferrin-Rezeptor (sTfR)
- Wird abhängig vom zellulären Eisenstatus reguliert.
- Ist beim Eisenmangel erhöht, unabhängig von Begleiterkrankungen.
- geeignet zur Diagnostik eines Eisenmangels bei chronischen Leberkrankheiten oder systemischen Entzündungsreaktionen
- Ggf. Retikulozytenhämoglobin (Ret-Hb), Content of Hemoglobin in Reticulocytes (CHr)
- Reflektiert die Effizienz der Hämoglobinisierung von Erythrozyten.
- CHr-Werte < 26 pg gelten als beweisend für eine eisendefizitäre Erythropoese.
Schwangerschaft
Mutterschaftsrichtlinien7
- Hämoglobin sollte gemessen werden.
- möglichst frühzeitig bei der ersten Untersuchung nach Feststellung der Schwangerschaft
- in der Regel ab dem 6. Schwangerschaftsmonat – und –
- innerhalb der ersten postpartalen Woche
- Ist der Hb > 11,2 g/dl (> 7 mmol/l), sind keine weiteren Maßnahmen oder Untersuchungen des Eisenstoffwechsels notwendig.
Untersuchung auf gastrointestinale Erkrankung
- Außer bei ganz offensichtlichen Ursachen (z. B. Menorrhagien) ist bei jeder Eisenmangelanämie die Suche nach okkulten Blutungsquellen im Gastrointestinaltrakt erforderlich (iFOBT, endoskopische Diagnostik des GI-Trakts).8
- Dies ist unabhängig davon, ob Blut im Stuhl sichtbar ist. Ein positives Ergebnis bestätigt die Blutungsanämie.
- Männer > 50 Jahre und postmenopausale Frauen haben beim Nachweis einer Eisenmangelanämie ein um das 20-Fache erhöhtes Risiko, innerhalb von 2 Jahren an Darmkrebs zu erkranken (III).
Diagnostik bei Spezialist*innen
- Gynäkologische Untersuchung
- bei starken Menstruationsblutungen oder postmenopausalen Blutungen
- Andere Untersuchungen in priorisierter Reihenfolge
- Gastroskopie mit Dünndarmbiopsie
- Koloskopie
- Röntgenaufnahme des Dünndarms
Indikationen zur Überweisung
- Weiterführende Diagnostik
- Koloskopie, ggf. Gastroskopie
- gynäkologische Untersuchung
- Erhebliche Allgemeinsymptome und ggf. Transfusionsbedarf
Therapie
Therapieziele
- Normalisierung von Hb und MCV sowie des Serumferritins (auf ca. 50 µg/dl [105 pmol/l])
Allgemeines zur Therapie
- Wenn möglich, eine evtl. Blutung stoppen.
Eisensubstitution
- Bietet eine viel schnellere Korrektur des Eisenmangels, als mit einer eisenreichen Ernährung möglich wäre.
- Indikationen
- eisendefizitäre Erythropoese
- Bei alleinigem Speichereisenmangel sollte nur in folgenden Situationen substituiert werden:
- Schwangerschaft
- dialysepflichtige Niereninsuffizienz
- Hochleistungssport
- frühere Behandlung einer Eisenmangelanämie.
- Berechnung des zu substituierenden Eisendefizits nach Ganzoni:
- Eisendefizit (mg) = [Soll-Hb (g/dl) – Ist-Hb (g/dl)] x Körpergewicht (kg) x 2,4 + Speichereisen (mg)
- Speichereisen bei Körpergewicht < 35 kg: 15 mg/kg KG
- Speichereisen bei Körpergewicht > 35 kg: pauschal 500 mg
- Bei adipösen Personen soll bei der Berechnung das geschätzte fettfreie Körpergewicht eingesetzt werden.
- Auch die Gewichtszunahme bei hydropischer Dekompensation ist bei der Bewertung des Eisenbedarfs zu berücksichtigen.
- Eisendefizit (mg) = [Soll-Hb (g/dl) – Ist-Hb (g/dl)] x Körpergewicht (kg) x 2,4 + Speichereisen (mg)
- Dauer der Eisensubstitution4
- Bei adäquater Eisensubstitution kann ein Hb-Anstieg von 1 g/dl (0,62 mmol/l) im Laufe von 2–3 Wochen erwartet werden.
- Nach Korrektur des Hb-Werts dauert es meist 4–6 Monate, bis die Eisenspeicher aufgefüllt sind.
Ursachen bei fehlendem Ansprechen der Substitutionstherapie
- Falsche Diagnose
- Gleichzeitiges Vorliegen einer anderen Anämieform
- Anhaltender Blutverlust
- Zu niedrig dosierte Eisensubstitution oder ein Eisenpräparat, das schlecht resorbiert wird.
- Komplizierende Erkrankung mit verminderter Knochenmarksaktivität
- Unzureichende Therapietreue der behandelten Person
Empfehlungen für Patient*innen
- Umstellung der Ernährung auf eine eisenreiche Kost (siehe Abschnitt Ernährung)
Medikamentöse Therapie
Eisensubstitution9
- Eisenpräparate gibt es in Form von Tabletten, dünndarmlöslichen Kapseln, Depottabletten, Tropfen oder Injektionslösungen.
- Zweiwertige Eisensalze (Fe2+) bevorzugen.
- als Sulfate, Gluconate, Chloride oder Fumarate verfügbar
- Dosis
- je nach Verträglichkeit 50–200 mg/d
- Eine intermittierende Dosierung, z. B. mit 60–100 mg einmal pro Woche, scheint bei Frauen mit Eisenmangelanämie den Hb-Wert wirksam zu erhöhen, bei besserer Verträglichkeit im Vergleich zur täglichen Einnahme.10
- Bei älteren Personen mit Eisenmangelanämie scheint auch mit einer niedrigen Dosis (15 oder 50 mg/d) ein adäquater Anstieg des Hb erreicht zu werden, bei besserer Verträglichkeit im Vergleich zur konventionellen Dosis (150 mg/d).
- Einnahmemodus
- eine halbe Stunde vor oder 2 Stunden nach dem Essen
- Nebenwirkungen, die die orale Zufuhr häufig limitieren:
- Magenschmerzen
- Obstipation (Prophylaxe: ausreichende Trinkmenge und ggf. Laxanzien)
- Übelkeit
- Diarrhö
- Ascorbinsäure (Vitamin C)
- Die Resorption von ionisiertem Eisen lässt sich durch gleichzeitige Aufnahme von Vitamin C (25–100 mg) erhöhen.
- Faktoren, die Eisenresorption hemmen:
- Lebensmittel, die reich an Tannin (z. B. Tee) oder Phytaten (z. B. Kleie, Vollkornprodukte) sind.
- Medikamente, die den pH-Wert des Magens erhöhen (Antazida, H2-Blocker, Protonpumpenhemmer).
Parenterale Eisensubstitution
- Indikationen
- Zwei verschiedenen Eisenpräparate wurden nicht vertragen.
- Eisenresorptionsstörung
- Orale Medikation reicht nicht aus oder wird nicht toleriert.
- Intravenöse Eisenpräparate können schwere allergische Reaktionen verursachen.
EMA-Empfehlungen: Risikomanagement allergischer Reaktionen bei intravenöser Anwendung von Eisenpräparaten11
- Eisenpräparate zur intravenösen Anwendung sollten nur in einem Umfeld, das für die Durchführung von Wiederbelebungsmaßnahmen ausgerüstet ist, gegeben werden, sodass Personen, die eine allergische Reaktion erleiden, umgehend behandelt werden können.
- Die Praxis, dass die Behandelten zuerst eine niedrige Testgabe erhalten, ist keine zuverlässige Vorgehensweise, um vorauszusagen, wie die Person reagiert, wenn die volle Dosis gegeben wird. Eine Testgabe wird daher nicht mehr empfohlen.
- Bei jeder Dosis von intravenös angewendetem Eisen wird zu Vorsicht geraten, auch wenn vorherige Gaben gut vertragen wurden.
In der Schwangerschaft
- Eisenenthaltende Arzneimittel zur intravenösen Anwendung sollten nicht während der Schwangerschaft angewendet werden, es sei denn, dies ist eindeutig erforderlich. Die Behandlung sollte auf das 2. und 3. Trimenon begrenzt sein, sofern der Nutzen der Behandlung eindeutig gegenüber den Risiken für das ungeborene Kind überwiegt.
- Studien zeigen, dass bei intravenöser Eisensubstitution der Hb-Wert etwas mehr ansteigt, als bei peroraler Einnahme und der Bedarf an Erythrozytenkonzentraten reduziert wird.12
- Besonders relevant z. B. bei entzündlichen Darmerkrankungen, die sich durch perorale Eisenpräparate verschlechtern können.
- Verabreichungsart
- Eisen(III)-Komplex Verbindungen werden intravenös, bevorzugt als Kurzinfusion verabreicht.
- Siehe Tabelle Eisenmangelanämie, Liste der in Deutschland zugelassenen Dextra-freien i. v. Eisenkomplexe.
- Bei jeder intravenösen Verabreichung besteht die Gefahr einer anaphylaktischen Reaktion: Überwachung ca. 20 Minuten nach der Verabreichung, bei gleichzeitig verfügbarer Bereitschaft zur Akutbehandlung.
- Nebenwirkungen
Bluttransfusion
Sekundärbehandlung
- Kausaltherapie, wenn durchführbar
- z. B. Kolonresektion bei Kolonkarzinom
Prävention
- Gesunde Ernährung. Siehe auch Patientenartikel Ernährung bei Eisenmangel.
Verlaufskontrolle
- Erste Kontrolle: 3–4 Wochen nach Behandlungsbeginn
- Normaler Hb-Anstieg unter Eisensubstitution: 0,5–0,7 g/dl (0,3–0,4 mmol/l) pro Woche, wenn keine akute Blutung vorliegt.
- Kontrolliert werden:
Patienteninformationen
Patienteninformationen in Deximed
Illustrationen
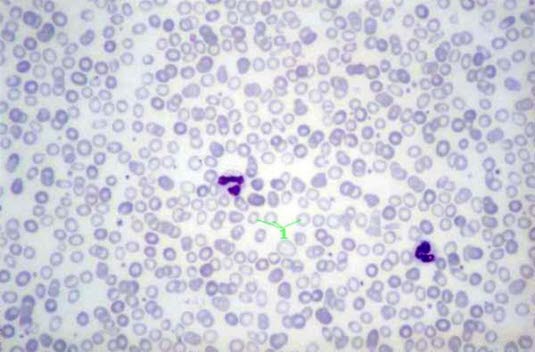
Blutausstrich, Nachweis der Eisenmangelanämie
Quellen
Leitlinien
- Gesellschaft für Pädiatrische Onkologie und Hämatologie (GPOH). Eisenmangelanämie. AWMF-Leitlinie Nr. 025-021. S1, Stand 2021. www.awmf.org
- Deutsche Gesellschaft für Hämatologie und Medizinische Onkologie (DGHO). Onkopedia Leitlinien. Eisenmangel und Eisenmangelanämie. Stand Juli 2021. www.onkopedia.com
- Gemeinsamer Bundesausschuss (G-BA). Richtlinien des Gemeinsamen Bundesausschusses über die ärztliche Betreuung während der Schwangerschaft und nach der Entbindung (Mutterschafts-Richtlinien). Berlin 2021. www.g-ba.de
Literatur
- Camaschella C. Iron-deficiency anemia. Review article. N Engl J Med 2015; 372: 1832-43. doi:10.1056/NEJMra1401038 DOI
- Gesellschaft für Pädiatrische Onkologie und Hämatologie (GPOH). Eisenmangelanämie. AWMF-Leitlinie Nr. 025-021, Stand 2021. www.awmf.org
- Deutsche Gesellschaft für Hämatologie und Medizinische Onkologie (DGHO). Onkopedia Leitlinien. Eisenmangel und Eisenmangelanämie. Stand Juli 2021. www.onkopedia.com
- Goddard AF, James MW, McIntyre AS, Scott BB; British Society of Gastroenterology. Guidelines for the management of iron deficiency anaemia. Gut. 2011;60(10):1309-1316. PubMed
- Lam JR, Schneider JL, Quesenberry CP, Corley DA. Proton pump inhibitor and histamine-2 receptor antagonist use and iron deficiency. Gastroenterology 2017; 152(4): 821-829. pmid:27890768 PubMed
- Deutsches Institut für Medizinische Dokumentation und Information (DIMDI): ICD-10-GM Version 2022. Stand 17.09.2021; letzter Zugriff 28.12.2021. www.dimdi.de
- Gemeinsamer Bundesausschuss (G-BA). Richtlinien des Gemeinsamen Bundesausschusses über die ärztliche Betreuung während der Schwangerschaft und nach der Entbindung (Mutterschafts-Richtlinien). Berlin 2021. www.g-ba.de
- Müller A, Krause SW. Anämie. Diagnostische Schritte für die Hausarztpraxis. Der Allgemeinarzt 2012; 3: 26-31. www.allgemeinarzt-online.de
- Gurusamy KS, Nagendran M, Broadhurst JF, Anker SD, Richards T. Iron therapy in anaemic adults without chronic kidney disease. Cochrane Database of Systematic Reviews 2014, Issue 12. Art. No.: CD010640. DOI: 10.1002/14651858.CD010640.pub2 DOI
- Fernández‐Gaxiola AC, De‐Regil LM. Intermittent iron supplementation for reducing anaemia and its associated impairments in adolescent and adult menstruating women. Cochrane Database of Systematic Reviews 2019, Issue 1. Art. No.: CD009218. DOI: 10.1002/14651858.CD009218.pub3. www.cochranelibrary.com
- European Medicines Agency. Neue Empfehlungen für das Risikomanagement allergischer Reaktionen im Zusammenhang mit Eisen enthaltenden Arzneimitteln zur intravenösen Anwendung. London, EMA, 2013 www.ema.europa.eu
- Litton E, Xiao J, Ho KM. Safety and efficacy of intravenous iron therapy in reducing requirement for allogeneic blood transfusion: Systematic review and meta-analysis of randomised clinical trials. BMJ 2013; 347: f4822. BMJ (DOI)
- Avni T, Bieber A, Grossman A. The safety of intravenous iron preparations: systematic review and meta-analysis. Mayo Clin Proc 2015; 90(1): 12-23. pmid:25572192 PubMed
- Bundesärztekammer (BÄK). Querschnitts-Leitlinien zur Therapie mit Blutkomponenten und Plasmaderivaten. Gesamtnovelle 2020 in der vom Vorstand der Bundesärztekammer auf Empfehlung des Wissenschaftlichen Beirats am 21.08.2020 beschlossenen Fassung. www.bundesaerztekammer.de
Autor*innen
- Thomas M. Heim, Dr. med., Wissenschaftsjournalist, Freiburg
- Die ursprüngliche Version dieses Artikels basiert auf einem entsprechenden Artikel im norwegischen hausärztlichen Online-Handbuch Norsk Elektronisk Legehåndbok (NEL, https://legehandboka.no/).