Zusammenfassung
- Definition:Infektion mit Echinococcus multilocularis, auch Fuchsbandwurm genannt, die zu schwerer tumorähnlicher Erkrankung führen kann. Sie betrifft zunächst nur die Leber, kann sich aber in metastatischem Muster ausbreiten.
- Häufigkeit:Insgesamt sehr seltene Erkrankung, nördliche Hemisphäre. Hochendemisch sind Süddeutschland (Baden-Württemberg, Bayern), die Nordschweiz, Westösterreich und Ostfrankreich.
- Symptome:Nach Jahren leichte Symptome im oberen Gastrointestinaltrakt. Im fortgeschrittenen Stadium Symptome durch Leberbeteiligung.
- Befunde:Keine oder geringe Auffälligkeiten in der klinischen Untersuchung, evtl. Vergrößerung der Leber.
- Diagnostik:Ultraschall als Erstuntersuchung, Biopsie/Histologie und PCR-Untersuchung zur Bestätigung der Diagnose.
- Therapie:Ohne Behandlung hohe Sterblichkeit, deutliche Verbesserung der Prognose durch medikamentöse und chirurgische Behandlung. Kurative Behandlung durch Operation bei bestehender Operabilität, eine medikamentöse Behandlung kann das Fortschreiten der Erkrankung verhindern.
Allgemeine Informationen
Definition
- Infektion mit E. multilocularis, auch Fuchsbandwurm genannt, die zu schwerer tumorähnlicher Erkrankung führen kann. Sie betrifft zunächst nur die Leber, kann sich aber in metastatischem Muster ausbreiten.
- Es gibt 4 Arten von Echinokokken, die Infektionen beim Menschen verursachen können:1
- E. multilocularis, auch Fuchsbandwurm genannt: Verursacht die alveolare Echinokokkose, eine Infektion, die in einigen Fällen zu schweren tumorartigen Lebererkrankungen beim Menschen führt.
- E. granulosus, auch Hundebandwurm genannt: verursacht die zystische Echinokokkose oder Hydatidose, siehe Echinokokkose.
- E. vogeli und E. oligarthrus verursachen die polyzystische Echinokokkose, nur sehr selten Ursache einer Infektion beim Menschen.
- Die Bandwürmer vom Typus T. solium, T. saginata, Hymenolepsis subsp. und Diphyllobothrium subsp. werden im Artikel Bandwurminfektion behandelt.
Häufigkeit
- Vorkommen der Erkrankung beim Menschen vor allem in Gebieten, wo der Bestand an Füchsen mit E. multilocularis infiziert ist.
- Der E. multilocularis kann endemisch in Fuchspopulationen in weiten Teilen der nördlichen Hemisphäre (Sibirien, Nord-Japan, China, Kanada, der Türkei und Mitteleuropa) vorkommen.2
- In Europa gelten Süddeutschland (Baden-Württemberg, Bayern), die Nordschweiz, Westösterreich und Ostfrankreich als hochendemisch
- in Deutschland v. a. in ländlichen Regionen in Bayern und Baden-Württemberg3-4
- zunehmende Ausbreitung auf der nördlichen Hemisphäre über die klassischen Endemiegebiete hinaus2-3
- Häufigkeit in Deutschland: ca. 50 Fälle pro Jahr5
- Infektionen beim Menschen werden mit geringer Inzidenz aus den meisten Länder Europas berichtet, die durchschnittliche Inzidenz liegt bei 0,26 Fällen auf 100.000 Einw. pro Jahr.6
- Risikogruppen: Landwirt*innen, Wald- und Forstarbeiter*innen4
- Die Infektion mit Echinokokken ist leichter möglich geworden, da die Lebensräume von Fuchs und Mensch näher zusammengerückt sind.
- Der E. multilocularis kann endemisch in Fuchspopulationen in weiten Teilen der nördlichen Hemisphäre (Sibirien, Nord-Japan, China, Kanada, der Türkei und Mitteleuropa) vorkommen.2
- Opportunistische Infektion: Die Anzahl immunsupprimierter Menschen nimmt zu und damit auch die Gefahr der Entwicklung einer Erkrankung nach Kontakt mit der Infektion.7
Ätiologie und Pathogenese
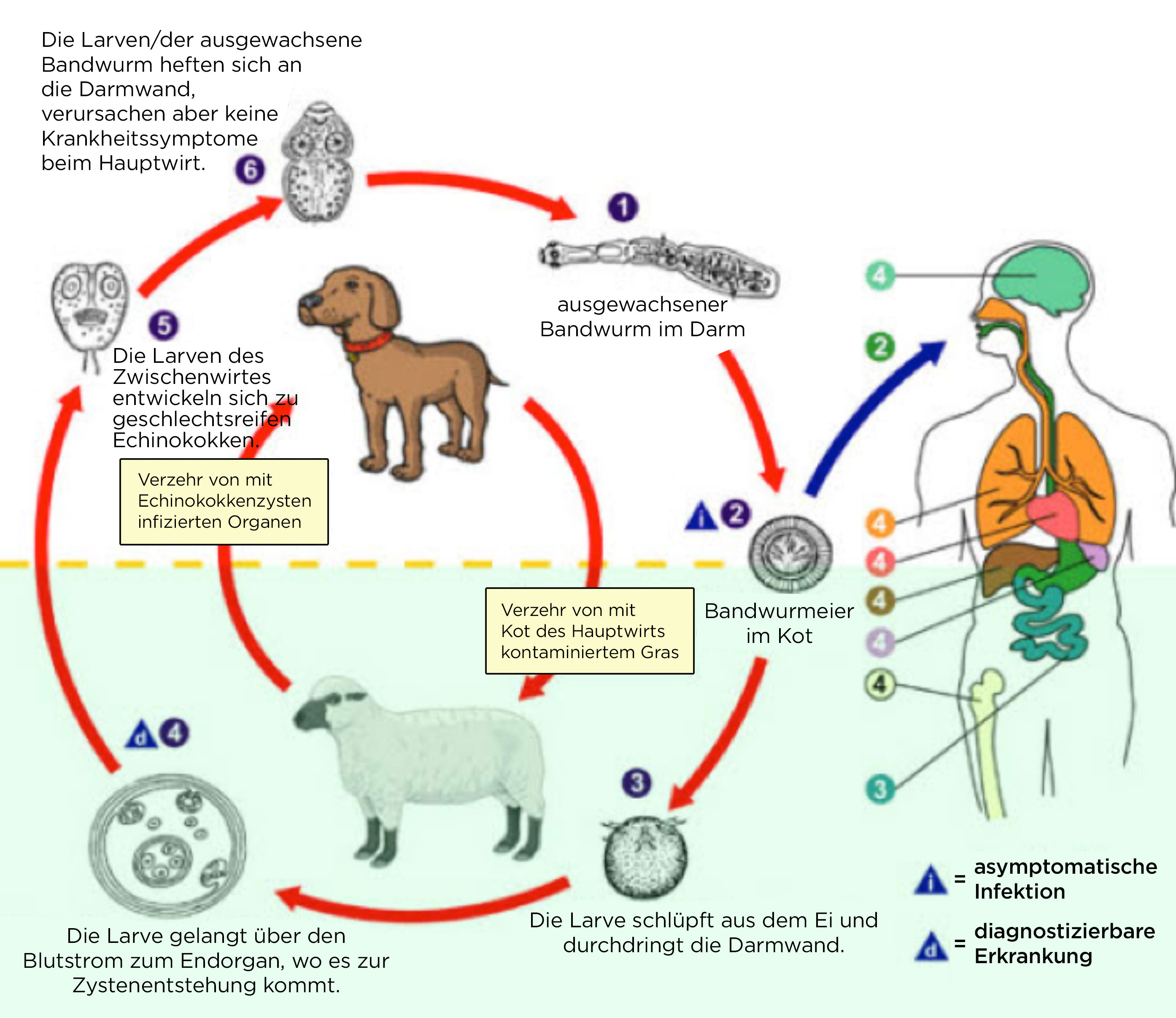
Echinokokken, Lebenszyklus
- Die E.-multilocularis-Bandwürmer sind 2–3 mm lang. Der Mensch ist Fehlzwischenwirt und kann eine lebensbedrohliche Erkrankung entwickeln.
- Hauptwirt: Füchse, auch andere Raubtiere, die sich von den Zwischenwirten ernähren.
- Sie scheiden die infektiösen Bandwurmeier über den Kot aus, die in der Umwelt bis zu Monaten infektiös bleiben.
- Ein infizierter Hund oder eine Katze können über ihren Pelz auch Eier auf den Menschen übertragen.
- Zwischenwirte: Kleinnagetiere, Schafe
- Ansteckung fäkal-oral, wahrscheinlich durch infizierte Beeren oder Pilze8
- Der Lebenszyklus der Echinokokken
- Sexuelle Fortpflanzung im Darm des Hauptwirtes (oft der Fuchs). Geschlechtsreife Bandwürmer produzieren Eier, die mit dem Kot ausgeschieden werden, der dann wiederum den Zwischenwirt infiziert.2
- Beim Zwischenwirt Eindringen in die inneren Organe (besonders die Leber), wobei Zysten mit infiltrativem Wachstum ausgebildet werden.
- Entwicklung des geschlechtsreifen Bandwurms, wenn der Hauptwirt wieder mit Bandwürmern im Larvenstadium infiziert wurde: Wenn der Hauptwirt einen Zwischenwirt frisst.2
- Pathogenese
- Inkubationszeit: nicht genau bekannt, meist vergehen 10–15 Jahre bis zur Diagnose4
- Die Eier der Bandwürmer schlüpfen im Dünndarm des (Fehl-)Zwischenwirtes. Die Larven bohren sich durch die Darmwand und folgen dem Blutfluss, in der Regel zunächst über die Pfortader in die Leber.
- Die Larven verursachen langsam wachsende, geschwulstähnliche, zystische, infiltrierende Veränderungen von geleeartiger Struktur, die sich sowohl kontinuierlich auch als fernmetastasierend ausbreiten können, v. a. in Lunge und Gehirn.2
- Die Infektion wird nicht von Mensch zu Mensch übertragen.
Disponierende Faktoren
- Aufenthalt in einer Region, in der die Infektion auftritt (insbesondere Mitteleuropa). Landwirt*innen und andere Menschen, die in direktem Kontakt mit der Natur leben, sind besonders gefährdet.9
- Verbreitung durch:
- Beeren, Pilze, Gemüse, Fallobst und Trinkwasser
- Kontakt mit dem Pelz des Fuchses
- Haustiere (Hund und Katze)
- Kontakt mit Kot und Erdboden.9
ICPC-2
- D96 Würmer/andere Parasiten
ICD-10
- B67 Echinokokkose (inklusive Hydatidose)
- B67.5 Echinococcus-multilocularis-Infektion [alveoläre Echinokokkose] der Leber
- B67.6 Echinococcus-multilocularis-Infektion [alveoläre Echinokokkose] an mehreren und sonstigen Lokalisationen
- B67.7 Echinococcus-multilocularis-Infektion [alveoläre Echinokokkose], nicht näher bezeichnet
Diagnostik
Diagnostische Kriterien nach WHO-Falldefinition
- Der Abschnitt basiert auf diesen Referenzen.10-11
- Mögliche Infektion
- positive Echinokokken-Serologie oder Nachweis kleiner verkalkter Leberläsionen
- Wahrscheinliche Infektion
- bildgebend typische Organläsion
- positive Echinokokken-Serologie
- Bestätigte Infektion
- bildgebend typische Organläsion
- positive Echinokokken-Serologie in 2 Tests (sensitiver Suchtest und spezifischer Bestätigungstest)
- kompatibler histopathologischer Befund und/oder positiver PCR-Nachweis von E.-multilocularis-Nukleinsäure
Differenzialdiagnosen
- Bösartige Lebertumoren
- Metastasen
- Abszesse
- Hämangiome
Anamnese
- Oft asymptomatisch für 10–15 Jahre nach Infektion4
- Häufig Diskrepanz zwischen großem bildgebendem Befund (meist als Zufallsbefund) und leichten Beschwerden
- Unspezifische Symptome: Druckgefühl im Oberbauch, Schmerzen, Übelkeit, Fieber
- Je nach Lage der Zysten Ikterus, Cholangitis, Zeichen der portalen Hypertension4
Klinische Untersuchung
- Häufig unauffällig
- Hepatomegalie
- perkutorische Dämpfung, tastbare Resistenz, Empfindlichkeit der Leber
- leichte Bauchschmerzen
- Gelbsucht (Ikterus), dank früherer Diagnostik seltener geworden
- Die Pathologie in anderen Organen bietet organspezifische Befunde.2
Ergänzende Untersuchungen in der Hausarztpraxis
- Ultraschall: wichtigste Untersuchung bei der Abklärung symptomatischer Patient*innen und erster Schritt zur Diagnose4
Diagnostik bei Spezialist*innen
- Computertomografie: detaillierteres Bild der Leberanatomie
- Kontrastverstärkte Sonografie und MRT geben zusätzliche auch differenzialdiagnostische Information.
- FDG-PET-CT: zur Beurteilung der Aktivität einer Erkrankung
- Serologische Tests: initial ein sensitiver Suchtest, gefolgt von einem spezifischen Bestätigungstest4
- Punktion der verdächtigen Herde zur histologischen Abklärung und PCR-Diagnostik ist sinnvoll und nicht kontraindiziert.4,8
Indikationen zur Krankenhauseinweisung
- Beim Verdacht auf alveolare Echinokokkose, möglichst in ein spezialisiertes interdisziplinäres Zentrum
Therapie
Therapieziele
- Reduktion der Sterblichkeit
- Wenn möglich, Heilung der Erkrankung
- Verhinderung von Wachstum und Ausbreitung der Veränderungen
- Symptomkontrolle
Allgemeines zur Therapie
- Therapeutische Prinzipien wie bei einer Tumorerkrankung, im interdisziplinären Team festzulegen.
- Zunächst immer medikamentöse Therapie
- Bei lokal begrenztem Wachstum auch chirurgische Therapie
- Nur 30 % der Patient*innen kommen bei Diagnosestellung für eine chirurgische Therapie infrage.
- Operative Therapie nach onkologischen Kriterien11
- Langzeitbehandlung mit Benzimidazolen11
- Wird für inoperable Patient*innen angewendet, um eine Progression zu hemmen.
- Patient*innen, bei denen eine Leberresektion oder Lebertransplantation durchgeführt wurde, sollten noch 2 Jahre nach dem Eingriff weiter damit behandelt werden.
Medikamentöse Therapie
- Medikamentöse Therapie mit Benzimidazolen (Mebendazol, Albendazol)
- Nebenwirkungen der Benzimidazole
- Spiegelbestimmung von Albendazol sinnvoll, da große interindividuelle Schwankungen der Resorption bestehen. Blutabnahme 4 Std. nach Einnahme der Medikation.4
Operative Therapie
- Kurativer Ansatz. Ziel: radikale (R0)-Resektion im Gesunden
- Eine lokale Operabilität ohne Infiltration nichtoperabler Strukturen und ohne Fernmetastasierung muss vorliegen.
- Lebertransplantation: bei weit fortgeschrittenen Befunden ohne Fernmetastasen, ist als Ultima Ratio nur in Einzelfällen beschrieben.4
Prävention
- E. multilocularis ist von Mensch zu Mensch nicht ansteckend, es gibt keinen Impfstoff gegen E. multilocularis, der für Menschen verwendet werden kann.
- Parasiteneier überleben das übliche Einfrieren, sterben aber durch Abkochen und Austrocknen.
- Maßnahmen zur Verminderung des Infektionsrisikos
- Wasser aus Bächen und Seen abkochen.
- Handschuhe tragen, wenn Sie in Berührung mit einem Fuchs kommen.
- Nach der Berührung eines Fuchses, eines Hundes oder einer Katze Hände waschen.
- Vor allen Mahlzeiten Hände waschen.
- sorgfältiges Waschen bodennah wachsender Nahrungsmittel
Meldepflicht
- Meldepflicht gemäß Infektionsschutzgesetz Deutschland (IfSG)13
- Gemäß § 7 Abs. 3 IfSG ist der direkte oder indirekte Nachweis von Echinococcus sp. nichtnamentlich direkt an das RKI zu melden. Primär meldepflichtig sind die diagnostizierenden Labore, die den einsendenden Ärzt*innen einen Durchschlag des Meldebogens schicken. Die einsendenden Ärzt*innen sind verpflichtet, dem Labor nicht zur Verfügung stehende demografische, anamnestische und klinische Angaben auf dem Meldebogen zu ergänzen und den so ergänzten Meldebogen direkt an das RKI zu senden.
- Eindeutige Ultraschallbefunde oder eindeutige Befunde mit anderen bildgebenden Verfahren sind auch ohne serologische Bestätigung meldepflichtig.
Verlauf, Komplikationen und Prognose
Verlauf
- Die Infektion mit E. multilocularis hat in der Regel eine initial symptomfreie Periode von 10–15 Jahren.
- Ohne Behandlung liegt die Mortalität bei 90 %. 4
Komplikationen
- Durch Veränderungen in der Leber:
- portale Hypertonie mit Darmblutungen
- Budd-Chiari-Syndrom
- Cholangitis
- biliäre Zirrhose
- Leberabszess mit Sepsis
- sekundäres Leberversagen.
- Ausbreitung auf benachbarte Organe
- Metastasen bei fortgeschrittener Erkrankung
Prognose
- Unbehandelt 10-Jahres-Mortalität von 90 %2
- Um 1970: durchschnittliche Überlebenszeit in Europa 3 Jahre nach Diagnosestellung
- Mit Behandlung sind 30 % der Fälle heilbar.
- Gesamtmortalität in Europa derzeit unter 5 %, Lebenserwartung nahezu normal2
Verlaufskontrolle
- Multidisziplinäre Behandlung und Nachsorge durch Infektiologie, Hepatologie und Leber- und Transplantationschirurgie11
- Auch kurativ behandelte Fälle sollten mindestes 10 Jahre in regelmäßiger Nachsorge verbleiben.4
- Kontaktpersonen von infizierten Tieren (z. B. Hund, Fuchs, Katze) sollten nach 4 Wochen sowie 6, 12 und 24 Monate nach dem wahrscheinlichen Kontakt serologisch untersucht werden, da so im Falle einer Infektion eine frühzeitige Überwachung und ggf. rechtzeitige Therapieeinleitung möglich wird. Bei anhaltendem Infektionsrisiko sollten die Kontrollen 2-mal jährlich weitergeführt werden. Positive Testergebnisse sollen mit bildgebenden Verfahren verifiziert werden.13
Patienteninformationen
Patienteninformationen in Deximed
Illustrationen

Echinokokken, Lebenszyklus
Quellen
Literatur
- Eckert J, Deplazes P. Biological, epidemiological, and clinical aspects of echinococcosis, a zoonosis of increasing concern. Clin Microbiol Rev. 2004; 17(1): 107-135. pubmed.ncbi.nlm.nih.gov
- Bresson-Hadni S, Spahr L, Chappuis F. Hepatic Alveolar Echinococcosis. Semin Liver Dis 2021; 41(03): 393-408. pmid:PMID: 34161992 PubMed
- Baumann S, Shi R, Liu W, et al., interdisciplinary Echinococcosis Working Group Ulm. Worldwide literature on epidemiology of human alveolar echinococcosis: a systematic review of research published in the twenty- first century. Infection 2019 May 30. pubmed.ncbi.nlm.nih.gov
- Kratzer W, Schmidberger J, Hillenbrand A, Henne-Bruns D, Gräter T, Barth TFE, Grüner B. Alveoläre Echinokokkose: Eine Herausforderung für Diagnostik, Therapie und Klinisches Management Epid Bull 2019;41:423-430. www.rki.de
- Robert Koch-Institut. Infektionsepidemiologisches Jahrbuch meldepflichtiger Krankheiten für 2019, Berlin 2020 ISBN: 978-3-89606-306-9 DOI: 10.25646/6948 www.rki.de
- Moro P, Schantz PM. Echinococcosis. a review. Int J Infect Disease. 2009. 13(2): 125-33 PMID: 18938096 pubmed.ncbi.nlm.nih.gov
- Chauchet A, Grenouillet F , Knapp J, Richou C, Delabrousse E, Dentan C, Millon L, Di Martino V, Contreras R, Deconinck E, Blagosklonov O, Vuitton DA, Bresson-Hadni S, . Increased incidence and characteristics of alveolar echinococcosis in patients with immunosuppression-associated conditions. Clin Infect Dis. 2014; 59(8): 1095-104. pubmed.ncbi.nlm.nih.gov
- Brehm K. Die Echinokokkose – Eine Übersicht und neue Erkenntnisse in der Diagnostik, Therapie und Parasitenbiologie Epid Bull 2017;15:127 – 132 DOI 10.17886/EpiBull-2017-019 www.rki.de
- Craig PS, McManus DP, Lightowlers MW et al. Prevention and control of cystic echinococcosis. Lancet Infect Dis 2007; 6: 285-94. pubmed.ncbi.nlm.nih.gov
- Weltgesundheitsorganisation, Falldefinition der alveolären Echinokokkose, europäische Falldefinition, Amtsblatt der Europäischen Union, 6.7.2018 eur-lex.europa.eu
- Brunetti E, Kern P, and Vuitton DA, Expert consensus for the diagnosis and treatment of cystic and alveolar echinococcosis in humans. Acta Trop. 2010; 114(1): 1-16. PubMed
- Vuitton D, Bresson-Hadni S. Alveolar echinococcosis: evaluation of therapeutic strategies. Expert Opinion on Orphan Drugs 2014; 2: 67-86. www.tandfonline.com
- Robert Koch-Institut. RKI-Ratgeber für Ärzte: Echinokokkose. Berlin, 2005. www.rki.de
Autor*innen
- Franziska Jorda, Dr. med., Fachärztin für Viszeralchirurgie, Ärztin in Weiterbildung Allgemeinmedizin, Kaufbeuren
- Die ursprüngliche Version dieses Artikels basiert auf einem entsprechenden Artikel im norwegischen hausärztlichen Online-Handbuch Norsk Elektronisk Legehåndbok (NEL, https://legehandboka.no/).