Zusammenfassung
- Definition:Als Spina bifida werden Fehlbildungen bezeichnet, die aus einer Differenzierungsstörung der Neuralplatte innerhalb der ersten 4 Schwangerschaftswochen abgeleitet werden. Pädisponierende Faktoren können die Familiengeschichte, Folatmangel in der Schwangerschaft, mütterlicher Diabetes und einzelne Medikamente sein.
- Häufigkeit:Bei den Neuralrohrdefekten zeigt sich eine europäische Gesamtprävalenz von 9,1/10.000 Geburten insgesamt. Laut der diagnosebezogenen Fehlbildungsprävalenz in Organkategorien im Mainzer Geburtenregister (MaMo, populationsbezogen 1990–2014; N = 79.344) zeigt sich eine Prävalenz von 18/10.000 in Deutschland.
- Symptome:Eine Reihe von Symptomen, die das Gehirn oder das Rückenmark betreffen.
- Befunde:Der klinische Befund hängt vom Stadium des Defektes und ggf. einem Hydrozephalus ab.
- Diagnostik:Mittels CT/MRT/Ultraschall können das Ausmaß des Defektes sowie ein evtl. Hydrozephalus diagnostiziert werden.
- Therapie:Als frühe Behandlungsmaßnahme wird der Spinaldefekt chirurgisch verschlossen. Die weitere Behandlung hängt vom Ausmaß des Defektes ab.
Allgemeine Informationen
Definition
- Mit Neuralrohrdefekten wird eine Reihe von Erkrankungen bezeichnet, die sich auf das Gehirn oder das Rückenmark auswirken. Die häufigsten Neuralrohrdefekte sind:
- Anenzephalie, bei der sich das Gehirn nicht entwickelt. Es besteht keine Lebensfähigkeit.
- Spina bifida, als mangelhafter Verschluss des unteren Teils des Neuralrohrs
- Spina bifida kann sich in verschiedenen Schweregraden darstellen und ist eine der häufigsten Fehlbildungen beim Menschen.1
- Spina bifida tritt klinisch auf mit verschiedenen Paralysen und Sensibilitätsverlusten in den unteren Extremitäten, orthopädischen Deformitäten, neurogener Störungen der Blase und des Darmes, Hydrozephalus und Chiari-Malformation Typ 2.
- Hydrozephalus und Chiari-Malformation Typ 2 sind häufig mit nonverbalen Lernschwierigkeiten und exekutiver Dysfunktion verbunden. Die Intelligenz ist in der Regel nicht eingeschränkt.
- Siehe auch den Artikel Neuralrohrdefekte.
Klassifikation2
- Offene Spina bifida (nicht von Haut bedeckt): Spina bifida cystica oder Spina bifida aperta
- Myelomeningozele
- Herniation der Hirnhäute und Spina
- Steht im Zusammenhang mit Hydrozephalus und Chiari-Malformation Typ 2.
- Myeloschisis/Myelozele
- Herniation der Hirnhäute und spinalen Elemente
- Zeichnet sich aus durch eine abgeflachte, plattenartige Masse aus unorganisiertem Nervengewebe.
- Meningozele
- Herniation der Hirnhäute ohne Beteiligung von spinalen Elementen
- Myelomeningozele
- Geschlossene Spina bifida (von Haut bedeckt)
- Spinaldefekte mit sichtbaren Veränderungen im Rücken wie einer asymmetrischen Glutealfalte, einem Hämangiom, behaarten Flecken oder anderen Hautveränderungen
- Die klinischen Symptome variieren erheblich von asymptomatischen bis hin zu schweren neurologischen, urogenitalen, gastrointestinalen oder Muskel-Skelett-Anomalien.
- Spina bifida occulta (mit Haut bedeckt; am Rücken ist nichts Ungewöhnliches zu sehen)
- Es liegt lediglich eine mangelhafte vertebrale Fusion vor, ohne dass die Spina (das Rückenmark betroffen wäre), und ohne klinische Relevanz.
Häufigkeit
- Neuralrohrdefekte sind nach angeborenen Herzfehlern die zweithäufigsten Geburtsdefekte.
- Spina bifida und Anenzephalie treten bei 1 von 1.000 Schwangerschaften auf.2
- Die Inzidenz ist im letzten Jahrhundert gesunken, was vor allem daran liegt, dass Schwangerschaften, bei denen eine Anenzephalie und schwere Ausprägungen von Spina bifida vorliegen, abgebrochen werden, sowie an der vorbeugenden Einnahme von Folsäure.
- Bei den Neuralrohrdefekten zeigt sich eine europäische Gesamtprävalenz von 9,1/10.000 Geburten insgesamt. Laut der diagnosebezogenen Fehlbildungsprävalenz in Organkategorien im Mainzer Geburtenregister (MaMo, populationsbezogen 1990–2014; N = 79.344) zeigt sich eine Prävalenz von 18/10.000 in Deutschland.3
- Spina bifida occulta
- Verläuft normalerweise asymptomatisch.
- häufig ein zufälliger radiologischer Befund bei 10‒15 % der Bevölkerung
- Geschlossene Spina bifida
- häufiger als Spina bifida aperta, seltener als Spina bifida occulta
- Offene Spina bifida
- Die Erkrankung gehört zu den häufigsten schweren Fehlbildungen beim Menschen.
- Bei den meisten gibt es kein zugrunde liegendes Fehlbildungssyndrom.
Ätiologie und Pathogenese
- In den meisten Fällen ist die Ursache unbekannt, aber es wurde ein Zusammenhang mit einem zu niedrigen Folsäure-Spiegel nachgewiesen.4
- Die Ursachen dafür sind heterogen und umfassen Chromosomenanomalien, einzelne Genmutationen und die Exposition mit teratogenen Stoffen.
- Evtl. genetische Ursachen sind komplex und können nicht auf spezifische oder eindeutige Genmutationen zurückgeführt werden.1
Verschluss des Neuralrohrs1
- Das Neuralrohr, die embryotische Struktur, die sich zu Rückenmark und Gehirn entwickelt, entsteht durch eine Reihe von Ereignissen, die Neurulation genannt werden.
- Primäre Neurulation
- Das Gehirn und ein Großteil des Rückenmarks werden durch primäre Neurulation gebildet, die die Ausformung, das Falten und das Zusammenwachsen der Neuralplatte an der Mittellinie beinhaltet.
- Beim Menschen breitet sich die primäre Neurulation kaudal in die Region vor den früheren 1.‒5. Sakralwirbeln aus und ist etwa am 25. Tag nach der Konzeption abgeschlossen.
- Sekundäre Neurulation
- Der am weitesten kaudal gelegene Teil des Rückenmarks wird bei einem spezifischen Prozess gebildet, der sekundäre Neurulation genannt wird.
- Dieser Verschluss erfolgt von Tag 26‒30 nach der Befruchtung.
- Myelomeningozele
- Bei der primären Neurulation entstandener Defekt, der durch ein mangelhaftes Zusammenwachsen im kaudalen Teil des Neuralrohr verursacht wird.
- Anenzephalie
- Defekte, die bei der primären Neurulation durch ein mangelhaftes Zusammenwachsen in der kranialen Region des Neuralrohrs verursacht werden, werden Anenzephalie genannt.
Spina bifida
- Spina bifida occulta
- Beruht auf einem fehlerhaften Verschluss des hinteren Teils der Wirbelsäule. Der Processus spinosus und möglicherweise auch die Lamina fehlen.
- Der Neuralkanal ist dadurch nach hinten offen, eine Beteiligung des Rückenmarks liegt aber nicht vor.
- Normalerweise ist der lumbosakrale Bereich der Wirbelsäule betroffen.
- Geschlossene Spina bifida
- Die Erkrankung verläuft normalerweise asymptomatisch, evtl. kann ein Hautsack zu sehen sein, in einigen Fällen eine ausgeprägte Behaarung über dem Defekt, evtl. Pigmentierung, ein Hämangiom oder ein Lipom in der Größe des Defekts.
- In einigen Fällen ist die Erkrankung mit Rückenschmerzen, eingeschränkter Kraft in den unteren Extremitäten, Gangstörungen oder Schwierigkeiten beim Wasserlassen verbunden.
- Offene Spina bifida (Spina bifida cystika)
- Hirnhäute mit umgebender Flüssigkeit wölben sich aus (Meningozele), oder ein Teil des Rückenmarks gelangt in die Ausbuchtung (Myelomeningozele/MMC).
- Die Erkrankung steht im Zusammenhang mit Fehlbildungen in umgebender Muskulatur, Bindegewebe und Haut.
- Die Symptome werden durch das Ausmaß der Herniation und der Lokalisation im Rücken bestimmt: Je höher im Rücken die Herniation lokalisiert ist, desto stärker sind die Symptome.
- Häufig liegt auch eine Chiari-Malformation Typ 2 mit einem erhöhten Risiko für Aquäduktstenosen und Hydrozephalus vor.
Prädisponierende Faktoren
- Familienanamnese
- Ist einer der stärksten Risikofaktoren.
- Das Risiko, dass Geschwister eines Kindes mit Spina bifida oder Anenzephalie die gleiche Erkrankung bekommen, liegt bei 3‒8 %.5
- Folsäure
- Eine unzureichende Zufuhr von Folsäure vor und während der frühen Schwangerschaft erhöht das Risiko für Spina bifida und Anenzephalie.
- Fehlende Einnahme von Folsäure während dieser Phase erhöht das Risiko von Fehlbildungen um das Zwei- bis Achtfache.4
- Vitamin B12
- Es gibt eine schwache Korrelation zwischen niedrigen B12-Werten und Spina bifida.6
- Mütterlicher Diabetes
- Mütter mit Diabetes vor der Konzeption sind einem erhöhten Risiko ausgesetzt, Kinder mit Spina bifida zu gebären.
- Im Vergleich zur allgemeinen Bevölkerung ist das Risiko 2- bis 10-mal höher.7
- Das Risiko ist am höchsten bei Müttern, die während des ersten Trimenons eine schlechte metabolische Kontrolle aufweisen.
- Medikamente
- Es besteht ein Zusammenhang zwischen Spina bifida und der Einnahme von Valproinsäure/Valproat oder Carbamazepin.8-10
- Übergewicht der schwangeren Mutter
- Erhöht das Risiko nachgewiesen 1,5- bis 3,5-fach.11
ICPC-2
- N85 Angeborene Anomalie Nervensystem
ICD-10
- Q05 Spina bifida
- Q05.0 Zervikale Spina bifida mit Hydrozephalus
- Q05.1 Thorakale Spina bifida mit Hydrozephalus
- Q05.2 Lumbale Spina bifida mit Hydrozephalus
- Q05.3 Sakrale Spina bifida mit Hydrozephalus
- Q05.4 Nicht näher bezeichnete Spina bifida mit Hydrozephalus
- Q05.5 Zervikale Spina bifida ohne Hydrozephalus
- Q05.6 Thorakale Spina bifida ohne Hydrozephalus
- Q05.7 Lumbale Spina bifida ohne Hydrozephalus
- Q05.8 Sakrale Spina bifida ohne Hydrozephalus
- Q05.9 Spina bifida, nicht näher bezeichnet
Diagnose
Diagnostische Kriterien
- Die Diagnose basiert auf dem Befund charakteristischer anatomischer Anomalien. Ultraschall ist das Goldstandard-Diagnosewerkzeug für Spina bifida. Der dreidimensionale Ultraschall und die Magnetresonanztomografie spielen ebenfalls eine Rolle bei der Charakterisierung der offenen Spina bifida.12
Differenzialdiagnosen
- Neonatale Meningitis
- Rückenmarksblutung
- Spinaler Epiduralabszess
- Syringomyelie
- Hydrozephalus
Pränataldiagnostik
- Nichtinvasive pränatale Bluttests (NiPT) stellen eine gefahrlose und zuverlässige Untersuchungsvariante zur Diagnose von Chromosomenaberrationen wie der Trisomie 13, 18 oder 21 beim Fetus dar. Der Bluttest erfolgt nach individueller Beratung in der 9. oder 10. Schwangerschaftswoche.
- Eine Myelomeningozele kann normalerweise bei der routinemäßigen Ultraschalluntersuchung rund um die 18. Schwangerschaftswoche nachgewiesen werden.
- Risikoschwangerschaft
- Bei Vorliegen einer Risikoschwangerschaft sollte eine frühzeitige Ultraschalluntersuchung in der 12. Schwangerschaftswoche angeboten werden.
- Darüber hinaus können eine Amniozentese sowie die Bestimmung des Alpha-1-Fetoproteins (AFP) indiziert sein.13
Anamnese
- Es besteht ein erhöhtes Risiko für Paresen und Paralysen in den unteren Extremitäten, sensorische Einschränkungen, Darm- und Blasendysfunktionen sowie orthopädische Fehlbildung (Klumpfuß, Kontrakturen, Hüftgelenksluxation, Skoliose, Kyphose u. a.).
- Bei vielen Patient*innen verursachen assoziierte Erkrankungen wie Hydrozephalus und Chiari-Malformationen Typ 2 schwere Funtionsstörungen.14
- Die meisten Kinder mit MMC sind normal intelligent, weisen jedoch spezifische kognitive Störungen und Sprachstörungen auf.15-16
- Häufig besteht die Indikation zu einem thorakalen Shunt.
- Chiari-Malformationen Typ 2
- Apnoe, Schluckbeschwerden und Stridor bei Neugeborenen
- Kopfschmerzen, Quadriparese, Skoliose und Gleichgewichts- und Koordinationsstörungen bei älteren Kindern
Klinische Untersuchung
- Die klinischen Befunde hängen von der Art des Neuralrohrdefektes und der Höhe evtl. Nervenläsionen ab.
- Mögliche Befunde bei Spina bifida occulta sind ein behaartes, subkutanes Lipom oder eine anomale Pigmentierung.13
- Mögliche Befunde bei Meningozele ist eine protrudierende Aussackung an der Mittellinie, offen oder mit Haut bedeckt.
- Mögliche Befunde bei Myelomeningozele sind:
- Der Herniensack ist deutlich zu sehen und nicht mit Haut bedeckt.
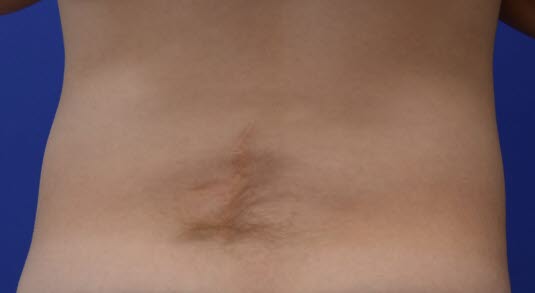 Spina bifida occulta
Spina bifida occulta - denervierte Lähmungen in den unteren Extremitäten13
- sensorische Ausfälle unterhalb eines bestimmten Niveaus13
- denervierte neuropathische Blase, Sphinkterparese17
- autonome Störungen in den unteren Extremitäten
- orthopädische Deformitäten an Knöcheln und Füßen aufgrund anomaler fetaler Positionen
- Hüftgelenksluxation
- Muskelatrophie
- Hydrozephalus
- mentale Retardierung
- Augenprobleme.
- Der Herniensack ist deutlich zu sehen und nicht mit Haut bedeckt.
Diagnostik bei Spezialist*innen
- Röntgen und CT
- Bei Neugeborenen mit Spina bifida sollte eine bildgebende Diagnostik des zentralen Nervensystems durchgeführt werden, auch um den Bedarf eines Shunts einzuschätzen.
- Konventionelle Röntgenaufnahmen oder ein CT der Wirbelsäule können das Ausmaß der knöchernen Defekte darstellen.
- MRT
- Empfohlen, um Weichteildefekte und den Grad der Medulla-Infiltration festzustellen.
- Ultraschall und urodynamische Messungen17
Indikationen zur Überweisung
- Die Kinder werden in der Regel 1- bis 2-mal pro Jahr in einem spezialisierten Zentrum untersucht. Die Hausärzt*innen sollten sich während des Wachstums so oft wie möglich am Follow-up beteiligen.
Checkliste zur Überweisung
Deformitäten der Wirbelsäule bei Kindern
- Zweck der Überweisung
- Diagnostik? Therapeutisches Prozedere (Operation oder konservatives Vorgehen) ?
- Anamnese
- Beginn? Trauma? Familiär? Entwicklung?
- Asymptomatisch (nur Deformität)? Symptomatisch? Schmerzen? Ruheschmerz? Nachtschmerz? Funktionseinschränkung? Entwicklungsstörung?
- Deformitäten anderer Organsysteme?
- Behandlungsversuche?
- Andere relevante Krankheiten? Rehabilitationsmaßnahmen?
- Regelmäßig einzunehmende Medikamente?
- Klinische Untersuchung
- lokale Anzeichen für Spina bifida
- Wirbelsäule: Position/Schiefstellungen? Ggf. in Bauchlage, Rückenlage und sitzend (bei Kindern, die nicht laufen)? Mobilität? Schmerzauslöser?
- Nervenausfälle: Motorisch? Sensorisch? Reflexe? Lasègue?
- Ergänzende Untersuchungen
- Röntgen Wirbelsäule, von vorne und von der Seite, evtl. mit Skolioseaufnahme
Therapie
Therapieziele
- Bei umfangreicheren Neuralrohrdefekten ist das Ziel, neonatale Komplikationen zu vermeiden und langfristig die Voraussetzungen für ein selbstbestimmtes Leben zu optimieren.
Allgemeines zur Therapie
- Patient*innen mit MMC benötigen sowohl chirurgische als auch konservative Therapie.
- Eine lebenslange medizinische Behandlung ist notwendig. Diese sollte durch ein interdisziplinäres Team erfolgen.
- Relevante Fachrichtungen sind Pädiatrie, Krankenpflege, pädiatrische Neurochirurgie, Urologie, Orthopädie, Physiotherapie, soziale Arbeit und Allgemeinmedizin.
- Von großer Bedeutung ist die Aufklärung der Eltern.
Neugeborenenalter
Operation
- Nach der Geburt
- Ein Verschluss der Spinalläsion wird normalerweise innerhalb von 48 Stunden nach der Geburt durchgeführt.18
- In utero
- Auch wenn ein chirurgischer Verschluss der Fehlbildung normalerweise im Neugeborenenalter erfolgt, gibt es Studien zu einem In-utero-Verschluss.19
- Shunt
- häufig notwendig aufgrund der Entwicklung eines Hydrozephalus
- Orthopädische Chirurgie
- Fehlstellungen sollten kurz nach der Geburt behandelt werden.
Nach dem Neugeborenenalter
- Kontinuierliche Überwachung mit Fokus auf Neurologie, Urologie und das muskeloskelettale System ist notwendig.
- Medikamente
- ggf. Therapie mit Antiepileptika
- Urologie
- evtl. Operation aufgrund von urologischen Komplikationen und rezidivierenden Harnwegsinfektionen
- Orthopädie
- Überwachung der Entwicklung orthopädischer Deformitäten wie Skoliose, Kyphose und Hüftgelenksdysplasie
- Außerdem zu erwägen:
- Überwachung der neuropsychologischen Entwicklung, der Mobilität, des Gewichts (Übergewicht) und der Hautpflege
- Zukunftsplanung
- Das interdisziplinäre Team sollte gemeinsam mit den Patient*innen sowie Erziehungsberechtigten und den Hausärzt*innen einen Zukunftsplan im Hinblick auf die Ausbildung, das Arbeitsleben und die Fähigkeit, für sich selbst zu sorgen, entwickeln.
- Es empfiehlt sich, diesen Prozess frühzeitig zu beginnen (vor dem 15. Lebensjahr).20
- Durch die Teilnahme an individuellen Ausbildungsprogrammen wird es Kindern ermöglicht, notwendige Fähigkeiten für ein selbstbestimmtes Leben zu entwickeln. 15
- lebenslanges Follow-up
Kontinenzprogramme
- Harnblase und Harnwege
- z. B. durch eine Kombination aus intermittierender Katheterisierung, der Gabe von Medikamenten und chirurgischen Interventionen21
- Darmfunktion
Vorbeugende Behandlung
- Folsäure
- Nimmt die Mutter bereits vor der Konzeption Folsäure ein, beugt dies in mehr als 50 % der Fälle Myelomeningozele vor.24-26
Verlauf, Komplikationen und Prognose
Verlauf
- Die Veränderungen sind dauerhaft, und die Erkrankung erfordert ein lebenslanges Follow-up.
Komplikationen
- Neurologische Komplikationen
- Paresen in den unteren Extremitäten
- Hydrozephalus
- Epilepsie
- Haut
- Orthopädische Fehlstellungen
- Deformitäten in den unteren Extremitäten
- Skoliose
- Hüftgelenksluxation
- Urologische
- Blasenparese und Blasenfunktionsstörungen
- Inkontinenz
- rezidivierende Harnwegsinfekte, Pyelonephritiden und schließlich Nierenfunktionsstörungen
- Tod
- Häufige Todesursache ist eine Niereninsuffizienz infolge einer rezidivierenden Pyelonephritis.
Prognose
- Die Mortalität bei jungen Patient*innen mit Spina bifida liegt im Alter von 5–30 Jahren bei etwa 1 % pro Jahr.27
- Die Mortalität ist bei Patient*innen mit den höherliegenden Läsionen am höchsten.27
- Die Qualität der Gesundheit sinkt in der Zeit zwischen Adoleszenz und jungem Erwachsenenalter, vermutlich aufgrund von Schwierigkeiten beim Übergang zur Gesundheitsversorgung für Erwachsene.27
- In Bezug auf die psychosoziale Anpassung besteht ein erhöhtes Risiko für depressive Symptome und Angstzustände.27
Myelomeningozele
- Ca. 75 % der Patient*innen mit Myelomeningozele erleben das frühe Erwachsenenalter.28
- Die Langzeitergebnisse variieren erheblich in Abhängigkeit von der Lage der Myelomeningozele, dem Vorhandensein eines Hydrozephalus und dem Schweregrad der Chiari-II-Fehlbildung.28
Verlaufskontrollen
- Allgemeines
- Die Patient*innen benötigen eine Betreuung durch ein interdisziplinäres Team.1
- Die Hausärzt*innen können die routinemäßigen Gesundheitsuntersuchungen übernehmen und die Familien beratend unterstützen.
- Nach dem Neugeborenenalter
- Eine kontinuierliche Überwachung der neurologischen, urologischen und des muskeloskelettalen Systems ist notwendig.
- Es sollten Routinemessungen des Kopfumfangs durchgeführt werden.
- Anzeichen für neurologische Komplikationen in Form von Krämpfen sollte regelmäßig erfragt werden.
Patienteninformationen
Patienteninformationen in Deximed
Illustrationen

Spina bifida occulta verläuft normalerweise asymptomatisch. Evtl. kann ein Hautsack zu sehen sein, in einigen Fällen eine ausgeprägte Behaarung über dem Defekt, evtl. Pigmentierung, ein Hämangiom oder ein Lipom in der Größe des Defektes.
Quellen
Leitlinien
- Deutsche Gesellschaft für Urologie. Diagnostik und Therapie der neurogenen Blasenfunktionsstörungen bei Kindern und Jugendlichen mit spinaler Dysraphie. AWMF-Leitlinie Nr. 043-047. S2k, Stand 2019. www.awmf.org
Literatur
- Mitchell LE, Scott Adzick N, Melchionne J, Pasquariello PS, Sutton LN, Whitehead AS. Spina bifida. Lancet 2004; 364: 1885-95. pubmed.ncbi.nlm.nih.gov
- Dosa NP, Katz DA, Riddell JV, Tovar-Spinoza Z. Spina bifida and neural tube defects. BMJ Best Practice, last updated Apr 08, 2015. bestpractice.bmj.com
- Queißer-Wahrendorf A. Angeborene körperliche Anomalien: Epidemiologie. In: Hoffmann G., Lentze M., Spranger J., Zepp F., Berner R. (Hrsg.): Pädiatrie. Berlin, Heidelberg, New York: Springer 2018; S. 1-5.
- De Wals P, Tairou F, Van Allen MI, et al. Reduction in neural-tube defects after folic acid fortification in Canada. N Engl J Med. 2007;357:135-142. PubMed
- Foster MR. Spina bifida. Medscape, last updated May 19, 2014. emedicine.medscape.com
- Ray JG, Blom HJ. Vitamin B12 insufficiency and the risk of fetal neural tube defects. QJM 2003; 96: 289-95. PubMed
- McLeod L, Ray JG. Prevention and detection of diabetic embryopathy. Community Genet 2002; 5: 33-39. PubMed
- Koren G. Safe use of valproic acid during pregnancy. Can Fam Physician 1999; 45: 1451-53. PubMed
- Matalon S, Schechtman S, Goldzweig G, Ornoy A. The teratogenic effect of carbamazepine: a meta-analysis of 1255 exposures. Reprod Toxicol 2002; 16: 9-17. PubMed
- Jentink J, Dolk H, Loane MA, et al. Intrauterine exposure to carbamazepine and specific congenital malformations: systematic review and case-control study. BMJ 2010; 341: c6581. BMJ (DOI)
- Watkins ML, Ratashak SA, Honein MA, Botto LD, Moore CA. Maternal obesity and risk for birth defects. Pediatrics 2003; 111: 1152-58. Pediatrics
- Trudell AS, Odibo AO.. Diagnosis of spina bifida on ultrasound: always termination? . Best Pract Res Clin Obstet Gynaecol. 2014; 28(3): 367-77. pmid:PMID: 24373566 PubMed
- StatPearls Publishing: Spina Bifida. Treasure Island 2020. www.ncbi.nlm.nih.gov
- Rintoul NE, Sutton LN, Hubbard AM, et al. A new look at myelomeningceles: functional level, vertebral level, shunting and the implications for fetal intervention. Pediatrics 2002; 109: 409-13. pubmed.ncbi.nlm.nih.gov
- Northrup H, Volcik KA. Spina bifida and other neural tube defects. Curr Probl Pediatr 2000; 30: 313-32. PubMed
- Vachha B, Adams R. Language differences in young children with myelomeningocele and shunted hydrocephalus. Pediatr Neurosurg 2003; 39: 184-89. PubMed
- Deutsche Gesellschaft für Urologie. Diagnostik und Therapie der neurogenen Blasenfunktionsstörungen bei Kindern und Jugendlichen mit spinaler Dysraphie. AWMF-Leitlinie Nr. 043-047, Stand 2019. www.awmf.org
- McLone DG, Bowman RM. Overview of the management of myelomeningocele (spina bifida). UpToDate, last updated Nov 17, 2015. UpToDate
- Adzick NS, Thom EA, Spong CY et al. A randomized trial of prenatal versus postnatal repair of myelomeningocele. N Engl J Med 2011; 364: 993-1004. pmid:21306277 PubMed
- American Academy of Pediatrics Committee on Children with Disabilities. The role of the pediatrician in transitioning children and adolescents with developmental disabilities and chronic illness from school to work and college. Pediatrics 2000; 106: 854-56. Pediatrics
- Bauer SB. The management of the myelodysplastic child: a paradigm shift. Br J Urol 2003; 92 :(suppl 1) 23-28. bjui-journals.onlinelibrary.wiley.com
- Leibold S, Ekmark E, Adams RC. Decision making for a successful bowel continence program. Eur J Pediatr Surg 2000; 10: 26-30. PubMed
- Perez M, Lemelle JL, Barthelme H, Marquand D, Schmitt M. Bowel management with antegrade colonic enema using a malone or monti conduit--clinical results. Eur J Pediatr Surg 2001; 11: 315-18. PubMed
- US Preventive Services Task Force. Folic acid for the prevention of neural tube defects: US Preventive Services Task Force recommendation statement. Ann Intern Med. 2009;150:626-631. PubMed
- Berry RJ, Li Z, Erickson JD, et al. Prevention of neural-tube defects with folic acid in China. N Engl J Med 1999; 341: 1485-90. New England Journal of Medicine
- De-Regil LM, Peña-Rosas JP, Fernández-Gaxiola AC, Rayco-Solon P. Effects and safety of periconceptional oral folate supplementation for preventing birth defects. Cochrane Database of Systematic Reviews 2015, Issue 12. Art. No.: CD007950. DOI: 10.1002/14651858.CD007950.pub3. pubmed.ncbi.nlm.nih.gov
- Copp, Andrew J et al.: Spina bifida. Nature reviews 2015; 1: 15007. www.ncbi.nlm.nih.gov
- Bowman RM, McLone DG, Grant JA, Tomita T, Jacobsen JS. Spina bifida outcome: a 25-year prospective. Pediatr Neurosurg 2001; 34: 114-20. PubMed
Autor*innen
- Mana Schmidt-Haghiri, Dr. med., Ärztin in Weiterbildung Allgemeinmedizin, München
- Die ursprüngliche Version dieses Artikels basiert auf einem entsprechenden Artikel im norwegischen hausärztlichen Online-Handbuch Norsk Elektronisk Legehåndbok (NEL, https://legehandboka.no/).