Zusammenfassung
- Definition:Nebenwirkung eines Medikaments in Form von Hautreaktionen.
- Häufigkeit:Bei etwa 10–20 % der Patient*innen, die sich in stationärer Behandlung befinden, und bei etwa 1–5 % der Personen, die in einer Hausarztpraxis behandelt werden, lösen Medikamente erhebliche Nebenwirkungen aus.
- Symptome:Äußert sich in Hautausschlag und Juckreiz in milden Formen. Seltener sind schwere Verlaufsformen und systemische Beteiligungen.
- Befunde:Makulopapulöse Ausschläge in milden Formen, Blasenbildung und Erythrodermie in schweren Formen.
- Diagnostik:Mögliche apparative Diagnostik: Tryptasespiegel im Serum, spezifisches IgE, Hautbiopsie und ggf. Allergietests abhängig von Klinik und vermuteter Pathogenese.
- Therapie:Absetzen des auslösenden Medikaments, ggf. Antihistaminika bei Juckreiz. Stationäre, ggf. intensivmedizinische Behandlung bei schweren Verrlaufsformen notwendig.
Allgemeine Informationen
Definition
- Nebenwirkung eines Medikaments in Form von Hautreaktionen, häufig in Form von Urtikaria als Form von Sofort-Typ-Reaktionen oder Exanthemen als Ausdruck einer immunologischen Spätreaktion1
- Von einer unerwünschten Arzneimittelwirkung (UAW) T88.7 spricht man, wenn ein indikationsgerecht verabreichtes Arzneimittel in korrekter Dosierung eine unvorhersehbare Reaktion z. B. an der Haut hervorruft.
- Unerwünschte Arzneimittelreaktionen sollten, wenn möglich, der Arzneimittelkommission der deutschen Ärzteschaft gemeldet werden.
- Die Pathogenese dieser Hautreaktionen ist nicht immer sicher zu klären, neben immunologischen Sofort-Typ-Reaktionen (IgE, allergische Reaktionen) gibt es eine Vielzahl von Reaktionen der Haut auf eingenommene Medikamente, die teils immunologisch (nicht IgE-vermittelt) oder nichtimmunologisch bedingt sind.
- Siehe auch den Artikel Arzneimittelinduzierte allergische Reaktionen.
- Der Mechanismus der nichtallergischen Arzneimittelhypersensitivität ist meist unbekannt.2
- Zudem gibt es vorhersehbare pharmakologische Nebenwirkungen (z. B. photochemische Reaktionen), toxische und kumulativ-toxische Effekte.
- Viele Reaktionen an der Haut scheinen auf einer gestörten T-Zell-vermittelten Immunität zu beruhen. Dafür spricht auch, dass Hautreaktionen häufig durch eine Koinzidenz einer Virusinfektion mit einer Medikamenteneinnahme auftreten.
- Da sich arzneimittelinduzierte Hautreaktionen ähnlich anderen Erkrankungen der Haut äußern können, lässt das äußere Erscheinungsbild eines Ausschlags zunächst häufig nicht eindeutig auf ein Medikament als Ursache schließen.
- Weiter erschwert wird die Abklärung arzneimittelinduzierter Hautreaktionen dadurch, dass das gleiche Arzneimittel verschiedene Reaktionen hervorrufen und die gleiche Reaktion durch verschiedene Arzneimittel verursacht sein kann.
- Die Vielzahl der Pathomechanismen und die Vielzahl der klinischen Erscheinungsformen erschwert die Diagnostik.
- Wichtig ist vor allem die klinische Einteilung in milde und schwere Verlaufsformen, um eine adäquate Therapie einzuleiten, und die Unterscheidung in allergisch oder nicht-allergische Genese, da bei allergischen Reaktionen eine erneute Exposition fatale unmittelbare Folgen haben könnte.1
Zeitliche Einteilung2
- Eine unerwünschte Arzneimittelwirkung (UAW) kann sofort (Soforttyp-Arzneimittelreaktion vom IgE-Typ: Urtikaria, Asthma, Anaphylaxie) – oder –
- Tage/Wochen nach Beginn der Behandlung ( UAW vom verzögerten Typ: makulopapulöses Arzneimittelexanthem, Stevens-Johnson-Syndrom/TEN) – oder –
- Seltener erst mehrere Wochen/Monate (UAW vom Spättyp) nach Behandlungsbeginn des auslösenden Arzneimittels auftreten (DRESS, Drug Reaction with Eosinophilia and Systemic Symptoms).
Klinische Einteilung
- Häufige arzneimittelinduzierte Hautreaktionen
- Arzneimittelexanthem (makulopapulöses Exanthem)
- Urtikaria, Angioödem und Anaphylaxie
- Pruritus
- Seltene arzneimittelinduzierte Hautreaktionen
- pustulöse Reaktionen (akute generalisierte exanthematöse Pustulosis)
- dermatitische Reaktionen
- Erythema (exsudativum) multiforme
- Vaskulitis
- Purpura
- photochemische Reaktionen
- fixe Arzneimittelreaktion
- Schwere arzneimittelinduzierte Hautreaktionen
- Stevens-Johnson-Syndrom und toxische epidermale Nekrolyse (TEN, Lyell-Syndrom)
- DRESS (Drug Reaction with Eosinophilia and Systemic Symptoms)
Leitlinie: Überempfindlichkeitsreaktionen auf Arzneimittel, allergologische Diagnostik1
- Arzneimittelüberempfindlichkeitsreaktionen sind unvorhersehbare, durch Arzneimittel hervorgerufene Reaktionen.
- Sie manifestieren sich entweder innerhalb von 1–6 Stunden nach Arzneimittelzufuhr („Sofortreaktionen") mit geringgradigen bis lebensbedrohlichen Symptomen der Anaphylaxie – oder –
- mehrere Stunden bis Tage später („Spätreaktionen") vorwiegend als Exantheme.
- Eine Beteiligung des Immunsystems (Allergie) ist nicht immer nachweisbar. Eine Allergie-Diagnostik sollte jedoch angestrebt werden.
- Der Verzicht auf eine Diagnostik kann einerseits schwere Reaktionen bei erneuter Exposition zur Folge haben, andererseits zu ungerechtfertigter Einschränkung der Therapiemöglichkeiten führen.
Häufigkeit
- Nebenwirkungen
- Bei etwa 10–20 % der Patient*innen, die sich in stationärer Behandlung befinden, und bei etwa 1–5 % der Personen, die in der Hausarztpraxis behandelt werden, lösen Medikamente erhebliche Nebenwirkungen aus.3
- In etwa 15 % der Fälle handelt es sich dabei um Hautreaktionen.
- Hautreaktionen
- Während die allermeisten arzneimittelinduzierten Hautreaktionen mehr oder weniger harmlos verlaufen, gibt es auch seltene Formen, die einen sehr schweren Verlauf nehmen, ein erhebliches Sterblichkeitsrisiko aufweisen und eine interdisziplinäre intensivmedizinische Betreuung erforderlich machen können.4
- Schätzungen zufolge ist dies bei etwa 0,36–3 % aller stationär aufgenommenen Patient*innen (Erwachsene und Kinder) der Fall.4-5
- Verschiedene Arten von Hautreaktionen
- Die häufigste arzneimittelinduzierte Hautreaktion ist das makulopapulöse Exanthem.
- Die zweithäufigsten arzneimittelinduzierten Hautreaktionen sind Urtikaria, Angioödem und Anaphylaxie (Typ-1-Reaktion).
- Häufigste Auslöser
- Penicilline (am häufigsten Typ-I-Allergien)6-7, Chemotherapeutika, Sulfonamide und Chinolone
- Auch Acetylsalicylsäure und NSAR lösen häufig Reaktionen aus, bei denen es sich in der Regel um Unverträglichkeiten/pseudoallergische Reaktionen handelt.8
- Allopurinol und Antikonvulsiva lösen häufig schwere Reaktionen aus.9-10
- Das Risiko für ein SJS/TEN (Stevens-Johnson-Syndrom/Toxische epdermale Nekrolyse) nach Allpurinol steigt mit vorbestehenden Herz- oder Nierenerkrankungen, Alter > 70, weibl. Geschlecht und asiatischer Herkunft. 11
- Alter und Geschlecht
- Medikamenteninduzierte Hautreaktionen treten bei Frauen häufiger auf als bei Männern. Das Risiko ihres Auftretens ist umso höher, je älter die Betroffenen sind und je mehr Medikamente eingenommen werden.12
Ätiologie und Pathogenese
- Unvorhergesehene Reaktionen auf Medikamente können auf einer unmittelbaren toxischen Wirkung oder auf einer Reaktion des Immunsystems beruhen.
Pathogenese
- Viele medikamenteninduzierten Hautreaktionen stellen keine typisch allergischen Reaktionen dar.
- Zu allergischen Reaktionen siehe Artikel Arzneimittelinduzierte allergische Reaktionen.
- Manche Reaktionen sind auf Überdosierung, pharmakologische Wirkung, Toxizität, die Erkrankung der Patient*innen oder Wechselwirkungen mit anderen Medikamenten zurückzuführen.2
- Einige Formen werden von verschiedenen immunologischen Reaktionstypen ausgelöst12-14, wobei bei den meisten arzneimittelinduzierten Reaktionen die Aktivierung der T-Zellen eine Rolle spielt.
- Bei vielen Reaktionen sind die verursachenden Mechanismen noch nicht vollständig geklärt: Hierzu gehören auch einige der schwersten Formen wie das Stevens-Johnson-Syndrom und die toxische epidermale Nekrolyse.
- Diese Erkrankung wird als T-Lymphozyten-vermittelte zytotoxische Reaktion gegen die Epidermis aufgefasst, was zum programmierten Zelltod (Apoptose) der Keratinozyten führt.
Auslöser eines Arzneimittelexanthems (makulopapulöses Exanthem)
- In mehreren großen Studien wurden verschiedene Antibiotika als häufigste Auslöser dieser Art von Hautausschlag ermittelt.
- In der Regel handelt es sich hierbei um eine durch T-Zellen ausgelöste, verzögerte Typ-IV-Reaktion, bei der die ersten Symptome normalerweise 2–14 Tage nach Beginn der Medikamenteneinnahme auftreten.
- Tritt vor allem bei Anwendung folgender Substanzen auf:
- Ampicillin/Amoxicillin
- Penicillin
- Phenazon (Pyrazolon-Derivat)
- Sulfonamide
- Phenytoin
- Carbamazepin
- Gold
- Gentamycin.
- Weniger häufig bei Anwendung von:
- Cephalosporine
- Barbiturate
- Thiazide
- NSAR
- Phenothiazine.
Urtikaria, Angioödem und Anaphylaxie
- Urtikaria und Angioödem stellen in der Regel eine Typ-I-Allergie (allergische Sofortreaktion) dar, können in seltenen Fällen aber auch auf die direkte Freisetzung von Histamin oder eine Typ-III-Reaktion in Verbindung mit Gelenkschmerzen und Fieber zurückgehen.
- Die meisten urtikariellen Reaktionen sind jedoch nicht allergisch bedingt.
- Die Einnahme von Salizylsäure, NSAR, Kodein, Opiaten, Atropin und (radioaktiven) Kontrastmitteln kann zu einer direkten Freisetzung von Histaminen führen, die dann die häufigste Ursache milder Reaktionen auf diese Substanzen ist.
- Daher kann eine Urtikaria ohne vorherige Sensibilisierung auftreten.
- Allerdings können diese Substanzen eine IgE-Sensibilisierung und damit eine tatsächliche Allergie auslösen.
- ACE-Hemmer können ein nicht histaminvermitteltes Angioödem auslösen.
- Diese Art von Reaktionen tritt z. B. bei Anwendung folgender Substanzen auf:
- Kodein
- Penicillin
- Salizylsäure
- NSAR
- Sulfonamide
- Opiate
- Röntgenkontrastmittel
- Impfstoffe.
Akute generalisierte exanthematische Pustulose15
- Die generalisierte exanthematische Pustulose ist eine seltene arzneimittelinduzierte Hautreaktion und kann auch nach Infekten beobachtet werden.
- In den meisten Fällen ist eine Medikamenteneinnahme vorausgegangen.
- Sie tritt häufig in Verbindung mit Fieber auf.
- Hierbei bilden sich auf einem ödematösen Erythem sehr viele nichtfollikuläre sterile Pusteln.
- Die Pathogenese ist unbekannt, aber die Beteiligung immunologischer Faktoren gilt als wahrscheinlich.
Vaskulitis
- Bei einer Vaskulitis liegt eine Typ-III-Allergie mit zirkulierenden Immunkomplexen vor.
- Sie kann z. B. bei Einnahme folgender Substanzen auftreten:
- Ampicillin/Amoxicillin
- Penicillin
- Sulfonamide
- Chinidin
- Amiodaron
- Hydralazin
- Furosemid
- Thiazide
- Salizylsäure
- NSAR
- Phenothiazine
- Phenytoin
- Cimetidin
- Röntgenkontrastmittel.
Purpura
- Eine arzneimittelinduzierte Purpura kann auf einem Rückgang der Thrombozyten (thrombozytopenische Purpura), veränderten Gerinnungsprozessen oder einer Schwächung des kollagenen Bindegewebes beruhen.
- Eine Purpura kann u. a. bei Einnahme folgender Substanzen auftreten:
- Sulfonamide
- Thiazide
- Furosemid
- Trimethoprim
- Cephalosporine
- Carbamazepin.
Erythema (exsudativum) multiforme
- Hierbei handelt es sich um eine Überempfindlichkeitsreaktion mit häufig unklarer Ursache.
- Die Reaktion tritt gehäuft nach Infektionen auf und wird meist durch das Herpes-simplex-Virus, seltener durch eine Mykoplasmeninfektion oder eine Streptokokken-Tonsillitis ausgelöst.
- 10 % der Fälle werden durch Medikamente verursacht oder durch Medikamenteneinnahme bei begleitendem Virusinfekt.
- Sie kann z. B. bei Einnahme folgender Substanzen auftreten:
- Sulfonamide
- Penicillin
- Tetrazykline
- Salizylate
- NSAR
- Pyrazolon-Derivate
- Carbamazepin
- Barbiturate
- Furosemid
- Thiazide
- Phenothiazine
- Mianserin
- Benzodiazepine.
- 2013 hat die Europäische Arzneimittelbehörde (EMA) die Rücknahme der Zulassung für Tetrazepam angeordnet, da der Benefit des Muskelrelaxans (Benzodiazepin) die teils erheblichen kutanen Nebenwirkungen (Erythema multiforme, SJS/TEN) nicht aufwiegt.16
Stevens-Johnson-Syndrom (SJS)/toxische epidermale Nekrolyse (TEN)
- Kann von den gleichen Medikamenten wie ein Erythema multiforme hervorgerufen werden.
- Sehr schwere Verlaufsform einer Medikamentenreaktion an der Haut17
Direkte Histaminfreisetzung
- Dieses Phänomen beruht teilweise auf einer Aktivierung der Mastzellen durch chemische Prozesse.
- Für die direkte Histaminfreisetzung besteht eine genetische Prädisposition.
- Es handelt sich um eine pseudoallergische Reaktion.
- Eine direkte Histaminfreisetzung kann von folgenden Substanzen ausgelöst werden:
- Salizylsäure
- NSAR
- Kodein und Opiate.
- Azofarbstoffe und Benzoesäure ähneln in ihrer chemischen Zusammensetzung der Salizylsäure und können daher die gleiche Wirkung haben.
- Salizylsäure und ähnliche Substanzen kommen in bestimmten Lebensmitteln wie Bier, Wein, Obst und Beeren (Apfelsinen, Zitronen, Bananen und Preiselbeeren), Lakritze und einigen Gewürzen vor.
- Benzoesäure wird als Konservierungsmittel (E 210) eingesetzt. Benzoesäure kommt als natürlicher Bestandteil vor allem in säuerlichen Beerensorten wie Preiselbeeren vor, ist aber auch in Blaubeeren, Moltebeeren, Erdbeeren, Rosinen, grünen Weintrauben und Erbsen enthalten.
Photochemische Reaktionen
- Zu den Auslösern einer systemischen phototoxischen Arzneimittelreaktion zählen u. a. Diuretika wie Hydrochlorothiazid, Antiarrhythmika wie Amiodaron, nichtsteroidale Antiphlogistika wie Naproxen und Ketoprofen, antibakterielle Substanzen wie Fluorochinolone (Ciprofloxacin, Levofloxacin u. a.), Tetrazykline (vor allem Doxycyclin) oder systemische Psoralene.18
- Dieser phototoxische Effekt wird aktuell für die erhöhte Inzidenz von nicht-melanotischen Hauttumoren unter langjähriger Einnahme von Hydrochlorothiazid (Hct) diskutiert.19
- Photochemische Reaktionen können vom phototoxischen oder photoallergischen Typ sein, wobei der photoallergischen Reaktion eine Sensibilisierung vorangegangen sein muss.
- Diese Art des Ausschlags tritt stets auf sonnenexponierten Hautpartien auf.
- Können einer allergischen Kontaktdermatitis oder einem Sonnenbrand ähneln.
- Siehe auch Artikel Lichtdermatosen.
Prädisponierende Faktoren
Patientenbezogen
- Polypharmazie
- Das Risiko steigt mit der Anzahl der gleichzeitig verabreichten Medikamenten.7
- Chronische Erkrankung
- Internistische Patient*innen sind häufiger betroffen als chirurgische.
- Infektion parallel
- Scheint das Risiko eines Exanthems zu erhöhen.20
- Dies gilt insbesondere für Infektionen mit dem HI-, Epstein-Barr-, Coxsackie- oder ECHO-Virus.
- Bei Patient*innen mit geschwächtem Immunsystem ist das Risiko arzneimittelinduzierter Hautreaktionen erhöht. Insbesondere HIV-infizierte Patient*innen haben ein deutlich erhöhtes Risiko, dass Medikamente schwere Nebenwirkungen auslösen.
- Alter
- Ältere Menschen sind in der Regel häufiger betroffen als jüngere.
- Dies gilt vor allem für die nicht-IgE-allergisch induzierten Reaktionen.
- Atopie
- Erhöht das Risiko arzneimittelinduzierter (allergischer) Hautreaktionen.
- Immundefekt
Medikamentenbezogen
- Relevante Faktoren sind Molekülgröße, Struktur, Dosierung, Verabreichung und Dauer der Exposition.
- Etwa 80 % aller arzneimittelinduzierter Hautreaktionen treten 5–15 Tage nach Beginn der Einnahme auf (meist bei Antibiotika und NSAR).
ICPC-2
- A85 Unerwünschte Wirkung eines Medikaments
- S99 Hautkrankheit, andere
ICD-10
- L27.- Dermatitis durch oral, enteral oder parenteral aufgenommene Substanzen
- L27.0 Generalisierte Hauteruption durch Drogen oder Arzneimittel
- L27.1 Lokalisierte Hauteruption durch Drogen oder Arzneimittel
- L27.2 Dermatitis durch aufgenommene Nahrungsmittel
- L27.8 Dermatitis durch sonstige oral, enteral oder parenteral aufgenommene Substanzen
- L27.9 Dermatitis durch nicht näher bezeichnete oral, enteral oder parenteral aufgenommene Substanz
Sonstige
- L10.5 Arzneimittelinduzierter Pemphigus
- L23.3 Allergische Kontaktdermatitis durch Drogen oder Arzneimittel bei Hautkontakt
- L24.4 Toxische Kontaktdermatitis durch Drogen oder Arzneimittel bei Hautkontakt
- L25.1 Nicht näher bezeichnete Kontaktdermatitis durch Drogen oder Arzneimittel bei Hautkontakt
- L50.- Urtikaria
- L56.0 Phototoxische Reaktion auf Arzneimittel
- L56.1 Photoallergische Reaktion auf Arzneimittel
- L51.2 Toxische epidermale Nekrolyse
- T78.4 Allergie, nicht näher bezeichnet
- T88.7 Nicht näher bezeichnete unerwünschte Nebenwirkung eines Arzneimittels oder einer Droge
Diagnostik
Diagnostische Kriterien
- Arzneimittelinduzierte Hautreaktionen können in den unterschiedlichsten Formen auftreten.
- Grundlage für die Diagnose einer arzneimittelinduzierten Hautreaktion ist die gründliche Anamnese mit genauer Erfassung eingenommener Medikamente, Untersuchung der Haut einschließlich Morphologie der Hautreaktion und Erhebung ggf. vorliegender systemischer Befunde (Fieber, Blutbildveränderungen; insbesondere Eosinophilie, Lymphadenopathie, Leberfunktionsstörungen).4,8
- Bei Verdacht auf eine Arzneimittelallergie ist eine möglichst sichere Diagnose von größter Bedeutung.1
- Der Verdacht auf eine Allergie ist ebenso einzuordnen wie eine nachgewiesene.
- Der Verzicht auf eine Allergie-Diagnostik kann einerseits schwere Reaktionen bei erneuter Exposition zur Folge haben, andererseits zu ungerechtfertigter Einschränkung der Therapiemöglichkeiten führen.
Differenzialdiagnosen
- (Unspezifisches) Virusexanthem
Anamnese
Allgemeines
- In der überwiegenden Mehrheit werden arzneimittelinduzierte Hautreaktionen durch Medikamente ausgelöst, die in den letzten 2–3 Wochen vor Auftreten der ersten Symptome eingenommen wurden. Wird ein bekanntes Medikament erneut eingenommen, treten die Symptome häufig wenige Tage nach der erneuten Einnahme auf.
- Alle eingenommenen Medikamente sind genau zu erfassen. Dies gilt für verschreibungspflichtige und frei verkäufliche Präparate gleichermaßen.
- Eine Allergie ist höchstwahrscheinlich durch ein Medikamente verursacht, das erst seit kurzer Zeit eingenommen wird.
- Exantheme nicht-allergischer Genese können u. U. auch verzögert nach Tagen bis Wochen auftreten.
- Wurde die als Ursache vermutete oder eine chemisch ähnliche Substanz bereits zuvor eingenommen?
- Sind bereits zuvor arzneimittelinduzierte Reaktionen aufgetreten und durch welche Medikamente wurden diese ggf. verursacht?
- Arzneimittelinduzierte Reaktionen treten in der Regel in Verbindung mit Juckreiz auf, was bei virusbedingten Exanthemen nur selten der Fall ist.
- In einigen Fällen kann auch ein ohne Rötung/Reizung der Haut auftretender Juckreiz arzneimittelinduziert sein.
Beurteilung eines möglichen Kausalzusammenhangs
- Ein möglicher Kausalzusammenhang zwischen Medikament und Hautreaktion sollte geprüft, kann aber häufig nicht mit abschließender Sicherheit nachgewiesen werden.
- Da eine möglichst frühe Absetzung des verursachenden Medikaments die Prognose günstig beeinflusst, soll eine solche Beurteilung für jedes eingenommene Medikament erfolgen.22
- Wenn mehrere Medikamente mit der gleichen Wahrscheinlichkeit als Verursacher vermutet werden, lautet die Empfehlung, zuerst das Medikament mit der niedrigsten medizinischen Dringlichkeit abzusetzen oder – wenn ein vollständiges Absetzen nicht empfehlenswert ist – herunterzudosieren.
Zeichen einer schweren Arzneimittelreaktion
- Zunehmende allgemeine Symptome (Bronchitis, Fieber), Ödembildung im Gesicht und Beteiligung der Schleimhäute (Lippen, Bindehaut, Genitalien) deuten auf eine schwere Arzneimittelreaktion hin.
- In diesem Fall ist eine rasche Krankenhauseinweisung indiziert.
- Die Weltgesundheitsorganisation definiert eine schwere Arzneimittelreaktion als Reaktion, die tödlich oder lebensbedrohlich verläuft, eine Krankenhauseinweisung erfordert, einen Krankenhausaufenthalt verlängert oder zu dauerhaften oder erheblichen Funktionsbeeinträchtigungen oder Folgeerkrankungen führt.22
- Gemäß dieser Definition sind etwa 2 % aller Arzneimittelreaktionen als schwer einzustufen.
Klinische Untersuchung
- Arzneimittelallergien treten meist symmetrisch auf.
- Von Juckreiz bei äußerlich unauffälliger Haut über die zuvor genannten, relativ häufig auftretenden exanthematischen Symptome sowie seltenere lichenoide und lupusähnliche Erscheinungen bis hin zu schweren bullösen Hautreaktionen, Erythrodermie und Epidermolysis können arzneimittelinduzierte Hautreaktionen die verschiedensten Formen annehmen.
Vaskulitis
- Evtl. liegen urtikariaähnliche Papeln, tastbare Purpura und nekrotische Hautpartien vor.
- Bei Entwicklung der Serumkrankheit kommen Fieber, Gelenkschmerzen und Lymphadenitis hinzu.
- Vereinzelt tritt auch das Erythema nodosum auf.
Purpura
- Hierbei handelt es sich um einen erythematös-kleinfleckigen Hautausschlag (seltener auch mit Bildung von Papeln), der durch Kapillarblutungen in der Unterhaut verursacht wird.
- Die Begriffe Petechien und Purpura werden teilweise nicht klar voneinander abgegrenzt.
- Während der Begriff Petechien das äußere Erscheinungsbild eines Ausschlags bezeichnet, ist der Begriff Purpura die klinische Bezeichnung für petechiale Blutungen.
- Ein ggf. vorliegender Blutaustritt kann durch Thrombozytopenie, Gerinnungsstörungen, Vaskulitis, unzureichend stützendes Bindegewebe an den Gefäßwänden, vaskuläre Defekte oder erhöhten intravaskulären Druck verursacht sein.
Stevens-Johnson-Syndrom (SJS)/Toxische epidermale Nekrolyse (TEN)
-
Nach einigen Tagen mit leichtem Krankheitsgefühl bilden sich großflächige ödematöse Erytheme und große Blasen; im weiteren Verlauf kommt es zur Abstoßung nekrotischer Haut- und Schleimhautpartien.
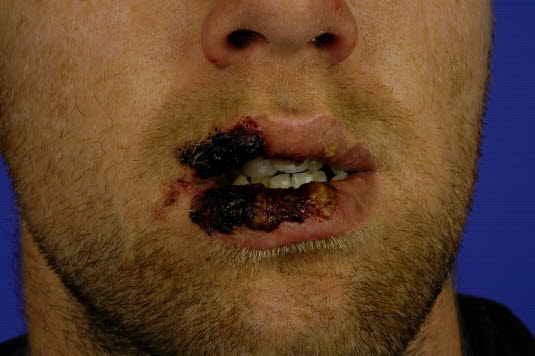 Stevens-Johnson-Syndrom
Stevens-Johnson-Syndrom - Diese Form der Hautreaktion kann zu Störungen des Flüssigkeits- und Elektrolythaushalts, gestörter Thermoregulation und erhöhter Infektionsanfälligkeit führen und lebensbedrohlich sein.
- Sie stellt die Maximalvariante einer Arzneimittelreaktion dar. Das Stevens-Johnson-Syndrom (SJS) ist dabei die etwas mildere Variante einer TEN, die maximal 10 % der Hautoberfläche betrifft, ansonsten aber die gleiche Pathogenese und Klinik bietet.
Fixe Arzneimittelreaktion
- In Verbindung mit der Einnahme von Medikamenten akut auftretendes, immunologisch induziertes Exanthem
- Runder, geröteter Fleck, manchmal mit zentraler Blasenbildung, von roter oder rotbrauner Färbung, Ödembildung
- Geht nach einigen Wochen zurück und hinterlässt eine leichte Hyperpigmentierung.
- Bei erneuter Einnahme des gleichen Medikaments tritt der Fleck an der gleichen Stelle erneut auf.
Ergänzende Untersuchungen in der Hausarztpraxis
- Bei Verdacht auf eine Typ-I-Penicillinallergie kann ein RAST-Test indiziert sein.
- Einschränkung: RAST-Tests dienen der Orientierung und beweisen NICHT eine vorliegende, relevante Allergie.
- Evtl. Blutuntersuchungen – Blutbild: Hb, Thrombozytenzahl; Leber- und Nierenwerte; Gerinnungsparameter
- Bei 36–75 % der Patient*innen liegt eine periphere Eosinophilie vor.23
Diagnostik bei Spezialist*innen
Leitlinie: Überempfindlichkeitsreaktionen auf Arzneimittel1
Allergologische Diagnostik
- Eine allergologische Diagnostik bei arzneimittelinduzierten Hautausschlägen ist wichtig, um Typ-1-allergische Reaktionen von Hautausschlägen anderer Pathogenese zu unterscheiden.
- Der Verzicht auf eine Diagnostik kann einerseits schwere Reaktionen bei erneuter Exposition zur Folge haben, andererseits zu ungerechtfertigter Einschränkung der Therapiemöglichkeiten führen.
- Eine allergologische Klärung möglichst innerhalb von 4 Wochen bis 6 Monaten nach Abheilung der Symptome ist anzustreben.
Anamnese/zeitliches Auftreten
- Typische Zeitintervalle zwischen erster Arzneimittelzufuhr und erstmaligem Auftreten von Symptomen:
- Urtikaria, Asthma, Anaphylaxie: typisch bis 1 Stunde, selten bis 12 Stunden nach Exposition
- makulopapulöses Arzneimittelexanthem: 4–14 Tage nach Beginn der Zufuhr
- akute generalisierte exanthematische Pustulose (AGEP): 1–12 Tage nach Beginn der Zufuhr
- SJS/TEN: 4–28 Tage nach Beginn der Zufuhr
- DRESS: 2–8 Wochen nach Beginn der Zufuhr
Diagnostik
- Hauttests
- Hauttests erfolgen bei Überempfindlichkeitsreaktionen mit Symptomen allergischer Reaktionen, um eine Sensibilisierung zu erfassen.
- Es gibt bisher jedoch keinen einheitlichen Standard für die Hauttestung mit Arzneistoffen.
- Testablauf Hauttests
- ausreichendes Intervall zur Arzneimittelreaktion und zu antiallergischer Medikation
- bei Risiko des Tests zur Auslösung einer systemischen Reaktion adäquate ärztliche Überwachung der Patient*innen über einen ausreichenden Zeitraum, ggf. Schwellentest mit verdünnten Lösungen
- Reihenfolge der Testverfahren: Prick-Test vor Intradermaltest; Epikutantest (ggf. offen vor geschlossen vor Abrissepikutantest); bei Verdacht auf photoinduzierte Reaktionen zusätzliche Tests in Kombination mit UV-Bestrahlung (z. B. Photopatchtest)
- Bei Kindern, insbesondere Säuglingen und Kleinkindern sollten schmerzhafte Intradermaltests zurückhaltend eingesetzt werden.
- Wahl des zeitlichen Ablaufs (simultane oder konsekutive Diagnostik verschiedener Substanzen oder Substanzkonzentrationen) entsprechend dem vermuteten Pathomechanismus, der Schwere der Reaktion und dem Risiko der gewählten Hauttestmethodik
- Ablesung der Testreaktion bei Prick- bzw. Intradermaltest typischerweise nach 15–20 Minuten, beim Epikutantest nach 24 bzw. 48 und 72 Stunden. Bei Exanthemen sollte bei Prick- und Intradermaltest auch eine Spätablesung nach 24 und 48 (oder 48 und 72) Stunden erfolgen (Beispiel: Abklärung eines Amoxicillinexanthems). Bei anaphylaktischen Symptomen und höherem Testrisiko kann ein offener Epikutantest mit Frühablesung nach 20–30 Minuten durchgeführt werden (Beispiel: Abklärung einer Anaphylaxie nach topischer Applikation von Bacitracin). Weitere Ablesezeitpunkte können sinnvoll sein, z. B. Epikutantestablesung nach 7 Tagen bei Glukokortikoid-Allergie. Anmerkung: Hauttestreaktionen können auch zu anderen Zeitpunkten auftreten, manchmal auch erst nach mehr als einer Woche. Weisen Sie die Patient*innen darauf hin, dass sie sich dann umgehend vorstellen sollen.
- In-vitro-Untersuchungen
- Laboruntersuchungen können insbesondere bei negativen Hauttests sowie bei schweren lebensbedrohlichen Reaktionen hilfreich sein, vor allem in Situationen, in denen kein Provokationstest durchgeführt werden kann bzw. der Hauttest selber eine mögliche Gefährdung ist, wie z. B. bei anaphylaktischen Reaktionen auf Beta-Laktam-Antibiotika.
- Tests zur Messung spezifischer IgE-Antikörper auf verschiedene Arzneimittel werden angeboten.
- Validierte Tests zum Nachweis spezifischer Immunglobulin-E(sIgE)-Antikörper im Serum sind nur für wenige Arzneistoffe, vor allem Beta-Laktam-Antibiotika, verfügbar.
- Zelluläre Tests sind in manchen Fällen hilfreich, stehen allerdings nur in einigen Zentren zur Verfügung.
- Ein sicherer Nachweis oder Ausschluss einer Arzneimittelüberempfindlichkeit allein auf Basis von In-vitro-Tests ist nicht möglich. Die Interpretation der Ergebnisse von In-vitro-Tests ist nur im Zusammenhang mit Anamnese/klinischer Manifestation und ggf. In-vivo-Tests möglich.
- Provokationstests
- Provokationstests sind angezeigt, wenn der Auslöser einer Arzneimittelüberempfindlichkeit durch Anamnese, Hauttest und In-vitro-Untersuchungen nicht mit hinreichender Sicherheit identifiziert werden kann, und wenn der Nutzen des Informationsgewinns das Risiko übersteigt.
Gesamtbeurteilung
- Die abschließende Beurteilung der Befunde muss neben dem Ergebnis von Haut-, In-vitro- und Provokationstests insbesondere die Anamnese der klinischen Reaktion berücksichtigen.
- Ein sicherer Ausschluss einer Überempfindlichkeit auf ein Arzneimittel ist auch bei Anwendung aller verfügbaren Testverfahren nicht immer möglich, jedoch wird die Risikoabschätzung erleichtert.
- Tryptasespiegel im Serum?
- Der Test weist bei Patient*innen mit akuten allergischen Reaktionen eine Aktivierung der Mastzellen nach, ist aber nicht spezifisch und wird daher nicht routinemäßig eingesetzt.
- Die Konzentration im Serum ist 3–4 Stunden nach dem ersten Auftreten der Symptome am höchsten und sinkt dann innerhalb von 24 Stunden auf den normalen Wert.
- Evtl. sind mehrere Blutuntersuchungen im Abstand von jeweils 2 Stunden indiziert.24
- Hautbiopsie?
- Eine Stanzbiopsie von 3–4 mm Hautgewebe kann Aufschluss über die Art der Hautveränderung geben.
- Bei Blasenbildung und Verdacht auf Vaskulitis wird außerdem eine Immunfluoreszenzuntersuchung durchgeführt.
- Bei Arzneimittelexanthemen ist eine Biopsie des betroffenen Gewebes nicht sehr aufschlussreich und wird nicht routinemäßig eingesetzt.
Allergietests
- Spezifisches Immunglobulin E
- Kann bei Verdacht auf eine IgE-vermittelte Reaktion (Urtikaria, Angioödem, Anaphylaxie) relevant sein. Dies gilt insbesondere für Typ-I-Reaktionen auf Beta-Laktam-Antibiotika.
- RAST-Tests für das Hauptallergen von Ampicillin und Amoxicillin stehen zur Verfügung.
- Der Test auf Penicillin-spezifisches lgE weist eine niedrige Sensitivität (18 %), aber eine hohe Spezifität (90 %) auf.25
- Da den meisten Arzneimittelexanthemen jedoch keine Typ-I-Reaktion zugrunde liegt, sind Serumtests (RAST) in der Regel nicht routinemäßig indiziert.
- Kann bei Verdacht auf eine IgE-vermittelte Reaktion (Urtikaria, Angioödem, Anaphylaxie) relevant sein. Dies gilt insbesondere für Typ-I-Reaktionen auf Beta-Laktam-Antibiotika.
- Patch-Test
- Prick-Test
- Bei Verdacht auf eine IgE-vermittelte Reaktion werden verdünnte Allergene auf die leicht eingeritzte Haut aufgetragen.
- Der Test wird bei Typ-I-Reaktionen (Urtikaria) eingesetzt und ist bei einem Arzneimittelexanthem daher meist nicht indiziert.
- Intrakutantest
- Der Test erfolgt mittels Allergenzufuhr in zunehmender Verdünnung und Negativkontrollen.
- Systemischer Provokationstest
- Liefert den zuverlässigsten Nachweis eines Kausalzusammenhangs zwischen der Verabreichung eines bestimmten Medikaments und einer dadurch ausgelösten Hautreaktion.28-29
- Da ein solcher Test ein gewisses Risiko birgt, kommt er erst zum Einsatz, wenn andere Testverfahren nicht zum gewünschten Ergebnis geführt haben und eine sichere Diagnose sehr wichtig ist.
- Es besteht die Gefahr einer relevanten klinischen Reaktion auf die Testsubstanz, sodass Provokationstest nur unter Notfallbereitschaft durchgeführt werden dürfen.
- Ein weiterer Nachteil des Tests besteht darin, dass sich die bei Auftreten der Hautreaktion herrschenden Bedingungen nicht exakt wiederherstellen lassen.
- Bei bestimmten Erkrankungen sind systemische Provokationstests zudem kontraindiziert.29
- Fazit
- Nach Abschluss der Untersuchungen ist kritisch zu prüfen, mit welcher Wahrscheinlichkeit ein Zusammenhang zwischen Medikament und Hautreaktion vorliegt.
Indikationen zur Überweisung/Klinikeinweisung
- Bei sehr akuten und schweren Hautreaktionen kann eine fachärztliche Beurteilung und ggf. stationäre Aufnahme zwecks Beobachtung und Therapie erforderlich sein.
- Patient*innen mit toxischer epidermaler Nekrolyse bedürfen häufig einer intensivmedizinischen Versorgung.
Klinische Formen
Arzneimittelexanthem
Anamnese
- Makulopapulöser Hautausschlag
- Dies ist die häufigste arzneimittelinduzierte Hautreaktion.
- Tritt relativ häufig in Verbindung mit leichtem Fieber auf, das aber oft keine Reaktion auf das Medikament, sondern vielmehr ein Zeichen der behandelten Erkrankung darstellt.
- Häufig breitet sich der Ausschlag vom Rumpf her aus.
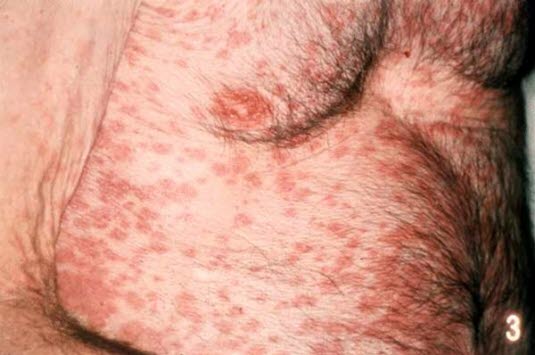 Arzneimittelexanthem
Arzneimittelexanthem - Anders als bei den meisten virusbedingten Exanthemen sind Schleimhäute, Gesicht und Handflächen selten betroffen.
- Schätzungen zufolge werden Hautreaktionen dieser Art bei Erwachsenen zu etwa 50–70 % und bei Kindern zu etwa 10–20 % von Medikamenten verursacht.
- Ein Arzneimittelexanthem bildet sich in der Regel im Laufe weniger Wochen zurück.
- Werden bei bestimmten Viruserkrankungen wie dem Pfeiffer-Drüsenfieber Aminopenicilline eingenommen, liegt das Risiko für ein Arzneimittelexanthem bei knapp 90 %.
- Eine vorliegende HIV-Infektion erhöht das Risiko für Hautreaktionen bei Einnahme von Sulfonamiden um das Zehnfache.
Klinische Untersuchung
- 70–95 % aller Arzneimittelexantheme äußern sich in einem generalisierten Hautausschlag, der ohne oder mit nur leichten Allgemeinsymptomen auftritt.4,22
- Sie manifestieren sich in der Regel in einem generalisierten makulopapulösen, morbilliformen oder urtikariellen Exanthem, das meist Juckreiz auslöst.
- Meist ohne Juckreiz tritt dagegen die lymphozytäre Arzneimittelreaktion auf, die sich in lokalisierten oder generalisierten, meist wenig symptomatischen roten oder braunen Papeln, Plaques oder Knoten mit meist glatter Oberfläche äußert.30
- Wenn keine extrakutane Manifestation vorliegt, wie z. B. schlechter Allgemeinzustand, Fieber oder spezifische Organbefunde, fällt die Prognose in der Regel günstig aus.4
Urtikaria, Angioödem und Anaphylaxie
Anamnese
- Die Urtikaria ist die zweithäufigste arzneimittelinduzierte Hautreaktion und steht für 6–25 % aller generalisierten Nebenwirkungen von Medikamenten.
- Insgesamt werden jedoch nur 10 % aller Fälle von Urtikaria durch Medikamente verursacht.
- Typisch für die Urtikaria sind juckende Quaddeln ohne epidermale Veränderungen.
- Das wichtigste Merkmal, anhand dessen sich die Urtikaria auch von einem Arzneimittelexanthem unterscheiden lässt, ist der flüchtige Charakter der Quaddeln.
- Anaphylaxie
- Tritt einmal pro 50.000 Verabreichungen von Penicillin auf, kommt bei parenteraler Gabe häufiger vor als bei peroraler Gabe und manifestiert sich innerhalb weniger Minuten nach der Exposition.
- Kann auch z. B. nach der Gabe von Lokalanästhetika und Kontrastmitteln auftreten.
- Allergien und Anaphylaxien nach Kontakt mit Latex sind seltener, aber möglich.
Klinische Untersuchung
- Urtikaria
- zweithäufigste arzneimittelinduzierte Hautreaktion
- Typisch sind juckende und flüchtige Bläschen.
- Angioödem
- Flüchtiges Ödem der Haut und tieferer Gewebeschichten, das in der Regel nicht juckt und manchmal, aber nicht immer, in Verbindung mit einer Urtikaria auftritt.
- Unter 1.000 Anwendern von ACE-Hemmern kommt es in 1–2 Fällen zur Bildung eines Angioödems, das im Übrigen noch Monate nach Behandlungsbeginn auftreten kann.
Akute generalisierte exanthematische Pustulose (AGEP)
Anamnese
- Seltene arzneimittelinduzierte Hautreaktion
- Die Reaktion tritt häufig wenige Tage nach Gabe eines Medikaments auf.1
- Wird besonders häufig durch Beta-Laktam-Antibiotika, seltener durch Kalziumantagonisten und Antikonvulsiva ausgelöst.
- Hierbei handelt es sich um eine in Verbindung mit Fieber auftretende Hautreaktion, die in über 90 % der Fälle durch Medikamente hervorgerufen wird.15
- Auf ödematösen, erythematösen Hautpartien bilden sich in großer Zahl nicht follikuläre, sterile Pusteln.
- Häufig beginnt der Hautausschlag im Gesicht oder in den großen Beugen und der Leistengegend sowie zeitgleich mit oder kurz nach dem Auftreten von Fieber.
- Blutuntersuchungen zeigen häufig keine Eosinophilie, die bei anderen arzneimittelinduzierten Hautreaktionen vorkommen kann, sondern eine Neutrophilie.14
- Es besteht Verwechslungsgefahr mit Psoriasis pustulosa, die jedoch langsamer fortschreitet.
- Der Patch-Test fällt bei bis zu 80 % der Patient*innen positiv aus.31
Klinische Untersuchung
- In Verbindung mit Fieber auftretende Hautreaktion, bei der sich auf ödematösen, erythematösen Hautpartien in großer Zahl nicht-follikuläre, sterile Pusteln bilden.
- Häufig beginnt der Hautausschlag im Gesicht oder in den großen Beugen und der Leistengegend sowie zeitgleich mit oder kurz nach dem Auftreten von Fieber.
Dermatitische Reaktionen
- Großflächige Ekzeme werden relativ selten durch Medikamente verursacht, können aber vorkommen, wenn bereits zuvor eine perkutane Sensibilisierung mit dem fraglichen Medikament erfolgt ist.
- Medikamente können auch eine generalisierte, exfoliative Dermatitis oder Erythrodermie (Rötung des gesamten Hautorgans) auslösen.
- Dann kommen ggf. geschwollene Lymphknoten, Fieber und Flüssigkeitsverlust über die Haut hinzu, die Untersuchungen im Krankenhaus und eine stationäre Aufnahme erforderlich machen.
- In der Regel gehen solche Fälle mit einer günstigen Prognose einher.
Erythema (exsudativum) multiforme
- Weitere Informationen finden Sie im Artikel Erythema multiforme und im Artikel Generalisierter Hautausschlag.
- Typisch für das Erythema multiforme sind symmetrisch und distal an den Extremitäten auftretende, ringförmige Rötungen (Kokarden), in deren Mitte sich oft Papeln finden, die sich wiederum zu Blasen entwickeln können.
- Abgesehen vom Gesicht und ggf. der Mundhöhle breitet sich der Ausschlag peripher aus. Er ist auf den Streckseiten der Extremitäten (insbesondere Handrücken) am stärksten ausgeprägt, tritt aber auch an den Handflächen und Fußsohlen auf.
- Die Erkrankung wird am häufigsten durch eine Virusinfektion (insbesondere mit dem Herpes-simplex-Virus) oder eine Infektion mit Mycoplasma pneumoniae ausgelöst.
- Ein Erythema multiforme ist nur selten mit einer malignen Grunderkrankung, Gefäßerkrankung oder HIV-Infektion assoziiert und geht mit einer günstigen Prognose einher.4
- Man geht davon aus, dass die Erkrankung in etwa 10 % der Fälle durch Medikamente und in den restlichen Fällen durch Virusinfektionen ausgelöst werden.
Stevens-Johnson-Syndrom (SJS) und toxische epidermale Nekrolyse (TEN)
- Siehe Artikel Toxische epidermale Nekrolyse.
- Definition
- Hierbei handelt es sich um generalisierte Reaktionen, die mit einer zunehmenden Verschlechterung des Allgemeinzustands sowie einer unterschiedlich stark ausgeprägten Ablösung der Haut und Beteiligung der Schleimhäute einhergehen.
- Bei manchen Patient*innen können sich diese Erkrankungen in einem klinischen Bild manifestieren, das dem des Erythema multiforme major ähnelt.
- Häufigkeit
- Klassifizierung
- Nachdem die Erkrankungen bisher als zwei separate Diagnosen behandelt wurden33-34, herrscht mittlerweile dahingehend ein breiter Konsens, dass es sich um verschiedene Ausprägungen des gleichen klinischen Syndroms handelt.35
- In der jüngeren internationalen Literatur4 werden mittlerweile Stevens-Johnson-Syndrom, Übergangsform zur toxischen epidermalen Nekrolyse und toxische epidermale Nekrolyse unterschieden.
- Auslösende Medikamente
- Als häufigste Ursache in Europa gilt Allpurinol.10-11
- Weitere häufige Auslöser sind Carbamazepin, Cotrimoxazol, Nevirapin, Phenobarbital, Phenytoin und Lamotrigin.10
- Das Stevens-Johnson-Syndrom und die toxische epidermale Nekrolyse werden zudem durch Sulfonamide, andere Antikonvulsiva und nichtsteroidale Entzündungshemmer ausgelöst, können aber auch durch andere Medikamente hervorgerufen werden.4,22,36
- Tetrazepam als einem der möglichen Auslöser ist mittlerweile die Zulassung entzogen worden.16
- Bei Kindern werden diese Reaktionen am häufigsten durch Penicilline und Sulfonamid-Verbindungen verursacht.
- Wichtigstes Diagnosekriterium
- Für die 3 genannten Ausprägungen beträgt der Grad der Hautablösung < 10 %, 10–30 % und > 30 %.
- Prognose
- Die Prognose hängt davon ab, in welchem Grad es zu einer vollständigen Ablösung der Haut kommt.
- Je nach Grad der Hautablösung, Alter und Grunderkrankung (Infektion, Malignität) schwankt die Letalität zwischen etwa 5 % beim Stevens-Johnson-Syndrom und bis zu etwa 30 % bei der toxischen epidermalen Nekrolyse.
Arzneimittelkommission der deutschen Ärzteschaft: SJS/TEN10
- Bitte teilen Sie der AkdÄ alle beobachteten Nebenwirkungen (auch Verdachtsfälle) mit.
- Sie können dafür den Berichtsbogen verwenden, der regelmäßig im Deutschen Ärzteblatt abgedruckt wird oder über die Homepage der AkdÄ abrufbar ist.
- Es besteht auch die Möglichkeit, über www.akdae.de direkt online einen UAW-Verdachtsfall zu melden.
- Bei Verdacht auf das akute Vorliegen von SJS oder TEN sollten sich behandelnde Ärzte rasch mit dem Dokumentationszentrum schwerer Hautreaktionen (dZh) an der Universitäts-Hautklinik Freiburg in Verbindung setzen (Telefon: 07 61/2 70-67 23, E-Mail: dzh@uniklinik-freiburg.de).
Kutane Überempfindlichkeitsreaktionen
- DRESS-Syndrom (Arzneimittelexanthem mit Eosinophilie und systemischen Manifestationen)
- DRESS steht für Drug Reaction with Eosinophilia and Systemic Symptoms.9
- Synonym: Carbamazepin-Phenytoin-Hypersensitivitäts-Syndrom
- Neben dem auslösenden Medikament (auslösend häufig Carbamazepin und Phenytoin, aber auch Allopurinol u. a.) spielt eine Reaktvierung von Virusinfektionen (HHV-6) eine pathogenetische Rolle.9
- Verlauf
- Klinisch beginnt das DRESS-Syndrom häufig mit einem morbilliformen oder urtikariellen Hautausschlag mit zunehmender Ödembildung, wobei das Gesichtsödem das Hauptsymptom darstellt.
- Auch die Bildung von Bläschen und Blasen ist möglich.
- Weitere klinische Zeichen sind eine deutliche Verschlechterung des Allgemeinzustands, Eosinophilie, geschwollene Lymphknoten, Gelenkschmerzen sowie eine Beteiligung innerer Organe (Lunge, Leber, Nieren, Herz).
- Symptome treten meist mit einer Latenz von 2–8 Wochen nach erster Einnahme und damit später als die meisten anderen Hautreaktionen auf.1
- Auslösende Medikamente
- Das DRESS-Syndrom wird meist durch Antikonvulsiva und Sulfonamide ausgelöst.
- Auch Allopurinol ist ein häufiger Auslöser (5 % aller DRESS-Fälle werden durch Allopurinol ausgelöst).9,37
- Rezidive des DRESS-Syndroms sind manchmal nicht arzneimittelinduziert, sondern durch die Reaktivierung von Viren verursacht (VRESS).38
- Prognose
- Die Letalität wird mit 10 % angegeben.36
Therapie
Therapieziele
- Allergische Reaktionen unterdrücken.
- Symptome lindern.
- Folgeerscheinungen vorbeugen.
Allgemeines zur Therapie
- Das auslösende Medikament ist abzusetzen.
- Für Typ-I-Allergien (Urtikaria, Angioödem, Anaphylaxie) gilt:
- Betroffene Patient*innen dürfen keinesfalls erneut der gleichen oder einer chemisch ähnlichen Substanz ausgesetzt werden.
- Die erneute Exposition gegenüber einer Substanz, die bei Patient*innen bereits akute allergische Reaktionen ausgelöst hat, kann katastrophale Folgen haben: Von einer Provokation ist daher in der Regel abzuraten.
- Für mild ausgeprägte Arzneimittelexantheme gilt:
- Wenn wahrscheinlich eine Typ-IV-Allergie vorliegt und das auslösende Medikament dringend erforderlich ist, kann die symptomatische Therapie der Hautreaktion und eine Fortsetzung der medikamentösen Therapie in bestimmten Fällen ggf. vertretbar sein.
- Sobald sich die Symptome verstärken, muss das Medikament jedoch abgesetzt werden.
Schwere arzneimittelinduzierte Hautreaktionen
- Klinisches Bild
- Bei den meisten Patient*innen mit schweren arzneimittelinduzierten Hautreaktionen treten 1–14 Tage vor Ausbruch des Exanthems Fieber, Übelkeit, Husten, Kopfschmerzen und/oder Diarrhö auf.
- Typisch für das Stevens-Johnson-Syndrom und die toxische epidermale Nekrolyse sind Blasen oder Erosionen und im weiteren Verlauf eine unterschiedlich stark ausgeprägte Ablösung der Haut sowie eine Beteiligung der Schleimhäute, die mit Überempfindlichkeit, Brennen, Schwellungen und Schmerzen einhergeht.
- Das Exanthem breitet sich häufig vom Gesicht her aus und kann äußerst schmerzhaft sein.
- Maßnahmen
- Die wichtigste Maßnahme besteht im Absetzen des mutmaßlich auslösenden Medikaments.4,8
- Danach ist eine stationäre Überwachung und häufig auch intensivmedizinische Versorgung sowie eine infektiologische, ophthamologische und dermatologische Betreuung indiziert.
- Patient*innen, bei denen die Ablösung der Epidermis 30–40 % des Gesamtorgans übersteigt, sollten in ein entsprechend spezialisiertes Verbrennungszentrum verlegt werden.
- Bei diesen Patient*innen besteht durch Sekundärinfektionen (z. B. Sepsis, Pilzinfektionen oder Lungenentzündung) und Multiorganversagen ein hohes Sterblichkeitsrisiko.
- Wenn Patient*innen überleben, bleiben häufig Folgeerscheinungen an der Haut und insbesondere an den Schleimhäuten zurück.
- So sind z. B. zur Verhinderung von Synechien tägliche ophthalmologische Kontrollen erforderlich. Erblindungen sind als Folgeerscheinungen beschrieben.
Medikamentöse Therapie
- Allergische Hautreaktionen können symptomatisch behandelt werden.
- Bei Juckreiz und Urtikaria werden in der Regel Antihistaminika oral und/oder lokale Glukokortikoidexterna verabreicht.
- Exanthematische Hautreaktionen klingen nach Absetzen des Medikaments meist von allein ab, bei Juckreiz kann in Analogie zu allergischen Reaktionen behandelt werden.
Schwere arzneimittelinduzierte Hautreaktionen
- Systemische Steroidtherapie?
- Obwohl keine größeren randomisierten Studien zur spezifischen Therapie vorliegen9, wird meist von einer systemischen Therapie mit Glukokortikoiden über die gesamte Behandlungsdauer abgeraten, da die Wirkung nicht gesichert ist und Komplikationen auftreten können.4,36
- Eine kurzfristige Stoßtherapie wird dennoch immer noch empfohlen (1.000–250–100–20 mg Prednisolon am 1. bis 4. Tag i. v.).17
- Intravenöse Immunglobuline
- Die intravenöse Gabe humaner Immunglobuline stellte sich in einigen Untersuchungen als wirksam heraus, woraufhin mit dieser Methode große Hoffnungen verknüpft wurden.35
- Es wurden jedoch in der Folge unterschiedliche Erfahrungen mit der Methode gemacht.39
- Der Einsatz wird somit weiterhin kontrovers diskutiert.
- Cyclosporin
- Auch für Cyclosporin ist die Datenlage uneinheitlich, jedoch vorsichtig vielversprechend.17
- Vor Gabe von Cyclosporin oder Glukokortikoiden bei SJS/TEN (meist bei älteren Menschen) muss eine bakterielle Ursache (SSSS/staphylogenes Lyell-Syndrom; meist bei Kleinkindern) sicher ausgeschlossen sein.
- Antibiotika bei Superinfektion
- Schmerztherapie
- Flüssigkeitsbilanzierung
Weitere Therapien
- Die wichtigste Maßnahme besteht im Absetzen des auslösenden Medikaments.
Prävention
- Typ-I-Allergien (Urtikaria, Angioödem, Anaphylaxie) können lebensbedrohliche anaphylaktische Reaktionen auslösen. Patient*innen mit einer Typ-I-Allergie gegen ein Medikament dürfen dem auslösenden Wirkstoff oder einer chemisch ähnlichen Substanz keinesfalls erneut ausgesetzt werden.
- Eine solche Allergie ist unmissverständlich in der Patientenakte und in einem Allergiepass zu vermerken.
- Multimedikation ist generell kritisch zu sehen und jedes Medikament sollte auf seine Indikation und die Wechselwirkungen mit anderen Medikamenten regelmäßig kontrolliert werden, z. B. über einen Interaktionscheck der verordneten Medikamente über die Praxissoftware.
- Behandelt werden sollten vor allem Erkrankungen und nicht isoliert auffällige Laborwerte, wie z. B. ein erhöhter Harnsäurewerte mit Allopurinol.9-10
- Problematisch stellt sich dies u. U. bei der Behandlung von etablierten Risikofaktoren für Erkrankungen des Herz-Kreislauf-Systems dar, wenn bisher keine Erkrankung vorliegt (Primärprävention).
Verlauf, Komplikationen und Prognose
Verlauf
Makulopapulöses Exanthem
- Hautausschläge können 2 Wochen nach Behandlungsbeginn und manchmal mehrere Wochen nach Absetzen des auslösenden Medikaments auftreten.
- Ein makulopapulöses Exanthem kann von verschiedenen Medikamenten, aber auch von vielen Virusinfektionen hervorgerufen werden.
- Manchmal müssen Virusinfekt und Medikament gleichzeitig zusammentreffen, um ein Exanthem auszulösen (Beispiel: EBV-Infektion und Amoxicillin-Einnahme).
Urtikaria, Angioödem und Anaphylaxie
- Typ-I-Allergien können sich in den verschiedensten Formen äußern: Von einem nur leichten urtikariellen Hautausschlag bis hin zum anaphylaktischen Schock mit Bronchospasmus, Larynxödem, generalisierter Urtikaria, Blutdruckabfall und Tod sind alle Abstufungen möglich.
- Bei ggf. erneuter Exposition gegenüber dem auslösenden Allergen ist das Risiko einer stärker ausgeprägten Typ-I-Reaktion erhöht (Sensibilisierung).
Komplikationen
- Bei Typ-I-Allergie: anaphylaktische Reaktionen
- In seltenen Fällen kann ein Arzneimittelexanthem zu einer schweren Erythrodermie fortschreiten.
- Eine toxische epidermale Nekrolyse kann Störungen des Flüssigkeits- und Elektrolythaushalts sowie eine gestörte Thermoregulation und erhöhte Infektionsanfälligkeit nach sich ziehen.
Prognose
- Die meisten exanthematischen Arzneimittelreaktionen an der Haut sind milde und vorübergehend.
- Die Symptome medikamenteninduzierter Hautreaktionen können zwischen 3 Tagen und 3 Wochen bzw. in schweren Fällen mehrere Wochen anhalten.
- Typ-I-Allergie-sensibilisierte Personen gelten lebenslang als allergisch.
- Typ-I-Allergien können lebensbedrohliche anaphylaktische Reaktionen auslösen.
- Schwere Arzneimittelreaktionen wie SJS/TEN gehen je nach Ausprägungsgrad mit einer Intensivpflichtigkeit und einer hohen Letalität einher.
Patienteninformationen
Worüber sollten Sie die Patient*innen informieren?
- Alle Patient*innen mit arzneimittelinduzierten Hautreaktionen sind mündlich und schriftlich über die künftig zu meidenden Medikamente zu informieren (Allergiepass).
- Hierbei ist über die Art der Reaktion, den Grad des Kausalzusammenhangs, evtl. Testergebnisse und alternative Medikamente bei ggf. künftigem Bedarf zu informieren.
- Patient*innen, bei denen schwere Ausprägungen arzneimittelinduzierter Hautreaktionen aufgetreten sind, sollten diese Informationen grundsätzlich mit sich führen.
Patienteninformationen in Deximed
Illustrationen
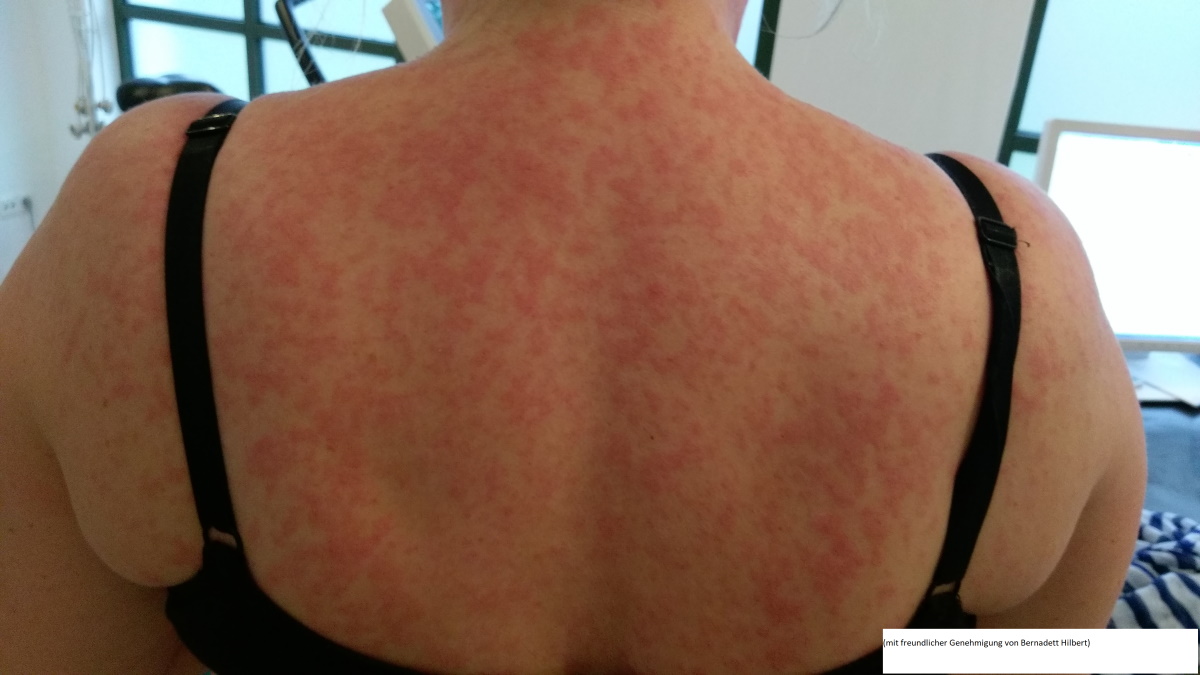
Arzneimittelexanthem (mit freundlicher Genehmigung von Bernadett Hilbert)
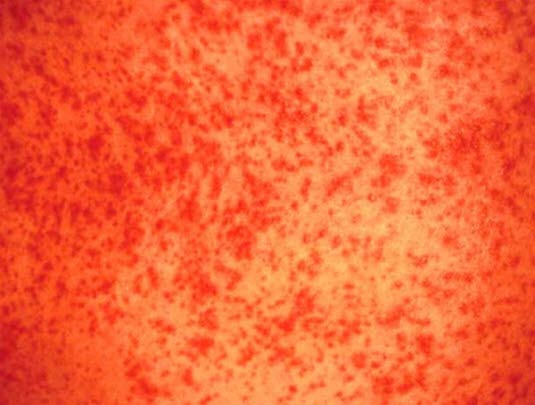
Generalisierter, symmetrischer, morbilliformer, makulopapulöser Ausschlag bei arzneimittelinduzierter Hautreaktion.
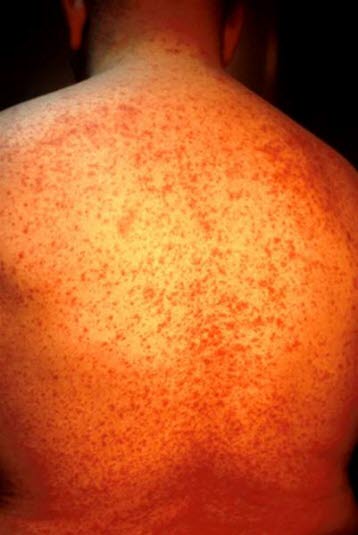
Das makulopapulöse Exanthem ist die häufigste arzneimittelinduzierte Hautreaktion.

Ein Arzneimittelexanthem breitet sich häufig langsam und vom Rumpf her aus.
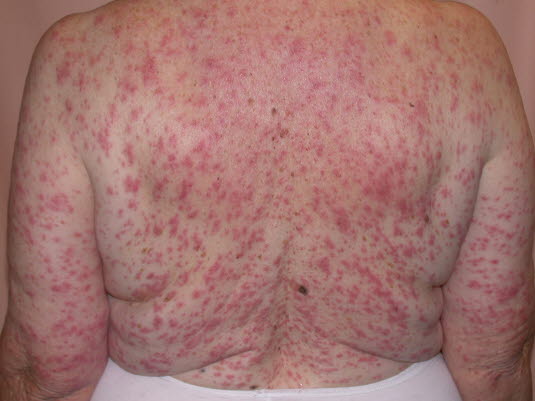
Arzneimittelexantheme treten relativ häufig in Verbindung mit leichtem Fieber auf, das aber oft keine Reaktion auf das Medikament, sondern vielmehr ein Zeichen der behandelten Erkrankung darstellt.
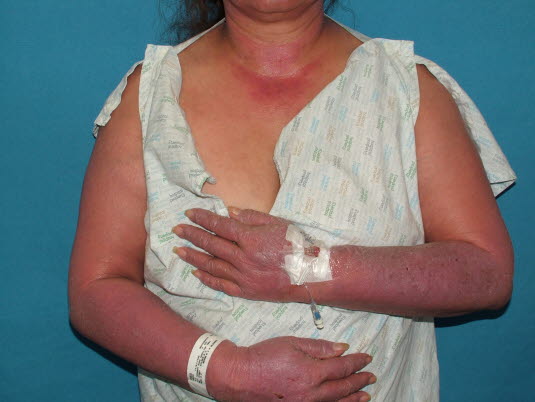
Photochemische Reaktionen können vom phototoxischen oder photoallergischen Typ sein. Diese Art des Ausschlags tritt stets auf sonnenexponierten Hautpartien auf.
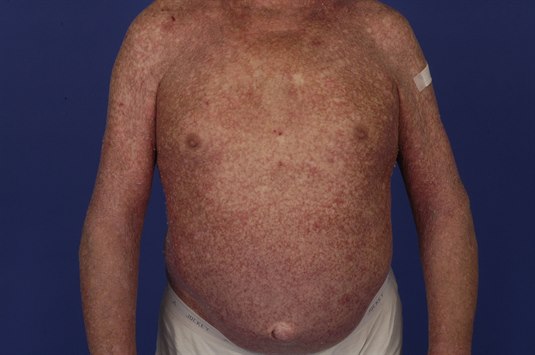
In der überwiegenden Mehrheit werden arzneimittelinduzierte Hautreaktionen durch Medikamente ausgelöst, die in den letzten zwei bis drei Wochen vor Auftreten der ersten Symptome eingenommen wurden. Wird ein bekanntes Medikament erneut eingenommen, treten die Symptome häufig schon wenige Tage nach der erneuten Einnahme auf.

Das Stevens-Johnson-Syndrom geht mit einer zunehmenden Verschlechterung des Allgemeinzustands sowie einer unterschiedlich stark ausgeprägten Ablösung der Haut und Beteiligung der Schleimhäute einher.
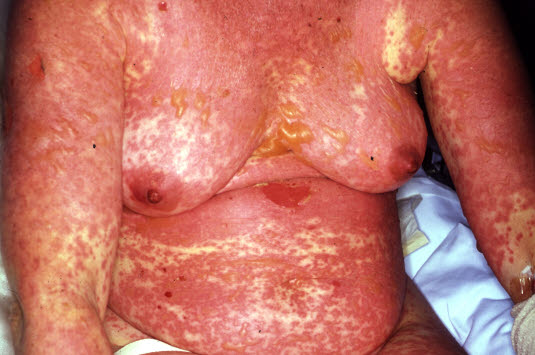
Je nach Grad der Hautablösung, Alter und Grunderkrankung (Infektion, Malignität) beträgt die Letalität bei der toxischen epidermalen Nekrolyse bis zu etwa 30 %.
Quellen
Leitlinien
- Deutsche Gesellschaft für Allergologie und klinische Immunologie (DGAKI). Überempfindlichkeitsreaktionen auf Arzneimittel, Allergologische Diagnostik. AWMF-Leitlinie Nr. 061-021. S2k, Stand 2014. www.awmf.org
Literatur
- Deutsche Gesellschaft für Allergologie und klinische Immunologie. Überempfindlichkeitsreaktionen auf Arzneimittel, Allergologische Diagnostik. AWMF-Leitlinie Nr. 061-021, Stand 2014. www.awmf.org
- Altmeyer, P. Dermatologie-Enzyklopädie. Arzneimittelwirkung unerwünschte (Übersicht) L27.0. Stand 2018 www.enzyklopaedie-dermatologie.de
- Arzneimittelkommission der deutschen Ärzteschaft. Pharmakovigilanz. Arzneiverordnung in der Praxis, Band 32, 1. Auflage, 2005 www.akdae.de
- Nigen S, Knowles SR, Shear NH. Drug eruptions: approaching the diagnosis of drug-induced skin diseases. J Drugs Dermatol 2003; 2: 278-99. PubMed
- Fiszenson-Albala F, Auzerie V, Mahe E et al. A 6-month prospective survey of cutaneous drug reactions in a hospital setting. Br J Dermatol 2003; 149: 1018-22. PubMed
- Hunziker T Kunzi UP, Braunschweig S et al. Comprehensive hospital drug monitoring (CHDM): adverse skin reactions, a 20-year survey. Allergy 1997; 52: 388-93. PubMed
- Bigby M, Jick S, Jick H et al. Drug-induced cutaneous reactions. A report from the Boston collaborative drug surveillance program on 15,438 consecutive inpatients, 1975 to 1982. JAMA 1986; 256: 3358-63. Journal of the American Medical Association
- Djien V, Bocquet H, Dupuy A et al. Symptomatology and markers of the severety of erytematous drug eruptions. Ann Dermatol Venereol 1999; 126: 247-50. PubMed
- Altmeyer, P. Dermatologie-Enzyklopädie. DRESS. 2018 www.enzyklopaedie-dermatologie.de
- Arzneimittelkommison der deutschen Ärzteschaft (AKdÄ). Allopurinol ist die häufigste Ursache für Stevens-Johnson-Syndrom und Toxisch epidermale Nekrolyse in Europa und Israel (UAW-News International). 2010. www.akdae.de
- Deutsches Ärzteblatt. Allopurinol: Studie ermittelt Risikofaktoren für schwere Hautreaktionen. Oktober 2019 www.aerzteblatt.de
- Bigby M. Rates of cutaneous reactions to drugs. Arch Dermatol 2001; 137: 765-70. PubMed
- Naisbitt DJ. Drug hypersensitivity reactions in skin: understanding mechanisms and the development of diagnosic and predictive tests. Toxicology 2004; 194: 179-96. PubMed
- Pichler W, Yawalkar N, Schmid S et al. Pathogenesis of drug-induced exanthems. Allergy 2002; 57: 884-93. PubMed
- Altmeyer, P. Dermatologie Enzyklopädie. Pustulose akute generalisierte exanthematische L27.0. Stand 2018. www.enzyklopaedie-dermatologie.de
- Arzneitelegramm AT. EMA EMPFIEHLT SUSPENDIERUNG DER ZULASSUNG VON TETRAZEPAM (MUSARIL, GENERIKA). blitz-a-t 12.04.2013 www.arznei-telegramm.de
- Altmeyer, P. Dermatologie Enzyklopädie. TEN. 2018 www.enzyklopaedie-dermatologie.de
- Schauder, S. Phototoxische Reaktionen der Haut durch Medikamente. Dtsch Arztebl 2005; 102(34-35): A-2314 / B-1953 / C-1851 www.aerzteblatt.de
- Arzneimittelkommission der deutschen Ärzteschaft (AKdÄ). Rote-Hand-Brief zu Hydrochlorothiazid: Risiko von nichtmelanozytärem Hautkrebs (Basalzellkarzinom; Plattenepithelkarzinom der Haut). Drug Safety Mail 2018-62 www.akdae.de
- Cohen AD, Friger M, Sarov B et al. Which intercurrent infections are associated with maculopapular cutaneous drug reactions? Int J Dermatol 2000; 40: 41-4. PubMed
- Fagot JP, Mockenhaupt M, Bouwes-Bavinck JN et al. Nevirapine and the risk of Stevens-Johnson syndrome or toxic epidermal necrolysis. AIDS 2001: 15: 1843-8.
- Edwards IR, Aronson JK. Adverse drug reactions: definitions, diagnosis, and management. Lancet 2000; 356: 1255-9. PubMed
- Neukomm CB, Yawalkar N, Helbling A et al. T-cell reactions to drugs in distinct clinical manifestations of drug allergy. J Investig Allergol Clin Immunol 2001; 11: 275-84. PubMed
- Lynch JP, Renz CL, Laroche D et al. Value of baseline levels in assessing tryptase release. Inflamm Res 2000; 49 (suppl 1): S23-S24.
- Walker T, Jung EG, Bayerl C. Penizillinallergie als ein diagnostisches Problem. Hautarzt 2000; 51: 838-45. PubMed
- Barbaud A, Reichert-Penetrat S, Trechot P et al. The use of skin testing in the investigation of cutaneous adverse drug reactions. Br J Dermatol 1998; 139: 49-58. PubMed
- Bruynzeel DP, Maibach HI. Patch testing in systemic drug eruptions. Clin Dermatol 1997; 15: 479-84. PubMed
- Torres MJ, Blanca M, Fernandez J et al. Diagnosis of immediate allergic reactions to beta-lactam antibiotics. Allergy 2003; 58: 961-72. PubMed
- Aberer W, Bircher A, Romano A et al. Drug provocation testing in the diagnosis of drug hypersensitivity reactions: general considerations. Allergy 2003; 58: 854-63. PubMed
- Altmeyer, P. Dermatologie Enzyklopädie. Arzneimittelreaktion lymphozytäre T88.7. Stand 2018. www.enzyklopaedie-dermatologie.de
- Wolkenstein P, Chosidow O, Flechet L et al. Patch testing in severe cutaneous adverse drug reactions, including Stevens-Johnson syndrome and toxic epidermal necrolysis. Contact Dermatitis 1996; 35: 234-6. PubMed
- Roujeau JC, Kelly JP, Naldi L et al. Medication use and the risk of Stevens-Johnson syndrome or toxic epidermal nercrolysis. N Engl J Med 1995; 333: 1600-7. New England Journal of Medicine
- Stevens AM , Johnson FC. A new eruptive fever associated with stomatitis and ophthalmia. Am J Dis Child 1922; 24: 526-33. PubMed
- Lyell A. Toxic epidermal necrolysis: an eruption resembling scalding of the skin. Br J Dermatol 1956; 68: 355-61. PubMed
- Viard I, Werhly P, Bullani R et al. Inhibition of toxic epidermal necrolysis by blocade of CD95 with human intravenous immunoglobulin. Science 1998; 282: 490-3. PubMed
- Bachot N, Roujeau JC. Differential diagnosis of severe cutaneous drug eruptions. Am J Clin Dermatol 2003; 4: 561-72. PubMed
- Yaylaci S., Demir MV et al. Allopurinol-induced DRESS syndrome. Indian J Pharmacol. 2012 May-Jun; 44(3): 412–414 www.ncbi.nlm.nih.gov
- Almudimeegh A, Rioux C, Ferrand H, et al. Drug reaction with eosinophilia and systemic symptoms or virus reactivation with eosinophilia and systemic symptoms as a manifestation of immune reconstitution inflammatory syndrome in an HIV-infected patient. Br J Dermatol 2014. doi: 10.1111/bjd.13079 DOI
- Trent JT, Kirsner RS, Romanelli P et al. Analysis of intravenous immunoglobulin for the treatment of toxic epidermal necrolysis using SCORTEN: The University of Miami Experience. Arch Dermatol 2003; 39: 39 - 43. 24. Bachot N, Revuz J, Roujeau JC. Intravenous immunoglobulin treatment for Stevens-Johnson syndrome and toxic epidermal necrolysis: a prospective noncomparative study showing no benefit on mortality or progression. Arch Dermatol 2003; 139: 33-6. PubMed
Autor*innen
- Caroline Beier, Dr. med., Fachärztin für Allgemeinmedizin, Hamburg
- Die ursprüngliche Version dieses Artikels basiert auf einem entsprechenden Artikel im norwegischen hausärztlichen Online-Handbuch Norsk Elektronisk Legehåndbok (NEL, https://legehandboka.no/).