Zusammenfassung
- Definition:Durch das Hepatitis-B-Virus (HBV) ausgelöste akute oder chronische Entzündung der Leber. Bei Erwachsenen heilt die Mehrzahl der akuten Infektionen aus, bei bis zu 10 % der Patient*innen kommt es zur Chronifizierung (HBsAg > 6 Monate nachweisbar) mit chronischer Hepatitis oder chronischem Trägerstatus ohne klinische Aktivität.
- Häufigkeit:Prävalenz von akuten oder chronischen Infektionen in Deutschland 0,3 %. Inzidenz von 8.903 Fällen von Hepatitis B in Deutschland im Jahr 2019.
- Symptome:1/3 der Infektionen verläuft asymptomatisch. 1/3 verläuft anikterisch mit Allgemeinsymptomen wie Antriebslosigkeit, Fieber, Appetitlosigkeit, Übelkeit, abdominelle Beschwerden/Durchfall, Gelenkschmerzen. 1/3 der Infektionen mit Entwicklung eines Ikterus.
- Befunde:Ggf. Ikterus, Hepatomegalie, seltener Splenomegalie, Lymphadenopathie, Urtikaria.
- Diagnostik:Neben Anamnese (Risikogruppe?) und klinischem Befund umfasst die Diagnostik klinische Chemie (Transaminasen, Leberfunktionsparameter) und Serologie (initiales Screening mittels HBs-Ag und Anti-HBc).
- Therapie:Bei akuter Hepatitis B nur supportive Therapie (Ausnahme: fulminante Hepatitis). Die chronische Hepatitis B wird mit Interferon-alpha oder Nukleos(t)idanaloga behandelt. Bei Leberversagen Transplantation als Therapieoption.
Allgemeine Informationen
Definition
- Hepatitis B ist eine durch das Hepatitis-B-Virus (HBV) ausgelöste akute oder chronische Entzündung der Leber.1-4
Häufigkeit
Weltweit
- Eine der häufigsten Infektionserkrankungen
- Weltweit etwa 2 Mrd. Menschen mit durchgemachter oder aktueller HBV-Infektion2
- Etwa 257 Mio. Personen mit chronischer HBV-Infektion5
- Vor allem sind die Westpazifik-Region und Afrika betroffen, Europa und Nordamerika haben weltweit die geringste Prävalenz.5
- Geschätzt 887.000 Todesfälle pro Jahr als Folge von fulminanter Hepatitis, Zirrhose und Leberzellkarzinomen5
- Innerhalb Europas etwa 13 Mio. chronisch Infizierte6
- Prävalenz sehr unterschiedlich; zwischen 0,1 % in den Niederlanden und 7 % in der östlichen Türkei
Deutschland
- Prävalenz
- Inzidenz7
- Seit 2017 ist jeder Nachweis vom Hepatitis-B-Virus meldepflichtig (vorher nur akute Infektionen).
- durch Änderung der Erfassung Anstieg der Inzidenz
- Im Jahr 2019 wurden 8.903 neue Fälle von Hepatitis B in Deutschland gemeldet.
- höchste Inzidenz bei Erwachsenen – insbesondere Männern – in der Altersgruppe der 30- bis 39-Jährigen
- Höhere Prävalenzen bei Personen mit Migrationshintergrund2
- Prävalenz in der allgemeinärztlichen Versorgung bis 3,6 %
- Unter Drogenabhängigen Prävalenz zwischen 5 und 33 %2
Ätiologie und Pathogenese
- Hepatitis-B-Virus (HBV) ist ein kleines, teilweise doppelsträngiges DNA-Virus.
- HBV gehört zu den Hepadnaviridae, einer Familie hepatotroper Viren.
- Einteilung von HBV in 9 Genotypen (A–I) mit unterschiedlicher geografischer und ethnischer Verteilung2
- Struktur des HBV-Virus9
- Lipoproteinhülle mit eingelagerten Oberflächenproteinen (HBs-Ag = HBsurface Antigen)
- Die Hülle umgibt das Nukleokapsid mit Hepatitis-B-Kernantigen (HBcAg = Hbcore Antigen).
- Das HBV-Genom kodiert u. a. auch für das HBeAg (HBenvelope Antigen), die lösliche Variante des Core-Proteins, die von infizierten Leberzellen sezerniert wird.
- Ansatzpunkt der antiviralen Behandlung ist die reverse Transkriptase des Virus.10
- Die Hepatitis wird durch die Immunreaktion auf die Infektion verursacht.10
- T-Zell-vermittelte Elimination infizierter Hepatozyten11
- Das Virus selbst ist nicht zytopathogen.
- Chronifizierung der Hepatitis durch ineffektive T-Zell-Antwort11
- Chronische Hepatitis B kann zu Leberzirrhose und hepatozellulären Karzinomen (HCC) führen.
Risiko für chronische Infektionen
- Das Risiko für eine chronische Infektion ist stark davon abhängig, in welchem Alter die Person infiziert wird.2
- Infektion unter der Geburt: 90 %
- Kleinkinder bis zum Alter von 3 Jahren und immunkompromittierte Personen: 30–90 %
- Erwachsene: bis zu 10 %
Ansteckung
Allgemeines
- Der Mensch ist die einzige Ansteckungsquelle.
- Das HBV-Virus ist hochkontagiös und erreicht eine hohe Konzentration im Blut.2
- Ansteckungsgefahr, solange Marker Virusreplikation anzeigen (HBV-DNA, HBsAg, HBeAg).
- In der Frühphase der Infektion und bei HBeAg-positiven Träger*innen wird eine Infektion bereits durch geringste Blutmengen (nahezu jedes Viruspartikel im Blut infektiös) ausgelöst.2
- In der Spätphase der Infektion und bei HBeAg-negativen Träger*innen ist die Infektiosität geringer.2
- Das HBV ist sehr virulent und kann außerhalb des Körpers in getrocknetem Blut länger als 1 Woche überleben.12
- In geringen Konzentrationen ist HBV enthalten in:2
- Tränenflüssigkeit
- Speichel
- Sperma
- Vaginalsekret
- Kolostrum.
- Ansteckung überwiegend durch Schleimhautkontakte (Geschlechtsverkehr) und Blut
Sexuelle Kontakte (hetero- und homosexuelle)
- Erhöhtes Risiko bei:
- Kontakt mit Einreisenden aus Regionen mit hoher HBV-Prävalenz
- Kontakt während Reisen in Ländern mit hoher HBV-Prävalenz
- Kontakt mit Risikogruppen (z. B. Sexarbeiter*innen).
Übertragung durch Blut
- Gemeinsamer Gebrauch von kontaminierten Spritzen bei Drogenabhängigen
- gleichzeitig gehäuftes Auftreten von anderen Infektionen wie Hepatitis C und HIV
- Übertragung durch Nadelstichverletzungen im Gesundheitswesen
- 24 als Berufskrankheit anerkannte Fälle bei 55 Verdachtsmeldungen im Jahr 20132
- Bluttransfusionen
- Im Gegensatz zu früher ist heute das Risiko der Übertragung durch Testung von Blutprodukten nur noch gering: < 1:500.0002
- Hygienemängel in Pflegeeinrichtungen, insbes. bei unsachgemäßer Anwendung von Blutzuckermessgeräten6
- Die epidemiologische Bedeutung von unsachgemäßem Tätowieren/Piercen ist noch unklar.2
Perinatale Infektion
- Übertragung durch HBsAg-positive Mütter
- Das Infektionsrisiko für das Kind liegt bei 70–90 %, falls die Mutter HBsAg-positiv und HBeAg-positiv ist und keine Prophylaxe erhält.13
- Falls HBeAg negativ ist, beträgt das Risiko einer Übertragung auf das Kind 25–30 %.
- Das Risiko für chronische Hepatitis liegt bei 90 % bei perinataler Infektion.
- Infolge liegt das Risiko bei 15–25 % für Zirrhose oder Leberzellkarzinom im Erwachsenenalter.14
- Ein früher Nachweis und Prophylaxe mit Hepatitis-B-Impfung und Hepatitis-B-Immunglobulin ist zu 85–95 % effektiv.13
- Weltweit ist perinatale Infektion die wichtigste Ursache für chronische Hepatitis.4
Medizinische Fachkräfte und Hepatitis B
- Übertragungsrisiko von bis zu 30 % bei Stichverletzung durch infizierte Kanüle15 (siehe auch Artikel Nadelstichverletzungen)
- Nach Stichverletzung Gabe von Hepatitis-B-Immunglobulin und Impfung (falls noch kein Impfschutz vorhanden)16
- Siehe Abschnitt Postexpositionsprophylaxe.
Disponierende Faktoren
- Lebensalter
- chronische Hepatitis bei 90 % der Kinder mit perinataler Infektion
- Risikogruppen, u. a.:
- Drogenabhängige
- Personen mit häufig wechselnden Sexualkontakten
- Reisende in Endemiegebiete
- medizinisches Fachpersonal
- Patient*innen mit Hämodialyse.
Klinischer Verlauf
- Inkubationszeit 45–180 Tage, im Durchschnitt etwa 60–120 Tage2
- Unterschiedlicher klinischer Verlauf nach Infektion2
- 1/3 asymptomatisch
- 1/3 anikterisch verlaufende Erkrankung
- 1/3 ikterischer Verlauf
- Bei bis zu 65 % der Erwachsenen und bei 90 % der Kinder unter 5 Jahren anikterischer Verlauf17
- Siehe auch den Artikel Hepatitis B bei Kindern.
Akute Hepatitis
- Prodromalphasesymptome (3–10 Tage) vor evtl. Ikterus2
- Antriebslosigkeit, Müdigkeit
- Appetitlosigkeit, Übelkeit, Erbrechen
- abdominelle Beschwerden
- Diarrhö
- Fieber
- Gelenkschmerzen
- Urtikaria
- Ikterische Phase
- Bei immunkompetenten Erwachsenen in > 90 % der Fälle Ausheilung der akuten Infektion2
- serologischer Status: HBsAg negativ, Anti-HBc positiv, Anti-HBs positiv1
- Auch nach serologischer Ausheilung verbleibt das Genom in den Hepatozyten und kann unter Immunsuppression reaktiviert werden.2
Chronische Hepatitis/chronische Infektion
- Definition: Nachweis von HBsAg > 6 Monate nach akuter Infektion19
- keine Serokonversion zu Anti-HBs
- Chronifizierung erfolgt bei: 2
- bis zu 10 % der immunkompetenten Erwachsenen
- 90 % der bei Geburt infizierten Kinder
- 30–90 % der immunkompromittierten Erwachsenen.
- Häufig nur geringe (oder keine) Beschwerden
- Die Transaminasen sind unterschiedlich hoch.
- Einteilung der chronischen Infektion in Abhängigkeit von der Virämie1
- Sowohl Viruslast als auch entzündliche Aktivität können im Verlauf variieren.
- Übergang in Zirrhose
- Hepatozelluläres Karzinom (HCC)
- Bei hochvirämischen Träger*innen können auch Immunkomplexerkrankungen auftreten:2
ICPC-2
- D72 Virushepatitis akut
ICD-10
- Nach ICD-10-GM Version 202120
- B16 Akute Virushepatitis B
- B16.0 Akute Virushepatitis B mit Delta-Virus (Begleitinfektion) und mit Coma hepaticum
- B16.1 Akute Virushepatitis B mit Delta-Virus (Begleitinfektion) ohne Coma hepaticum
- B16.2 Akute Virushepatitis B ohne Delta-Virus mit Coma hepaticum
- B16.9 Akute Virushepatitis B ohne Delta-Virus und ohne Coma hepaticum
- B17 Sonstige akute Virushepatitis
- B17.0 Akute Delta-Virus-(Super-)Infektion eines Hepatitis-B-(Virus-) Trägers
- B18 Chronische Virushepatitis
- B18.0 Chronische Virushepatitis B mit Delta-Virus
- B18.1 Chronische Virushepatitis B ohne Delta-Virus
- B16 Akute Virushepatitis B
Diagnostik
Diagnostische Kriterien
- Verdacht auf die Erkrankung durch Anamnese und klinischen Befund
- Serologischer Nachweis einer HBV-Infektion1
- akute Hepatitis B
- HBsAg-positiv und Anti-HBc-IgM hoch positiv
- chronische Hepatitis B
- HBsAg positiv > 6 Monate
- ausgeheilte Hepatitis B
- Nachweis von Anti-HBc und Anti-HBs ≥ 10 IU/l
- HBsAg negativ
- Zustand nach Impfung
- Anti-HBs positiv
- Anti-HBc negativ
- okkulte Hepatitis B
- Nachweis von Anti-HBc (bestätigt)
- HBsAg negativ
- HBV-DNA positiv (≥ 20 IU/ml)
- akute Hepatitis B
- Für die Beurteilung einer möglichen Leberfibrose zur Therapieindikationsstellung kann die transiente Elastografie als nichtinvasives Verfahren eingesetzt werden.1
- Die Leberbiopsie ist hilfreich zur Einstufung der entzündlichen Aktivität.1
Leitlinie: Bei wem soll eine Diagnostik auf HBV-Infektion erfolgen? 1
- Bei allen Schwangeren wird ein Screening empfohlen.
- Aufgrund der schwerwiegenden Folgen einer chronischen HBV-Infektion ist es gerechtfertigt, die Indikation zur HBV-Diagnostik großzügig zu stellen.
- Daher soll eine HBV-Diagnostik erfolgen bei:
- Personen mit erhöhten Leberwerten und/oder klinischen Zeichen einer Hepatitis
- allen Personen mit vorbestehender Erkrankung oder
Immunsuppression, bei denen ein schwerer Verlauf einer Hepatitis B zu erwarten ist.- Patient*innen mit Leberzirrhose/-fibrose
- Patient*innen mit hepatozellulärem Karzinom
- Dialyse-Patient*innen
- HIV-und/oder HCV-infizierte Personen
- Patient*innen mit einer angeborenen Immunschwäche
- Patient*innen vor bzw. während einer immunsuppressiven Therapie, einer Therapie mit B-Zell-depletierenden Antikörpern (Rituximab) oder Chemotherapie
- allen Personen mit erhöhtem Expositionsrisiko für eine Hepatitis B
- Personen mit Migrationshintergrund aus Regionen mit erhöhter HBsAg-Prävalenz
- Familien- oder Haushaltsangehörige, insbesondere Kinder von HBsAg-positiven Müttern und Geschwister sowie Eltern von (aktuell oder ehemals) HBV-infizierten Personen
- Sexualpartner*innen von HBV-infizierten Personen
- medizinisches Personal
- Patient*innen oder Personen in psychiatrischen Einrichtungen, Fürsorgeeinrichtungen für Zerebralgeschädigte oder Verhaltensgestörte, Justizvollzugsanstalten
- Personen mit häufig wechselnden Sexualkontakten
- aktive und ehemalige i. v. Drogenbenutzer*innen
- Empfänger*innen von Knochenmarks- oder Organtransplantaten vor und nach Transplantation
- Blut-, Gewebe-, Samen- und Organspender*innen.
- Bei Personen der o. g. Risikogruppen, die HBsAg- und Anti-HBc-negativ sind und über keinen ausreichenden Impfschutz verfügen, soll eine Impfung angeboten werden
- Cave: Impfindikation in Schwangerschaft soll streng geprüft werden!
Differenzialdiagnosen
- Hepatitis A
- Hepatitis C
- Hepatitis D
- Hepatitis E
- EBV-Hepatitis
- CMV-Hepatitis
- Bakterielle Infektionen
- Toxische/medikamentöse Hepatitis
- Autoimmunhepatitis
Anamnese
- Allgemeinsymptome?
- Antriebslosigkeit, Müdigkeit
- Appetitlosigkeit
- Übelkeit, Erbrechen
- Fieber
- Gelenkschmerzen
- Abdominelle Beschwerden, Diarrhö?
- Dunkler Urin?
- Gelbfärbung der Skleren?
- Fernreisen?
- I. v. Drogen?
- Häufig wechselnde Sexualkontakte?
- Infizierte in Familie oder näherem Umfeld?
- Dialyse-Patient*in?
- Essen von Wildschweinfleisch?
- häufig mit Hepatitis E infiziert (Differenzialdiagnose)
- Berufsanamnese
- Tätigkeit im Gesundheitswesen?
- Tätigkeit in Pflegeeinrichtung?
Klinische Untersuchung
- Mögliche Befunde umfassen:
- Ikterus
- Hepatomegalie
- Splenomegalie
- Lymphadenopathie
- Urtikaria.
Ergänzende Untersuchungen in der Hausarztpraxis
Allgemeine Laboruntersuchungen
- Siehe Labortests im Leitlinienkasten.
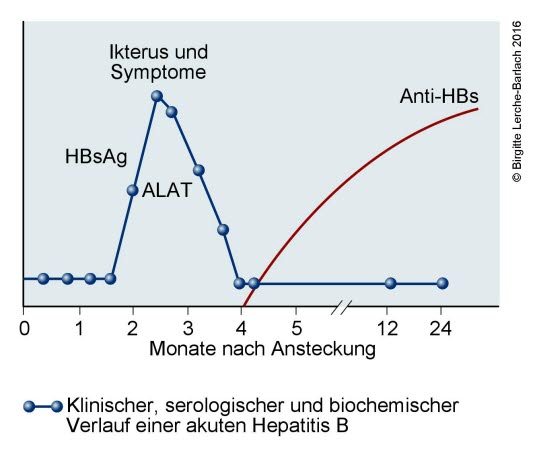
Hepatitis-B-Verlaufskurve
Bedeutung der serologischen Marker
- HBsAg
- Weist das Vorhandensein des Virus und somit Ansteckungsgefahr nach.
- Kommt sowohl bei akuter Infektion als auch bei chronischem Trägerstatus vor.
- HBeAg
- Parameter für aktive Virusreplikation
- Nachweis deutet auf hohes Ansteckungsrisiko hin.
- Anti-HBs
- Zeigt eine durchlaufene Infektion oder Impfung an und damit Immunität.
- Anti-HBe
- Zeigt bei chronischen Träger*innen eine leichtere Form chronischer Hepatitis und eine geringere Ansteckungsgefahr im Vergleich zu HBeAg-positiven Patient*innen an.
- Anti-HBc
- IgM weist auf eine Infektion in den letzten 6 Monaten hin.
- IgG zeigt eine frühere Infektion an.
- Bleibt nach Infektion lebenslang positiv.
- Positives HBsAg und Anti-HBc-IgG weisen auf eine chronische HBV-Infektion hin.
- HBV-DNA
- Zeigt aktive Replikation an und gibt quantitativ die Viruslast an.
- Ist zur Überwachung der Behandlung einer HBV-Infektion nützlich.
- Andere Viren?
Leitlinie: Diagnostik1
Serologische Diagnostik bei V. a. akute HBV-Infektion
- Initiales Screening
- HBsAg
- Anti-HBc
- Falls HBsAg und Anti-HBc positiv
- HBe-Ag, Anti-HBe (Virusaktivität)
- Anti-HBc-IgM (DD akute vs. chronische Hepatitis)
- ggfs. HBV-DNA quantitativ
- Falls HBsAg isoliert positiv
- HBsAg-Bestätigungstest (Ausschluss falsch positiver Reaktion)
- falls bestätigt positiv: HBe-Ag, HBV-DNA (DD akute/okkulte HBV-Infektion)
- nach 2–4 Wochen Kontrolle: HBs-Ag, Anti-HBc, Anti-HBc-IgM
- Falls Anti-HBc isoliert positiv
- Anti-HBs
- falls Anti-HBs positiv: durchgemachte HBV-Infektion mit klinischer Ausheilung; evtl. Kontrolle im Verlauf bis Anti-HBs ≥ 10 IU/l
- falls Anti-HBs negativ oder ALT (= GPT) erhöht: Anti-HBc-IgM, HBV-DNA quantitativ; DD: frische HBV-Infektion, HBV-Escape-Variante (Mutation, die durch Test-AK nicht erkannt wird), „Anti-HBc only“ (keine Hepatitis, aber mögliche*r Überträger*in, mögliche Reaktivierung)
- Anti-HBs
Weitere Diagnostik bei Erstdiagnose
- Bei Erstdiagnose einer HBV-Infektion sollen zusätzlich folgende Maßnahmen durchgeführt werden:
- Anamnese (inkl. Risikofaktoren, Familien-, Partneranamnese)
- körperliche Untersuchung
- Ausschluss einer Koinfektion mit HCV, HDV und HIV
- Hepatitis-A-Immunstatus (Frage Impfung)
- klinisch-chemische Labortests
- Leberentzündungs- und Lebersynthese-Parameter, Gesamtbilirubin, Vollblutbild, Gerinnungsstatus
- Ultraschall des Abdomens
- Raumforderungen in der Leber und Begleiterkrankungen (z. B. Gallensteine, Fettleber)
Diagnostik bei Spezialist*innen
HBV-Genotypisierung
- Bei Therapie mit Interferon oder Immunmodulatoren wird vor der Therapie bzw. zum Therapiemonitoring eine Genotypisierung empfohlen.1
Leberbiopsie
- Goldstandard bei der chronischen Hepatitis für die Bestimmung der entzündlichen Aktivität (Grading) und des Fibroseausmaßes (Staging)1
- Maßgebliche Grundlage der Entscheidung für eine Leberbiopsie ist die Frage, ob das diagnostische Ergebnis der Biopsie für das therapeutische Vorgehen von Bedeutung ist.
Transiente Elastografie
- Für die Beurteilung der Leberfibrose sollte die transiente Elastografie anderen nichtinvasiven Verfahren vorgezogen werden.1
- Dient auch zur Erfassung einer Fibroseverbesserung während oder nach einer antiviralen Therapie.
Indikationen zur Klinikeinweisung/Überweisung
- Bei asymptomatischen Patient*innen nicht erforderlich (Mehrheit der Betroffenen)
- Bei akuter, ikterischer Hepatitis stationäre Einweisung
- Therapie einer chronischen Hepatitis durch Spezialist*in (Gastroenterologie)
Therapie
Therapieziele
Akute Hepatitis B
- Symptomlinderung, da bei Erwachsenen überwiegend Spontanheilung1
Chronische Hepatitis B1
- Senkung von Morbidität und Mortalität
- Verbesserung und, idealerweise, Reversion einer Leberfibrose oder Zirrhose
- Senkung von HBV-DNA unter die Nachweisgrenze
- Serokonversion von HBs-Ag zu Anti-HBs
- Vorbeugung einer Ansteckung weiterer Personen
- Normalisierung der Transaminasen
Allgemeines zur Therapie
Akute Hepatitis B
- Bei Erwachsenen besteht aufgrund der hohen Rate an Spontanheilungen in der Regel keine Therapieindikation für die aktuell verfügbaren antiviralen Medikamente.1
- Ausnahme bei fulminanter Hepatitis: Therapie mit Nukleos(t)idanalogon und frühzeitige Betreuung in Lebertransplantationszentrum
Chronische Hepatitis B
- Patient*innen mit chronischer Hepatitis-B-Infektion sind grundsätzlich Kandidat*innen für eine antivirale Therapie.1
- Zur Indikationsstellung werden herangezogen:1
- Viruslast: > 2.000 IU/ml
- Entzündungs- und Fibrosestatus in der Biopsie bzw. Leberelastografie
- ALT-Aktivität im Serum (wiederholt erhöht).
- Eine sichere Indikation zur antiviralen Behandlung besteht bei Patient*innen mit chronischer Hepatitis B, die1
- eine Virusreplikation von ≥ 2.000 IU/ml zeigen und
- eine entzündliche Aktivität mit wiederholt erhöhter Transaminasen-Aktivität im Serum aufweisen und
- unter Berücksichtigung von Lebensalter und Begleiterkrankungen ein Risiko haben, eine Leberzirrhose und deren Komplikationen wie insbesondere ein HCC zu entwickeln.
Empfehlungen für Patient*innen
- Alkoholkarenz
- Spezielle Diäten sind ohne Einfluss auf den Krankheitsverlauf.2
- In der akuten Krankheitsphase sind kohlenhydratreiche und fettarme Kost besser verträglich für die Patient*innen.2
- Ratschläge zur Ansteckungsprophylaxe im Verhältnis zur Umgebung
- Information über Prophylaxe und Impfung bei gefährdeten Gruppen
Medikamentöse Therapie
Interferon-alpha
- Bei der Therapieauswahl sollte geprüft werden, ob eine Therapie mit pegyliertem (PEG-)Interferon möglich und sinnvoll ist.1
- HBeAg-Serokonversion und HBsAg-Verlust werden mit einer PEG-Interferon basierten Therapie häufiger erreicht als mit einer gleichlangen (meist 48-wöchigen) Nukleos(t)idanaloga-Therapie.
- PEG-Interferon-alpha ist gegenüber Standard-Interferon-alpha vorzuziehen.1
- gleiche Wirksamkeit
- patientenfreundlichere Applikation (1 x wöchentlich)
- Indikation21
- Bei Patient*innen mit chronischer Hepatitis B und kompensierter Lebererkrankung (max. Child-A-Zirrhose)
- mit Nachweis viraler Replikation, erhöhten ALT-Werten und (histologisch) verifizierter Leberentzündung und/oder -fibrose
- Dosierung21
- 180 μg 1 x wöchentlich subkutan über 48 Wochen
- Kontraindikationen, u. a.:21
- Schwangerschaft und Stillzeit
- schwere Dysfunktion der Leber oder dekompensierte Leberzirrhose
- Leberzirrhose Child-Pugh B und C
- Neugeborene und Kleinkinder bis zu 3 Jahren, da das Arzneimittel Benzylalkohol enthält.
- Kinder und Jugendliche mit gegenwärtigen schwerwiegenden psychiatrischen Erkrankungen oder solchen in der Vorgeschichte
- Wirkmechanismus
- kombinierter Wirkungsmechanismus: immunmodulierend, antiproliferativ und direkt antiviral
- Nebenwirkungen, u. a.:21
- influenzaähnliche Symptome, Thrombozytopenie, Leukopenie, Depression, Gewichtsabnahme, Ausschlag, Husten, Hypo- oder Hyperthyreose, Tinnitus, Autoantikörperbildung und Retinopathie.
- Cave: Peginterferon alfa-2a wird von der Herstellerfirma nicht mehr produziert und die Restbestände werden in Deutschland bis zum Jahresende 2022 verfügbar sein. Rechtzeitig dazu soll ein Addendum der Leitlinie veröffentlich werden.1
Nukleos(t)idanaloga (NA)
- Therapie mit NA indiziert bei:1
- dekompensierter Zirrhose (CHILD B und C)
- behandlungsbedürftigen Patient*innen mit eingeschränkter Nierenfunktion und Dialyse-Patient*innen
- Patient*innen mit extrahepatischen Manifestationen einer Hepatitis-B-Virus-Infektion, z. B. Autoimmunerkrankungen
- Patient*innen mit HCC und positiver HBV-DNA
- behandlungsbedürftigen Patientinnen in Schwangerschaft und Stillzeit
- Prophylaxe einer HBV-Reaktivierung, z. B. unter Chemotherapie.
- Bei Therapie mit NA sollen Entecavir (Nucleosidanalogon) oder Tenofovir (Nucleotidanalogon) bevorzugt werden.1
- Wirkmechanismus
- Antimetabolite, die von der reversen Transkriptase des Virus anstelle der natürlichen Nukleotide eingebaut werden und zum Kettenabbruch der DNA führen.
- Regelmäßige Kontrolle der HBV-DNA alle 3 Monate bzw. alle 6 Monate bei stabilem Verlauf für:2
- Kontrolle der Therapieadhärenz
- Erkennung von Resistenzentwicklung.
- Therapiedauer
- Definition von Therapieansprechen1
- Optimales Ansprechen: HBV-DNA liegt unterhalb der Nachweisgrenze oder nicht quantifizierbar.
- Partielles Ansprechen: HBV-DNA fällt nicht kontinuierlich ab und Plateau > 2.000 IU/ml nach 96 Wochen.
- Nichtansprechen (Nonresponse): fehlender Abfall > 1 log nach 6 Monaten antiviraler Therapie
- Resistenz: nach primärem Ansprechen unter laufender Behandlung mit NA tritt ein bestätigter Anstieg der HBV-DNA ≥ 1 log-Stufe über dem Nadir auf.
- Nukleos(t)idanaloga haben im Vergleich zu Interferon weniger Nebenwirkungen.22
Lebertransplantation
- Bei Leberversagen Transplantation (LTX) als Therapieoption
- Bei Hepatitis B dient die LTX neben der Behandlung des Leberversagens auch der Infektsanierung.23
- Etwa 10 % der LTX werden wegen Leberversagens bei Hepatitis B durchgeführt.24
Meldepflicht
- Gemäß § 6 Abs. 1 Satz 1 Nr. 1 Buchstabe e IfSG besteht eine namentliche Meldepflicht für den Krankheitsverdacht, die Erkrankung sowie den Tod an akuter Virushepatitis.25
Anerkennung als Berufskrankheit
- Tritt Hepatitis B im Zusammenhang mit der beruflichen Tätigkeit auf, kann diese Erkrankung als Berufskrankheit anerkannt werden.26
- Zuständig hierfür sind die gesetzlichen Unfallversicherungsträger.
- Der Verdacht auf eine Berufskrankheit muss dort gemeldet werden (Meldebogen27).
- Es wird eine ausführliche Arbeits- und Gefährdungsanamnese erhoben, und ein Gutachten entscheidet über die Anerkennung als Berufskrankheit.
- Dann können bestimmte Maßnahmen auf Kosten der GUV durchgeführt werden:
- spezielle therapeutische Maßnahmen
- Minderung der Erwerbsfähigkeit bis zur Zahlung einer Rente.28
Impfung/Prävention
Präexpositionsprophylaxe
- Siehe auch TrainAMed Impfen (Uni Freiburg).
Impfempfehlung vom Robert Koch-Institut
- Eine effektive Prophylaxe ist nur durch aktive Impfung möglich.2
- Es steht ein sicherer und wirksamer Impfstoff zur Verfügung, der bei Immungesunden einen > 90-prozentigen Schutz vor Hepatitis B bietet.1
- Das Robert Koch-Institut spricht daher folgende Impfempfehlungen aus: 29-32
- Die Hepatitis-B-Impfung wird von der STIKO als Standardimpfung für alle Kinder sowie im Erwachsenenalter für besonders gefährdete Personengruppen empfohlen.
- Siehe Risikogruppen im Leitlinien-Kasten.
- Seit Juni 2020 Empfehlung zum reduzierten 2+1-Schema (vorher 3+1-Schema) einer Sechsfach-Impfung mit den Zielen:
- Impfplan vereinfachen.
- Arzttermine für Säugling und Eltern einsparen und
- so die zeitgerechte und vollständige Umsetzung der Sechsfachimpfungen für Ärzt*innen und Eltern erleichtern.
- Grundimmunisierung
- reife Neugeborene
- Beginn der Grundimmunisierung im Alter von 2 Monaten
- Für die 6-fach-Impfung bei der gegen Diphtherie, Tetanus, Pertussis, Polio, Haemophilus influenzae Typ b und Hepatitis B immunisiert wird, empfiehlt die STIKO ein 2+1-Schema mit Impfungen im Alter von 2, 4 und 11 Monaten.
- Um einen Langzeitschutz aufzubauen, ist es besonders wichtig, den Abstand von 6 Monaten zwischen der 2. und der 3. Impfung nicht zu unterschreiten.
- Frühgeborene (vor der 37. Schwangerschaftswoche)
- aufgrund des noch nicht ausgereiften Immunsystems 3+1-Impfschema, mit 4 Impfstoffdosen im Alter von 2, 3, 4 und 11 Monaten
- Erwachsene
- Impfung mit 3 Dosen nach dem Schema 0–1–6 Monate
- reife Neugeborene
- Auffrischimpfung
- bei Kindern und Jugendlichen nicht erforderlich
- nur für Personen mit erhöhtem Risiko für Infektion (z. B. Arbeit im Gesundheitswesen)
- In diesem Fall serologische Kontrolle 4–8 Wochen nach der Impfung
- Als erfolgreiche Grundimmunisierung wird hierbei das Erreichen eines Anti-HBs-Wertes von ≥ 100 IE/l 4–8 Wochen nach der letzten Impfstoffdosis definiert.
- Bei Low-Respondern (Anti-HBs 10–99 IE/l) weitere Impfstoffdosis und Kontrolle nach 4–8 Wochen; ggf. weitere Impfstoffdosen und Kontrolle30
- bei Non-Respondern (Anti-HBs < 10 IE/l) Bestimmung von HBsAg und Anti-HBc zum Ausschluss einer chronischen Infektion; falls beide negativ, Vorgehen wie bei Low-Respondern30
- Anschließend sind im Allgemeinen keine weiteren Auffrischimpfungen oder Anti-HBs-Testungen erforderlich.
- Auch nach späterem Absinken des Anti-HBs-Spiegels unter 100 IE/l wird aufgrund des immunologischen Gedächtnisses in der Regel von einem weiterbestehenden Impfschutz ausgegangen.
- Ein Kontakt mit dem Hepatitis-B-Virus führt zu einem schnellen Antikörperanstieg, der vor Erkrankung schützt.
- Ausnahmen
- jährliche Anti-HBs-Kontrollen bei Personen mit Immundefizienz
- Anti-HBs-Kontrolle 10 Jahre nach letzter Impfung bei Personen mit besonders hohem individuellem Expositionsrisiko
- Auffrischimpfung bei diesen beiden Personengruppen bei Anti-HBs-Wert < 100 IE/l
- Eine routinemäßige serologische Testung zum Ausschluss einer HBV-Infektion vor der Impfung ist nicht nötig.30
- Impfung gefahrlos durchführbar, aber wirkungslos
- Impfung von medizinischem Fachpersonal in Hochrisikoumgebungen sowohl effektiv als auch sicher33
Als Reiseimpfung31,34
- Indikationen
- Reiseunabhängig erhöhtes Risiko? (siehe Risikogruppen im Leitlinienkasten)
- bei Reise in hoch- und mittelendemische Regionen und einem oder mehreren Risikofaktoren, z. B.:
- Reisedauer > 4 Wochen, auch kumuliert über mehrere Reisen
- geplante ungeschützte sexuelle Kontakte mit Fremden, z. B. Sextourismus
- absehbarer Kontakt zum Gesundheitswesen des Ziellandes für invasive Maßnahmen (z. B. Injektionen, zahnmedizinische Eingriffe, Endoskopien, Operationen) oder für den Erhalt von Blutprodukten
- Tätigkeit im Reiseland mit hohem Verletzungsrisiko.
- Verkürztes Impfschema vor Reiseantritt für Erwachsene
- Falls ein besonders rascher Schutz gegen Hepatitis B gewünscht wird (z. B. vor einer kurzfristigen Reise), kann nach einem verkürzten Impfschema geimpft werden, z. B. an den Tagen 0–7–21 (maßgeblich sind die Angaben in der Fachinformation des jeweiligen Impfstoffs).
- Zum Aufbau eines langfristigen Impfschutzes wird in diesen Fällen eine zusätzliche 4. Impfdosis nach 12 Monaten empfohlen.
- Keine routinemäßige serologische Kontrolle nach erfolgter Grundimmunisierung
- Impferfolgskontrolle nur in Einzelfällen entsprechend des individuellen Expositionsrisikos
Postexpositionsprophylaxe (PEP)
Leitlinie: Allgemeine Sofortmaßnahmen bei Stich- und Schnittverletzungen35
- Mind. 1 min bluten lassen, ggf. Blutung provozieren, desinfizieren mit Ethanol Vol. > 82 % in Kombination mit PVP-Jod.
- Spritzer von Blut/Körperflüssigkeit auf intakter Haut: Desinfizieren mit Hautantiseptikum (Ethanol Vol. > 82 %), anschließend reinigen mit Wasser und Seife.
- Schleimhautspritzer (Mund, Nase, Augen): Reichlich spülen mit Wasser oder physiologischer Flüssigkeit (Aqua dest. oder NaCl 0,9 % steril) oder 1:4 verdünnter wässriger Jodlösung.
- Kontakt von Blut/Körperflüssigkeit bei lädierter Haut: grobes Entfernen von Blut/Körperflüssigkeit, desinfizieren mit Ethanol Vol. > 82 % plus PVP-Jod.
Bei Neugeborenen von HBsAg-positiven Müttern32
- Immunisierung innerhalb von 12 Stunden post partum bei Neugeborenen HBsAg-positiver Mütter (und Müttern mit unbekanntem HBs-Ag-Status)
- aktive Impfung und
- passiv mit Hepatitis-B-Immunglobulin an unterschiedlichen Extremitäten
- 2 Impfschemata können zur Grundimmunisierung mit einem monovalenten Impfstoff zur Anwendung kommen:
- 0–1–2–12 Monate oder
- 0–1–6 Monate, wobei das erste Schema eine raschere Immunantwort bewirkt.
- Kommt das 0–1–2–12-Monate-Schema zur Anwendung, können die Impfstoffdosen im Alter von 2 und 12 Monaten mit einem hexavalenten Impfstoff verabreicht werden.
- Frühgeborene sollten immer nach dem 0–1–2–12-Monate-Schema geimpft werden.
- Nach Abschluss der Grundimmunisierung des Neugeborenen einer HBsAg-positiven Mutter ist eine serologische Antikörperbestimmung beim Säugling erforderlich.
- 4–8 Wochen nach der letzten Impfstoffdosis der Grundimmunisierung Bestimmung der Hepatitis-B-Marker HBsAg, Anti-HBs und Anti-HBc
Empfehlungen der STIKO für die PEP
- Prophylaxe erforderlich nach:2
- Verletzungen mit erwiesenermaßen oder möglicherweise kontaminierten Gegenständen
- Blutkontakt mit Schleimhaut oder nichtintakter Haut.
- Abhängig von der Indexperson und dem Impfstatus der verletzten Person gibt die STIKO u. g. Empfehlungen für die PEP. 32
1. Bestimmung des HBsAg-Status der Indexpatient*in
- Indexpatient*in HBsAg-negativ
- bei nichtgeimpfter oder ungeimpfter exponierter Person Durchführung bzw. Komplettierung der Grundimmunisierung
- Indexpatient*in HBsAg positiv
- Vorgehen abhängig vom Impfstatus der exponierten Person (s. u.)
- Indexpatient*in mit unbekanntem HBs-Ag-Status
- Bestimmung des HBsAg-Status bei Indexpatient*in innerhalb von 48 Stunden
- abhängig vom Testergebnis weiteres Vorgehen wie bei HBs-Ag-positiven bzw. -negativen Indexpatient*innen
- falls Test innerhalb 48 Stunden nicht möglich, Vorgehen wie bei HBs-Ag-positiven Indexpatient*innen
2. Hepatitis-B-Prophylaxe abhängig vom aktuellen Anti-HBs-Wert der exponierten Person
- Anti-HBs ≥ 100 IE/l
- keine Maßnahmen
- Anti-HBs 10–99 IE/l
- Impfung
- kein Immunglobulin
- Anti-HBs < 10 IE/l (oder nicht innerhalb von 48 Stunden bestimmbar) und Anti-HBs ≥ 100 IE/l zu früherem Zeitpunkt
- Impfung
- kein Immunglobulin
- Anti-HBs < 10 IE/l (oder nicht innerhalb von 48 Stunden bestimmbar) und Anti-HBs nie ≥ 100 IE/l zu früherem Zeitpunkt oder unbekannt
- Impfung
- Gabe von Imunglobulin
- Ungeimpfte und bekannte „Non-Responder“ (d. h. dauerhaft Anti-HBs < 10 IE/l)
- Impfung
- Gabe von Immunglobulin
- Bei ungeimpften Personen sollten 2 weitere Impfstoffdosen (im Anschluss an die Erstimpfung) nach dem konventionellen Impfschema gegeben werden.
Tätigkeitseinschränkungen für Infizierte
- Die deutsche Leitlinie empfiehlt folgende Tätigkeitseinschränkungen für Infizierte, die im Gesundheitswesen arbeiten:1
- Bei HBV-DNA-Konzentrationen < 200 IU/ml sind keine Einschränkungen der Tätigkeit und keine zusätzlichen Sicherheitsmaßnahmen erforderlich.
- Kontrollen der HBV-DNA sollen alle 3 Monate durchgeführt werden.
- Bei Werten zwischen 200 und 20.000 IU/ml soll eine individuelle Bewertung des Übertragungsrisikos je nach Tätigkeit erfolgen und ggf. Maßnahmen zur Senkung der Übertragungsgefahr ergriffen werden.
- Konstant hohe HBV-DNA-Konzentrationen von > 20.000 IU/ml sind mit einer übertragungsträchtigen Tätigkeit gemäß Empfehlung der Deutschen Vereinigung zur Bekämpfung der Viruskrankheiten (DVV) nicht vereinbar.
- Bei HBV-DNA-Konzentrationen < 200 IU/ml sind keine Einschränkungen der Tätigkeit und keine zusätzlichen Sicherheitsmaßnahmen erforderlich.
Hepatitis B und Gemeinschaftseinrichtungen (z. B. Kindergärten, Schule, Pflegeeinrichtungen)
- Für Kinder mit Hepatitis B spricht das RKI folgende Empfehlungen aus:2
- Prinzipiell Besuch bzw. Tätigkeit durch HBs-Ag-Träger*in möglich
- unter Beachtung der Hygienemaßnahmen
- Sofern von der Person keine Gefährdung ausgeht.
- Eine aktive Impfung wird Gruppenmitgliedern und Beschäftigten empfohlen.
- Individuelle Entscheidung durch das Gesundheitsamt bei Kindern mit:
- aggressivem Verhalten
- Immunsupression
- Blutungsneigung
- entzündlichen Hauterkrankungen.
Verlauf, Komplikationen und Prognose
Verlauf
- Das Alter bei Ansteckung ist mitentscheidend für den zu erwartenden Verlauf der Infektion.4
- Infizierte Säuglinge und Kinder haben ein hohes Risiko, eine chronische Infektion zu entwickeln – epidemiologische Situation vor allem in Entwicklungsländern.
- Eine Infektion bei Jugendlichen und Erwachsenen geht einher mit einem niedrigen Risiko für eine chronische Infektion – epidemiologische Situation vor allem in westlichen Ländern.
- Bei 70 % der Erwachsenen und bei 90 % der Kinder unter 5 Jahren ist der Verlauf anikterisch.31,36
- Klinischer Verlauf nach Infektion bei Erwachsenen2
- 1/3 asymptomatisch
- 1/3 anikterisch verlaufende Erkrankung
- 1/3 ikterischer Verlauf
- Höhepunkt nach 1–2 Wochen und dann Rückbildung innerhalb von 2–4 Wochen
- 0,5–1 % fulminante Hepatitiden
- häufiger ab einem Alter von 40 Jahren, bei Schwangeren und bei Neugeborenen infizierter Mütter31
- Andere Wirtsfaktoren abgesehen vom Alter
- Immunstatus
- Infektionen mit anderen hepatotropen Viren
- Alkoholkonsum
Komplikationen
- Fulminante Hepatitis 0,5–1 %
- insbesondere bei Superinfektion mit Hepatitis D
- Chronische Infektion
- definiert als HBs-Ag-Nachweis > 6 Monate
- Chronische Hepatitis
- chronische Infektion mit Leberzellschädigung: Nachweis laborchemisch und/oder histologisch1
- Übergang in Zirrhose
- Hepatozelluläres Karzinom (HCC)
- weltweit über 300.000 neue Fälle pro Jahr als Folge einer chronischen Hepatitis B
- Positives HBsAg (RR = 9,6) und positives HBeAg (RR = 60) sind mit deutlich erhöhtem Risiko für die Entwicklung eines HCC verbunden.37
- Erhöhter Serum-HBV-DNA-Spiegel (≥ 10.000 Kopien/ml) ist ein Prädiktor für die Entwicklung eines HCC, unabhängig von HBeAg, Serum-GPT und Leberzirrhose.38
Prognose
- Morbidität und Mortalität sind assoziiert mit der Persistenz der Virusreplikation und der Progression zu Zirrhose und/oder HCC.39
- Von den Personen mit chronischem Trägerstatus entwickeln ca. 30 % über Jahre eine Zirrhose mit den Folgerisiken Leberinsuffizienz, portale Hypertension und HCC.40
- Das Risiko für diese Komplikationen ist besonders bei einer andauernden Virusreplikation hoch (erhöhte HBV-DNA und positives HBeAg).
- Serokonversion bei > 90 % der infizierten Erwachsenen, bei Säuglingen < 10 %31
Verlaufskontrolle
- Verlaufskontrolle einer akuten HBV-Infektion1
- Transaminasenaktivität und Prothrombinzeit nach klinischem Bedarf und Verlauf (cave: fulminantes Leberversagen!) wiederholen bis zur Normalisierung.
- HBsAg/Anti-HBs alle 3–12 Monate bis zur Anti-HBs-Serokonversion
- Immunität kann bei Anti-HBs > 10 IU/l angenommen werden, wenn
HBsAg negativ ist. - Bei HBsAg negativ/Anti-HBs < 10 IU/l: HBV-DNA; Kontrolle nach
12 Monaten
- Verlaufskontrolle bei chronischer HBV-Infektion1
- Bei allen Patient*innen im 1. Jahr mind. 3 ×, anschließend je nach klinischer Aktivität der Erkrankung alle 3–12 Monate Transaminasenaktivität und HBV-DNA quantitativ bestimmen.
- bei Vorliegen einer Leberfibrose oder -zirrhose Kontrolle alle 6 Monate
- Ultraschall des Abdomens und ggf. AFP zur HCC-Surveillance bei erhöhtem HCC-Risiko
- Bei allen Patient*innen im 1. Jahr mind. 3 ×, anschließend je nach klinischer Aktivität der Erkrankung alle 3–12 Monate Transaminasenaktivität und HBV-DNA quantitativ bestimmen.
- Verlaufskontrolle bei chronischer Hepatitis B alle 6 Monate1
- klinische Chemie (Leberentzündungs-und Lebersynthese-Parameter, Blutbild, Prothrombinzeit)
- HBV-DNA (quantitativ)
- HBeAg (sofern initial positiv), wenn negativ: Anti-HBe
- HBsAg (ggf. quantitativ), wenn negativ: Anti-HBs (Frage: Ausheilung?)
- Screening auf hepatozelluläres Karzinom1
- bei erhöhtem HCC-Risiko: alle 6 Monate Ultraschall durch erfahrene/n Untersucher*in
- hohes Risiko mit dringender Screening-Empfehlung bei Leberzirrhose
- mäßig hohes Risiko mit Screening-Empfehlung u. a. bei Leberfibrose, positiver Familienanamnese für HCC, HBV-DNA > 2.000 IU/ml, erhöhten Transaminasen, Männern > 40 Jahre, zusätzlichen hepatotoxischen Faktoren wie Alkoholabusus
- Kontrollintervall kann je nach Risikoabschätzung auf 12 Monate verlängert werden. Optional kann zusätzlich zum Ultraschall eine AFP-Bestimmung erfolgen.
- bei erhöhtem HCC-Risiko: alle 6 Monate Ultraschall durch erfahrene/n Untersucher*in
Illustrationen

Hepatitis-B-Verlaufskurve
Patienteninformationen
Patienteninformationen in Deximed
Video
- TrainAMed Impfen (Universität Freiburg)
Quellen
Leitlinien
- Deutsche Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten. Prophylaxe, Diagnostik und Therapie der Hepatitis-B-Virusinfektion. AWMF-Leitlinie Nr. 021–011. S3, Stand 2021. www.awmf.org
- Arbeitskreis „Krankenhaus- & Praxishygiene“ der AWMF. Prävention blutübertragbarer Virusinfektionen. AWMF-Leitlinie Nr. 029–026. S1, Stand 2017. www.awmf.org
Literatur
- Deutsche Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten. Prophylaxe, Diagnostik und Therapie der Hepatitis-B-Virusinfektion. S3, AWMF-Leitlinie 021–011. Stand 2021. www.awmf.org
- Robert Koch-Institut. Hepatitis B und D, RKI-Ratgeber für Ärzte. Stand 2016. Letzter Zugriff 04.03.2021. www.rki.de
- Lok AS, McMahon BJ. Chronic hepatitis B: update 2009. Hepatology. 2009;50:661-662. PubMed
- Lai CL, Ratziu V, Yuen M-F, Poynard T. Viral hepatitis B. Lancet 2003; 362: 2089-94. PubMed
- World Health Organization. Hepatitis B fact sheet. Stand Juli 2020. www.who.int
- Robert Koch-Institut. Epidemiologische Bulletin Nr. 29: Virushepatitis B und D im Jahr 2014. www.rki.de
- Robert Koch-Institut. Infektionsepidemiologisches Jahrbuch meldepflichtiger Krankheiten für 2019. www.rki.de
- Chen JD, Liu CJ, Lee PH, Chen PJ, Lai MY, Kao JH, Chen DS. Hepatitis B genotypes correlate with tumor recurrence after curative resection of hepatocellular carcinoma. Clin Gastroenterol Hepatol 2004; 2: 64-71. PubMed
- Hildt E, Bleifuß E, Brandenburg B. Molekulare Virologie am Beispiel des Hepatitis-B-Virus. Bundesgesundheitsbl - Gesundheitsforsch - Gesundheitsschutz 2003; 46: 508-513. doi:10.1007/s00103-003-0615-4 DOI
- Baumert TF, Thimme R, von Weizsücker F. Pathogenesis of hepatitis B virus infection. World J Gastroenterol 2007;13: 82-90. PubMed
- Chisari F, Isogawa M, Wieland S. Pathogenesis of Hepatitis B Virus Infection. Pathol Biol 2010; 58: 258–266. doi:10.1016/j.patbio.2009.11.001 DOI
- Ott MJ, Aruda M. Hepatitis B vaccine. J Pediatr Health Care 1999;13:211-6. PubMed
- Lam N-CV, Gotsch PB, Langan RC. Caring for pregnant women and newborns with hepatitis B or C. Am Fam Physician 2010; 82: 1225-9. europepmc.org
- Airoldi J, Berghella V. Hepatitis C and pregnancy. Obstet Gynecol Surv 2006; 61: 666-72. PubMed
- Sarrazin U, Brodt HR, Sarrazin C, et al. Prophylaxe gegenüber HBV, HCV und HIV nach beruflicher Exposition. Dtsch Arztebl 2005; 102(33): A-2234. www.aerzteblatt.de
- Wilkins T, Zimmermann D, Schade RR. Hepatitis B: diagnosis and treatment. Am Fam Physician 2010; 81: 965-72. www.aafp.org
- Lin KW, Kirchner JT. Hepatitis B. Am Fam Physician 2004; 69: 75-82. PubMed
- Aggarwal R, Ranjan P. Preventing and treating hepatitis B infection. BMJ 2004; 329: 1080-6. PubMed
- WHO. Guidelines for the prevention, care and treatment of persons with chronic hepatitis B infection. March 2015. apps.who.int
- Deutsches Institut für Medizinische Dokumentation und Information (DIMDI): ICD-10-GM Version 2021. Stand 18.09.2020; letzter Zugriff 23.06.2021. www.dimdi.de
- Europäische Arzneimittel-Agentur. Fachinformation Peginterferon alfa-2a (Pegasys). Letzter Zugriff 05.03.2021. www.ema.europa.eu
- Dienstag JL, Schiff ER, Wright TL, Perrillo RP, Hann HW, Goodman Z, et al. Lamivudine as initial treatment for chronic hepatitis B in the United States. N Engl J Med 1999;341:1256-63. New England Journal of Medicine
- Pascher A, Nebrig M, Neuhaus P. Irreversible liver failure: treatment by transplantation. Dtsch Arztebl Int 2013; 110: 167-73. DOI: 10.3238/arztebl.2013.0167 DOI
- Wiegand J, Berg T. The etiology, diagnosis and prevention of liver cirrhosis—part 1 of a series on liver cirrhosis. Dtsch Arztebl Int 2013; 110: 85-91. doi:10.3238/arztebl.2013.0085 DOI
- Robert Koch-Institut. Hepatitis B Antworten auf häufig gestellte Fragen (FAQ) zum Infektionsschutzgesetz und Meldewesen. Stand 17.01.2018. Letzter Zugriff 05.03.2021. www.rki.de
- Bundesanstalt für Arbeitsschutz und Arbeitsmedizin (BAuA). Dortmund. Merkblätter und wissenschaftliche Begründungen zu den Berufskrankheiten der Anlage 1 zur Berufskrankheiten-Verordnung (BKV), zuletzt aktualisiert durch die Dritte Verordnung zur Änderung der Berufskrankheiten-Verordnung vom 22. Dezember 2014. Zugriff 24.1.2017. www.baua.de
- DGVU Formtexte für Ärzte: Ärztliche Anzeige bei Verdacht auf eine Berufskrankheit. www.dguv.de
- Mehrtens, G. Valentin, H. Schönberger, A. Arbeitsunfall und Berufskrankheit: rechtliche und medizinische Grundlagen für Gutachter, Sozialverwaltung S.878ff. Berlin: Erich Schmidt Verlag 9: Auflage, 2017.
- RKI. Schutzimpfung gegen Hepatitis B: Häufig gestellte Fragen und Antworten. Stand: 23.6.2020. Letzter Zugriff 17.07.2020. www.rki.de
- Empfehlungen der Ständigen Impfkommission (STIKO) am Robert Koch-Institut. Epidemiologisches Bulletin 34/2020. Letzter Zugriff 05.03.2021. www.rki.de
- Kling K, Bogdan C, Ledig T et al. Empfehlungen der Ständigen Impfkommission (STIKO) zu Reiseimpfungen. Epid Bull 2021; 14: 1–182 www.rki.de
- RKI. Empfehlungen der STIKO. Stand 2022. Letzter Zugriff 19.04.22. www.rki.de
- Jefferson T, Demicheli V, Deeks J, et al. Vaccines for preventing hepatitis B in health-care workers. In: The Cochrane Library, Issue 1, 2003. pubmed.ncbi.nlm.nih.gov
- Robert Koch-Institut. Schutzimpfung gegen Hepatitis B: Häufig gestellte Fragen und Antworten. Stand 28.01.2021. Letzter Zugriff 05.03.2021. www.rki.de
- Arbeitskreis "Krankenhaus- & Praxishygiene" der AWMF. Prävention blutübertragbarer Virusinfektionen. AWMF-Leitlinie 029–026. Stand 2017. www.awmf.org
- Mauss S, Berg T, Rockstroh J, Sarrazin C, Wedemeyer H. Hepatology – a clinical textbook, 20th edition. 2020. www.hepatologytextbook.com Abrufdatum: 27.2.2021 www.hepatologytextbook.com
- Yang H-I, Lu S-N, Liaw Y-F, et al. Hepatitis B e antigen and the risk of hepatocellular carcinoma. N Engl J Med 2002; 347: 168-74. PubMed
- Chen CJ, Yang HI, Su J, et al. Risk of hepatocellular carcinoma across a biological gradient of serum hepatitis B virus DNA level. JAMA 2006; 295: 65-73. jamanetwork.com
- European Association for the Study of the Liver (EASL). Clinical Practice Guidelines: Management of chronic hepatitis B virus infection. J Hepatol 2012; 57: 167-185. www.easl.eu
- Fattovich G, Olivari N, Pasino M et al. Long-term outcome of chronic hepatitis B in caucasian patients: mortality after 25 years. Gut 2008; 57: 84-90. pubmed.ncbi.nlm.nih.gov
Autor*innen
- Lino Witte, Dr. med., Arzt in Weiterbildung, Innere Medizin, Frankfurt
- Michael Handke, Prof. Dr. med., Facharzt für Innere Medizin, Kardiologie und Intensivmedizin, Freiburg i. Br.
- Die ursprüngliche Version dieses Artikels basiert auf einem entsprechenden Artikel im norwegischen hausärztlichen Online-Handbuch Norsk Elektronisk Legehåndbok (NEL, https://legehandboka.no/).