Was ist die Chagas-Krankheit?
Die Chagas-Krankheit wird durch den Parasiten Trypanosoma cruzi verursacht, der von Wanzen übertragen wird. Die Krankheit kommt vor allem in Lateinamerika vor und wird auch als amerikanische Trypanosomiasis bezeichnet. Die Infektion erfolgt oft im Kindesalter, und bis zu 10 % der Kinder sterben in der akuten Phase. Bei 20–30 % der unbehandelten Patienten verläuft die Infektion chronisch. Nach einer symptomfreien Latenzzeit von 10–30 Jahren können Herzerkrankungen, Magen-Darm-Erkrankungen und Erkrankungen des Nervensystems auftreten. Eine durch die Infektion verursachte Herzinsuffizienz kann schließlich zum Tod führen.
In den letzten 20 Jahren wurden bei Prävention und Behandlung erhebliche Fortschritte gemacht. Durch den Einsatz von Insektiziden ist die Häufigkeit der Erkrankung deutlich zurückgegangen.
Schätzungen zufolge sind in Lateinamerika etwa 7 Millionen Menschen mit dem Parasiten infiziert. In vielen Ländern Südamerikas ist die Chagas-Krankheit die Hauptursache für nichtkoronare Herzerkrankungen. Jährlich sterben mindestens 10.000 Menschen an der Chagas-Krankheit.
Aufgrund der zunehmenden Mobilität in der Weltbevölkerung wird vermutet, dass mehr als 300.000 infizierte Patienten außerhalb der ursprünglichen Verbreitungsgebiete leben, vor allem in den USA und in Europa. Die Krankheit tritt in Deutschland selten auf und wird in der Praxis nur unter Einwanderern aus den Verbreitungsgebieten gefunden, sehr selten auch bei Touristen.
Ursache
Der Parasit wird über blutsaugende Insekten (10–30 mm lange Raubwanzen, siehe Abbildungen), die normalerweise in Rissen in den Wänden von Lehmhütten und Strohhäusern leben, auf Menschen übertragen. Die Infektion kann auch durch Bluttransfusionen, Organtransplantationen und Mutter-Kind-Übertragung während der Schwangerschaft/Geburt geschehen.

Triatominae – Raubwanzen in Lateinamerika
|
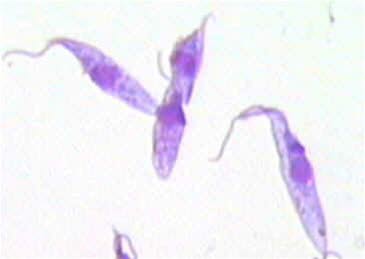
Trypanosoma cruzi
|
Die Wanzen hinterlassen beim Blutsaugen Kot, der Parasiten enthält. Diese werden durch den Juckreiz in die Haut eingekratzt oder dringen direkt in die Schleimhäute von Augen, Nase und Mund ein. Schließlich gelangen die Parasiten in den Blutkreislauf, worüber sie sich später in den Körperzellen ansiedeln. Am häufigsten kommen Trypanosomen im Herzmuskel (Myokard), in der glatten Muskulatur (z. B. in den Wänden des Magen-Darm-Traktes) und im Zentralnervensystem (Gliazellen) vor. Eine weitere Vermehrung der Trypanosomen verursacht die Zerstörung von Zellen und führt zu Entzündungen. Die Muskelzellen werden durch unelastisches Bindegewebe (Fibrose) ausgetauscht.
Die ersten Symptome treten 5–20 Tage nach Übertragung durch Raubwanzen auf. Die Infektion verläuft in mehreren Stadien. Das akute Stadium dauert 4–8 Wochen und verläuft größtenteils ohne Symptome oder bleibt unbemerkt, da die Symptome denen typischer Krankheiten ähneln: Fieber, geschwollene Lymphknoten, vergrößerte Leber und Milz. Etwa 15–40 % der infizierten Patienten entwickeln bis zu 30 Jahre nach der Ansteckung eine chronische Form der Krankheit. Eine Herzerkrankung macht 40 % der chronischen Fälle aus.
Symptome
Die akute Krankheitsphase verläuft bei einem Großteil der Betroffenen ohne Symptome. Die Symptome treten vor allem bei Kindern auf; sie können zwei bis vier Monate anhalten und sind unter Umständen lebensbedrohlich. Die ersten Anzeichen sind pickelähnliche Hautreaktionen mit lokaler Lymphknotenschwellung (sogenanntes Chagom) und finden sich an der Bissstelle in der Haut oder rund um das Auge. Die Lider des betroffenen Auges können geschwollen sein. Zu den späteren Symptomen gehören Fieber, Müdigkeit, Kopfschmerzen, vergrößerte Leber, leicht vergrößerte Milz, Durchfall und allgemein vergrößerte Lymphknoten. Zusätzlich können Hautausschläge und Wassereinlagerungen im Gewebe (Ödeme) auftreten. Ist der Herzmuskel akut entzündet (Myokarditis), kann dies zu Herzinsuffizienz führen. Bei jüngeren Kinern kann auch eine Hirnhautentzündung auftreten.

Die symptomfreie Latenzphase kann 10–30 Jahre dauern. Die Patienten haben während dieser Phase keine Symptome, aber Blutuntersuchungen können die Infektion bestätigen.
Die chronische Phase zeigt sich bei Personen im Alter von 30–40 Jahren oft in der Form von Herzerkrankungen; Betroffene leiden unter Herzrhythmusstörungen und Herzmuskelschwäche, und es bilden sich Blutgerinnsel. Die Nervenzentren im Verdauungstrakt können auch beschädigt werden, was zu Erweiterungen der Speiseröhre und des Dickdarms führen und u. a. Schluckbeschwerden, Aufstoßen und Verstopfung verursachen kann.
Diagnostik
Die Krankheit ist in Lateinamerika weit verbreitet, und die Diagnose kann auf der Grundlage der vorhandenen Symptome gestellt werden. Viele Betroffene haben jedoch keine Symptome, weshalb die Erkrankung oftmals nicht diagnostiziert wird. In der akuten Phase kann der Parasit direkt im Blut nachgewiesen werden, und in der späteren Phase können Antikörper-Tests zeigen, ob eine Infektion vorliegt oder nicht. Die Untersuchungen können jedoch nicht Aufschluss darüber geben, wer wieder gesund wird und wer später die chronische Form der Erkrankung entwickeln wird.
Bei Patienten mit Herzbeschwerden wird eine EKG-Untersuchung (Elektrokardiogramm) empfohlen.
Behandlung
Es gibt zwei Medikamente (Nifurtimox und Benznidazol), die in der akuten Phase wirksam sind. Beide Medikamente sind in Deutschland nicht zugelassen und haben starke Nebenwirkungen. Die medikamentöse Behandlung kann auch nach der akuten Phase wirksam sein, wenn die Krankheit noch nicht zu weit fortgeschritten ist. Daher werden alle Patienten behandelt, die akut erkrankt oder jünger als 18 Jahre sind. Es gibt allerdings keine spezielle Therapie für Kinder.
In der chronischen Phase steht die Behandlung der Herzerkrankung im Vordergrund.
Es gibt keinen Impfstoff gegen die Chagas-Krankheit. Nationale Präventionsprogramme konzentrieren sich auf die Bekämpfung von Wanzen. Die Wanzenbekämpfung ist erfolgreich und hat in den letzten 20 Jahren zu einem erheblich geringeren Vorkommen der Krankheit geführt.
Wenn Sie in die Verbreitungsgebiete reisen, sollten Sie Insektenschutzmittel und imprägnierte Moskitonetze verwenden.
Verlauf und Prognose
Etwa 20–30 % der infizierten Patienten entwickeln bis zu 30 Jahre nach der Ansteckung eine chronische Form der Krankheit. Infolge können Herzmuskelerkrankungen mit Herzschwäche und Rhythmusstörungen auftreten. Die Chagas-Krankheit kann auch in der chronischen Phase zum Tod führen, meist durch plötzlichen Herztod. Auch die Schädigungen im Magen-Darm-Trakt können schwerwiegende Komplikationen nach sich ziehen.
In etwa 70 % der Fälle heilt die Erkrankung von selbst aus. Sie betrifft vor allem arme Menschen in Lateinamerika.
Weitere Informationen
- Chagas-Krankheit – Informationen für ärztliches Personal
Autoren
- Martina Bujard, Wissenschaftsjournalistin, Wiesbaden
Link lists
Authors
Previous authors
Updates
Gallery
Snomed
References
Based on professional document Chagas-Krankheit. References are shown below.
- Bern C. Chagas´ disease. N Engl J Med 2015; 373: 455-66. DOI: 10.1056/NEJMra1410150 DOI
- Woodhall D, Jones JL, Cantey PT, et al. Neglected parasitic infections: what every family physician needs to know. Am Fam Physician. 2014 May 15;89(10):803-811. . www.ncbi.nlm.nih.gov
- Robert-Koch-Institut. Trypanosomiasis, amerikanische Form (Chagas-Krankheit) in "Steckbriefe seltener und importierter Infektionskrankheiten". Stand 2011. www.rki.de
- World Health Organization. Chagas disease (American trypanosomiasis). March 2015. www.who.int
- Rassi Jr A, Rassi A, Merin-Neto JA. Chagas disease. Seminar. Lancet 2010; 375: 1388-402. PubMed
- Chagas' disease - an epidemic that can no longer be ignored (editorial). Lancet 2006; 368: 619. PubMed
- Prata A. Clinical and epidemiological aspects of Chagas disease. Lancet Infect Dis 2001; 1: 92-100. PubMed
- Deutsche Gesellschaft für Neurologie. Atypische erregerbedingte Meningoenzephalitiden. AWMF-Leitlinie Nr. 030-061. Stand 2012. www.awmf.org
- Elizari MV. Arrhythmias associated with Chagas' heart disease. Card Electrophysiol Rev 2002; 6: 115-9. PubMed
- Rossi MA. Comparison of Chagas' heart disease to arrhythmogenic right ventricular cardiomyopathy. Am Heart J 1995; 129: 626-9. PubMed
- Agrelo RS. American trypanosomisis (Chagas disease). I: Heymann DL, red. Control of communicable diseases manual. 18. utg. Washington, D.C.: American Public Health Association, 2004: 557-60.
- Okumura M, Aparecida dos Santos V, Camargo ME et al. Prenatal diagnosis of congenital Chagas' disease (American trypanosomiasis). Prenat Diagn 2004; 24: 179-81. PubMed
- Urbina JA. Chemotherapy of Chagas disease. Curr Pharm Des 2002; 8: 287. PubMed
- Andrade AL, Martelli CM, Oliveira RM et al. Short report: Benznidazol efficacy among Trypanosoma Cruzi-infected adolenscents after a six-year follow-up. Am J Trop Med Hyg 2004; 71: 594-7. PubMed
- Bittencourt AL, Sadigursky M, Da Silva AA et al. Evaluation of Chagas' disease transmission through breast-feeding. Mem Inst Oswaldo Cruz 1988; 83: 37-9. PubMed
- Deutsche Gesellschaft für Pädiatrische Kardiologie. Tachykarde ventrikuläre Herzrhythmusstörungen im Kindes- und Jugendalter - Indikationen zur ICD Therapie. AWMF-Leitlinie Nr. 023-037. Stand 2013. www.awmf.org