Zusammenfassung
- Definition:Durch exogene und endogene Stimuli provozierbare, akut oder chronisch verlaufende polygenetische Hauterkrankung mit T-Zell-vermittelter Autoimmungenese.
- Häufigkeit:1-Jahres-Prävalenz in Deutschland: 2,5 % der Gesamtbevölkerung und 0,7 % der Kinder.
- Symptome:Effloreszenzen und Pruritus, in bis zu 40 % der Fälle im Verlauf auch Gelenkbeschwerden.
- Befunde:Charakteristische Effloreszenzen: scharf begrenzte, erythematöse und schuppende Hautveränderungen auf Streckseiten des Körpers und der Kopfhaut. Häufig auch Nagelveränderungen (Tüpfelnägel, Ölflecken).
- Diagnostik:Klinische Diagnose. Bei atypischen Varianten Biopsie zur Diagnosesicherung.
- Therapie:Bei leichter Form topische Therapie. Bei (mittel)schwerer Form systemische Therapie durch Spezialist*in.
Allgemeine Informationen
Definition
- Synonym: Schuppenflechte
- Durch exogene und endogene Stimuli provozierbare, akut oder chronisch verlaufende polygenetische Hauterkrankung mit T-Zell-vermittelter Autoimmungenese1
- bei 5–40 % der Patient*innen auch Gelenkbeteiligung1-3
- Charakteristische Effloreszenzen: scharf begrenzte, erythematöse und schuppende Hautveränderungen auf Streckseiten des Körpers und der Kopfhaut4-6
Klinische Varianten
- Klinische Varianten mit teilweise sehr unterschiedlichen Verlaufsformen1
- Psoriasis vulgaris (Plaque-Typ)
- stationär
- schubaktiv
- Psoriasis guttata (exanthematische Form der Psoriasis)
- Psoriasis inversa
- Psoriasis pustulosa palmoplantaris
- Psoriasis intertriginosa
- Erythrodermia psoriatica (Maximalvariante der Psoriasis vulgaris)
- Psoriasis pustulosa
- Psoriasis pustulosa (generalisierter Typ)
- Psoriasis pustulosa (lokalisierter Typ)
- Psoriasis arthropathica
- Sonderformen
- u. a. Nagelpsoriasis
- Psoriasis vulgaris (Plaque-Typ)
Häufigkeit
- Prävalenz in westlichen Industrienationen 1,5–2 %7
- Ungefähr 80 % davon entfallen auf Psoriasis vulgaris.
- 1-Jahres-Prävalenz in Deutschland8
- 2,5 % der Gesamtbevölkerung und 0,7 % der Kinder
- somit 2 Mio. Menschen, davon ca. 350.000 Kinder, in Deutschland betroffen.
- Alter und Geschlecht
- Beginn in jedem Alter möglich; durchschnittlicher Beginn mit 28 Jahren9
- keine geschlechtsspezifischen Unterschiede in der Häufigkeit
Ätiologie und Pathogenese
- Multifaktorielle Genese; genetische, immunologische und infektiöse Mechanismen sind von zentraler Bedeutung.
- Genetische Faktoren
- Mutationen bzw. Polymorphismen bei Vielzahl von Genen nachgewiesen
- Mehrere der Gene sind auch an der Entstehung anderer Autoimmun- und Entzündungserkrankungen (z. B. entzündliche Darmerkrankungen, Typ-1-Diabetes, multiple Sklerose und atopische Dermatitis) beteiligt.6
- Ebenfalls beschrieben sind Assoziationen mit HLA-B13, HLA-Bw57, HLA-Cw6, HLA-B27, HLACw2, HLA-DR4 und HLA-DR7.1
- bei Single Nucleotide Polymorphismus des TNF-alpha-Gens signifikante Veranlagung für Psoriasisarthritis1
- TNF-alpha-Gen-Polymorphismus steht in Relation zum Schweregrad der Psoriasis bzw. zu Ansprechen auf Etanercept.11
- Bei ca. 1/3 der Patient*innen gibt es weitere Fälle von Psoriasis in Familie; vor allem bei Patient*innen mit frühem Krankheitsbeginn.9,12
- Immunologisch
- Bildung von Autoantigenen in der Haut, die Lymphozyten zur Bildung von inflammatorischen Zytokinen und damit zur Aufrechterhaltung der Entzündung anregen.4,13-15
- Th17-Zellen dabei zentrale Effektorzellen
- Der Prozess kann vermutlich durch Umweltfaktoren, z. B. Virus-Antigen, ausgelöst werden.
- Infektiös
- Psoriasis guttata tritt häufig nach Infektion der oberen Atemwege auf.14
- in der Mehrzahl der Fälle (bei Kindern > 60 %) vorherige Streptokokken-Infektion (diskutiert werden streptogene Antigene mit Strukturähnlichkeiten zu Keratinozytenproteinen)
Pathophysiologie
- Hyperproliferative Erkrankung, die eine komplexe Kaskade von Entzündungsmediatoren involviert.
- Zellzyklus der Keratinozyten durch stimulierende Mediatoren (TNF-alpha, G-CSF, Interleukine) um mehr als 8-Fache beschleunigt1
- Die silbrige Schuppenschicht auf der Oberfläche der psoriatischen Läsionen besteht aus abgestorbenen Zellen.14
Prädisponierende Faktoren
Endogene Faktoren
- Familiäre Disposition (siehe Abschnitt Genetische Faktoren)
Exogene Faktoren
- Emotionale Belastung
- In mehr als der Hälfte der Fälle ist anamnestisch Stress der Auslöser für einen Schub.17
- Infektionen, v. a. Infektionen der oberen Luftwege mit Streptokokken
- Mechanische Hauttraumata (siehe Köbner-Phänomen unter Psoriasisphänomene)
- Arzneimittel: Lithium, Betablocker, Kalzium-Kanal-Blocker, Chloroquin, beim Absetzen oder Reduzieren von systemischen Kortikosteroiden, NSAR, einige Antibiotika (z. B. Makrolide) und hormonelle Kontrazeptiva18
- Sonnenlicht
- Hormonelle Faktoren
- Hypokalzämie
- Alkohol
Psychodermatologie
- Erkrankte Patient*innen leiden oft an deutlicher Einschränkung der Lebensqualität.7
- In Deutschland hat sich Lebensqualität der Patient*innen mit Psoriasis in letzten 15 Jahren jedoch deutlich verbessert.
- Wird auf den zunehmenden Einsatz leitlinienkonformer Therapien zurückgeführt.
- Psychische Faktoren haben insbesondere bei Exazerbation/Psoriasisschüben Bedeutung und sollten diagnostisch berücksichtigt werden.17
ICPC-2
- S91 Psoriasis
ICD-10
- L40 Psoriasis
- L40.0 Psoriasis vulgaris
- L40.1 Generalisierte Psoriasis pustulosa
- L40.2 Akrodermatitis continua suppurativa [Hallopeau]
- L40.3 Psoriasis pustulosa palmoplantaris
- L40.4 Psoriasis guttata
- L40.5† Psoriasis-Arthropathie (M07.0-M07.3*, M09.0-*)
- L40.8 Sonstige Psoriasis
Diagnostik
Diagnostische Kriterien
- Diagnose wird in erster Linie klinisch gestellt:
- positive Familienanamnese
- typische Effloreszenzen
- typische Verteilung der Effloreszenzen
- Nagelveränderungen (Tüpfelnägel).
- Diagnostisch hilfreich ist die Überprüfung verschiedener „Psoriasis-Phänomene“ innerhalb der Herde.11
- Kerzenfleckphänomen: Durch Kratzen lässt sich lamelläre Schuppung deutlich erkennen und entfernen.
- Phänomen des letzten Häutchens: Nach Auslösen des Kerzenfleckphänomens, d. h. Abkratzen der Schuppe, sieht man zusammenhängendes blattartiges, feucht wirkendes Häutchen.
- Auspitz-Zeichen: Nach Entfernung der obersten parakeratotischen Hornschuppen kommt es zu punktförmigen Blutungen, „blutiger Tau“.
- Köbner-Phänomen (oder isomorpher Reizeffekt): Auftreten von krankheitstypischen Hautveränderungen (Effloreszenzen) nach unspezifischer Reizung (mechanisch, thermisch, chemisch) an einer vorher nicht beeinträchtigten Stelle der Haut.
- Cave: Ein Köbner-Phänomen kann auch bei anderen Hauterkrankungen positiv sein und ist nicht spezifisch für Psoriasis.
- Bei Unsicherheit bezüglich der Diagnose ggf. Biopsie
- Die Bestimmung des Schweregrads ist essenziell für die Auswahl der Therapie.
Differenzialdiagnosen
- Seborrhoisches Ekzem
- Nummuläres Ekzem
- Pityriasis rosea
- Lichen planus
- Dermatophytosen
- Mycosis fungoides
- Sekundäre Lues
Anamnese
- Beginn in der Regel mit 1–2 abgegrenzten Läsionen an Ellenbogen oder Kopfhaut
- Monate oder Jahre später sind auch Gliedmaßen und der Körper betroffen.
- Typischer Hautausschlag und teilweise starker Pruritus5
- Oft positive Familienanamnese
- Exazerbation des Krankheitsbilds bei:
- Infektionen, insbesondere bei bakteriellen Infektionen der oberen Luftwege
- Stress und psychischer Belastung
- der Einnahme von Arzneimitteln wie Betablockern, ACE-Hemmern, Chloroquin und Lithium.
- Ca. 5–40 % aller Patient*innen entwickeln Gelenkbeschwerden.1-3
Komorbidität
- Psoriasisarthritis
- Zusammenhang zwischen Psoriasis, metabolischem Syndrom, koronarer Herzerkrankung und arterieller Hypertonie1
- Die Wahrscheinlichkeit einer kardiovaskulären Komorbidität steigt mit der Ausbreitung der Krankheit.
- Bei schwerer Psoriasis ist das Risiko, an einer koronaren Herzkrankheit zu erkranken, um das 2- bis 3-Fache erhöht.20
- Die steigende Häufigkeit von Psoriasis hängt möglicherweise mit einem vermehrten Auftreten von Adipositas in Bevölkerung zusammen und lässt sich evtl. durch Gewichtsreduktion lindern.21
- Zöliakie und chronisch-entzündliche Darmerkrankungen treten vermehrt auf.1
- Vermutlich ist auch Risiko für einige Krebserkrankungen (u.a. Lymphome) erhöht.22-23
Klinische Untersuchung
Allgemeines
- Die Krankheit befällt vor allem die Streckseiten.
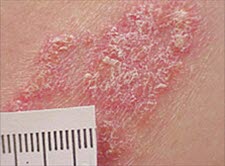 Psoriasisplaques
Psoriasisplaques- In der Regel sind Handflächen, Fußsohlen oder Gesicht nicht betroffen.
- Häufigste Lokalisationen sind Kopfhaut, Ellbogen und Knie.
- Den Hautsymptomen können Nagelveränderungen vorausgehen.
- Die Ausbreitung ist interindividuell sehr variabel.
- Bis zu 40 % aller Patient*innen entwickeln Arthritis.3
Primäre Hautveränderungen
- Oft bilateral und symmetrisch lokalisiert
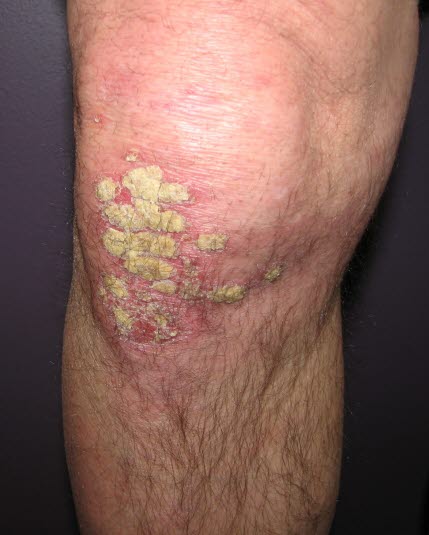 Psoriasis vulgaris
Psoriasis vulgaris - Läsionen beginnen als Papeln und wachsen schließlich zusammen, sodass scharf begrenzte, erythematöse Plaques entstehen, die mit dicken, weißen oder silbrig glänzenden, kerzenwachsartigen, teilweise festsitzenden Schuppen bedeckt sind.
- Beim Entfernen der Schuppen werden punktförmige Blutungen auf der erythematösen Oberfläche sichtbar (Auspitz-Phänomen).
- Traumata können das Köbner-Phänomen auslösen.
Verschiedene Arten der Psoriasis
- Psoriasis vulgaris
- großflächige, erhabene Plaques mit silbrig weißer, schuppender Oberfläche
- Schuppen können abgekratzt werden; darunter wird entzündete und in einigen Fällen sehr empfindliche Haut sichtbar.
- Psoriasis guttata
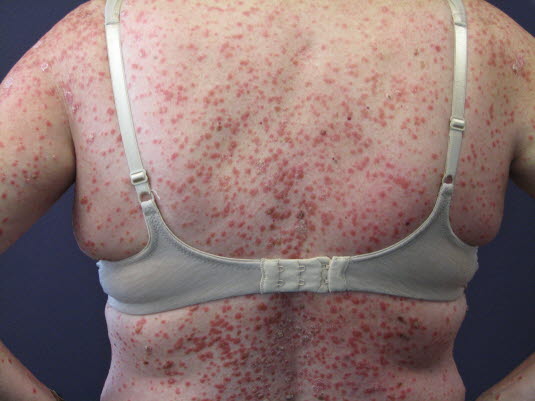 Psoriasis guttata
Psoriasis guttata
- weit verbreitete, erythematöse, kleine, schuppende Papeln an Rumpf, Armen und Beinen
- Häufig entstehen Läsionen nach Infektion der oberen Atemwege.
- Psoriasis pustulosa
- sterile Pusteln an Händen und Füßen (Pustulosis palmoplantaris)
- kreisförmige erythematöse Läsionen mit Pusteln und Schuppenbildung auch am Rumpf
möglich
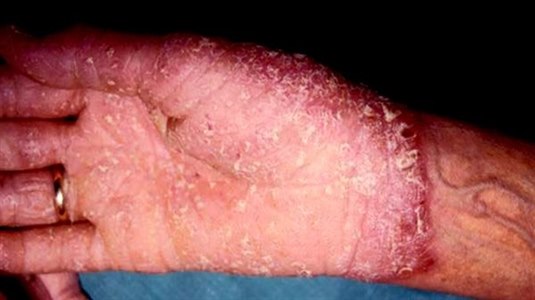 Pustulosis palmoplantaris
Pustulosis palmoplantaris
- Erythrodermische Psoriasis
- Maximalform der Psoriasis vulgaris
- generalisiertes Erythem mit feiner Schuppung
- häufig mit Schmerzen und in manchen Fällen auch mit starkem Pruritus verbunden
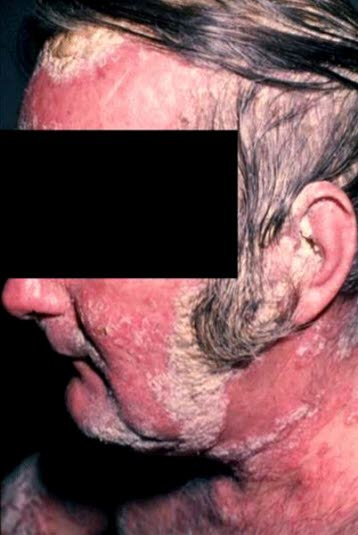 Erythrodermische Psoriasis
Erythrodermische Psoriasis
Nagelveränderungen
- Bei bis zu 80 % der Patient*innen1
- häufig auch erst im späteren Krankheitsverlauf
- Patient*innen mit Psoriasisarthritis haben häufiger Nagelveränderungen.24
- Veränderungen nahezu pathognomonisch
- Punktförmige Vertiefungen, die als Grübchen oder Tüpfelnägel bezeichnet werden.
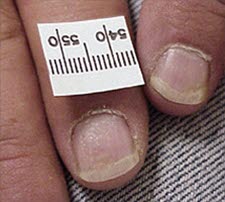 Tüpfelnägel bei Psoriasis
Tüpfelnägel bei Psoriasis
- Punktförmige Vertiefungen, die als Grübchen oder Tüpfelnägel bezeichnet werden.
- Onycholyse: Nagel löst sich vom Nagelbett ab.
- Teilweise bräunliche Verfärbungen des Nagels, die an Ölflecken erinnern.
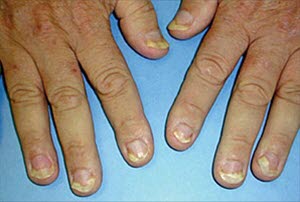 Onycholyse
Onycholyse - Gelegentlich kommt es zu subungualer Hyperkeratose.
Psoriasis inversa
- Vorwiegend beugeseitiges Auftreten
- Befällt intertriginöse Bereiche wie Glutealfalte, Axillae und Glans penis.
- Häufig keine Schuppung
Diagnostische Schwierigkeiten
- Bei neu entstandener Psoriasis, die nicht vom Plaque-Typ ist und bei der keine familiäre Vorbelastung vorliegt, kann die Diagnose schwierig sein. Bei folgenden Befunden sollte eine Psoriasis in Betracht gezogen werden:
- bei schuppenden Effloreszenzen
- bei atypischer Intertrigo und
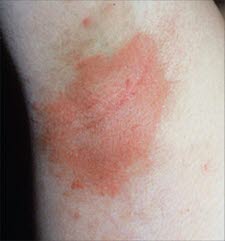 Psoriasis inversa
Psoriasis inversa - bei isolierten schuppenden Kopfhautveränderungen.
Bestimmung des Schweregrads
- Komplexes Unterfangen, bei dem klinische aber auch gesundheitsbezogene Lebensqualität betreffende Aspekte berücksichtigt werden müssen. 7
Leitlinie: Definition des Schweregrades7
- Leichte Psoriasis: BSA ≤ 10 und PASI ≤ 10 und DLQI ≤ 10
- Mittelschwere bis schwere Psoriasis: (BSA > 10 oder PASI > 10) und DLQI > 10
- Beim Vorliegen folgender Kriterien erfolgt zudem ebenfalls eine Einordnung als mittelschwere bis schwere Psoriasis („Upgrade-Kriterien"):
- ausgeprägte Erkrankung von sichtbaren Arealen
- ausgeprägte Erkrankung der Kopfhaut
- Erkrankung des Genitalbereichs
- Erkrankung der Handflächen und Fußsohlen
- Onycholyse oder Onychodystrophie von mindestens zwei Fingernägeln
- Jucken und damit einhergehendes Kratzen
- Vorliegen therapieresistenter Plaques.
BSA (Body Surface Area)
- Bestimmung des Ausmaßes der betroffenen Körperoberfläche
- Eine Handfläche entspricht etwa 1 % der Körperoberfläche.
PASI (Psoriasis Area and Severity Index)
- Beschreibt Ausdehnung der Erkrankung sowie Schweregrad anhand von Rötung und Dicke der Plaques sowie der Schuppung.
- Online-Rechner (PASI-Rechner)
DLQI (dermatologischer Lebensqualitäts-Index)
- Misst die Einschränkung der Lebensqualität von Menschen mit Schuppenflechte in den vorangegangenen sieben Tagen.
- Ist für Personen ab 16 Jahren konzipiert worden.
- Punkte: 0 (kein Einfluss der Erkrankung auf Lebensqualität) bis 30 (sehr starker Einfluss)
- Dermatologischer Lebensqualitäts-Index (DLQI)
Ergänzende Untersuchungen
Diagnostische Biopsie
- Bei unklarer Diagnose Biopsieentnahme
- Gewebeprobe aus dem zentralen Teil einer älteren, typischen Läsion entweder als größere Exzisionsbiopsie oder mit mehreren kleineren Stanzbiopsien
- Für eine aussagekräftige Biopsie darf keine Vorbehandlung der Läsion erfolgt sein.11
Andere Untersuchungen
- Bei Psoriasis guttata können ggf. zum Nachweis von Streptokokken ein Rachenabstrich und/oder Lues-Serologie (als Differenzialdiagnose) durchgeführt werden.
- Bei atypischen Nagelveränderungen ggf. Untersuchung auf Pilzinfektionen
Indikationen zur Überweisung
- Patient*innen mit mittelschwerer bis schwerer Psoriasis (Dermatologie)
- Einleitung einer Systemtherapie
- Patient*innen mit Psoriasisarthritis (Rheumatologie)
Checkliste zur Überweisung
Psoriasis
- Zweck der Überweisung
- Diagnostik? Therapie? Sonstiges?
- Anamnese
- Wann wurde die Diagnose gestellt? Krankheitsverlauf und Entwicklung?
- Lokalisation und Ausbreitung: Pruritus, sonstige Beschwerden? Gelenkschmerzen?
- Familiäre Disposition? Andere relevante Krankheiten?
- Versuchte Therapien: Wirkung?
- Berufliche, soziale oder sonstige Konsequenzen?
- Klinische Untersuchung
- Hautstatus
- Allgemeinzustand
Therapie
Therapieziele
- Schnelle Kontrolle der Symptome und Verringerung der betroffenen Körperoberfläche24
- für Betroffene persönlich das wichtigste Ziel der Behandlung25
- Verbesserung der Lebensqualität7
- Individuelle Festlegung eines Mindestziels, da nicht bei allen Patient*innen Erscheinungsfreiheit erreichbar ist.7
- für schnell wirkende Medikamente Überprüfung des Erreichens von Therapiezielen am Ende der Induktionstherapie nach 10–12 Wochen, bei Medikamenten mit langsam einsetzender Wirkung nach 16–24 Wochen
- bei Verfehlen des Mindestziels Anpassung der Therapie
Allgemeines zur Therapie
- Es gibt keine Kausaltherapie.
- Viele verschiedene klinische Bilder sind möglich.
- individuelle Anpassung der Therapie an Schweregrad, Komorbiditäten und Präferenzen der jeweiligen Patient*innen
- Die Nebenwirkungen der Therapie sollten nicht gravierender sein als die Psoriasis selbst.
- Entfernung von Schuppen vor topischer Therapie
- Topische Therapie der leichten Psoriasis in der Hausarztpraxis möglich
- Systemische Therapie der (mittel)schweren Psoriasis durch Dermatolog*in
Leitlinie: Therapie der Psoriasis vulgaris7
Allgemeine Therapieprinzipien
- Therapie abhängig von Schweregrad der Erkrankung
- Leichte Psoriasis: topische Therapie
- Mittelschwere bis schwere Psoriasis: systemische Therapie/Phototherapie + ggf. topische Therapie
Grundsätze der systemischen Therapie
- Entsprechend des Wirtschaftlichkeitsgebotes initial Einleitung einer „konventionellen“ Systemtherapie
- Einleitung einer Therapie mittels Biologikum, wenn die konventionelle Therapie keinen ausreichenden Therapieerfolg gezeigt hat, unverträglich oder kontraindiziert ist.
- Bei Vorliegen einer Psoriasis, bei der die konventionelle Therapie keinen ausreichenden Therapieerfolg erwarten lässt (z. B. besonders schwere Ausprägung mit PASI ≥ 20), kann Einleitung einer Therapie mit Biologikum mit „First Line Label“ (Zulassung durch EMA) empfohlen werden.
Topische Therapie – verfügbare Wirkstoffgruppen
- Calcineurin-Inhibitoren (Tacrolimus, Pimecrolimus) – cave: Off-Label-Use!
- Dithranol
- Kortikosteroide
- Teer
- Tazarotene
- Vitamin-D3-Analoga (Calcipotriol, Calcitriol, Tacalcitol)
- Lasertherapie lokal
Phototherapie
- UVB-/Photo-/Balneo-PUVA-Therapie
Systemische Therapie - verfügbare Wirkstoffgruppen
- „Konventionelle“ Systemtherapie
- Fumarsäureester
- Methotrexat
- Ciclosporin A
- Retinoide (Acitretin)
- Biologika „First Line Label“
- Adalimumab (Anti-TNF-alpha)
- Brodalumab (Anti-IL-17)
- Certolizumab (Anti-TNF-alpha)
- Guselkumab (Anti-IL-23)
- Ixekizumab (Anti-IL-17)
- Risankizumab (Anti-IL-23)
- Secukinumab (Anti-IL-17)
- Tildrakizumab (Anti-IL-23)
- Biologika „Second Line Label“
- Ustekinumab (Anti-IL-12/23)
- Infliximab (Anti-TNF-alpha)
- Etanercept (Anti-TNF-alpha)
- Apremilast (PDE-4-Hemmer, orale Einnahme)
Empfehlungen für Patient*innen
- Eine Eigentherapie mit Feuchtigkeitsbehandlung und Entfernung der Schuppen vor der topischen Therapie ist sehr wichtig.
- Tägliche Feuchtigkeitszufuhr mithilfe von Feuchtigkeitscremes und häufigen Ölbädern in Alltag integrieren.
- Die Entfernung der Schuppen ist eine Bedingung dafür, dass weitere lokale Therapiemaßnahmen wirken können.
- Natürliche Sonnenstrahlung und Salzwasser- bzw. Meerwasserbäder haben bei den meisten Patient*innen mit Psoriasis positive Wirkung.
- Cave: Sonnenbrände vermeiden, da diese im Sinne eines Köbner-Phänomens zur Verschlimmerung der Erkrankung beitragen können.
Topische Therapie – Wirkstoffgruppen
- Zusammenfassung der Wirkstoffgruppen mittels Appendix der S3-Leitlinie7
Calcineurin-Inhibitoren
- Indikationen
- bei Psoriasis vulgaris in den kortikosteroidempfindlichen Arealen, v. a. Gesicht, Körperfalten, Genito-Anal-Bereich
- Anwendung am übrigen Körper aufgrund der nicht ausreichenden Datenlage bei vorhandenen Therapiealternativen sowie aufgrund der fehlenden Zulassung nicht empfohlen
- Präparate: Tacrolimus, Pimecrolimus
- Empfohlene Initialdosis
- häufig kurzzeitige Vortherapie mit topischen Kortikoiden
- anschließend 1–2 x/d topische Applikation
- Erwarteter Wirkungseintritt: nach 2 Wochen
- Ansprechrate: 40–50 % der Patient*innen mit deutlicher Verbesserung oder vollständige Abheilung der Läsionen nach 6–12 Wochen
- Kontraindikationen
- Schwangerschaft und Stillzeit (fehlende Erfahrung)
- keine Kombination mit Phototherapie
- Nebenwirkungen: Brennen der Haut, Hautinfektionen
- Maßnahmen während der Behandlung: Lichtschutz
- Sonstiges: Off-Label-Use
Dithranol
- Indikationen: Induktionstherapie bei leichter und mittelschwerer Psoriasis vulgaris
- Präparate: Psoralon, Psoradexan, Micanol
- Empfohlene Initialdosis
- Beginn mit 0,5-prozentiger Zubereitung für die Langzeittherapie oder 1-prozentiger für die Kurzkontakttherapie, dann nach Verträglichkeit steigern.
- Langzeittherapie: Beginn mit schwächster Konzentration, wobei morgens und abends eine Applikation dünn auf die Plaques aufgetragen und nicht abgewaschen wird. Üblicherweise erfolgt je nach Hautreizung Verdopplung der Konzentration alle 3 Tage, wobei eine Zielkonzentration von 1–3 % angestrebt wird.
- Kurzkontakttherapie: Beginn mit schwächster Konzentration, in den ersten Tagen 10 min auf den betroffenen Hautstellen belassen und anschließend mittels lauwarmen Wassers abspülen. In den darauffolgenden Tagen Einwirkzeit auf 30 min verlängern und die Konzentration abhängig von der Hautreizung erhöhen.
- Beginn mit 0,5-prozentiger Zubereitung für die Langzeittherapie oder 1-prozentiger für die Kurzkontakttherapie, dann nach Verträglichkeit steigern.
- Erwarteter Wirkungseintritt: nach 2–3 Wochen
- Ansprechrate
- deutliche Besserung oder vollständiges Abheilen der Hautläsionen bei 30–70 % der Patient*innen
- Die Kombination mit calcipotriolhaltigen Cremes oder einer UV-B-Phototherapie kann Wirksamkeit erhöhen.
- Kontraindikationen
- akute, erythrodermische Formen der Psoriasis vulgaris
- pustulöse Psoriasis
- Nebenwirkungen: Brennen und Rötung der Haut in über >10 %
- Maßnahmen während der Behandlung: Kontrolle der Hautirritationen mit entsprechender Anpassung der Dosis
- Sonstiges
- nicht zur Langzeittherapie empfohlen
- keine gute Praktikabilität für die Patient*innen
Kortikosteroide
- Indikationen
- Induktionstherapie mit topischen Kortikoiden der Wirkstoffklasse III bei leichter bis mittelschwerer Psoriasis vulgaris
- Induktionstherapie mit topischen Kortikoiden der Wirkstoffklasse IV unter Abwägung von erhöhter Wirksamkeit und theoretisch erhöhtem Risiko unerwünschter Arzneimittelwirkungen bei leichter bis mittelschwerer Psoriasis vulgaris
- Cave: Wegen der Gefahr einer Hautatrophie zurückhaltender Einsatz an Gesicht, Genitalregion, Hals und intertriginösen Räumen!
- Präparate: diverse
- Empfohlene Initialdosis
- Applikation 1 x/d auf die betroffenen Hautareale, im Verlauf Ausschleichen
- typisches Protokoll für Betamethasondipropionat
- Anwendung 1 x/d über 3 Wochen
- dann für 1 Woche Anwendung nur jeden 2. Tag
- gefolgt von 1 Woche Anwendung nur jeden 3. Tag
- anschließend Absetzen des Präparates
- Erwarteter Wirkungseintritt: nach 1–2 Wochen
- Ansprechrate
- Betamethasondipropionat (Klasse III): 25–78 % der Patient*innen mit deutlicher Verbesserung oder vollständigem Abheilen der Hautläsionen
- Clobetasol-17-propionat (Klasse IV, Applikation 2 x/d): Therapieerfolg bei 68–89 % der Patient*innen
- Kombination mit Salicylsäure oder topischen Vitamin-D3-Derivaten kann zu einer verbesserten Remissionsraten führen.
- Kontraindikationen
- bakterielle oder virale Hautinfektionen
- Nebenwirkungen: Follikulitis, periorale Dermatitis, Hautatrophie
- Maßnahmen während der Behandlung: keine notwendig
- Sonstiges: Entstehen von typischen unerwünschten Kortikoidwirkungen wie Hautatrophien oder Teleangiektasien bei langer Anwendung
Steinkohleteer
- Indikationen
- Monotherapie angesichts wirksamerer, risikoärmerer und praktikablerer Therapiealternativen obsolet
- Unter sorgfältiger Abwägung des therapeutischen Nutzens und unter Berücksichtigung risikoärmerer therapeutischer Alternativen in Kombination mit UV-B ggf. ausnahmsweise zur Anwendung bei ansonsten therapierefraktärer Psoriasis vulgaris
- Präparate: Salbenzubereitungen mit meist 5-prozentiger Wirkstoffkonzentration
- Empfohlene Initialdosis
- Ein- bis mehrstündige Applikation teerhaltiger Externa, an die sich unmittelbar oder nach Entfernung der Teerzubereitung eine UV-B-Bestrahlung anschließt.
- Erwarteter Wirkungseintritt: nach 4–8 Wochen
- Ansprechrate: keine ausreichenden Daten
- Kontraindikationen
- Schwangerschaft und Stillzeit
- Xeroderma pigmentosum, dysplastisches Naevuszellnaevus-Syndrom, Basalzellnaevus-Syndrom
- Nebenwirkungen: Farbe, Geruch, kanzerogenes Risiko, Phototoxizität (Teil der gewünschten Wirkung)
- Maßnahmen vor der Behandlung: Aufklärung über mögliche kanzerogene Wirkung
- Maßnahmen während der Behandlung
- keine übermäßige UV-Exposition
- keine gleichzeitige Anwendung photosensibilisierender Substanzen
- Sonstiges: Nur in therapierefraktären Einzelfällen als Ausnahme erwägen.
Tazaroten (Retinoid der 3. Generation)
- Indikationen
- bei leichter bis mittelschwerer Psoriasis vulgaris in Kombination mit topischen Kortikoiden (Optimierung des Therapieerfolgs und Reduktion von Hautirritationen)
- Präparate: Tazaroten-Gel 0,1 %
- Empfohlene Initialdosis
- 1 x/d abends als dünner Film exakt auf die betroffenen Hautstellen auftragen.
- Erwarteter Wirkungseintritt: nach 1–2 Wochen
- Ansprechrate
- nach 12 Wochen Therapie bei ca. der Hälfte der Patient*innen Befundbesserung um mindestens 50 %
- Kontraindikationen
- Schwangerschaft, Stillzeit
- Nebenwirkungen: Pruritus, Hautbrennen, Erythem, Irritation
- Maßnahmen während der Behandlung: Nicht übermäßig UV-Licht aussetzen.
- Sonstiges: Zwar in Deutschland zugelassen, wird aber nicht mehr vertrieben und zurzeit in 0,1-prozentiger Formulierung nur über Auslandsapotheke erhältlich.
Vitamin-D3-Analoga
- Indikationen
- fixe Kombination mit Kortikoiden in ersten 4 Wochen zur Induktionstherapie der leichten bis mittelschweren Psoriasis
- synergistische Effekte mit systemischer Ciclosporintherapie bei schwerer Psoriasis
- Präparate: als Cremes, Salben und Lotionen in unterschiedlichen Konzentrationen sowie als Fixkombination mit Betamethason
- Empfohlene Initialdosis
- Calcipotriol: 1–2 x/d auf die betroffenen Hautstellen, maximal 30 % der Körperoberfläche (KÖF)
- Tacalcitol: 1 x/d auf die betroffenen Hautstellen, maximal 20 % der KÖF
- Calcitriol: 2 x/d auf die betroffenen Hautstellen, maximal 35 % der KÖF
- Erwarteter Wirkungseintritt: nach 1–2 Wochen
- Ansprechrate
- 30–50 % der Patient*innen mit deutlicher Verbesserung oder vollständiger Abheilung der Läsionen nach 4–6 Wochen
- Kontraindikationen
- Erkrankungen mit Veränderungen des Kalziumstoffwechsels
- schwere Leber- und Nierenerkrankungen
- Nebenwirkungen: Hautirritation (Rötung, Juckreiz, Brennen)
- Maßnahmen während der Behandlung: Kein Auftragen vor Phototherapie, da eine gegenseitige Wirkungsabschwächung erfolgen kann.
- Sonstiges
- keine gleichzeitige Anwendung mit salizylathaltigen topischen Präparaten (Inaktivierung)
- Interaktion mit Medikamenten, die den Kalziumspiegel erhöhen (z. B. Thiazid-Diuretika).
Phototherapie
- Zusammenfassung der Phototherapie mittels Appendix der S3-Leitlinie7
- Indikationen
- Induktionstherapie bei mittelschwerer und schwerer Psoriasis vulgaris, vor allem bei großflächiger Erkrankung
- Aufgrund der besseren Praktikabilität und des geringeren Malignitätsrisikos Schmalspektrum-UV-B-Therapie als Phototherapie der 1. Wahl gegenüber PUVA bevorzugen.
- Kombination mit topischem Vitamin-D3-Derivaten zur Verbesserung der Ansprechrate
- Excimer Laser für die gezielte Behandlung einzelner psoriatischer Plaques
- Wegen geringer Praktikabilität und Assoziation langfristiger unerwünschter Wirkungen mit kumulativer UV-Dosis keine Langzeittherapie
- Modalitäten
- Schmalspektrum-UVB-Licht (311-313nm) in der Hautarztpraxis26
- in der Regel 3 x wöchentlich
- PUVA: Psoralen plus UV-A-Bestrahlung
- etwas effektiver, jedoch mehr Nebenwirkungen27
- Grenzstrahlung: Röntgenstrahlen mit großer Wellenlänge an der Grenze zur UV-Strahlung, die bis zu 1 mm in Haut eindringen und die Aktivität von Entzündungszellen hemmen.28
- möglicher Einsatz bei therapieresistenten lokalisierten Psoriasisplaques
- Schmalspektrum-UVB-Licht (311-313nm) in der Hautarztpraxis26
- Empfohlene Initialdosis
- individuelle Dosierung gemäß Hauttyp, Steigerung gemäß Erythembildung
- Erwarteter Wirkungseintritt: nach 1–2 Wochen
- Ansprechrate
- UVB: 50–75 % der Patient*innen nach 4–6 Wochen
- PUVA: 75–100 % der Patient*innen nach 4–6 Wochen
- Kontraindikationen
- Photodermatosen, Malignome der Haut, Immunsuppression
- PUVA: Schwangerschaft und Stillzeit
- Nebenwirkungen
- Erytheme, Juckreiz, Blasenbildung, Malignome
- PUVA: Übelkeit
- Maßnahmen vor der Behandlung
- sorgfältige Inspektion des gesamten Integumentes zum Ausschluss von Malignomen der Haut
- Aufklärung über therapiebedingte Erhöhung des Hautkrebsrisikos
- vor PUVA augenärztliche Kontrolluntersuchung
- Maßnahmen während der Behandlung
- regelmäßige Kontrolle der Erythembildung
- Augenschutz durch UV-Brille
- adäquater Sonnenschutz im Alltag
- Maßnahmen nach der Behandlung
- Ermittlung der kumulativen UV-Dosis und Mitteilung an Patient*in
- lebenslang regelmäßige Hautkrebs-Früherkennungsuntersuchung
- Sonstiges
- Cave: Interaktion mit photosensibilisierenden Medikamenten!
- gleichzeitige Gabe von Ciclosporin A kontraindiziert
Systemische Therapie – Wirkstoffgruppen
- Systemische Therapie soll durch Spezialist*in (Dermatolog*in) erfolgen.
Konventionelle Systemtherapie
- Methotrexat
- Einsatz seit vielen Jahrzehnten
- bei Arthritis psoriatica Therapie der 1. Wahl
- Empfohlene Anfangs- und Erhaltungsdosis 15 mg s. c. 1 x/Woche 7
- 5 mg Folsäure 1 x wöchentlich 24 Stunden nach MTX-Gabe
- aufgrund der Hepatotoxizität und Myelosuppression genaue Verlaufskontrolle erforderlich29
- Methotrexat ist teratogen und wirkt sich auf Spermatogenese aus.
- Mind. 3 Monate vor angestrebter Empfängnis MTX absetzen.7
- Ciclosporin A
- Dosen von 2–5 mg/kg/d30
- In der Regel wirkt Ciclosporin schneller als Methotrexat.
- wegen Nebenwirkungsprofil seltener Einsatz, wenn überhaupt nur als Induktionstherapie bei schwerer Psoriasis7,31
- relevante Nebenwirkungen – vor allem Nephro- und Phototoxizität
- Überwachung von Blutdruck und Nierenfunktion
- Sonnenschutz, keine gleichzeitige PUVA-Therapie
- Dosen von 2–5 mg/kg/d30
- Acitretin (Retinoid)
- Einsatz vor allem bei erythrodermatischen und pustulösen Formen32
- Anfangsdosis 25 mg oral über 2–4 Wochen, anschließende Erhaltungsdosis 25–50 mg32
- Einnahme mit fetthaltigen Mahlzeiten oder mit Vollmilch, um Absorption zu verbessern.7
- stark teratogen7
- Notwendigkeit einer effektiven Langzeitverhütung (bis 3 Jahre nach Absetzen der Therapie)
- Fumarsäureester/Dimethylfumarat
- Einsatz vor allem als Langzeittherapie bei chronischer Plaque-Psoriasis
- Orale Dosis bis zum klinischen Ansprechen von 30–720 mg/d auftitrieren.7
- Nebenwirkungen: bis zu 60 % der Patient*innen mit Diarrhöen, Flush, leichte Leuko- und Lymphopenie7
- Flush-Symptomatik kann durch ASS verringert werden.
- G-BA sieht keinen Zusatznutzen gegenüber Vergleichstherapie (Ciclosporin, MTX, PUVA, Biologika).33
- Der Hersteller informierte im November 2020 in einem Rote-Hand-Brief über das Risiko einer progressiven multifokalen Leukenzephalopathie (PML); zudem Einsatz kontrainidiziert bei schwerer Lymphopenie (Lymphozyten < 0,5 × 109/l).
Biologika
- Einsatz durch spezialisierte niedergelassene Dermatolog*innen oder Ambulanzen
- Jahrestherapiekosten übersteigen konventionelle Therapien um Vielfaches7
- Acitretin (Retinoid) oral 1.485,60 €
- Fumarsäureester oral 3.342,55 €
- MTX s. c. 3.342,55 €
- Secukinumab s. c. 28.148,43 €
- Infliximab i. v. 25.191,19 €
- jeweils Kosten/Jahr (nach Lauer-Taxe; Stand 01.03.2017)
- Wirkungsmechanismus
- Hauptsächlich monoklonale Antikörper, die Entzündungsmediatoren blockieren.
- somit Verringerung der unerwünschten immunologischen Aktivität
- Indikationen7
- bei Therapieversagen der konventionellen Wirkstoffe
- Psoriasis, bei der die konventionelle Therapie keinen ausreichenden Therapieerfolg erwarten lässt (z. B. besonders schwere Ausprägung mit PASI ≥ 20).
- Nachteile
- hoher Preis
- Reaktivierung latenter Tuberkulose möglich
- Risiko opportunistischer Infektionen
- Entwicklung spezifischer Antikörper, die die Ansprechdauer auf die Therapie begrenzen.
- langfristige Auswirkungen unbekannt
- Kontraindikationen
- maligne oder demyelinisierende Erkrankungen
Systemische Therapie in speziellen Situationen
- Die S3-Leitlinie zur Therapie der Psoariasis von 2021 beinhaltet mehrere Entscheidungsmatrizes und Empfehlungen für die Systemtherapie in speziellen Situationen, u. a. bei den Komorbiditäten chronisch-entzündliche Darmerkrankungen, Herz- oder Nierenerkrankungen oder Schwangerschaft.
- Da die Systemtherapie, insbesondere bei Komorbiditäten, durch Spezialist*innen durchgeführt werden soll, verweisen wir für interessierte allgemeinmedizinische Kolleg*innen auf die Seiten 29 und 30 der S3-Leitlinie, aber gehen in diesem Artikel nicht weiter darauf ein.
Therapie der klinischen Varianten
Psoriasis vulgaris mit wenigen stabilen Plaques
- Verschiedene Therapieoptionen vorhanden
- Am gebräuchlichsten: topische Kortikosteroide der Klasse III–IV in Kombination mit Vitamin-D-Analogon
- wirksame Therapie und gut verträglich; wirksamer als das jeweilige Präparat in Monotherapie34-35
- Calcipotriol und Betamethason als Kombinationspräparat erhältlich
- Das Präparat wird 1-mal täglich über 4 Wochen auf psoriatischen Plaques angewendet, dann nach Bedarf.
- In Gelform sind die Wirkstoffe sowohl am Körper als auch insbesondere auf Kopfhaut anwendbar.
- Alternativ: Bestrahlung der lokalisierten Veränderungen mittels Phototherapie (UVB) oder Photochemotherapie (PUVA)36
Psoriasis der Kopfhaut
- Mittel der Wahl: Kombinationstherapie aus Klasse-III-Steroid und Vitamin-D-Analogon34-35
- Calcipotriol und Betamethason als Gel
- Bei mittelstarken Beschwerden und Verdacht auf gleichzeitig vorhandenes seborrhoisches Ekzem kann zunächst Therapieversuch mit Anti-Schuppen-Shampoo erfolgen.
- z. B. Ketoconazol 2-mal wöchentlich über 4 Wochen, danach Langzeitbehandlung, ca. 1-mal wöchentlich
- Bei leichten bis mäßigen Beschwerden können Kopfhaut und Gehörgänge mit flüssigen Klasse-II-Steroiden behandelt werden, vor allem, wenn die Veränderungen an ein seborrhoisches Ekzem erinnern.
- z. B. Hydrocortisonbutyrat als Lösung oder Emulsion
- Klasse-III- und Klasse-IV-Steroide sind ebenfalls wirksam und können bei Exazerbationen kurzzeitig angewendet werden.34-35
- Klasse-III-Steroide, z. B. Betamethason als Liniment oder Schaum, Mometason als Liniment
- Klasse-III-Steroide können evtl. auch in Kombination mit Salizylsäure verwendet werden.
- In schwierigen Fällen oder über kurze Zeiträume können Klasse-IV-Steroide verwendet werden.
- z. B. Clobetasol als Lösung oder Shampoo
- Klasse-III-Steroide, z. B. Betamethason als Liniment oder Schaum, Mometason als Liniment
- Bestrahlung der lokalisierten Veränderungen mittels Grenzstrahlung ist ebenfalls möglich, aber nur fraglich dauerhaft wirksam.28
- Die Psoriasis der Kopfhaut kann so schwer zu behandeln sein, dass eine systemische Therapie indiziert ist, obwohl Psoriasis am restlichen Körper nicht stark ausgeprägt ist.
Psoriasis im Gesicht
- Das Gesicht ist nur selten betroffen, evtl. vorhandene Effloreszenzen sollten jedoch, wenn überhaupt, nur mit niedrig-potenten Klasse-I- oder Klasse-II-Steroiden behandelt werden (Steroid-Nebenwirkungen: u. a. Hautatrophie und Teleangiektasien).
- Klasse I: z. B. Hydrocortison als Creme oder Salbe
- Klasse II: z. B. Hydrocortisonbutyrat als Creme oder Salbe
- Alternative: Calcineurininhibitoren
- Tacrolimus und in geringerem Umfang auch Pimecrolimus sind wirksam bei Psoriasis im Gesicht, im Genitalbereich und in den intertriginösen Bereichen.37-38
- Cave: Off-Label-Use, Calcineurininhibitoren nicht zur Behandlung der Psoriasis zugelassen!
Psoriasis der Nägel
- Einteilung nach Akuität39
- akute Nagelpsoriasis
- intensive, häufig schmerzhafte Entzündung der distalen und/oder proximalen Phalanx mit Deformierungen der Nagelplatte bis hin zum Verlust des Nagels
- chronische Nagelpsoriasis
- Nagelmatrixpsoriasis mit Grübchen (Tüpfelnägel)
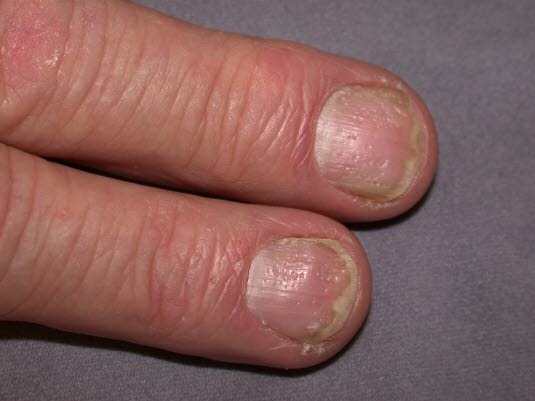 Grübchen oder Tüpfelnägel
Grübchen oder Tüpfelnägel - Nagelbettpsoriasis mit „Ölfleck“ (subunguales parakeratotisches Schuppenmaterial) und ggf. Onycholysis psoriatica (Abhebung des Nagels vom Nagelbett durch subunguales parakeratotisches Schuppenmaterial)
- psoriatischer Krümelnagel (Extremvariante der Nagelpsoriasis)
- Nagelmatrixpsoriasis mit Grübchen (Tüpfelnägel)
- akute Nagelpsoriasis
- Bei etwa 40–50 % aller Patient*innen mit Psoriasis bzw. bei 70–80 % aller Patient*innen mit Psoriasisarthritis40
- Allgemeinmaßnahmen39
- Provokationsfaktoren (aggressive Maniküre oder Pediküre, Manipulationen am Nagelhäutchen) meiden.
- Nägel kurz schneiden, insbes. bei Patient*innen, die in Beruf/Haushalt/Hobby mit manuellen Tätigkeiten konfrontiert sind.
- Vor dem Schneiden Nägel waschen und einfetten (z. B. Linola Fettsalbe), damit sie weniger splittern.
- Falls erforderlich, brüchige Nägel erst nach lauwarmem Öl- oder Teerbad (Linola Fett Ölbad, Balneum Hermal Ölbad) schneiden.
- Querrillen oder verdickte Nägel von erfahrenen medizinischen Fußpfleger*innen abfräsen lassen.
- Leichtes, weites Schuhwerk tragen, das nicht auf die betroffenen, verformten Fußnägel drückt.
- Künstliche Fingernägel sind als optische Verschönerung möglich.
- Externe Therapie39
- leichte Form: Calcipotriol Lösung/Salbe 1 x/d, vorzugsweise abends, möglichst okklusiv (Fingerlinge, Handschuhe) für mindestens 4–6 Monate
- alternativ: topische Glukokortikoide z. B. Mometason-Lösung/Fettcreme oder Lokalbehandlung mit 0,1-%-Tazaroten-Creme/Gel in gleicher Weise wie Calcipotriol
- schwere Form: lokaler Einsatz von 1-%-5-Fluorouracil oder Lösung mit 1-%- 5-Fluorouracil + Salicylsäure oder Harnstoff (Off-Label-Use). Lösung 1 x/d auftragen, anschließend Okklusivverband.
- alternativ: intraläsionale Injektionen von Glukokortikoiden
- Systemische Therapie39
- bei schwerer therapieresistenter Form: Fumarsäureester, Ciclosporin A, Acitretin oder Biologika
Psoriasis guttata
- Suche und Sanierung eines möglichen Infekts41
- z. B. Rachen-Abstrich auf Streptokokken
- Bei rezidivierender Psoriasis guttata kann Tonsillektomie erwogen werden, Ergebnisse sind jedoch widersprüchlich.7,42
- Therapie der Wahl: Dithranol-Lokaltherapie41
Psoriasis inversa
- Durch Lage in Körperfalten und ständige Mazeration häufig Superinfektion mit Kandida
- Die Therapie erfolgt oft als Kombinationstherapie mit Klasse-I- bis Klasse-II-Steroiden und hefepilzhemmenden Wirkstoffen.
- z. B. Hydrocortisonbutyrat in Kombination mit Miconazol oder Econazol
- Ein Kombinationspräparat, z. B. mit Hydrocortison und Miconazol oder mit Triamcinolon und Econazol, kann ebenfalls angewendet werden.
- Bei nässenden Superinfektionen Versuch lokaler Desinfektionsmaßnahmen
- Alternativ: UVB-Bestrahlung
- Calcineurininhibitoren können wirksam sein, sind jedoch off label.
Große Plaques, bei denen keine topische Therapie möglich ist (> 10 % der Körperoberfläche bzw. BSA > 10)
- Behandlung durch Dermatolog*in
- Therapie der Wahl: UV-B-Bestrahlung
- Alternativ: systemische Retinoide, Methotrexat, PUVA, Ciclosporin, Biologika
Generalisierte pustulöse Psoriasis
- Potenziell lebensbedrohliche Maximalvariante der Psoariasis43
- Erythrodermie mit Fieber, Bildung steriler Pusteln, starkem Krankheitsgefühl
- Einweisung ins Krankenhaus; schnelle und aggressive Therapie mit Immunsuppressiva erforderlich
Schwangere mit Psoriasis
- Risiko einer unbehandelten Psoriasis muss gegen mögliche Schädigung des Fetus durch Medikamente abgewogen werden.7
- Bei Frauen, die Empfängnis planen oder für die Therapie im 2. oder 3. Trimenon der Schwangerschaft erforderlich wird, kann Certolizumab-Pegol als Therapie der 1. Wahl empfohlen werden (wenn Behandlung mit Biologikum als essenziell erachtet wird).7
- In jedem Fall interdisziplinäre Betreuung unter Einbindung eines/einer Geburtsmediziner*in/Gynäkolog*in mit Erfahrung in diesem Bereich empfohlen7
Kinder und Jugendliche
Leitlinie: Therapie der Psoriasis bei Kindern und Jugendlichen44
Basistherapie
- „Wird empfohlen“ (höchster Empfehlungsgrad)
- Calcipotriol, zugelassen ab 6 Jahren
- Tacalcitol, zugelassen ab 12 Jahren
- „Kann empfohlen werden“
- Calcineurin-Inhibitoren bei Befall von Gesicht und/oder Intertrigines; cave: Off-Label-Use!
- „Kann erwogen werden bei nicht ausreichendem Therapieerfolg, Unverträglichkeit, Kontraindikation gegenüber anderen topischen Therapieoptionen“
- Tazaroten
- Dithranol (ambulant)
Systemische Therapie bei (mittel)schwerer Psoriasis
- „Wird empfohlen“ (höchster Empfehlungsgrad)
- Acitretin (nur für pustulöse Formen, bei weiblichen Jugendlichen nur im Ausnahmefall)
- Adalimumab (Anti-TNF-alpha), zugelassen ab 4 Jahren
- MTX
- „Wird empfohlen bei nicht ausreichendem Therapieerfolg, Unverträglichkeit, Kontraindikation von Adalimumab oder MTX“
- Etanercept (Anti-TNF-alpha), zugelassen ab 6 Jahren
- Ustekinumab (Anti-IL-12/23), zugelassen ab 12 Jahren
- „Kann empfohlen werden bei nicht ausreichendem Therapieerfolg, Unverträglichkeit, Kontraindikation von Adalimumab oder MTX“
- Ciclosporin
- Fumarsäurerester
- „Kann erwogen werden bei nicht ausreichendem Therapieerfolg, Unverträglichkeit, Kontraindikation anderer systemischer Therapieoptionen“
- Apremilast (PDE-4-Hemmer, orale Einnahme)
- Brodalumab (Anti-IL-17)
- Certolizumab-Pegol (Anti-TNF-alpha)
- Guselkumab (Anti-IL-23)
- Infliximab (Anti-TNF-alpha)
- Ixekizumab (Anti-IL-17)
- Secukinumab (Anti-IL-17)
Prävention
- Es gibt keine Belege dafür, dass eine Therapie mit Penicillin bei Streptokokkeninfektionen des Rachens den Verlauf einer Psoriasis guttata beeinflusst.42
- Langzeitergebnisse nach Tonsillektomie widersprüchlich42
- Aufgrund des Köbner-Phänomens ist es wichtig, Hauttraumata zu vermeiden.
- Adäquater Sonnenschutz, um Sonnenbrand zu vermeiden, insbesondere bei Einsatz photosensibilisierender Verfahren.
- UV-Licht-Exposition durch Sonnenbad in klimatisch günstigen Regionen (z. B. am Toten Meer) als Bestandteil einer Klimatherapie kann allerdings auch positive Effekte haben.7
- Häufig werden folgende Änderungen des Lebensstils empfohlen:
- Gewichtsreduktion
- Raucherentwöhnung
- kein oder maximal moderater Alkoholkonsum
- Stressmanagement.17
Verlauf, Komplikationen und Prognose
Verlauf
- Chronisch-entzündliche Hauterkrankung mit sehr unterschiedlichen klinischen Bildern und häufig schwankendem Krankheitsverlauf45
Komplikationen
- Erythrodermie
- Psoriasis pustulosa
- Arthritis psoriatica
- Psychische Reaktionen
- Auch bei Patient*innen mit weniger schwerer Erkrankung können Depression, Angst, sexuelle Dysfunktion, geringes Selbstwertgefühl und Suizidgedanken als Reaktion auf die Erkrankung auftreten.7,17,46
- Das Risiko für psychische Erkrankungen bei Patient*innen mit Psoriasis ist im Vergleich zur Allgemeinbevölkerung erhöht (HR 1,75).47
- Am stärksten ist das Risiko erhöht für bipolare Störungen (HR 2,33) und Persönlichkeitsstörungen (HR 2,06).
- Krebserkrankung
- Leicht erhöhtes Risiko, an nichtmelanotischen Hautkrebsformen und Lymphomen zu erkranken.48
- Herz-Kreislauf-Erkrankungen
- erhöhtes Risiko für Herz-Kreislauf-Erkrankungen
- bei Patient*innen > 65 Jahren mit leichter Psoriasis um ca. 20 % erhöht
- bei Patient*innen < 50 Jahren mit schwerer Psoriasis doppelt so hoch49
- Das Risiko, an kardiovaskulären Erkrankungen zu erkranken, ist bei Patient*innen, die mit biologischen Präparaten oder Methotrexat behandelt werden, im Vergleich zu anders behandelten Patient*innen wahrscheinlich geringer.50
- erhöhtes Risiko für Herz-Kreislauf-Erkrankungen
- AIDS kann zu explosionsartiger Entwicklung von Psoriasis führen.
- Schwere Infektionen
Prognose
- Psoriasis kann Lebensqualität erheblich reduzieren.52
- Leichte Formen sind ohne Einfluss auf die Lebenserwartung, schwere Formen reduzieren die Lebenserwartung.53
- bei Männern um 3,5 Jahre
- bei Frauen um 4,4 Jahre
- Psoriasisläsionen hinterlassen in der Regel keine Narben.
- 'Die Krankheit tendiert nach Remissionen stark zu Rezidiven.
- Die akute Psoriasis guttata klingt häufig vollständig ab, Patient*innen entwickeln später im Leben jedoch häufig Psoriasis vulgaris.
Verlaufskontrolle – Behandlungskonzept
- Chronische Erkrankung
- Patient*innen sollten regelmäßig von Ärzt*innen begleitet werden.
- Häufig ist eine Zusammenarbeit zwischen Hausärzt*innen und Dermatolog*innen notwendig.
- Bei neu diagnostizierter Psoriasis sind regelmäßige Kontrollen notwendig, um eine effektive und akzeptable Therapie zu finden und die Patient*innen zu schulen.
- Bei Beschwerden am Bewegungsapparat immer die Möglichkeit einer Arthritis psoriatica in Betracht ziehen.3
Patienteninformationen
Worüber sollten Sie die Patient*innen informieren?
- Schulung zum Umgang mit Erkrankung und Anwendung der topischen Medikamente, insbesondere Abtragen der Schuppen vor Applikation, um einen Wirkverlust zu verhindern.
- Ärztliche Konsultation, wenn Probleme mit Therapie oder Exazerbationen auftreten.
- Meidung von beeinflussbaren, exogenen Triggerfaktoren
- Betablocker, Kalzium-Kanal-Blocker, Glukokortikoide (inbesondere nach Absetzen oder Reduktion einer Therapie), Lithium, Antimalariamittel (z. B. Chloroquin), NSAR (Naprofen, Diclofenac, Indometacin), verschiedene Antibiotika (z. B. Makrolide)
- mechanische Traumata, Dermatitis solaris, irritative Lokaltherapien, Infekte (z. B. Streptokokkenangina), emotionale Belastungen
Patienteninformationen in Deximed
Patientenorganisationen
- Netzwerk für Menschen mit Schuppenflechte und Psoriasisarthritis
- Psoriasis Selbsthilfe Arbeitsgemeinschaft e. V. (PSOAG)
Illustrationen
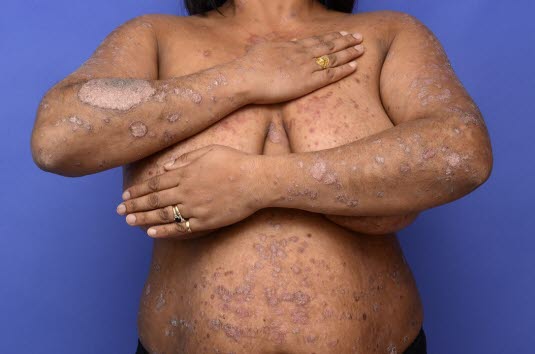
Die Psoriasis befällt vor allem die Streckseiten; in der Regel sind Handflächen, Fußsohlen und Gesicht nicht betroffen.

Die primären Hautveränderungen bei einer Psoriasis sind scharf begrenzte, erythematöse Plaques, die mit dicken, weißen oder silbrig glänzenden, stearinartigen, teilweise festsitzenden Schuppen bedeckt sind.

Vor allem die Streckseiten werden von Psoriasis befallen. Knie, Ellenbogen und Kopfhaut sind die häufigsten Lokalisationen.
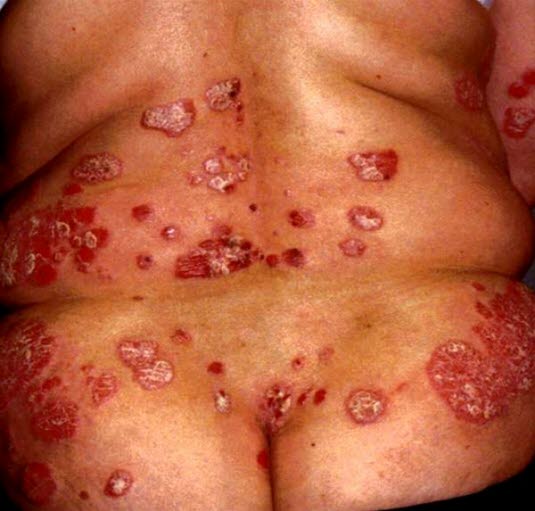
Typisches Aussehen bei Psoriasis vulgaris. Das Bild zeigt multiple gut definierte, erythematöse Plaques mit unterschiedlichem Grad der Infiltration und Schuppenbildung.
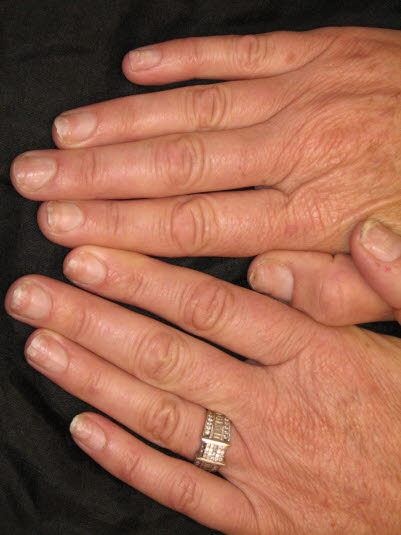
Etwa die Hälfte der Patient*innen mit Psoriasis entwickeln nach einer gewissen Erkrankungsdauer Nagelveränderungen.

Onycholyse: Der Nagel löst sich vom Nagelbett; dies ist bei Psoriasis nicht selten.

Grübchen oder Tüpfelnägel (punktförmige Vertiefungen) sind bei Psoriasis fast pathognomonisch.

Tüpfelnägel

Die Psoriasis pustulosa oder Pustulosis palmoplantaris ist durch Pusteln in den Handflächen und an den Fußsohlen gekennzeichnet. Die Erkrankung wird von manchen als eine Sonderform der Psoriasis, von anderen als eine eigenständige, aber verwandte Erkrankung betrachtet.

Psoriasis guttata bricht häufig nach einer Infektion der oberen Atemwege aus. Die Variante ist durch weit verbreitete, erythematöse, kleine, schuppende Papeln an Rumpf, Armen und Beinen gekennzeichnet.

Die Psoriasis inversa führt zu beugeseitigen Hautveränderungen und affiziert vor allem intertriginöse Bereiche wie die Glutealfalte, die Axillae und die Glans penis. In diesen Bereichen tritt häufig keine Schuppung auf.

Erythrodermische Psoriasis
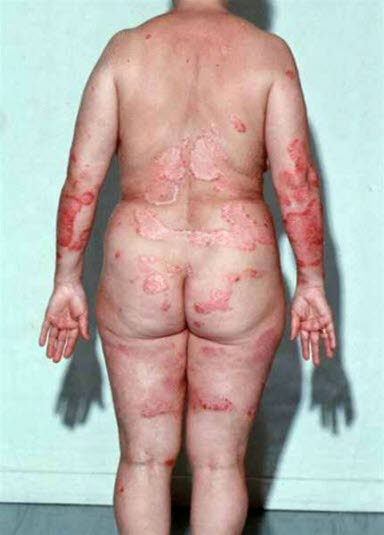
In den meisten Fällen ist eine topische Therapie ausreichend. Patient*innen mit (mittel)schweren Formen benötigen jedoch eine systemische oder Phototherapie.
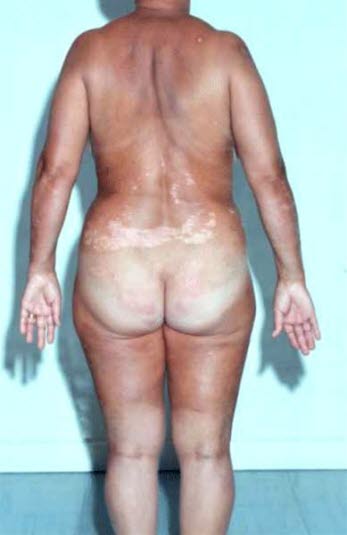
Hauttraumata wie Sonnenbrände können die Psoriasis verschlimmern und sind daher zu vermeiden.
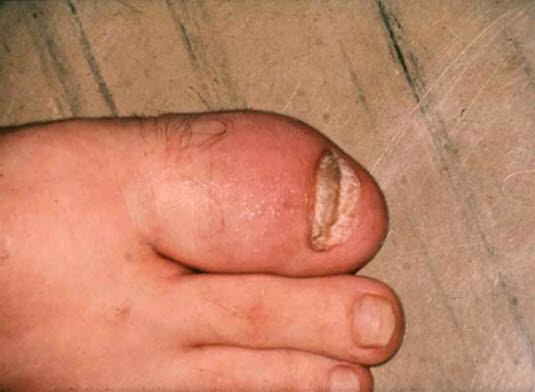
7–40 % der Patient*innen mit Psoriasis entwickeln eine Arthritis; diese entsteht meist ca. 10 Jahre nach Beginn der Hautkrankheit.
Quellen
Leitlinien
- Deutsche Dermatologische Gesellschaft (DDG). Therapie der Psoriasis vulgaris. AWMF-Leitlinie Nr. 013-001. S3, Stand 2021. www.awmf.org
- Appendix A: Topische Therapie, Phototherapie, Sonstige Therapien, Schnittstellendefinition, Fortbestand der Empfehlungen vom Update 2015.
- Deutsche Dermatologische Gesellschaft e. V. (DDG). Therapie der Psoriasis bei Kindern und Jugendlichen. AWMF-Leitlinie Nr. 013–094. S2k, Stand 2019. www.awmf.org
- Deutsche Dermatologische Gesellschaft (DDG). Psychosomatische Dermatologie (Psychodermatologie). AWMF-Leitlinie Nr. 013-024. S1, Stand 2018. www.awmf.org
Literatur
- Altmeyer P. Psoriasis (Übersicht). Enzyklopädie Dermatologie. Springer. Stand 07.01.2021. Letzter Zugriff 28.05.2021. www.enzyklopaedie-dermatologie.de
- Altmeyer P. Psoriasis arthropathica. Enzyklopädie Dermatologie. Springer. Stand 05.03.2021. Letzter Zugriff 28.05.2021. www.enzyklopaedie-dermatologie.de
- Mease P, Goffe BS. Diagnosis and treatment of psoriatic arthritis. J Am Acad Dermatol 2005; 52: 1-19. www.ncbi.nlm.nih.gov
- Lebwohl M. Psoriasis. Lancet 2003; 361: 1197-204. www.ncbi.nlm.nih.gov
- Luba KM, Stulberg DL. Chronic plaque psoriasis. Am Fam Physician 2006; 73: 636-44. www.ncbi.nlm.nih.gov
- Smith CH, Barker JNWN. Psoriasis and its management. BMJ 2006; 333: 380-4. www.ncbi.nlm.nih.gov
- Deutsche Dermatologische Gesellschaft (DDG). Therapie der Psoriasis vulgaris. AWMF Leitlinie Nr. 013-001. S3. Stand 2021. www.awmf.org
- Patrisi R, Symmons DP, Griffiths CE, et al. Global epidemiology of psoriasis: a systematic review of incidence and prevalence. J Invest Dermatol 2013; 133: 377-85. www.ncbi.nlm.nih.gov
- Gelfand JM, Stern RS, Nijsten T, et al. The prevalence of psoriasis in African Americans: results from a population-based. J Am Acad Dermatol. J Am Acad Dermatol 2005; 52: 23-26. www.ncbi.nlm.nih.gov
- Giardina E, Sinibaldi C, Novelli G. The psoriasis genetics as a model of complex disease. Curr Drug Targets Inflamm Allergy 2004; 3: 129-36. www.ncbi.nlm.nih.gov
- Altmeyer P. Psoriasis vulgaris. Enzyklopädie Dermatologie. Springer. Stand 07.01.2021. Letzter Zugriff 28.05.2021. www.enzyklopaedie-dermatologie.de
- Naldi L. Epidemiology of psoriasis. Curr Drug Targets Inflamm Allergy 2004; 3: 121-8. www.ncbi.nlm.nih.gov
- Asadullah K, Volk H-D, Sterry W. Novel immunotherapies for psoriasis. Trends Immunol 2002; 23: 47-53. www.ncbi.nlm.nih.gov
- Schön MP, Boehncke WH. Psoriasis. N Engl J Med 2005; 352: 1899-912. New England Journal of Medicine
- Ozawa M, Aiba S. Immunopathogenesis of psoriasis. Curr Drug Targets Inflamm Allergy 2004; 3: 137-44. www.ncbi.nlm.nih.gov
- Philipp S, Wolk K, Kreutzer S, et al. The evaluation of psoriasis therapy with biologics leads to a revision of the current view of the pathogenesis of this disorder. Expert Opin Ther Targets 2006; 10: 817-831. www.ncbi.nlm.nih.gov
- Deutsche Dermatologische Gesellschaft (DDG). Psychosomatische Dermatologie (Psychodermatologie). AWMF Leitlinie Nr. 013-024. S1. Stand 2018. www.awmf.org
- Habashy J. Psoriasis. Medscape, last updated Mar 17, 2021. emedicine.medscape.com
- Gladmann DD; Antoni C, Mease P, et al. Psoriatic arthritis: epidemiology, clinical features, course, and outcome. Ann Rheum Dis 2005; 64: 14-7. ard.bmj.com
- Mallbris L, Akre O, Granath F, Yin L, Lindelof B, Ekbom A, et al. Increased risk for cardiovascular mortality in psoriasis inpatients but not in outpatients. Eur J Epidemiol 2004; 19: 225-30. www.ncbi.nlm.nih.gov
- Ryan C, Menter A. Psoriasis and cardiovascular disorders. G Ital Dermatol Venereol 2012; 147: 189-202. pmid:22481581 PubMed
- Boffetta P. Cancer risk in a population-based cohort of patients hospitalised for psoriasis in Sweden. J Invest Dermatol 2001; 117: 1531-7. www.sciencedirect.com
- Gelfand JM, Berlin J, Van Voorhees A, Margolis DJ. Lymphoma rates are low but increased in patients with psoriasis: results from a population-based cohort study in the United Kingdom. Arch Dermatol 2003; 139: 1425-9. www.ncbi.nlm.nih.gov
- Al-Suwaidan SN, Feldman SR. Clearance is not a realistic expectation of psoriasis treatment. J Am Acad Dermatol 2000; 42: 796-802. www.ncbi.nlm.nih.gov
- Augustin M, Eissing L, Langenbruch A. The German National Program on Psoriasis Health Care 2005–2015: results and experiences. Arch Dermatol Res (2016) 308: 389. doi:10.1007/s00403-016-1637-8 DOI
- Lapolla W, Yentzer BA, Bagel J, et al. A review of phototherapy protocols for psoriasis treatment. J Am Acad Dermatol. 2011; 64: 936-949. www.ncbi.nlm.nih.gov
- Stern RS. Psoralen and ultraviolet A light therapy for psoriasis. N Engl J Med 2007; 357: 682-90. www.ncbi.nlm.nih.gov
- Psoriasis-Netz. Psoriasis Selbsthilfe Arbeitsgemeinschaft (PSOAG). Grenzstrahlung. 10/2016. www.psoriasis-netz.de
- Montaudie H, Sbidian E, Paul C, et al. Methotrexate in psoriasis: a systematic review of treatment modalities, incidence, risk factors and monitoring of liver toxicity. J Europ Acad Dermatol Venereol. 2011;25(suppl 2):12-18. www.ncbi.nlm.nih.gov
- Griffiths CE, Clark CM, Chalmers RJ, Li Wan Po A, Williams HC. A systematic review of treatments for severe psoriasis. Health Technol Assess 2000; 4: 1-125. www.ncbi.nlm.nih.gov
- Maza A, Montaudie H, Sbidian E, et al. Oral cyclosporin in psoriasis: a systematic review on treatment modalities, risk of kidney toxicity and evidence for use in non-plaque psoriasis. J Euro Acad Dermatol Venereol. 2011;25(suppl 2):19-27. www.ncbi.nlm.nih.gov
- Fachinformation Neotigason. Stand 2017. Letzter Zugriff 30.05.2021. s3.eu-central-1.amazonaws.com
- GBA. Nutzenbewertungsverfahren zum Wirkstoff Dimethylfumarat (neues Anwendungsgebiet: Psoriasis vulgaris). Beschlussfassung 16.03.2018. www.g-ba.de
- Mason AR, Mason J, Cork M. Topical treatments for chronic plaque psoriasis. Cochrane Database of Syst Rev 2013; 3: CD005028. doi:10.1002/14651858.CD005028.pub3. DOI
- Samarasekera EJ, Sawyer L, Wonderling D, et al. Topical therapies for the treatment of plaque psoriasis: systematic review and network meta-analyses. British Journal of Dermatology 2013; 168: 954-67. doi:10.1111/bjd.12276 DOI
- Altmeyer P. PUVA-Therapie. Enzyklopädie Dermatologie. Springer 2017 www.enzyklopaedie-dermatologie.de
- Wang C, Lin A. Efficacy of topical calcineurin inhibitors in psoriasis. J Cutan Med Surg 2014; 18(1): 8-14. www.ncbi.nlm.nih.gov
- Lebwohl M, Freeman AK, Chapman S, Feldman SR, Hartle JE, Henning A. Tacrolimus ointment is effective for facial and intertriginous psoriasis. J Am Acad Dermatol 2004; 51: 723-30. www.ncbi.nlm.nih.gov
- Altmeyer P. Psoriasis der Nägel. Enzyklopädie Dermatologie. Springer. Stand 30.09.2019. Letzter Zugriff 29.05.2021. www.altmeyers.org
- Langenbruch A, Radtke MA, Krensel M, Jacobi A, Reich K, Augustin M. Nail involvement as a predictor of concomitant psoriatic arthritis in patients with psoriasis. Br J Dermatol. 2014 Nov. 171(5):1123-8. www.ncbi.nlm.nih.gov
- Altmeyer P. Psoriasis guttata. Enzyklopädie Dermatologie. Springer. Stand 22.12.2020. Letzter Zugriff 30.05.2021. www.altmeyers.org
- Owen CM, Chalmers RJG, O'Sullivan T, Griffiths CEM. Antistreptococcal interventions for guttate and chronic plaque psoriasis. Cochrane Database of Syst Rev. 2000;2:CD001976. DOI:10.1002/14651858.CD001976 DOI
- Orphanet. Portal für seltene Krankheiten. Generalisierte pustulöse Psoriasis. Letzter Zugriff 30.05.2021. www.orpha.net
- Deutsche Dermatologische Gesellschaft e.V. (DDG). Therapie der Psoriasis bei Kindern und Jugendlichen. AWMF-S2k-Leitlinie Nr. 013 - 094. Stand 2019. www.awmf.org
- Green MS, Prystowsky JH, Cohen SR, Cohen JI, Lebwohl MG. Infectious complications of erythrodermic psoriasis. J Am Acad Dermatol 1996; 34: 911-14. www.ncbi.nlm.nih.gov
- Russo PA, Ilchef R, Cooper AJ. Psychiatric morbidity in psoriasis: a review. Australas J Dermatol 2004; 45: 155-61. www.ncbi.nlm.nih.gov
- Leisner MZ, Riis JL, Schwartz BS et al. Psoriasis and Risk of Mental Disorders in Denmark. JAMA Dermatol 2019.0039 pmid:31066861. www.ncbi.nlm.nih.gov
- Margolis D, Bilker W, Hennessy S, et al. The risk of malignancy associated with psoriasis. Arch Dermatol 2001; 137: 778-83. www.ncbi.nlm.nih.gov
- Ahlehoff O, Gislason GH, Charlot M et al. Psoriasis is associated with clinically significant cardiovascular risk: a Danish nationwide cohort study. J Intern Med 2011; 270: 147-57. www.ncbi.nlm.nih.gov
- Ahlehoff O, Skov L, Gislason G, et al. Cardiovascular disease event rates in patients with severe psoriasis treated with systemic anti-inflammatory drugs: a Danish real-world cohort study. J Intern Med 2012. doi:10.1111/j.1365-2796.2012.02593.x DOI
- Li X, Andersen KM, Chang H-Y, et al. Comparative risk of serious infections among real-world users of biologics for psoriasis or psoriatic arthritis. Ann Rheum Dis 2019. pmid:31672774. www.ncbi.nlm.nih.gov
- Hammadi AA. Psoriatic arthritis. Medscape, last updated Dec 11, 2014. emedicine.medscape.com
- Gelfand JM, Troxel AB, Lewis JD, et al. The risk of mortality in patients with psoriasis: results from a population-based study. Arch Dermatol 2007; 143(12): 1493-9. pubmed.ncbi.nlm.nih.gov
Autor*innen
- Lino Witte, Dr. med., Arzt in Weiterbildung, Innere Medizin, Frankfurt
- Die ursprüngliche Version dieses Artikels basiert auf einem entsprechenden Artikel im norwegischen hausärztlichen Online-Handbuch Norsk Elektronisk Legehåndbok (NEL, https://legehandboka.no/).