Zusammenfassung
- Definition:Der Begriff der Knotenstruma umfasst das gesamte Spektrum von kleinen, solitären Schilddrüsenknoten bis hin zu großen intrathorakalen Strumen. Lange liegt eine euthyreote Stoffwechsellage vor, die jedoch in einen hyperthyreoten Zustand umschlagen kann.
- Häufigkeit:Bei der überwiegenden Zahl der Strumen handelt es sich um mehrknotige Strumen. In Jodmangel-Gebieten haben ca. 30 % der Erwachsenen eine euthyreote Struma und ca. 20 % eine Knotenstruma.
- Symptome:Im frühen Stadium zeigen sich meist keine Symptome. Im weiteren Verlauf kann eine Struma klinisch sichtbar werden (ab ca. 40 ml Volumen). Es kann sich eine Hyperthyreose entwickeln. Bei sehr großen Strumen können Kompressionssymptome auftreten.
- Befunde:Als klinischer Befund liegt eine Struma vor. Knoten können tastbar sein.
- Diagnostik:Als Basisdiagnostik TSH-Bestimmung und Sonografie. Bei speziellen Auffälligkeiten in dieser Untersuchung ggf. Szintigrafie, eine Feinnadelaspirationszytologie/Feinnadelbiopsie sowie evtl. eine CT oder MRT.
- Therapie:Kontrolle, ggf. befristet Jodid und/oder Schilddrüsenhormongabe, eine operative Therapie oder Radiojodtherapie.
Prüfungsrelevant für die Facharztprüfung Allgemeinmedizin1
Allgemeine Informationen
Definition
- Von einer Struma spricht man, sobald das Schilddrüsenvolumen oberhalb des geschlechts- und altersspezifischen Normbereichs liegt.2
- Bei Frauen bedeutet dies ein Schilddrüsenvolumen > 18 ml, bei Männern > 25 ml.
- Eine Struma stellt lediglich ein Symptom dar.2
- Sie hat vielfältigste Ursachen und Morphologien und kann mit einer euthyreoten, hyperthyreoten oder hypothyreoten Stoffwechsellage einhergehen.
- Eine Struma kann sich als Struma diffusa (simplex) ohne Knoten, als Struma uninodosa oder multinodöse Struma sowie als Struma nodosa colloides (zystische Knoten/Zysten) präsentieren.
- Der Begriff der Knotenstruma umfasst das gesamte Spektrum von kleinen, solitären Schilddrüsenknoten bis hin zu großen intrathorakalen Strumen, die neben kosmetischen Auffälligkeiten auch mechanische Kompressionssymptome verursachen können.
- Meist liegt über einen langen Zeitraum eine euthyreote Stoffwechsellage vor (atoxische Knotenstruma), die jedoch in einen hyperthyreoten Zustand umschlagen kann (toxische Knotenstruma). Hypothyreot werden Patient*innen nur in Ausnahmefällen.
Karzinomrisiko?
- Das Karzinomrisiko wird in der älteren Literatur auf etwa 3–5 % beziffert und ist unabhängig davon, ob in der Schilddrüse ein solitärer Knoten oder mehrere Knoten vorliegen.3-4
- Dies bezieht alle, auch klinisch nicht relevante histologisch nachgewiesene Mikrokarzinome ein.5
- Neuere Studien legen eine wesentlich niedrigere Rate an klinisch relevanten Schilddrüsenmalignomen nahe und betonen das Risiko einer Überdiagnose.6-8
- Prävalenz von Schilddrüsenkarzinomen in Deutschland: 4 von 100.000 Männern bzw. 9 von 100.000 Frauen, wobei die Erkrankungsrate hauptsächlich aufgrund vermehrter Diagnostik zugenommen hat, die Sterberate jedoch konstant für beide Geschlechter bei unter 1 zu 100.000 geblieben ist.9
- Nach Schätzungen der IRAC (Internationale Agentur für Krebsforschung) beträgt in allen untersuchten Ländern der Anteil der Überdiagnosen von Schilddrüsenkarzinomen bei Frauen zwischen 40 % (Japan) und 83 % (Südkorea).6
- Einziger gesicherter, wenn auch vergleichsweise selten auftretender umweltbezogener Risikofaktor ist die Exposition gegenüber ionisierender Strahlung, vor allem im Kindesalter.9
- So hat die Aufnahme von radioaktivem Jod, z. B. nach dem Reaktorunfall von Tschernobyl, das Risiko für Schilddrüsenkrebs in den damaligen betroffenen Sowjetrepubliken erhöht.
- Das Risiko ist ebenfalls erhöht bei einer Strahlentherapie, wenn die Schilddrüse im Strahlenfeld liegt.
- Genetische Faktoren gibt es beim medullären Schilddrüsenkarzinom.
- Siehe auch den Artikel Schilddrüsenkarzinom.
Häufigkeit
- Schilddrüsenvergrößerung und Schilddrüsenknoten sind häufige Befunde in der Allgemeinbevölkerung.
- Bei der überwiegenden Zahl der großen Strumen handelt es sich um mehrknotige Strumen.
- In der 2003 publizierten ersten Untersuchung der „Study of Health in Pomerania"-(SHIP-)Kohorte wurden bei 35,9 % der 3.941 Proband*innen mit bislang nicht bekannter Schilddrüsen(SD)-Erkrankung eine Struma und bei 20,2 % der Proband*innen SD-Knoten nachgewiesen.2
- In der Papillon-Studie, in der 96.278 Werktätige ohne vorbekannte SD-Erkrankung untersucht wurden, lag die Knotenprävalenz bei 23,3 % und die Strumaprävalenz bei 9,7 %.2
- Schilddrüsenknoten können mithilfe der Sonografie bei rund 20 % der 20- bis 79-Jährigen in Deutschland nachgewiesen werden.10
- Struma- und Knotenprävalenz korrelieren eng mit der Jodversorgung der Bevölkerung.
- In Jodmangel-Gebieten haben ca. 30 % der Erwachsenen eine euthyreote Struma. In der SHIP-Studie hatten ca. 20 % eine Knotenstruma. Knoten treten auch in nicht vergrößerten Schilddrüsen auf, allerdings deutlich seltener.
- In der Verlaufsuntersuchung der SHIP-Kohorte zeigte sich ein Rückgang von Struma und Knotenprävalenz infolge einer verbesserten Jodversorgung.2
- Geschlecht
- Das Verhältnis zwischen betroffenen Frauen und Männern liegt bei der Struma im Bereich von 5:1 bis 10:1.
Ätiologie und Pathogenese
- Die Ursachen, die zur Entwicklung einer Struma führen, sind komplex und von mehreren Faktoren abhängig.
- Die genetische Prädisposition und Umweltfaktoren spielen eine wichtige Rolle.11
- Ursachen einer Schilddrüsenvergrößerung2
- Struma diffusa
- Struma nodosa (uni-/multinodosa)
- Schilddrüsen-Malingom (selten)
- Autoimmunthyreoiditis (M. Hashimoto oder M. Basedow)
- Thyreoiditis de Quervain
- Riedelstruma (eisenharte, fibrotische Struma)
- Zyste(n)
- Schilddrüsenhormon-Synthesestörung und Schilddrüsenhormon-Resistenz (TSH-getriggerte Struma)
- Akromegalie (IGF-1-bedingt)
- Medikamente (Lithium, Amiodaron, Thyreostatika)
- TSH-bildende Hypophysenadenome (selten)
- Die Strumabildung beginnt mit einer uniformen Hypertrophie und Hyperplasie der Thyreozyten, was klinisch als diffuse Struma bezeichnet wird.
- Bei großen Strumen zeigt sich meist ein heterogeneres Bild mit fokaler Follikelhypertrophie und -hyperplasie, Fibrose, kleinen Blutungen und Kolloidzysten.
- Die molekularbiologische Ursache für die Entwicklung von Schilddrüsenknoten und -adenomen besteht vermutlich in einer verstärkten Expression von Wachstumsfaktoren und -rezeptoren sowie somatischen Mutationen des TSH-Rezeptorgens.12
- Dies kann zu einer Proliferation von Thyreozyten und einer funktionellen Autonomie führen, wodurch es wiederum zu einer subklinischen oder manifesten Hyperthyreose kommen kann.11
- Das Wachstum und die evtl. gleichzeitige Entwicklung einer Hyperthyreose erfolgen langsam über einen Zeitraum vieler Jahre oder Jahrzehnte, und in der Regel gibt es eine Phase, in der eine subklinische Hyperthyreose vorliegt. Dies wird dann als toxische Knotenstruma bezeichnet. Zur Entwicklung einer Hypothyreose kommt es nur selten.
Prädisponierende Faktoren
- Jodmangel13
- Gilt als wichtigste und gleichzeitig vermeidbare Ursache einer Struma.2
- Die Struma simplex ist in bestimmten Regionen der Erde weiterhin endemisch.
- Erkrankungsfälle in der Familie
- Es lässt sich jedoch nicht sagen, ob hierbei genetische oder umweltbezogene Faktoren ausschlaggebend sind.11
- Weibliches Geschlecht
- 10- bis 15-fach höhere Prävalenz
- Auswirkung von Wachstumsfaktoren in der Schwangerschaft
- Diskutiert werden zudem:2
- Rauchen
- natürlich vorkommende strumigene Faktoren
- Selenmangel
- Zinkmangel
- Eisenmangel
- emotionaler Stress.
ICPC-2
- T81 Struma
ICD-10
- E01 Jodmangelbedingte Schilddrüsenkrankheiten und verwandte Zustände
- E01.0 Jodmangelbedingte diffuse Struma (endemisch)
- E01.1 Jodmangelbedingte mehrknotige Struma (endemisch)
- E01.2 Jodmangelbedingte Struma (endemisch), nicht näher bezeichnet
- E01.8 Sonstige jodmangelbedingte Schilddrüsenkrankheiten und verwandte Zustände
- E04 Sonstige nichttoxische Struma
- E04.0 Nichttoxische diffuse Struma
- E04.1 Nichttoxischer solitärer Schilddrüsenknoten
- E04.2 Nichttoxische mehrknotige Struma
- E04.8 Sonstige näher bezeichnete nichttoxische Struma
- E04.9 Nichttoxische Struma, nicht näher bezeichnet
- E05 Hyperthyreose
- E05.0 Hyperthyreose mit diffuser Struma
- E05.1 Hyperthyreose mit toxischem solitärem Schilddrüsenknoten
- E05.2 Hyperthyreose mit toxischer mehrknotiger Struma
Diagnostik
Diagnostische Kriterien
- Zu den wichtigsten Untersuchungen zählen die klinische Untersuchung von Hals und Schilddrüse, die Bestimmung von TSH sowie die Sonografie.
- Die Diagnose wird bei klinischem Nachweis einer Struma gestellt.
- Die meisten Strumen sind asymptomatisch.
- Evtl. ist die Schilddrüsenloge druckempfindlich.
- Von einer sichtbaren Schilddrüsenvergrößerung ist ab einem Volumen von etwa 40 ml auszugehen.2
- Knoten > 1 cm können evtl. palpiert werden.
- Bei sonografischem Nachweis von Knoten sind auszuschließen:
- Schilddrüsenautonomie?
- bei Eu- oder Hypothyreose unwahrscheinlich
- Schilddrüsenmalignom?
- Schilddrüsenautonomie?
Diagnostikproblem bei Schilddrüsenknoten
- Weder Sonografie, Szintigrafie noch die Feinnadelbiopsie sind geeignet, ein Schilddrüsenkarzinom in einem Schilddrüsenknoten sicher nachzuweisen und können allenfalls Hinweise liefern.
- Wichtig für die Hausärzt*innen ist die Anamnese (Wachstumstendenz? Beschwerden? Familienanamnese? Strahlenexposition?) und die klinische Untersuchung (Lymphknoten? Konsistenz? Verschieblichkeit?).
- Nahezu alle Schilddrüsenknoten sind benigne, auch Knoten > 1 cm!
- Nur wenige Knoten > 1 cm müssen radiologisch/szintigrafisch oder zytologisch/bioptisch weiter abgeklärt werden.
- Da fast alle Schilddrüsenknoten gutartig sind bzw. allenfalls klinisch nichtrelevante Mikrokarzinome enthalten, die sich auf Morbidität und Mortalität nie auswirken würden, besteht durch eine forcierte Diagnostik eine große Gefahr der Überdiagnostik.6-9
- Daraus ergibt sich, dass kein generelles Schilddrüsenscreening angeboten werden sollte.7
- Ist ein Schilddrüsenknoten nachgewiesen, kann eine hausärztliche sonografische Kontrolle in größeren Abständen (initial halb-, dann jährlich, später alle 2–5 Jahre) zur Beruhigung von Patient*in und Untersucher*in beitragen. Sie ist nicht routinemäßig nötig.
- Bei Auftreten von sog. Red Flags sollte die Diagnostik selbstverständlich erweitert werden.
- Z. n. Strahlenexposition
- schnelle Wachstumstendenz
- Lymphknotenvergrößerungen regional
- derbe Konsistenz, fehlende Verschieblichkeit
- sonografisch (sowie ggf. elastografisch) hochverdächtiger Knoten
- positive Familienanamnese
- Vorliegen eines MEN-Syndroms (multiple endokrine Neoplasie)
- Besorgnis der Betroffenen (Shared Decision Making)
Differenzialdiagnosen
- Schilddrüsenkarzinom
- Autoimmunerkrankung der Schilddrüse
- Thyreoiditis
- Hyperthyreose: Kann Teil des Krankheitsbildes sein.
- Hypothyreose: Ist selten Teil des Krankheitsbildes.
Anamnese
- Im frühen Stadium zeigen sich meist keine Symptome. Im weiteren Verlauf ist eine Struma erkennbar, und es kann sich eine Hypo-/Hyperthyreose entwickeln.
- Besteht eine große multinodöse Struma, kommt es relativ häufig zu einer subklinischen oder manifesten Hyperthyreose. 14
- Kompressionssymptome sind zu erfragen.
- Eine schmerzhafte Schilddrüsenloge ist differenzialdiagnostisch bedeutsam (Thyreoiditis?).
- Bei älteren Patient*innen verursacht die Struma u. U. kaum Symptome; sie wird anhand der Bestimmung von TSH und einer Sonografie diagnostiziert.
Wichtige Fragen
- Wie groß ist die Struma?
- Liegen wesentliche mechanische Komplikationen vor: Kompression der Luftröhre?
- Liegt eine Hypo-/Hyperthyreose vor?
- Wie schnell ist die Struma gewachsen?
- Besteht ein Verdacht auf Malignität?
- Zusätzlich kardiopulmonale oder sonstige Erkrankungen?
- Wünschen die Betroffenen eine Behandlung?
Klinische Untersuchung
- Klinische Zeichen einer Schilddrüsenunterfunktion oder -überfunktion?
- Klinisch ist manchmal die Schilddrüse mit unebener und knotiger Oberfläche sichtbar/tastbar.
- Die klinische Untersuchung von Größe, Morphologie und Funktion ist jedoch sehr ungenau.15
- Bei bis zu 50 % der Patient*innen, bei denen ein solitärer Knoten tastbar ist oder eine diffus vergrößerte Schilddrüse vorliegt, werden in der sonografischen Untersuchung multiple Knoten nachgewiesen.16
- Knoten < 1 cm sind in der Regel nur sonografisch nachweisbar.
Schilddrüse
- Beurteilung der Größe der Schilddrüse
- klein: das Ein- bis Zweifache der normalen Größe
- groß: mehr als das Zweifache der normalen Größe
- Form und Konsistenz
- Bewegung beim Schlucken
- Druckschmerz?
- Sind die zervikalen Lymphknoten vergrößert?
- Nach Möglichkeit untere Kante der Schilddrüse identifizieren.
- Gelingt es selbst bei nach hinten gebeugtem Kopf oder beim Schlucken nicht, die untere Kante zu ertasten, deutet dies auf eine intrathorakale Struma hin.
- Bei den meisten Patient*innen mit intrathorakaler Struma liegt auch eine zervikale Struma vor.
Mechanische Komplikationen?
- Infolge einer Trachealkompression kann es zu einer Dyspnoe mit inspiratorischem Stridor kommen.
- Liegen eine Ruhedyspnoe und ein inspiratorischer Stridor vor, deutet dies auf eine erhebliche Trachealkompression hin.
- Ausgehend von spirometrischen Untersuchungen ist die Größe der Struma nicht unbedingt mit dem Ausmaß der respiratorischen Beeinträchtigung assoziiert.17
- Mitunter kann die Spirometrie dabei helfen, zwischen einer strumainduzierten Atemwegsobstruktion und einer Lungenerkrankung zu unterscheiden.
- Die Dyspnoe und eine venöse Stauung können verstärkt werden, indem die Arme angehoben und der Kopf nach hinten gebeugt oder gedreht wird. Dies ist das sog. Pemberton-Zeichen.18
- Alternative Erklärungen für eine Dyspnoe sind:
- kardiopulmonale Erkrankungen, insbesondere bei älteren Patient*innen
- COPD/Asthma
- Hyperthyreose
- Stimmbandparese bei Beteiligung des Nervus recurrens
- akute interkurrente Erkrankungen wie eine progrediente Herzinsuffizienz oder Atemwegsinfektionen.
Ergänzende Untersuchungen in der Hausarztpraxis
Labor
- TSH-Wert, bei Abweichungen von der Norm auch FT4
- Je größer die Struma, desto größer auch das Risiko, dass erniedrigte TSH-Werte und auch eine manifeste Hyperthyreose vorliegen.11
- Die Bestimmung von Schilddrüsenautoantikörpern (Thyreoperoxidase-Antikörper [TPO-Ak] und TSH-Rezeptor-Antikörper [TRAK]) wird nur bei sonografischem Verdacht auf eine Autoimmunthyreopathie oder Vorliegen einer Hyper- oder Hypothyreose empfohlen.2
- Eine Thyreoglobulin-Bestimmung ist bei der Struma nodosa nicht indiziert (Werte i. d. R. erhöht, haben aber keine diagnostische Wertigkeit).2
Sonografie
- Bestimmung der Schilddrüsengröße und Diagnose von Knoten
- Liegt bei euthyreoten Patient*innen eine klinisch und sonografisch diffuse Struma vor, die nicht oder nur langsam wächst, besteht in der Regel keine Indikation für eine weitere bildgebende Diagnostik.
- Befunde eines oder mehrerer kleiner Knoten mit einer Größe von weniger als 1 cm werden für gewöhnlich nicht eingehender untersucht. Davon ausgenommen sind Situationen, in denen der Verdacht auf ein Schilddrüsenkarzinom besteht. Knoten von unter 1 cm Größe können ggf. einmal im Jahr (oder seltener) sonografisch auf ihr Größenwachstum überprüft werden.
- Diagnose von „malignitätsverdächtigen" Knoten, die eine weitere Abklärung mittels Feinnadelzytologie (FNZ) oder die histologische Abklärung erfordern.
- Sonografische Malignitätskriterien von Schilddrüsenknoten:2
- Echoarmut
- Mikrokalzifikationen
- unscharfe Begrenzung/kein Halo-Effekt
- intranoduläre Vaskularisation
- erhöhter Tiefendurchmesser.
- Sonografische Befunde mit Malignitätskriterien gehen mit einer erhöhten Prävalenz von SD-Malignomen einher, jedoch ist die Spezifität jedes einzelnen Ultraschallparameters für die Malignitätsprädiktion gering.2
- Bei Nachweis mehrerer verdächtiger Ultraschallbefunde in einem SD-Knoten wird in der Literatur eine Sensitivität von 83–99 % und eine Spezifität von 56–85 % für das Vorliegen eines SD-Malignoms beschrieben.2
- zur Beurteilung des Malignitätsrisikos und damit einer Operationsindikation können die TIRADS-Kriterien herangezogen werden.19
- Der positiv prädiktive Wert der Schilddrüsensonografie zur Knotenbeurteilung ist gering und erreicht in Kombination mehrerer Ultraschallparameter einen maximalen Wert von 39 %.20Das bedeutet, dass max. 4 von 10 Knoten, die mehrere suspekte Sonokriterien aufweisen, tatsächlich maligne sind, während die anderen 6 von 10 nicht bösartig sind. Auch besteht zusätzlich das Problem der Überdiagnose.
Diagnostik bei Spezialist*innen
- Bei Knoten mit einer Größe von mehr als 1 cm kann nach Abwägung aller Risiken (Strahlenbelastung, Überdiagnostik) und evtl. Vorteile (Detektion von heißen Arealen bei (subklinischer) Hyperthyreose) eine Szintigrafie erwogen werden.21
- Die Szintigrafie liefert keinen Nachweis von Malignität.
- Kalte Knoten sollten weiter mit FNP abgeklärt werden.
- Bei Nachweis einer SD-Autonomie kann auf eine Dignitätsabklärung des Knotens verzichtet werden, da autonome Adenome in aller Regel benigne Tumoren sind.
- Neben der SD-Sonografie und der farbkodierten Duplexsonografie kommt in den letzten Jahren zunehmend die Elastografie in der Differenzialdiagnostik einer Struma nodosa zum Einsatz.2
- Schilddrüsenmalignome zeichnen sich typischerweise durch eine veränderte Gewebekonsistenz aus, die sich durch eine verminderte Komprimierbarkeit in der Elastografie nachweisen lässt.
- Bei Verdacht auf Kompressionssymptome kann eine CT- oder MRT-Untersuchung von Hals und Mediastinum indiziert sein.
Szintigrafie21
- Im Vorfeld einer etwaigen Radiojodtherapie sollte eine Szintigrafie erfolgen, um die Jodaufnahme zu beurteilen.
- Bei einer Szintigrafie der Schilddrüse können anhand des Jod-Uptakes und des Verteilungsmusters kalte und heiße Knoten unterschieden werden.11
- Kalte Knoten, die in der Sonografie nicht echofrei sind (Zysten), können mit der Feinnadelaspirationszytologie resp. Feinnadelpunktion (FNP) abgeklärt werden.
- Bei multinodösen Knotenstrumen ist eine inhomogene Aufnahme in einer vergrößerten Schilddrüse typisch.
- In großen Knotenstrumen sind häufig Bereiche mit geringer Aufnahme und größere oder kleinere „kalte Knoten“ zu beobachten.
- Die Szintigrafie allein kann eine Malignität nicht ausschließen oder nachweisen.
- Heiße Knoten sind jedoch nahezu immer benigne, meist liegt hier eine (ggf. subklinische) Hyperthyreose vor.
- Bei kalten Knoten, die auch sonografisch suspekt erscheinen, ist eine Feinnadeldiagnostik anzuschließen.
Feinnadelzytologie oder -biopsie2
- Bei euthyreoten, szintigrafisch kalten Knoten > 1 cm, die auf der Basis von sonografischen Kriterien als malignitätsverdächtig gelten.
- Cave: Überdiagnostik – Mikrokarzinome, ohne klinische Relevanz!
- Knoten bei Patient*innen mit erhöhtem Malignitätsrisiko (externe Radiatio, positive Familienanamnese)
Indikationen zur Überweisung
- Bei dringendem Verdacht auf Malignität (verdächtige Knoten in der Sonografie, Knoten > 1 cm)
- Bei Anzeichen mechanischer Komplikationen von großer Struma oder großer Knoten
- Wenn eine Behandlung von Patient*in gewünscht wird.
Checkliste zur Überweisung
Schilddrüsenknoten, Struma
- Zweck der Überweisung
- Bestätigende Diagnostik? Operative Therapie?
- Anamnese
- Dauer und Beginn? Ist der Knoten gewachsen?
- Anzeichen einer Hyperthyreose oder Hypothyreose? Dyspnoe oder Stridor? Heiserkeit? Schluckbeschwerden? Schmerzen?
- Sonstige relevante Krankheiten?
- Regelmäßige Medikamente?
- Klinische Untersuchung
- Allgemeinzustand? Besteht eine Hyper- oder Hypothyreose?
- Lage? Größe? Form? Konsistenz? An Haut oder umliegendem Gewebe fixiert? Bewegung beim Schlucken? Druckschmerz?
- Lokale Lymphknoten?
- Ergänzende Untersuchungen
- TSH
- Sonografie
- Evtl. Szintigrafie?
Therapie
Therapieziele
- Etwaige Kompressionssymptome lindern.
- Etwaige Hypo-/Hyperthyreose korrigieren.
- Ggf. kosmetische Korrektur
Allgemeines zur Therapie
- Der gesamte Abschnitt basiert auf diesen Referenzen.22-24
- Beobachtung
- Viele große Strumen wachsen nicht oder nur langsam. Liegen keine Komplikationen, kein Malignitätsverdacht und keine erheblichen kosmetischen Beeinträchtigungen vor, sollte insbesondere bei älteren Patient*innen die Beobachtung als Behandlungsstrategie gewählt werden.
- Diese Patient*innen können einmal jährlich (oder seltener) klinisch untersucht werden. Ggf. wird TSH bestimmt und eine Sonografie durchgeführt. Bleiben die Patient*innen vollkommen beschwerdefrei, müssen keine Routine-Verlaufskontrollen erfolgen.
- Bei Kompressionssymptomen oder dringendem Malignitätsverdacht sollte operiert werden.
- Euthyreote Struma mit Nachweis von autonomen Arealen
- Gefahr der Entwicklung einer manifesten Hyperthyreose, z. B. nach Jodkontamination (Kontrastmittel, Amiodaron)
- Siehe auch Artikel Subklinische Hyperthyreose.
Medikamentöse Therapie
- Da der Jodmangel die wichtigste Ursache der euthyreoten Struma diffusa darstellt, ist die Korrektur des intrathyreoidalen Jodmangels primäres Behandlungsziel.2
- Bei Kindern und Jugendlichen vor der Pubertät ist die Gabe von Jodid (150–200 µg Jodid/d) die Therapie der Wahl.
- Auch bei Jugendlichen in der Pubertät und bei jungen Erwachsenen kann die Jodidmonotherapie erfolgreich sein, allerdings ist die Evidenzlage hier eher spärlich.
- Cave: Bei Knotenstrumen mit autonomen Bereichen erhöht sich infolge der Jodzufuhr das Risiko einer Hyperthyreose, und zwar insbesondere, wenn zuvor ein Jodmangel vorlag.11
- Levothyroxin bei euthyreoter Knotenstruma?
- Bei ausreichender Jodversorgung in Kombination mit Jod zu erwägen, nicht als Monotherapie.
- Alternativ zur Monotherapie mit Jod kommt bei Erwachsenen die zeitlich begrenzte Jodid- und Levothyroxin-Kombinationstherapie (Verhältnis 2:1; z. B. 150 µg Jodid/75 µg Levothyroxin) infrage, unter der eine Volumenabnahme einer Struma über einen Zeitraum von einem Jahr erreicht werden kann.2
- Bei ausreichender Jodversorgung kann eine Kombination aus Jod mit Levothyroxin das Knotenvolumen stärker senken als Jod allein oder als Levothyroxin allein oder als Placebo (LISA-Studie, Laufzeit 1 Jahr).25
- Knoten: –17,3 % Reduktion des Knotenvolumens unter Levothyroxin und Jod, –4,0 % unter Jod allein
- Struma: Strumareduktion unter Levothyroxin und Jod –7,9 %, unter Jod allein –5,2 % und unter Placebo –1,6 %
- Eine Levothyroxin-Monotherapie war der Kombinationstherapie nicht überlegen.
- Obsolet sind eine TSH-suppressive Therapie ebenso wie die Monotherapie einer euthyreoten Struma diffusa mit Levothyroxin, die zu einer weiteren intrathyreoidalen Jodverarmung und zum erneuten Schilddrüsenwachstum führt, sobald die Medikation abgesetzt wird.2,26
- Die auch heute noch häufige Therapie der uni-/multinodösen Struma mit L-Thyroxin allein wird somit nicht mehr empfohlen.2,10
- Von einer Dauertherapie der Struma nodosa mit Levothyroxin rät auch die Deutsche Gesellschaft für Innere Medizin (DGIM) im Rahmen ihrer Initiative Klug Entscheiden ab.
- Zudem bestehen bei 91 %/75 % der Patien*innen mit uni-/multinodöser Struma und in der Regel bei älteren Patient*innen Kontraindikationen für eine Therapie der Schilddrüsenknoten mit L-Thyroxin.10
- Die Risiken einer iatrogenen (subklinischen) Hyperthyreose insbesondere bei älteren Patient*innen sind zu beachten; vermehrte Rate an Vorhofflimmern sowie erhöhtes Risiko einer Osteoporose. Siehe auch den Artikel Subklinische Hyperthyreose.
- Thyreostatika?
- Thyreostatika können bei einer manifesten Hyperthyreose, insbesondere im Vorfeld eines operativen Eingriffs oder einer Radiojodtherapie, indiziert sein.27
- Betablocker?
- Betablocker können die adrenergen Symptome (z. B. Tremor, Schwitzen, Tachykardie) einer Hyperthyreose abmildern.28
- Zugelassen zur Therapie bei Hyperthyreose in Deutschland ist einzig Propranolol!
Operative Therapie
- Die Knotenstruma kann je nach Größe, klinischer Symptomatik und Labor (TSH) operativ, radiojodtherapeutisch oder medikamentös behandelt oder beobachtet werden.22
- Indikationen zur Operation sind Malignitätsverdacht, lokale Beschwerden oder eine subklinische bzw. manifeste Hyperthyreose.
- Bei ausgedehnter retrosternaler Struma oder dystoper Lage kann eine Operationsindikation auch bei fehlender Symptomatik oder fehlenden Malignitätshinweisen bestehen.22
- Resektionsverfahren22
- Bei malignitätsverdächtigen Knoten sollte aufgrund des Risikos eines erst postoperativ möglichen Karzinomnachweises grundsätzlich eine Hemithyreoidektomie durchgeführt werden.
- Bei Solitärknoten ohne Malignitätshinweis ist, je nach Knotengröße und intrathyreoidaler Lage, eine Knotenexzision mit Entfernung des umgebenden Randsaumes normalen Schilddrüsengewebes, eine subtotale Lappenresektion oder eine Hemithyreoidektomie angezeigt.
- Bei vollkommen knotig umgewandeltem Schilddrüsengewebe oder multiplen Knoten in beiden Schilddrüsenlappen sollte eine Thyreoidektomie oder fast-totale Thyreoidektomie angestrebt werden.
- Rezidivrisiko
- Liegen erhebliche oder lebensbedrohliche Kompressionssymptome vor, stellt die operative Therapie die schnellste Methode dar, um die Situation unter Kontrolle zu bekommen, dies ist jedoch selten notwendig.
- Komplikationsrisiko
- Permanente operationsspezifische Komplikationen wie eine Parese des Nervus recurrens oder ein Hypoparathyreoidismus treten in 0–3 % der Fälle auf.11,18
- Bei großen Strumen ist das Rezidiv- und Operationsrisiko erhöht.
- Als seltene lebensbedrohliche Komplikation kann infolge einer großen Struma eine Tracheomalazie auftreten. Insbesondere bei intrathorakalen Strumen kann es postoperativ zu einem Kollaps der Luftröhre und einem Atemstillstand kommen.11
- Postoperative Substitutionsbehandlung
- Nach einer totalen oder subtotalen Thyreoidektomie ist eine Substitutionsbehandlung mit L-Thyroxin erforderlich.
- Das TSH sollte in der unteren Hälfte des Referenzbereichs liegen.
- Nach einer teilweisen Strumektomie (z. B. Hemithyreoidektomie) ist bei postoperativ euthyreoten Patient*innen eine routinemäßige Rezidivprophylaxe mit L-Thyroxin nicht notwendig.11
Radiojodtherapie
- Wenn die Indikation zur definitiven Therapie gegeben ist, muss individuell zwischen Operation und Radiojodtherapie (RJT) abgewogen werden.24
- Durchführung stationär nach Strahlenschutzverordnung
- Ziele der RJT24
- Beseitigung einer Hyperthyreose
- Beseitigung einer Autonomie
- Volumenreduktion einer Struma
- In Deutschland ist vor Durchführung einer Radiojodtherapie ein sog. Radiojodtest vorgeschrieben, der die individuelle Aktivität der Schilddrüse ermittelt.
- Indikation24
- (rezidivierender) Morbus Basedow
- toxisches Adenom
- toxische Knotenstruma
- großvolumige Struma
- Rezidivstruma
- Am häufigsten eingesetzt bei:
- älteren Patient*innen
- Personen mit Begleiterkrankungen, wenn eine andere Behandlung erfolglos geblieben ist.
- Die Radiojodtherapie ist insbesondere bei Patient*innen mit hohem Operationsrisiko, Rezidivstrumen, Strumen in höherem Lebensalter sowie bei Patient*innen, die keine Operation wünschen, indiziert.11,14,24
- Es kann durchschnittlich eine Größenreduktion um etwa 40 % erreicht werden, die Ergebnisse variieren jedoch stark.
- Selbst kleinere Größenreduktionen der Struma können zur Linderung der Kompressionssymptome von entscheidender Bedeutung sein.31
- Nebenwirkungen
- In den nachfolgenden Wochen kommt es meist zur Entwicklung einer Hypothyreose, die mithilfe von L-Thyroxin zu kompensieren und lebenslang zu behandeln ist.
- Insgesamt muss bei mehr als der Hälfte der Patient*innen nach einer RJT mit der Entwicklung einer latenten oder manifesten Hypothyreose gerechnet werden, die oft erst Jahre nach der Therapie als sog. Späthypothyreose auftritt.
- Weitere Nebenwirkungen sind selten, und die Behandlung scheint das Krebsrisiko nicht zu erhöhen.
- Mögliche Nebenwirkungen sind leichte Schmerzen im vorderen Halsbereich aufgrund einer Strahlenthyreoiditis und eine vorübergehend verstärkte Hyperthyreose (kann durch Vorbehandlung mit Thyreostatika vorgebeugt werden).32
- Es besteht ein erhöhtes Risiko für die Entwicklung eines Hyperparathyreoidismus aufgrund von Adenombildung.
Verlauf, Komplikationen und Prognose
Verlauf
- Der natürliche Verlauf variiert stark in Bezug auf Wachstum und Schilddrüsenfunktion, sodass die Vorhersage des Krankheitsverlauf im Einzelfall schwierig ist.11
- Somit ist es zu entscheiden, ob die betroffene Person zunächst nicht behandelt, sondern beobachtet werden soll, oder ob sofort eine Therapie erfolgen sollte, bevor es zu einem weiteren Wachstum der Struma kommt und keine optimalen Therapieergebnisse mehr erzielt werden können.
- Mehrere Studien haben gezeigt, dass es bei einem nicht unwesentlichen Teil der Betroffenen (5–60 %) zu einer spontanen Rückbildung der Struma kommt!33-34
- Das Wachstum von Knotenstrumen scheint mit dem Alter nachzulassen (nach dem 40. Lebensjahr).35
Komplikationen
- Kompressionssymptome
- Hyperthyreose
- Hypothyrose (selten)
- Malignomentwicklung (selten)
- Hypoparathyreoidismus nach subtotaler oder totaler Thyreoidektomie mit akzidenteller Entfernung der Nebenschilddrüsen
Verlaufskontrolle
- Patient*innen unter Beobachtung („Watch and Wait“)
- Patient*innen, bei denen lediglich eine Beobachtung erfolgt, können einmal jährlich klinisch untersucht werden, ggf. wird ihr TSH bestimmt sowie eine Sonografie durchgeführt.
- Bei Beschwerdefreiheit kann ein größeres Kontrollintervall gewählt werden (gemeinsame Entscheidungsfindung).
- Nach der operativen Therapie oder Radiojodtherapie
- Der TSH-Wert sollte regelmäßig kontrolliert und ggf. die Thyroxin-Dosis angepasst werden.
Patienteninformationen
Patienteninformationen in Deximed
Illustrationen
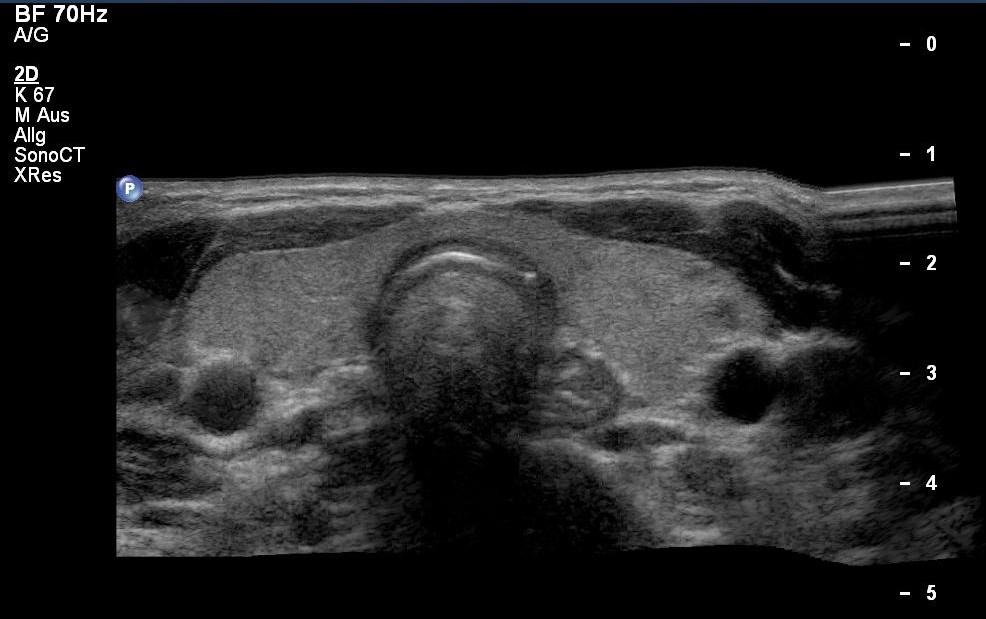
Normalbefund der Schilddrüse mit oberem Ösophagus in der Sonografie (mit freundlicher Genehmigung von sonographiebilder.de ©Albertinen-Diakoniewerk e. V., Hamburg)
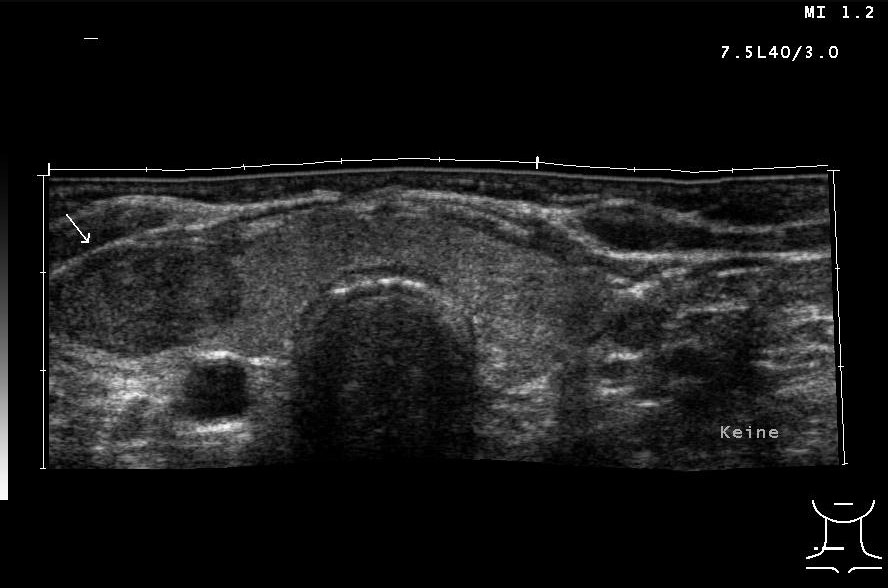
Solider Schilddrüsenknoten rechts in der Sonografie (mit freundlicher Genehmigung von sonographiebilder.de ©Albertinen-Diakoniewerk e. V., Hamburg)
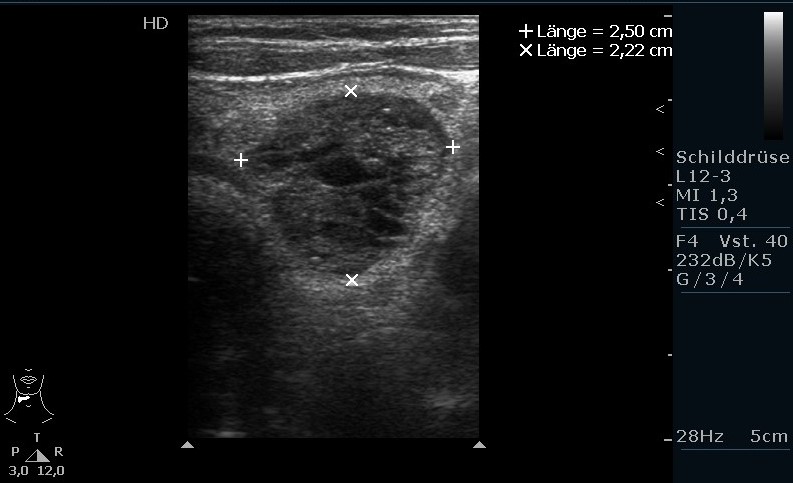
Struma multinodosa in der Sonografie, großer Knoten im linken SD-Lappen (mit freundlicher Genehmigung von sonographiebilder.de ©Albertinen-Diakoniewerk e. V., Hamburg)

Schilddrüsenkarzinom in der Sonografie: echoarmer Knoten, kein Halo, Mikrokalzifikationen, inhomogen (mit freundlicher Genehmigung von sonographiebilder.de ©Albertinen-Diakoniewerk e. V., Hamburg)

Normalbefund Schilddrüse mit oberem Ösophagus in der Sonografie (mit freundlicher Genehmigung von sonographiebilder.de ©Albertinen-Diakoniewerk e. V., Hamburg)
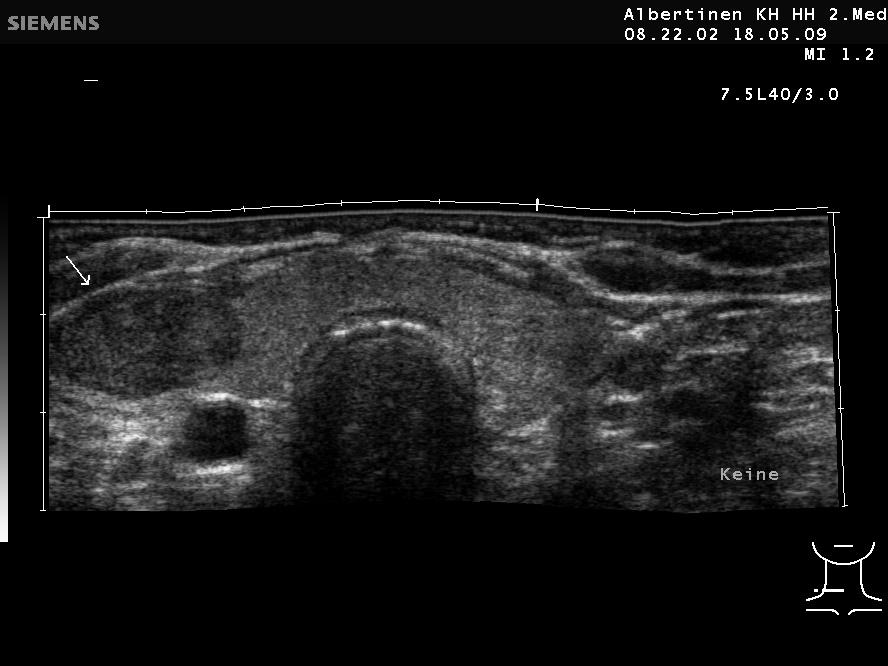
Solider Schilddrüsenknoten rechts in der Sonografie (mit freundlicher Genehmigung von sonographiebilder.de ©Albertinen-Diakoniewerk e. V., Hamburg)
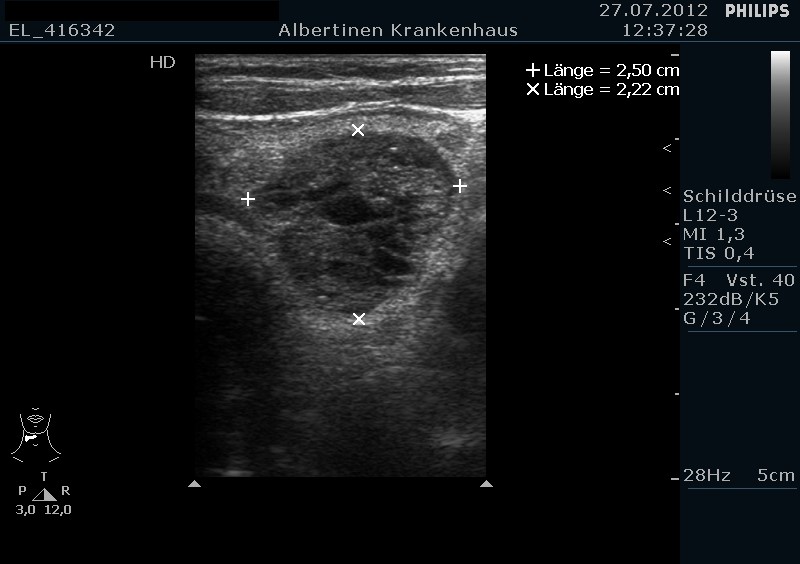
Struma multinodosa in der Sonografie, großer Knoten im linken SD-Lappen (mit freundlicher Genehmigung von sonographiebilder.de ©Albertinen-Diakoniewerk e. V., Hamburg)
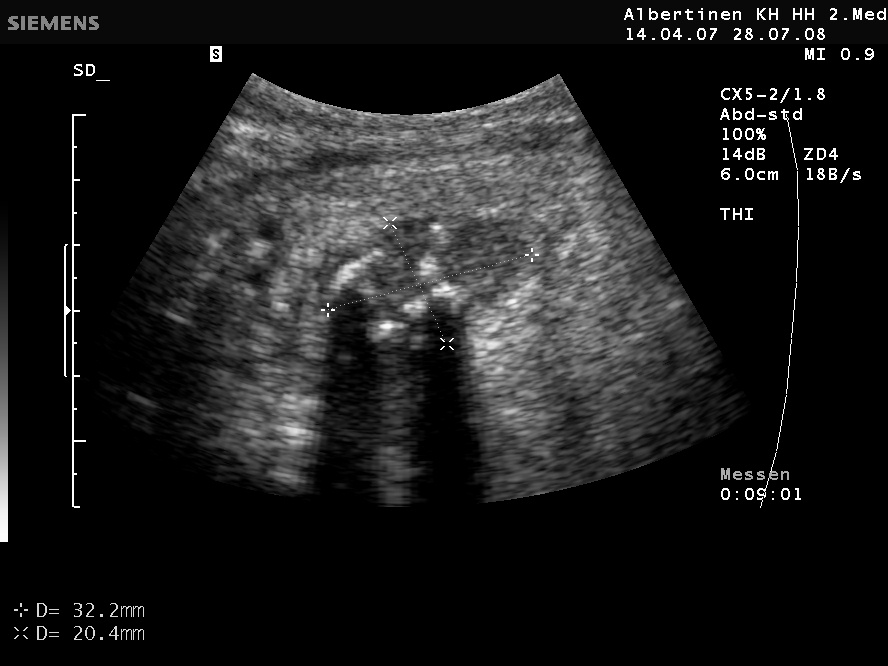
Schilddrüsenkarzinom in der Sonografie, echoarm, Mikrokalk, kein Halo (mit freundlicher Genehmigung von sonographiebilder.de ©Albertinen-Diakoniewerk e. V., Hamburg)
Quellen
Leitlinien
- Deutsche Gesellschaft für Allgemein- und Viszeralchirurgie. Benigne Schilddrüsenerkrankungen, operative Therapie. AWMF-Leitlinie Nr. 088–007. S2k, Stand 2015. (abgelaufen) www.awmf.org
- Deutsche Gesellschaft für Nuklearmedizin. Radioiodtherapie bei benignen Schilddrüsenerkrankungen. AWMF-Leitlinie Nr. 031-003. S1, Stand 2015 (abgelaufen) www.awmf.org
- Deutsche Gesellschaft für Kinder- und Jugendmedizin. Hyperthyreose. AWMF-Leitlinie Nr. 027–041. S1, Stand 2011. (abgelaufen) www.awmf.org
- Deutsche Gesellschaft für Ernährung. Die Referenzwerte für die Nährstoffzufuhr. Jod. Empfohlene Zufuhr. www.dge.de
Literatur
- Lohnstein M, Eras J, Hammerbacher C. Der Prüfungsguide Allgemeinmedizin - Aktualisierte und erweiterte 3. Auflage. Augsburg: Wißner-Verlag, 2018.
- Führer D, Bockisch A, Schmid KW: Euthyroid goiter with and without nodules—diagnosis and treatment. Dtsch Arztebl Int 2012; 109(29–30): 506–16. DOI: 10.3238/arztebl.2012.0506 www.aerzteblatt.de
- Giuffrida D, Gharib H. Controversies in the management of cold, hot, and occult thyroid nodules. Am J Med 1995; 99: 642-50 PubMed
- Marqusee E, Benson CB, Frates MC, et al. Usefulness of ultrasonography in the management of nodular thyroid disease. Ann Intern Med 2000; 133: 696-700. www.ncbi.nlm.nih.gov
- Pellegriti G, Frasca F, Regalbuto C, Squatrito S, Vigneri R. Worldwide increasing incidence of thyroid cancer: update on epidemiology and risk factors. J Cancer Epidemiol. 2013;2013:965212. doi: 10.1155/2013/965212. www.ncbi.nlm.nih.gov
- Schilddrüsenkrebs: IARC warnt vor Überdiagnose in mehreren Ländern. Deutsches Ärzteblatt. 19. August 2016. www.aerzteblatt.de
- Überdiagnose von Schilddrüsenkrebs in Südkorea. Deutsches Ärzteblatt. 7. November 2014 www.aerzteblatt.de
- Vaccarella S et al. Worldwide Thyroid-Cancer Epidemic? The Increasing Impact of Overdiagnosis. N Engl J Med 2016; 375:614-617 DOI: 10.1056/NEJMp1604412 www.nejm.org
- Robert-Koch-Institut (RKI). Zentrum für Registerdaten. Schilddrüsenkrebs. Stand: 06.12.2017 www.krebsdaten.de
- Wienhold R, Scholz M, Adler JB, Günster C, Paschke R. Versorgung bei Schilddrüsenknoten. Dtsch Arztebl Int 2013; 110(49): 827-34. www.aerzteblatt.de
- Hegedus L, Bonnema SJ, Bennedbaek FN. Management of simple nodular goiter: current status and future perspectives. Endocr Rev 2003; 24: 102-32. PubMed
- Derwahl M. From diffuse goiter to nodular goiter. Internist (Berl) 1998; 39: 577-83. www.ncbi.nlm.nih.gov
- Deutsche Gesellschaft für Ernährung. Die Referenzwerte für die Nährstoffzufuhr. Jod. Empfohlene Zufuhr. www.dge.de
- Howarth DM, Epstein MT, Thomas PA et al. Outpatient management of patients with large multinodular goitres treated with fractionated radioiodine. Eur J Nucl Med 1997; 24: 1465-9. PubMed
- Jarløv AE, Nygaard B, Hegedüs L, Hartling SG, Hansen JM. Observer variation in the clinical and laboratory evaluation of patients with thyroid dysfunction and goiter. Thyroid 1998; 8: 393-8. PubMed
- Hegedüs L. Thyroid ultrasound. Endocrinol Metab Clin North Am 2001; 30: 339-60. PubMed
- Gittoes NJ, Miller MR, Daykin J et al. Upper airways obstruction in 153 consecutive patients presenting with thyroid enlargement. BMJ 1996; 312: 484. www.ncbi.nlm.nih.gov
- Rios A, Rodriguez JM, Canteras M et al. Surgical management of multinodular goiter with compression symptoms. Arch Surg 2005; 140: 49-53. PubMed
- Bartsch D K, Luster M, Buhr H J, Lorenz D, Germer C, Goretzki PE. Indications for the Surgical Management of Benign Goiter in Adults Dtsch Arztebl Int 2018; 115: 1-7. DOI: 10.3238/arztebl.2018.0001. www.aerzteblatt.de
- Papini E et al. Risk of Malignancy in Nonpalpable Thyroid Nodules: Predictive Value of Ultrasound and Color-Doppler Features. The Journal of Clinical Endocrinology & Metabolism, Volume 87, Issue 5, 1 May 2002, Pages 1941–1946, https://doi.org/10.1210/jcem.87.5.8504 academic.oup.com
- Deutsche Gesellschaft für Nuklearmedizin. Schilddrüsenszintigraphie. AWMF-Leitlinie Nr. 031–011, Stand 2014. www.nuklearmedizin.de
- Deutsche Gesellschaft für Allgemein- und Viszeralchirurgie. Benigne Schilddrüsenerkrankungen, operative Therapie. AWMF-Leitlinie Nr. 088–007, Stand 2015. www.awmf.org
- Deutsche Gesellschaft für Kinder- und Jugendmedizin. Hyperthyreose. AWMF-Leitlinie Nr. 027–041, Stand 2011. www.awmf.org
- Deutsche Gesellschaft für Nuklearmedizin. Radioiodtherapie bei benignen Schilddrüsenerkrankungen. AWMF-Leitlinie Nr. 031-003, Stand 2015. www.awmf.org
- Grussendorf M, Reiners C, Paschke R, Wegscheider K; LISA Investigators. Reduction of thyroid nodule volume by levothyroxine and iodine alone and in combination: a randomized, placebo-controlled trial. J Clin Endocrinol Metab. 2011 Sep;96(9):2786-95. doi: 10.1210/jc.2011-0356. Epub 2011 Jun 29 www.ncbi.nlm.nih.gov
- Wesche MF, Tiel V, Lips P et al. A randomized trial comparing levothyroxine with radioactive iodine in the treatment of sporadic nontoxic goiter. J Clin Endocrinol Metab 2001; 86: 998-1005. PubMed
- Cooper DS. Antithyroid drugs. N Engl J Med 2005;352:905-917. New England Journal of Medicine
- Bahn RS, Burch HB, Cooper DS, et al. Hyperthyroidism and other causes of thyrotoxicosis: management guidelines of the American Thyroid Association and American Association of Clinical Endocrinologists. Endocr Pract 2011;17:456-520. PubMed
- Hermus AR, Huysmans DA. Treatment of benign nodular thyroid disease. N Engl J Med 1998; 338: 1438-47. New England Journal of Medicine
- Bononi M, de Cesare A, Atella F et al. Surgical treatment of multinodular goiter: incidence of lesions of the recurrent nerves after total thyroidectomy. Int Surg 2000; 85: 190-3. PubMed
- Bonnema SJ, Bertelsen H, Mortensen J, et al. The feasibility of high dose iodine 131 treatment as an alternative to surgery in patients with a very large goiter: effect on thyroid function and size and pulmonary function. J Clin Endocrinol Metab 1999; 84: 3636-41. PubMed
- Nygaard B, Knudsen JH, Hegedus L et al. Thyrotropin receptor antibodies and Graves' disease, a side-effect of 131I treatment in patients with nontoxic goiter. J Clin Endocrinol Metab 1997; 82: 2926-30. PubMed
- Vanderpump MP, Tunbridge WM, French JM, et al. The incidence of thyroid disorders in the community: a twenty-year follow-up of the Whickham Survey. Clin Endocrinol (Oxf) 1995; 43: 55-68. www.ncbi.nlm.nih.gov
- Rallison ML, Dobyns BM, Meikle AW, Bishop M, Lyon JL, Stevens W. Natural history of thyroid abnormalities: prevalence, incidence, and regression of thyroid diseases in adolescents and young adults. Am J Med 1991; 91: 363-70. PubMed
- Knudsen N, Bülow I, Jørgensen T, Laurberg P, Ovesen L, Perrild H. Goitre prevalence and thyroid abnormalities at ultrasonography: a comparative epidemiological study in two regions with slightly different iodine status. Clin Endocrinol (Oxf) 2000; 53: 479-85. www.ncbi.nlm.nih.gov
Autor*innen
- Lino Witte, Dr. med., Arzt in Weiterbildung, Innere Medizin, Frankfurt
- Hannes Blankenfeld, Dr. med., Facharzt für Innere und Allgemeinmedizin, München (Review)
- Caroline Beier, Dr. med., Fachärztin für Allgemeinmedizin, Hamburg
- Die ursprüngliche Version dieses Artikels basiert auf einem entsprechenden Artikel im norwegischen hausärztlichen Online-Handbuch Norsk Elektronisk Legehåndbok (NEL, https://legehandboka.no/).